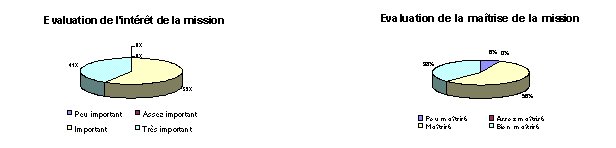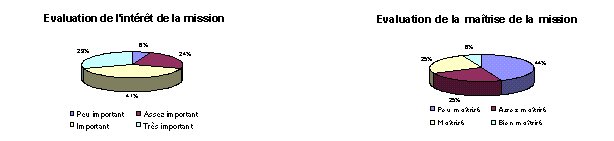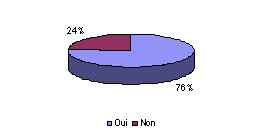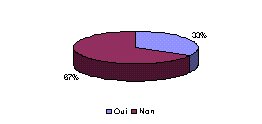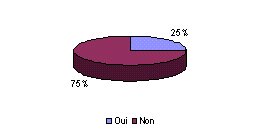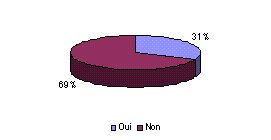|
Avertissement
|
|
Si vous arrivez directement sur cette
page sachez que ce travail est un rapport
d'étudiant(e)s et doit être pris comme tel. Il
peut donc comporter des imperfections ou des
imprécisions que le lecteur doit admettre et donc
supporter. Il a été réalisé lors
de la période d'enseignement théorique
à l'UTC
et constitue avant-tout un travail de compilation
bibliographique, d'initiation et d'analyse sur des
thématiques associées aux technologies
biomédicales.
Nous ne faisons aucun
usage commercial et la duplication est libre. Si vous avez
des raisons de contester ce droit d'usage, merci
de nous en faire
part.
L'objectif de la présentation sur le Web est de
permettre l'accès à l'information et
d'augmenter ainsi les échanges professionnels. En cas
d'usage du document, n'oubliez pas de le citer comme source
bibliographique. Bonne lecture...
|
Réference
à rappeler : Etat de l'art des missions des
services biomédicaux, réflexions sur des
bonnes pratiques de l'ingénierie biomédicale,
G. MANIBAL - C. RONCALLI ,
Projet DESS "TBH", UTC,
00-01, pp 68 , URL :
https://www.utc.fr/~farges/dess_tbh/00-01/Projets/BPIB/BPIB.htm
Etat de l'état
des missions des services
biomédicaux
-
Réflexions sur
des Bonnes Pratiques de l'Ingénierie
Biomédicale
|

Ghislaine
MANIBAL
|

Christophe
RONCALLI
|
|
RESUME
De par ses fonctions,
l'ingénieur biomédical est un acteur
participant à la qualité et à la
continuité des soins. Pourtant, cette profession
n'est actuellement pas reconnue par le Code de la
Santé Publique. Par conséquent, un des besoins
actuels, pour obtenir une réelle reconnaissance, est
l'élaboration d'un guide des Bonnes Pratiques de
l'Ingénierie Biomédicale.
Deux enquêtes menées
en décembre 2000 ont mis en évidence
l'importance de chacune des missions des services
biomédicaux ainsi que leur maîtrise. A partir
de cet état de l'art, ce rapport propose des
réflexions sur ces bonnes pratiques, en s'appuyant
sur des références et standards
internationaux, européens et nationaux.
Mots-clés :
client, organisation, qualité, service
biomédical, bonnes pratiques, missions
|
|
ABSTRACT
Among his functions, the
biomedical engineer is actively involving in the quality and
the continuity of the health care. However, this
profession is currently not recognized by the Public Health
Code. Consequently, one of the present needs, to
obtain a real recognition, is the elaboration of a guide of
the Good Practices of Biomedical Engineering.
Two surveys were carried out in
December 2000 that highlighted the significance of each
missions of the biomedical wards as well as their
control. From this state, this report proposes
reflexions on these good practices, whilst being pressed on
references and international standards, european and
national ones.
Key Words :
customer, organisation, quality, biomedical wards, good
practices, missions
|
REMERCIEMENTS
Ce projet est l'aboutissement d'un travail
mené en collaboration avec de nombreuses personnes.
Nous tenons à remercier Monsieur Gilbert
FARGES qui nous a conseillé et orienté dans notre
travail de recherche et dans l'élaboration de notre
réflexion sur des Bonnes Pratiques de l'Ingénierie
Biomédicale.
Nous exprimons notre profonde reconnaissance
à Monsieur Nicolas BELLEGOU, Ingénieur
Biomédical à l'Hôpital d'Instruction des
Armées du Val de Grâce, pour ses précieux
conseils et sa grande disponibilité.
Ces remerciements s'adressent également
à :
- M.
François DURAND-GASSELIN, Ingénieur biomédical
au C.H.U. de Montpellier,
- M.
Stéphane GEYSSENS, Ministère de l'Emploi et de la
Solidarité,
- M.
Mourad GHOMARI, Ingénieur Biomédical au C.H.U. de
Rouen,
- M.
Eric JULLIAN, Ingénieur Biomédical au C.H.U.
d'Amiens,
-
aux membres du Conseil d'Administration de l'A.F.I.B., Association
Française des Ingénieurs Biomédicaux,
pour leur disponibilité, leurs nombreux
conseils et les documents fournis utiles à notre
travail.
Un grand merci à tous les ingénieurs
et techniciens biomédicaux qui ont montré un
réel intérêt à notre projet en
répondant aux différentes enquêtes, merci pour
leur disponibilité, leurs conseils et leur soutien.
Que toutes ces personnes veuillent trouver ici
l'expression de notre reconnaissance et de notre
gratitude.
SOMMAIRE
INTRODUCTION
PARTIE 1 : Etat de l'art
des missions des services biomédicaux
1)
Introduction
2)
Identification des missions
2.1. Elaboration
de l'enquête
2.2. Analyse de
l'enquête
2.3. Conclusion de
l'enquête
3)
Evaluation de l'importance et de la maîtrise des
missions
3.1. Elaboration
de l'enquête
3.2. Analyse et
interprétation de l'enquête
3.3. Conclusion
PARTIE 2 :
Réflexions sur des Bonnes Pratiques de l'Ingénierie
Biomédicale
1)
Critères relatifs aux clients
1.1.
Identification des clients
1.2. Besoins et droits des
clients
1.3.
Evaluation de la satisfaction des clients
2)
Critères relatifs à l'organisation
2.1.
Gestion des ressources humaines
2.2. Gestion de
l'environnement
2.3. Gestion des
dispositifs médicaux
3)
Critères relatifs à la qualité et à la
prévention
3.1. Gestion de la
qualité
3.2.
Gestion des risques - Matériovigilance
CONCLUSION
BIBLIOGRAPHIE
REFERENCES
NORMATIVES ET REGLEMENTAIRES
INTRODUCTION
A l'heure actuelle, la profession
d'ingénieur biomédical regroupe diverses fonctions
telles que l'achat des équipements, la maintenance mais aussi
le management du personnel ou la mise en place d'un système
qualité.
Par ces fonctions, le service biomédical
est un acteur participant à la qualité et à la
continuité des soins. Pourtant, aucun texte officiel ne
définit cette profession précisément et elle
n'est actuellement pas reconnue par le Code de la Santé
Publique, contrairement aux autres professions du secteur
hospitalier, qui sont, entres autres, les pharmaciens, les
médecins et les directeurs.
Par conséquent, un des besoins actuels de
la communauté biomédicale, pour obtenir une
réelle reconnaissance, est une réflexion sur
l'élaboration d'un guide de Bonnes Pratiques au sein d'un
service biomédical.
Actuellement, plusieurs études sont
menées et certaines ont donné naissance à des
guides ou des documents équivalents, mais il n'en existe aucun
concernant les Bonnes Pratiques de l'Ingénierie
Biomédicale proprement dite.
Le but de notre étude est, dans un premier
temps, de faire un état de l'art des missions d'un service
biomédical. A partir de cette première enquête,
nous avons orienté nos questions pour évaluer, d'une
part, l'intérêt de chacune des missions retenues et,
d'autre part, leur maîtrise par les différents
services biomédicaux.
La seconde partie de ce rapport concerne les
réflexions sur des Bonnes Pratiques de l'Ingénierie
Biomédicale.
A l'aide des résultats obtenus à
l'issue des deux enquêtes mais également à partir
de références et standards internationaux,
européens et nationaux, nous avons élaboré une
première étude permettant la constitution d'une base
solide pour aboutir à un guide des Bonnes Pratiques de
l'Ingénierie Biomédicale.
Retour sommaire
I.
Etat de l'art des missions des services
biomédicaux
1°)
Introduction
Le but de cette première partie est de
faire un état de l'art des missions actuelles d'un service
biomédical. Notre étude se déroule en plusieurs
étapes.
Tout d'abord, afin de mieux cerner et identifier
les diverses missions, nous avons décidé de recueillir
l'avis d'ingénieurs et techniciens biomédicaux,
à travers toute la France, pour compléter nos acquis et
avoir différents points de vue professionnels. A la suite de
cela, nous avons regroupé les réponses en plusieurs
items en dégageant les grandes missions communes à
l'ensemble des services biomédicaux. Cette première
enquête se voulait générale afin de mieux
orienter nos réflexions sur des points
particuliers.
Une seconde étude a été
réalisée auprès d'un même
échantillon, en prenant, comme base, les réponses
recueillies ultérieurement. Ce travail s'est
déroulé sous forme de questions à choix unique
ou multiple, son but étant d'évaluer l'importance des
missions ainsi que leur maîtrise au sein du service
biomédical.
Pour cet état de l'art, nous avons
contacté un échantillon de 75 ingénieurs et
techniciens biomédicaux. Sur l'ensemble, 33 services
biomédicaux ont participé à nos enquêtes,
mais seulement 29 réponses ont été
validées.
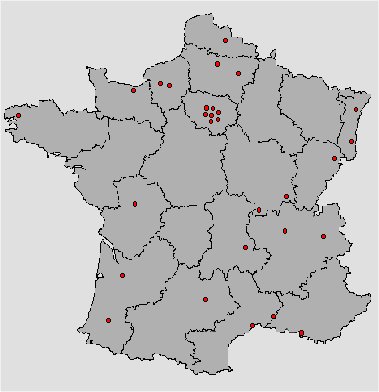
Fig. A : Représentation
géographique des réponses à l'enquête
validées.
Retour sommaire
2°)
Identification des missions
2.1. Elaboration de
l'enquête : La méthodologie
d'élaboration d'une enquête est présentée
dans la partie
2 - §1.3. Par conséquent,
l'élaboration de l'enquête consiste en un
récapitulatif sous forme de tableau.
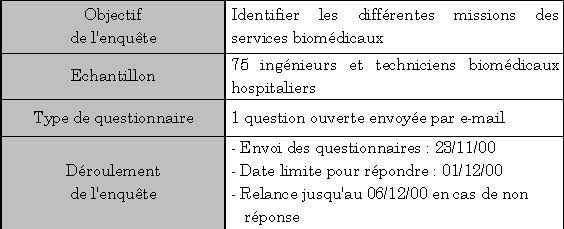
2.2. Analyse de
l'enquête : 21 % des services
biomédicaux contactés ont répondu à cette
enquête. Les réponses ont été
regroupées en treize thèmes
principaux.
- Procédures d'achat
- Analyse des besoins avant l'achat de
dispositifs médicaux
- Analyse de la cohérence du parc
existant
- Aide à l'élaboration et
à l'exécution du plan
d'équipement
- Planification des achats de dispositifs
médicaux
- Rédaction des cahiers des charges pour
les appels d'offre, marchés négociés et
mises en concurrence
- Participation au choix des
équipements
- Acquisition des équipements
- Préparation des plans d'investissement
des dispositifs médicaux en relation avec les services
économiques et les médecins
- Respect de la réglementation en
matière d'achat public
- Installation des dispositifs
médicaux
- Installation du matériel en
tenant compte de l'ergonomie du poste de travail
- Installation du matériel en tenant
compte des interconnections avec les autres membres de
l'hôpital
- Mise en service et réforme des
dispositifs médicaux
Retour sommaire
- Maintenance
- Maintenance
préventive
- Maintenance corrective
- Maintenance du système de manutention
légère
- Maintien des performances des dispositifs
médicaux
- Suivi de la maintenance -
traçabilité par Gestion de Maintenance
Assistée par Ordinateur (G.M.A.O.)
- Suivi des contrôles
techniques
- Veille technologique
- Sécurité et sûreté
des dispositifs médicaux
- Formation des utilisateurs
- Conseil auprès des
utilisateurs
- Formation des utilisateurs
- Actions pour favoriser l'utilisation optimale
des dispositifs médicaux
- Contrôle continu de la
qualité
- Mise en place de la démarche
qualité en maintenance
- Accréditation
- Suivi de la réglementation
- Conformité aux normes et aux
réglementations
- Gestion
- Gestion du magasin
biomédical
- Gestion des crédits de
maintenance
- Gestion des budgets
- Management du personnel du service
biomédical
- Matériovigilance
- Suivi des prestataires
extérieurs
- Recherche et développement
- Coopérations
inter-hospitalières
- Participation au Comité de Lutte contre
les Infections Nosocomiales (C.L.I.N.)
2.3. Conclusion de
l'enquête : Cette première
enquête ayant pour objectif l'identification des missions des
services biomédicaux, a permis de dégager plusieurs
grandes missions communes à l'ensemble de ces services.
A partir de ces données, l'évaluation
de l'importance de chacune d'entre elles et de leur maîtrise
peut être envisagée.
Retour sommaire
3°)
Evaluation de l'importance et de la maîtrise des
missions
3.1. Elaboration de
l'enquête
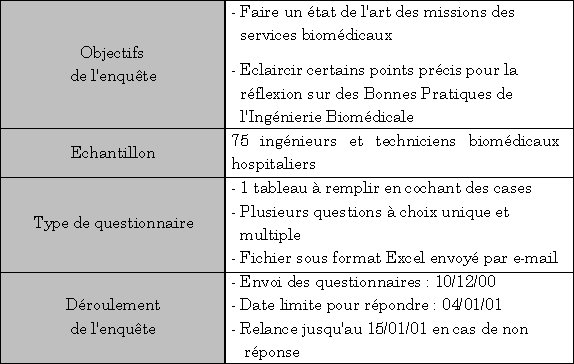
Retour sommaire
3.2. Analyse et
interprétation de l'enquête : 23 % des services
biomédicaux contactés ont répondu à cette
enquête. Les résultats de chaque question sont
présentés sous forme de diagrammes sectoriels
accompagnés d'une analyse plus précise.
- 3.2.1 Analyse de la première page de
l'enquête
- Maintenance corrective : Les chiffres le confirment,
la maintenance corrective est bien l'une des principales
missions des services biomédicaux. En effet, 94 %
d'entres eux l'estiment comme importante et elle peut
être considérée comme parfaitement
maîtrisée.

- Maintenance préventive : La maintenance
préventive est un élément qui suscite un
intérêt important au sein des services
biomédicaux (pour 88 % des services interrogés).
Malheureusement, seulement 56 % la maîtrisent, or, cette
mission peut s'avérer très importante si elle est
réalisée, puisqu'elle contribue à la
diminution des actions correctives et, par conséquent,
aboutit à une diminution des coûts de maintenance,
ce qui est non négligeable.

Si nous comparons, en moyenne, les deux types
de maintenance, il apparaît que la maintenance corrective
est plus importante mais aussi mieux maîtrisée que
la maintenance préventive. Un effort quant à la
réalisation et au suivi d'un planning de maintenance
préventive doit être entrepris par de nombreux
services biomédicaux.
Retour sommaire
- Formations des utilisateurs : L'avis des
différents services biomédicaux interrogés
sur l'intérêt des formations des
utilisateurs est partagé (50/50). Il en est de
même pour la maîtrise de cette mission. A nouveau,
l'analyse précédente peut s'appliquer, puisque si
les utilisateurs ont les formations nécessaires et
suffisantes, le taux de pannes et donc le nombre d'actions
correctives risquent de diminuer considérablement.

- Formations pour les ingénieurs et techniciens
biomédicaux : La formation des ingénieurs et
techniciens biomédicaux a son importance au sein du
service biomédical pour 75 % des personnes
interrogées. Elle est moyennement maîtrisée
et, vue l'importance de cette mission, il s'avère qu'il
existe un manque à ce niveau. Pourtant, il convient au
service biomédical de s'adapter face aux nouvelles
technologies.

Retour sommaire
- Procédures d'achat : Les commentaires sont
peu nombreux pour cette mission puisque tous les services
biomédicaux interrogés la considèrent
comme importante et que 94 % d'entre eux la maîtrisent.
Son intérêt n'est donc plus à
démontrer. La maîtrise des achats, en fonction de
leur influence sur la qualité des services de
l'établissement de santé, est une condition
nécessaire pour obtenir la qualité au moindre
coût et en toute sécurité.
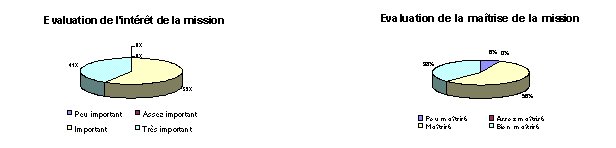
- Gestion budgétaire : La gestion
budgétaire est relativement importante pour 70 % des
services biomédicaux mais quelques difficultés
semblent exister puisque seulement 50 % maîtrisent cette
mission. Le manque de formation, d'outils adéquats ou
tout simplement d'intérêts peuvent être la
cause de ce manque de maîtrise.

Retour sommaire
- Gestion administrative : En ce qui concerne la
gestion administrative, les commentaires sont identiques
à la gestion budgétaire. Toutefois, cette mission
est encore moins maîtrisée et présente un
intérêt moins important.

- Recherche et développement : La recherche et
le développement des dispositifs médicaux est une
mission qui suscite très peu d'intérêt, 18%
seulement, et qui n'est pas maîtrisée. Une
question peut donc se poser : Est ce vraiment un des
rôles des services biomédicaux ?

Retour sommaire
- Mise en place d'un système qualité au sein
du service biomédical : De nos jours, la
qualité est devenue très importante dans tous les
domaines. Cette tendance se confirme dans le biomédical.
Néanmoins, elle reste encore peu maîtrisée
et les démarches entamées par de nombreux
services doivent se poursuivre et ainsi représenter un
modèle pour les autres.
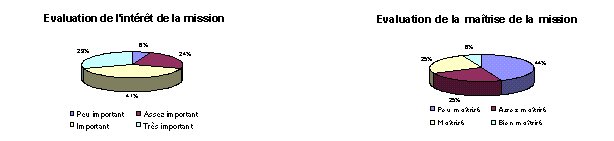
- Contrôle continu de la qualité au sein du
service biomédical : Les services biomédicaux
considèrent le contrôle continu de la
qualité aussi important que la mise en place d'un
système qualité. Par contre, cette mission est
peu maîtrisée, ce qui reste logique puisque seuls
les services biomédicaux qui maîtrisent
déjà la mise en place d'un système
qualité peuvent maîtriser le contrôle
continu de la qualité.

Retour sommaire
- Suivi des prestataires extérieurs : Le suivi
des prestataires extérieurs est important pour 82 % des
services biomédicaux interrogés mais reste
moyennement maîtrisé. Pourtant le taux de
sous-traitance tend à augmenter et il paraît donc
important de s'investir pour une réalisation correcte de
cette mission.

- Sécurité et sûreté des
dispositifs médicaux : Tous les services
biomédicaux ont conscience que leur rôle dans la
sécurité et la sûreté des
dispositifs médicaux est primordial. En effet, 82 % les
considèrent comme importantes et 81 % les
maîtrisent.

- Matériovigilance : Tout comme la
sécurité et la sûreté des
dispositifs médicaux, la matériovigilance est une
mission importante au sein des services biomédicaux.
Elle est relativement bien maîtrisée malgré
le fait qu'elle soit récente.

Retour sommaire
3.2.2 Analyse de la deuxième page de
l'enquête
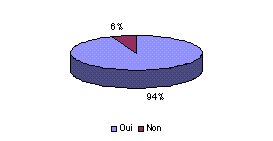
- Possédez vous une G.M.A.O. ? : Pratiquement
l'ensemble des services biomédicaux possèdent une
G.M.A.O. En effet, cet outil de Gestion de Maintenance
Assistée par Ordinateur est incontournable pour la bonne
gestion des dispositifs médicaux. De plus, il permet une
traçabilité de l'ensemble des fiches saisies, ce
qui, à l'heure actuelle, est indispensable.
- Existe-t-il un plan d'établissement au sein du
service biomédical ? : La plupart des services
interrogés réalise un plan d'investissement pour
l'achat des dispositifs médicaux. L'intérêt
d'une telle pratique n'est plus à démontrer et
l'ensemble des services biomédicaux doivent s'efforcer
de la réaliser.
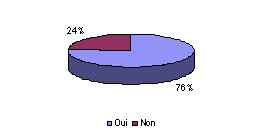
Retour sommaire
- Dans le cas d'une maintenance externe, devez vous en
faire part à une direction ? : Tous les services
biomédicaux ne sont pas totalement indépendants
dans leur gestion de la maintenance. En effet, 33% doivent
demander l'autorisation de la direction pour effectuer une
maintenance externe. Par contre, l'ensemble des services
biomédicaux font signer les bons de commande par les
services économiques.
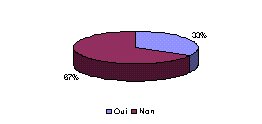
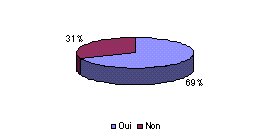
- Réalisez vous des statistiques sur le
fonctionnement du service biomédical ? : Les
services biomédicaux, pour 69% d'entres eux,
maîtrisent les outils statistiques. Une analyse plus
approfondie montre que les services biomédicaux, qui ont
entamé une démarche qualité, ont
déclaré réaliser des statistiques.Il est
donc indispensable de mettre en place ces études
statistiques afin de contrôler, évaluer et
améliorer ses missions.
Retour sommaire
- Evaluez vous le nombre de pannes par service du à
une mauvaise utilisation ? : Contrairement à la
question précédente, cette étude
statistique est peu réalisée, ce qui paraît
en contradiction avec la mise en place de démarche
qualité. Pourtant, une telle mesure peut s'avérer
intéressante pour identifier les besoins en formation
des utilisateurs.
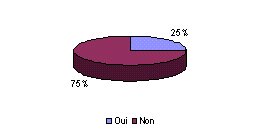
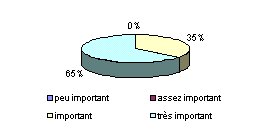
- Dans le cas de mauvais
résultat, que pensez vous d'une formation au service
concerné ? : Même si les services
biomédicaux n'évaluent pas le nombre de
pannes, ils sont 35% à s'accorder sur l'importance
des formations en cas de mauvais résultats.
Retour sommaire
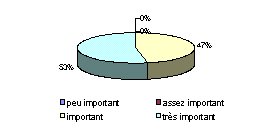
- Comment évaluez vous l'importance du service
biomédical pour :
- Les utilisateurs (médecins,
infirmiers,...) ? : Tous les services biomédicaux
se considèrent au service des utilisateurs, ce qui
justifie bien que les services cliniques sont les clients du
service biomédical.
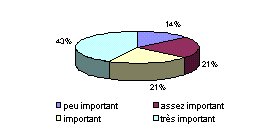
- Patients ? : Par contre,
seulement 75 % pensent être au service des patients,
or, les dispositifs médicaux sont utilisés sur
les patients et ce chiffre peut donc paraître
relativement faible.
Retour sommaire
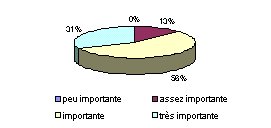
- Que pensez vous d'une communication entre SBM de
différents établissements ? : 87 % des
services biomédicaux désirent mettre en place un
système de communication entre eux. Un tel partage
d'informations et de connaissances représente un
intérêt considérable pour la
communauté biomédicale.
- Vous assurez vous que le dispositif médical est
employé dans l'utilisation clinique pour laquelle il est
destiné ? : Une bonne utilisation diminue le nombre
d'interventions de maintenance corrective. Malheureusement, 38
% des services interrogés ne s'assurent pas que les
dispositifs médicaux sont employés dans
l'utilisation clinique pour laquelle ils sont
destinés.

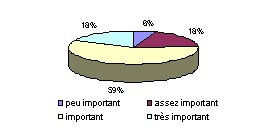
- Comment évaluez vous les critères prix et
ergonomie du poste de travail lors de l'achat d'un
équipement ?
- Critère prix : Les services
biomédicaux considèrent l'ergonomie du poste
de travail comme un critère plus important que le
prix des dispositifs médicaux, 94 % contre 76 %.
Retour sommaire
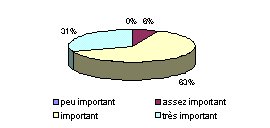
- Critère ergonomie du
poste de travail : La priorité est donc
donnée aux critères des services cliniques
plutôt qu'à ceux des services
économiques. En veillant toutefois à faire un
achat à un rapport qualité/prix raisonnable.
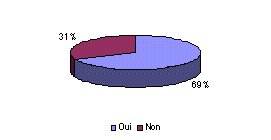
- Avez vous réalisé un plan
d'étalonnage des appareils de contrôle ? : La
majorité des services réalisent un plan
d'étalonnage. Néanmoins, 31 % ont répondu
négativement à cette question. Pourtant, bien
contrôler régulièrement et efficacement les
dispositifs médicaux est nécessaire pour
réaliser une maintenance corrective et préventive
correcte.
Retour sommaire
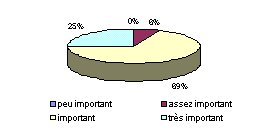
- Quelle importance y
accordez-vous ? : Les services biomédicaux qui
n'ont pas réalisé ce plan d'étalonnage
sont toutefois conscients de son intérêt,
puisqu'ils considèrent cette pratique comme
importante à 94 %.
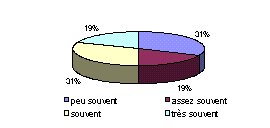
- La maintenance préventive implique-t-elle les
utilisateurs ? : La maintenance préventive
n'implique que moyennement les utilisateurs.
Pourtant, puisque cette mission est peu maîtrisée
(cf. analyse première page de l'enquête), une
sensibilisation des utilisateurs à une maintenance de
premier niveau peut s'avérer utile
Retour sommaire
- Evaluez vous la satisfaction des utilisateurs par
rapport au service biomédical ? : Les utilisateurs
étant les clients principaux des services
biomédicaux, ils sont aptes à évaluer leur
travail et par conséquent, leur opinion et leur
satisfaction sont importantes. Pourtant, seulement 31 %
réalisent cette enquête auprès des services
cliniques et médico-techniques, malgré
l'importance qui lui est donnée (75 %).
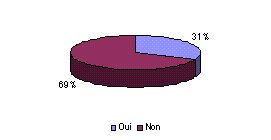
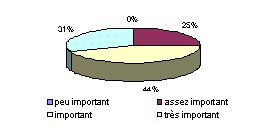
- Quelle importance y
accordez-vous ? : Cette analyse confirme l'importance de
réaliser ce type d'enquête et montre
l'intérêt que cela peut susciter pour les
services biomédicaux.
3.3. Conclusion de
l'enquête
Le bilan de cette enquête est très positif. En effet,
en plus du taux de participation relativement correct, les
résultats nous ont permis de mettre en évidence
certaines missions considérées comme importantes mais
malheureusement mal maîtrisées.
Lors de l'élaboration des réflexions sur des Bonnes
Pratiques de l'Ingénierie Biomédicale, il conviendra de
fournir les éléments et informations nécessaires
aux services biomédicaux pour améliorer la
réalisation de ces missions.
En outre, cet état de l'art nous a permis d'aborder toutes
les pratiques des services biomédicaux et leur analyse a
constitué une base solide et un apport de connaissance
indispensable pour poursuivre notre projet.
Retour sommaire
II.
Réflexions sur des Bonnes Pratiques de l'Ingénierie
Biomédicale
1°)
Critères relatifs aux clients
1.1. Identification
des clients : Pour déterminer qui sont les principaux
clients, il est bon de connaître l'organisation de
l'établissement de soins. Dans un contexte interne, le service
biomédical se situe dans une relation de type «
fournisseur ñ client ». Il fournit une prestation de
service à deux types de clients qui sont les services
cliniques et médico-techniques d'une part, et les services
économiques d'autre part.Il est tout de même bon de
retenir que le client final du service biomédical est le
patient. Il est donc indispensable de tenir compte de ses besoins
interprétés et traduits par les clients
intermédiaires.
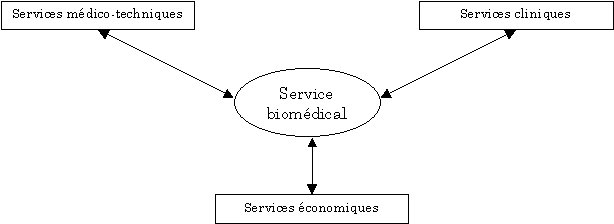
Fig. B : Les clients du service
biomédical
Retour sommaire
1.2. Besoins et droits des
clients : Les services cliniques et médico-techniques
d'une part, et le service économique d'autre part, n'ont pas
la même vocation. Les premiers sont orientés directement
vers les soins délivrés aux patients tandis que le
second est orienté vers la gestion du patrimoine. De part leur
mission, ils n'auront pas les mêmes besoins.
- Le principal besoin des services cliniques et
médico-techniques est la disponibilité des
dispositifs médicaux. La maintenance au sens large du terme
permet d'assurer cette disponibilité.Voici donc les besoins
principaux de ces services :
- - Disponibilité des dispositifs médicaux
- Sûreté de fonctionnement des dispositifs
médicaux
- Formation de l'utilisateur
- Sécurité des utilisateurs
- Sécurité du patient
- La matière première du service économique
est une donnée financière. Elle est exprimée
en coût. Le service biomédical a pour mission, non
seulement d'optimiser au maximum les coûts (investissement
ou fonctionnement), mais également de fournir les
éléments essentiels à la continuité de
la prestation de service en facilitant l'accès aux
données désirées. Voici donc les besoins
principaux de ces services :
- - Coût de fonctionnement
- Coût d'achat
- Coût de maintenance
- Avis technique
Le service biomédical, comme tout autre service, n'existe
qu'à travers les besoins de ses clients. Par
conséquent, il doit leur apporter la satisfaction et surtout
la confiance. La figure qui suit permet d'approfondir cette
définition :
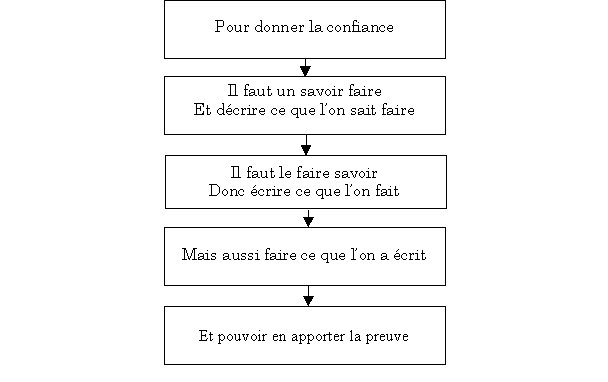
Fig. C : Comment apporter la confiance aux
clients
Ce schéma est d'ailleurs bouclé puisque si l'on
apporte la preuve de la réalisation d'une activité
selon des dispositions préétablies, on tend
effectivement à donner confiance, ce qui constitue l'objectif
principal du service biomédical.
Retour sommaire
1.3.
Evaluation de la satisfaction des clients : L'objectif du
service biomédical est donc de satisfaire ses clients en
apportant une solution concrète à leur demande. De ce
fait, seul le client peut juger du travail fourni par le service
biomédical. Connaître son sentiment sur les pratiques
permet d'apprécier réellement la qualité du
service rendu et d'en tirer de réels atouts pour
l'amélioration et la valorisation de la fonction à
partir des dysfonctionnements décelés. Par ailleurs, la
volonté de prendre en compte l'avis de ses clients,
mécontentements ou souhaits, établit
indéniablement une relation de confiance. L'évaluation
de la satisfaction des clients peut être réalisée
à partir d'une enquête.
1.3.1. Méthodologie d'élaboration d'une
enquête : L'élaboration d'une enquête
pertinente doit être le fruit d'une réflexion afin de
ne pas recueillir des informations inappropriées ou
inutiles aboutissant à une mauvaise analyse et
interprétation. A cet effet, il convient de respecter une
méthodologie. La littérature en propose de
nombreuses, cependant, le principe de base reste toujours le
même.
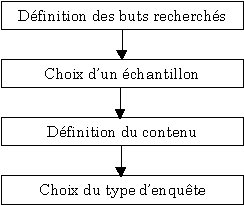
Fig. D : Les différentes étapes pour
élaborer une enquête
- Définition des buts recherchés : Il est
indispensable de s'interroger sur les objectifs à
atteindre. Cela permettra à la fois de s'assurer de la
pertinence de chaque question mais aussi de structurer leur
enchaînement.
- Choix d'un échantillon
: Un questionnaire ne peut cibler qu'un type de client.
Dans le contexte biomédical, les clients sont les services
cliniques et le service économique (cf. partie 2 -
§ 1.1.).
Le choix du client doit être associé aux buts
recherchés. Ensuite, il est important de déterminer
la ou les personnes, parmi la catégorie de clients, qui
sera sondée. En effet, le service biomédical dispose
de plusieurs interlocuteurs au sein d'un même service
clinique.
- Définition du contenu : Le contenu du
questionnaire doit traduire l'objectif de la recherche, en
d'autres termes, la question posée en fonction du but
donné, doit susciter une réponse en relation avec le
but poursuivi et traduisant fidèlement l'attitude de
l'enquêté.
L'objectif de l'enquête étant fixé, il suffit
de préciser les thèmes à aborder.
Les questions doivent être simples pour éviter
l'incompréhension et au contraire susciter les
réponses vraies. Il faut distinguer les questions
fermées (à choix unique ou à choix multiple)
des questions ouvertes (numériques ou non
numériques).
La technique dite de l'entonnoir, c'est à dire une
enquête commençant par des questions
générales et simples pour aborder progressivement
des questions de plus en plus précises, doit être
appliquée.
Retour
sommaire
- Choix du type de l'enquête: L'enquête peut
être à administration :
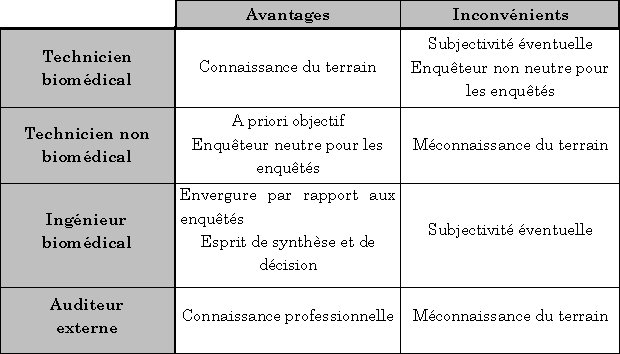
Fig. E : Choix de l'enquêteur pour l'enquête de
satisfaction client
Retour sommaire
1.3.2. Règles d'interprétation des
résultats d'une enquête : Il n'existe pas de
méthodologie « type » permettant
l'interprétation des résultats d'une enquête,
cependant quelques règles doivent être
respectées afin de mener, au plus juste, ce travail :
- · Analyser les réponses par type de
questions.
- · Prioriser les remarques manuscrites : mettre en
évidence les points négatifs.
- · Outre le cliché initial donné par
l'enquête, l'évaluation portera surtout sur
l'évolution de la satisfaction des clients. Il serait
donc plus intéressant, pour une démarche plus
pertinente, de cibler les enquêtés sur les points
ayant posé problème.
- · Avant de conclure sur une enquête,
vérifier que :
- l'enquête a été
scrupuleusement réalisée
- qu'elle apporte bien une
réponse à la problématique de
départ
- les résultats sont
fiables
- leur analyse a été
méthodiquement effectuée
- les destinataires des conclusions
sont identifiés
- le contenu des conclusions
correspond à son destinataire
- · Cibler les axes prioritaires d'action, apporter dans
un premier temps une réponse aux insatisfactions les
plus flagrantes.
- · Informer les clients des résultats.
Retour sommaire
2°)
Critères relatifs à l'organisation
2.1. Gestion
des ressources humaines
2.1.1. Objectifs : Le service
biomédical doit disposer d'un personnel qualifié et
compétent, en nombre suffisant, pour couvrir tous les
domaines de sa responsabilité. Il existe donc des besoins
en personnel et il appartient au service biomédical d'y
répondre.
2.1.2. Cycle de vie du personnel
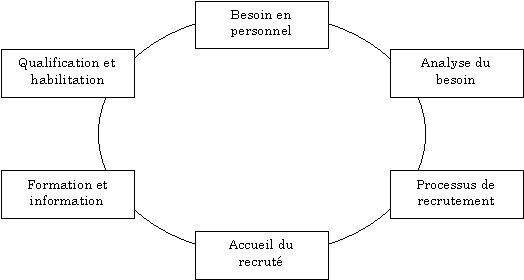
Retour sommaire
2.1.3. Description
a) Analyse du besoin : Lorsqu'il
existe un besoin en personnel, le service biomédical
réalise une analyse afin de cibler un profil de
recrutement. Ce profil répond à des
critères prédéfinis qui sont
généralement :
- nature du poste à
pourvoir
- expériences professionnelles
requises
- connaissances requises
- niveau d'études requis
- salaire maximum
Ces critères sont précisés pour chaque
fonction. Par conséquent, le service biomédical
possède des fiches de fonction définissant les
tâches spécifiques des membres du personnel. Des
fiches de poste définissent chaque poste de travail.
b) Processus de recrutement :
L'analyse du besoin terminée, le processus de
recrutement peut alors commencer. Le processus de recrutement
étant propre à chaque établissement de
soins, le service biomédical établit ses
procédures de recrutement pour chaque fonction.
c) Accueil du recruté : Une
première présentation du service et de l'ensemble
des employés est réalisée pour le
personnel nouvellement recruté. Mais le recruté
ne doit pas être considéré comme accueilli
dès lors qu'il a franchi le seuil du service
biomédical mais, lorsque les deux étapes qui
suivent sont terminées.
d) Formation et information : Chaque
nouvel employé bénéficie d'un programme de
préformation. Le service biomédical forme et
informe tout nouvel arrivant sur ce qu'il est susceptible de
devoir mettre en úuvre dans le cours normal de son
activité.
Chacun des membres du personnel bénéficie d'une
formation initiale et continue adaptée aux tâches
qui lui seront confiées.
e) Qualification et habilitation : Les
responsabilités individuelles sont comprises par chaque
membre du personnel et définies par écrit. Le
service biomédical met à jour des enregistrements
concernant les qualifications, la formation et les
expériences appropriées du personnel
technique.
2.1.4. Evaluation et amélioration : La
compétence réelle de tous les membres du service
biomédical est passée en revue et archivée
à fréquence régulière.
L'évaluation des compétences permet de
définir les besoins en formation. Un plan de formation est
donc établi et il dépendra des besoins mais aussi
des ressources. Toute fonction peut être
déléguée à d'autres personnes
désignées et possédant des qualifications
adéquates. Il ne doit y avoir aucune lacune ni de double
emploi inexpliqué. Les indicateurs utiles pour le service
biomédical peuvent être, à titre d'exemple
:
- taux de formation du personnel
- taux d'absentéisme
- part du budget du personnel
Retour sommaire
2.2. Gestion de
l'environnement
2.2.1. Objectifs : La qualité des
conditions de travail nécessaires doit être garantie
et doit permettre de faciliter l'exécution
appropriée des activités du service
biomédical.
2.2.2. Description : Les locaux sont
situés, conçus, construits, adaptés et
entretenus de façon à convenir aux
différentes activités du service
biomédical.
Une réelle attention est portée quant aux
contaminations biologiques, aux poussières, aux
interférences électromagnétiques, à
l'humidité relative qui pourraient interagir lors des
contrôles, maintenances et étalonnages. Une
séparation pertinente est prévue entre des zones
voisines ne présentant pas des activités compatibles
entres elles. L'entretien et la maintenance des locaux et des
matériels sont assurés selon des procédures
écrites et détaillées.
2.2.3. Evaluation et amélioration : Des
revues régulières des locaux et de l'environnement
sont exécutées, documentées et
répertoriées.
Retour sommaire
2.3. Gestion
des dispositifs médicaux
2.3.1. Objectifs : Le service
biomédical doit mettre à disposition des dispositifs
médicaux en nombre suffisant et doit les maintenir en
parfait état de fonctionnement. Par conséquent, il
se doit de répondre aux différentes étapes du
cycle de vie des dispositifs médicaux.
2.3.2. Cycle de vie des dispositifs
médicaux
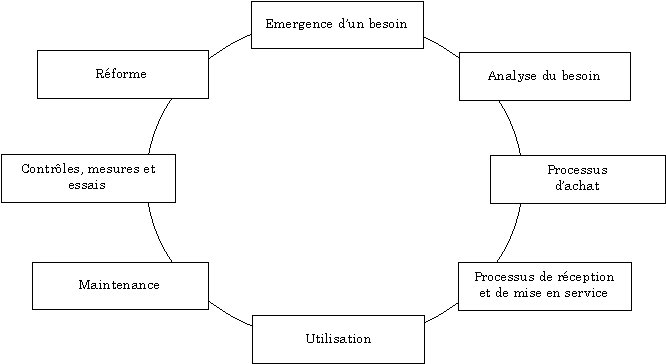
Retour sommaire
a) Analyse du besoin
- Objectifs : L'analyse des besoins est une phase
importante de la procédure d'achat car elle va
influencer les achats liés à ce dispositif,
tout au long de son utilisation. Dans ce cadre, les besoins
des services cliniques ou médico-techniques doivent
faire l'objet d'une attention particulière. Cette
procédure doit permettre de formaliser les besoins et
de les traiter avant que la procédure d'achat ne soit
véritablement lancée.
- Description : Cette phase est essentielle, elle
doit être menée de concert entre les «
médicaux » et les « administratifs »
(administration et service biomédical). Des
informations sont fournies par le service clinique ou
médico-technique afin d'argumenter les besoins.
Chaque demande d'investissement s'inscrit dans une
cohérence avec le projet médical, le projet
d'établissement et l'activité médicale
du service. La préparation du plan d'investissement
passe nécessairement par plusieurs étapes qui
s'intègrent dans le processus global de la gestion du
parc biomédical. Le programme d'équipement est
une démarche qui permet une projection de
l'investissement de l'hôpital. Etant donné le
volume de dépenses que représente l'achat de
dispositifs médicaux, il permet d'établir des
prévisions dans la gestion du budget.
- Evaluation et amélioration : Il est mis en
place une évaluation des renouvellements par la
réalisation d'un échéancier
théorique de renouvellement sur une période de
référence. La prise en compte des
évolutions de l'offre du marché et de
l'environnement réglementaire nécessite de
mettre en place un dispositif de veille technique et
réglementaire continu. Cette veille
déclenchera le remplacement ou la modification de
l'existant.
Retour
sommaire
b) Processus d'achat
- Objectifs : Une fois le besoin défini, le
service biomédical doit s'assurer que ce qu'il
achète puisse permettre à ses clients
d'assurer la qualité des soins au niveau du patient
en toute sécurité et avec le maximum de
performances pour les dispositifs médicaux.
- Description : En matière d'acquisition de
matériels biomédicaux, les responsables et
partenaires sont tenus de bien gérer tout un ensemble
de procédures générant des
délais de réalisation. En tant que partie d'un
établissement public, le service biomédical
entreprend ses marchés suivant le Code des
Marchés Publics (C.M.P.). Il convient donc d'adapter
la procédure en fonction des volumes financiers
estimés :
· Inférieurs à
300 KF : marché sur simple facture
· Entre 300 KF et 700 KF :
marché négocié
· Supérieurs à
700 KF : marché sur appel d'offres (A.O.)
A ceci il faut ajouter des obligations de formes
(diffusion, délai...) pour chaque catégorie.
Le marché négocié et l'A.O. ouvert
demandent de suivre une procédure clairement
définie par le C.M.P. Elle se compose de plusieurs
phases :
· Réalisation du cahier des charges
:
- Le C.C.A.P. : Cahier des Clauses
Administratives Particulières
- Le C.C.T.P. : Cahier des Clauses Techniques
Particulières
· Diffusion :
- Montant inférieur à
900 KF : parution soit au Journal d'Annonces Locales
(J.A.L.), soit au Bulletin Officiel d'Annonces des
Marchés Publics (B.O.A.M.P.), avec un
délai de réponse d'au moins 15
jours.
- Montant entre 900 KF et 1,3 MF : parution au
B.O.A.M.P. et un délai minimum de 36 jours est
accordé aux intéressés.
- Montant supérieur à 1,3 MF : parution
au Journal Officiel de la Communauté
Européenne (J.O.C.E.) et les offreurs ont un
délai d'au moins 52 jours.
Le choix du dispositif médical est fonction de
plusieurs critères dont l'importance peut varier d'un
établissement à un autre. Néanmoins,
l'ordre des critères qui suivent respecte une
certaine hiérarchie :
- Conformité aux normes en
vigueur
- Adaptation aux besoins réels des
utilisateurs
- Convivialité et simplicité
d'utilisation
- Technologie du matériel
- Fiabilité, réputation de
l'entreprise
- Caractéristiques du S.A.V.,
réputation, fiabilité
- Evolutivité du matériel
- Prix de l'investissement
- Coût de l'exploitation
- Coût de la maintenance
- Solidité financière de l'entreprise
- Evaluation et amélioration : Les
différents partenaires du service biomédical
doivent obtenir la meilleure corrélation entre les
performances techniques, cliniques ainsi que l'approche
économique et financière aboutissant à
différents choix.
Par conséquent, l'évaluation de la
satisfaction des clients reste le principal indicateur pour
ce processus (cf. partie 2 - § 1.3).
Retour
sommaire
c) Processus de réception et de mise en
service
d) Utilisation
- Objectifs : La compétence du personnel
médical doit être suffisante pour assurer une
utilisation sûre des dispositifs médicaux.
- Description : Le service biomédical
planifie les formations dans ce domaine. Il développe
et offre des programmes de formation pour des technologies
existantes et nouvelles. La formation peut être
exécutée par le service biomédical
lui-même ou par des sous-traitants (fournisseurs,
organismes de formation), à la demande du service
clinique ou après constat d'une mauvaise utilisation
du matériel.
- Evaluation et amélioration : Le service
biomédical évalue le nombre de pannes par
service dues à une mauvaise utilisation. Ces
résultats seront discutés avec le service
concerné, sans citer nominativement une personne.
Retour
sommaire
e) Maintenance
- Maintenance préventive
- Objectifs : Les visites et interventions de
maintenance préventive ont pour but de
réduire les risques de panne et de maintenir dans
le temps les performances des dispositifs médicaux
à un niveau proche de celui des performances
initiales, en vue d'assurer une utilisation
satisfaisante. Elles doivent donc permettre :
· une maîtrise des
dispositifs médicaux en bon état de
fonctionnement
· une amélioration
de leur disponibilité
· une amélioration
de leur sécurité
· une amélioration
de leur fiabilité
· une mise en
conformité avec la réglementation en
vigueur
- Description : Durant le procédé
de fourniture, le mode d'entretien ainsi que le plan
documenté sont évalués et
décidés pour chaque dispositif
médical spécifique. L'utilisateur est
impliqué dans le processus de décision
ainsi que dans le programme d'utilisation et d'entretien.
Celui-ci est formé à la maintenance de
premier niveau, il doit prendre connaissance des manuels
d'utilisation des fournisseurs. L'entretien
préventif implique l'inspection et le remplacement
des pièces de rechange critiques et le
contrôle à partir de plusieurs
paramètres comme :
· les recommandations
constructeurs
· le temps
opérationnel
· le temps
chronologique
· les besoins cliniques
· les ressources
accessibles
L'entretien préventif peut être
entièrement, ou en partie, réalisé
par le service biomédical, ou bien être
réalisé de façon partielle ou totale
par un service externe au service biomédical. Il
peut donc être réalisé par des
équipes techniques du constructeur ou d'une
entreprise de tierce maintenance.
Les contrats de maintenance couvrent la détection
et la correction des pannes.
Les personnes qualifiées exécutent
l'entretien préventif basé sur un
procédé documenté distribuant les
différentes responsabilités.
Toute intervention de maintenance préventive
fait l'objet d'une fiche d'intervention.
Les écarts rencontrés pendant l'entretien
préventif sont répertoriés.
Les dispositifs médicaux sont
étiquetés de façon à informer
l'utilisateur sur un prochain entretien
préventif.
- Evaluation et amélioration : Le service
biomédical met en place plusieurs indicateurs
comme, par exemple :
· taux de maintenance
préventive
· part du budget de
maintenance préventive
· nombre de dispositifs
médicaux suivis en maintenance préventive
planifiée
· respect du plan de
maintenance
A partir de ces indicateurs, des fiches
d'interventions et des documentations, le service
biomédical modifie le planning d'entretien des
dispositifs médicaux et obtient une meilleure
rentabilité de la maintenance
préventive.
Retour sommaire
- Maintenance corrective
- Pièces de rechange des dispositifs
médicaux
- Objectifs : Le service biomédical doit
posséder une politique adéquate concernant
les pièces de rechange afin de diminuer le temps
d'immobilisation du dispositif médical.
- Description : Le service biomédical
définit et documente une politique
d'approvisionnement, un fournisseur de pièces de
rechange devra répondre aux critères
qualité de base, définis par le service
biomédical. En projetant un système pour la
gestion des stocks, les besoins critiques du service
clinique sont satisfaits sans coût excessif. Le
service biomédical définit et met à
jour des procédures documentées pour
s'assurer que les pièces de rechange
achetées répondent aux exigences
définies. Les pièces de rechange sont
étiquetées et rangées de telle
manière que leur qualité n'en soit pas
affectée.
- Evaluation et amélioration : Des
examens périodiques, par exemple, du temps
d'entreposage des pièces de rechange, sont
réalisés et peuvent avoir comme
conséquence la modification de la politique
d'achat pour les pièces de rechange
concernées.
Le service biomédical évalue
également la part du budget de pièces
détachées.
Retour
sommaire
- Transport des dispositifs médicaux
- Objectifs : Le but est de s'assurer que le
temps de transport est le plus court possible, sans
ajouter de dommage au dispositif médical.
- Description : Le service biomédical
nomme un employé qui est responsable de la
réception des dispositifs médicaux entrants
et sortants.
Les méthodes de transport d'un dispositif
médical entre le service clinique et le service
biomédical sont documentées. En arrivant au
service biomédical, le dispositif est
enregistré sur le registre. Après
l'entretien ou la réparation, le dispositif est
transporté à nouveau au service avec une
fiche décrivant le problème survenu et une
déclaration, où il est notifié que
le dispositif médical a été
testé et qu'il est sûr d'utilisation.
- Evaluation et amélioration : Les
méthodes de transport sont évaluées
et ajustées périodiquement à partir
d'une auto-évaluation du service biomédical
mais également à partir des
déclarations de panne et des plaintes des
utilisateurs.
- Sous-traitance de l'entretien
- Objectifs : Le service biomédical doit
s'assurer que seulement des sous-traitants
compétents, fiables réalisent des actions
sur des dispositifs médicaux.
- Description : Le service biomédical
enregistre les informations concernant la
compétence et la conformité aux normes de
ses sous-traitants. Il s'assure que les services
sous-traités sont réalisés
conformément à la commande ou au
contrat.
Lorsque la direction l'y oblige, le service
biomédical l'informe de l'intention de
sous-traiter l'entretien.
- Evaluation et amélioration : Le
registre des sous-traitants est passé en revue
périodiquement pour apporter les modifications
nécessaires. Le service biomédical
évalue la part du budget de sous-traitance et le
taux de sous-traitance.
f) Contrôles, mesures et essais
- Objectifs : Les moyens dont dispose le service
biomédical doivent permettre d'assurer, sur les
dispositifs médicaux de l'établissement, les
contrôles et essais nécessaires avant leur
remise en service.
- Description
- Tests de contrôle : Le service
biomédical possède tous les
éléments pour l'exécution correcte
des contrôles des dispositifs médicaux, dans
le cas contraire, il fait appel à la
sous-traitance. Si les tests sont effectués en
interne, le service biomédical documente
l'utilisation de l'ensemble de ses appareils de
contrôle. Ces appareils sont identifiés par
une date d'expiration de l'étalonnage.
Les résultats des tests sont documentés et
analysés.
- Etalonnage : Afin que les dispositifs
médicaux soient contrôlés
correctement, les équipements de mesure
utilisés sont inclus dans un programme
d'étalonnage. Le service biomédical utilise
des méthodes et des procédures
appropriées pour tous les étalonnages des
équipements de contrôle. Les méthodes
sont conformes à l'exactitude exigée et aux
différentes normes applicables. Les
résultats des étalonnages et des mesures
sont documentés de telle façon que la
traçabilité nécessaire soit
obtenue.
- Evaluation et amélioration : Les
procédures d'étalonnage des dispositifs
médicaux sont revues périodiquement. Dans le
cas où l'étalonnage n'a pas été
réalisé et où le dispositif
médical concerné ne peut plus être
étalonné, le dispositif est
étiqueté comme non conforme et n'est pas
utilisé pour des mesures essentielles.
Retour
sommaire
g) Réforme : Le service
biomédical établit des procédures
écrites concernant le processus de réforme. Le
renouvellement des équipements biomédicaux passe
par la définition de critères qui permettent
d'évaluer le niveau d'obsolescence et, le cas
échéant, de réformer le
matériel.
Les critères utilisés
régulièrement sont :
· somme de la maintenance
depuis l'achat > coût d'achat
· valeur nominale <
coût d'une intervention
· évaluation
scientifique : technologie obsolète
· évaluation
réglementaire et normative : non-conformité
Ce point sera approfondi dans le chapitre 3.2., Gestion
des risques-Matériovigilance.
Retour sommaire
3°)
Critères relatifs à la qualité et à la
prévention
3.1. Gestion de la
qualité
3.1.1. Principe
a) Politique qualité : La
politique qualité comprend des objectifs pertinents et
mobilisateurs avec l'engagement de tous les décideurs
concernés. Elle intègre les objectifs
généraux de l'établissement. La prestation
de soins, incluant un diagnostic et un traitement, est
l'activité dominante des établissements. La
gestion correcte des interfaces entre les unités de
soins et les autres services est un des objectifs de la mise en
place du système qualité. Le service
biomédical a une incidence importante sur la
qualité des soins apportés aux patients. Le
conseil d'administration ou l'organe qualifié de
l'établissement définit la politique
qualité de l'établissement. La direction s'assure
que celle-ci est connue, comprise et mise en oeuvre à
tous les niveaux.
La politique qualité permet de définir :
· le niveau de service à
fournir
· les objectifs
qualité
· la façon de
procéder pour atteindre les objectifs qualité
· le rôle du personnel dans
la mise en oeuvre de la politique qualité
b) Système qualité : Le service
biomédical s'intègre dans le système
qualité de l'établissement. Si ce système
n'existe pas à l'échelle de
l'établissement, l'ingénieur biomédical
chargé de la gérance du service biomédical
le met en place à l'échelle de son service dans
la limite des moyens qui lui sont attribués. Il s'appuie
sur un personnel qualifié afin de garantir que le
produit, le service rendu, l'activité et la prestation
sont conformes aux exigences spécifiées en
rapport avec les objectifs et obligations du service
biomédical et de l'établissement.
Le système qualité est l'ensemble
constitué par l'organisation, les processus, les
procédures et les moyens nécessaires pour la mise
en oeuvre de la gestion de la qualité. La
nécessité de s'organiser et de maîtriser
les moyens mis à disposition implique que des directives
claires et des informations précises soient
écrites et connues. L'étendue et le niveau de
détail des procédures dépendent de la
complexité des tâches, de la compétence et
de la formation du personnel impliqué.
Le système qualité est formalisé sans
excès et permet de maintenir une dynamique
d'amélioration. La mise en place d'un système
qualité permet de diffuser l'information en la rendant
et en la maintenant claire, fiable, accessible, pour que,
à tous les niveaux, les bonnes décisions soient
prises et appliquées.
Un système qualité mis en place est
cohérent avec l'organisation des autres services de
l'établissement qui peuvent avoir une incidence sur les
activités ou les prestations du service
biomédical.
c) Organisation du système
qualité
- Responsabilité : La responsabilité,
l'autorité et les relations entre les personnes qui
dirigent, exécutent et vérifient des
tâches qui ont une incidence sur la qualité
sont définies par écrit.
- Responsable de l'assurance qualité : La
direction de l'établissement désigne un
responsable de l'assurance qualité qui s'assure de la
mise en place et du bon fonctionnement du système
qualité. Le responsable assurance qualité
dispose de l'autorité et des moyens
nécessaires. A défaut d'un système
qualité mis en place à l'échelle de
l'établissement, il appartient à
l'ingénieur biomédical chargé de la
gérance de désigner un responsable assurance
qualité du service biomédical. Il en informe
la direction de l'établissement.
- Moyens : L'organisation du système
qualité repose sur l'identification de tous les
moyens nécessaires à l'exécution et
à la vérification des tâches afin de
fournir des prestations conformes à la
réglementation et aux exigences sur lesquelles
l'établissement s'est engagé. Ces moyens,
constitués par le personnel, les équipements
et les locaux, sont organisés,
maîtrisés, adaptés et évolutifs.
Retour
sommaire
d) Revues du système qualité :
Elles permettent de s'assurer que le système
qualité demeure approprié et efficace, en
particulier par l'analyse des audits qualité, des
actions préventives et correctives mises en oeuvre et
des indicateurs qualité mis en place. Les revues du
système qualité sont effectuées par la
direction de l'établissement ou l'ingénieur
biomédical chargé de la gérance, selon
l'organisation mise en place dans l'établissement avec
une fréquence définie et suffisante. Des
enregistrements de ces revues sont conservés.
e) Maîtrise des documents et des
données : Le système documentaire est un
outil de conservation et de transmission de l'information. Tous
les documents nécessaires et suffisants au
fonctionnement efficace de la structure et du système
qualité, et eux seuls, sont répertoriés et
gérés de manière cohérente selon
des procédures appropriées, ils peuvent exister
sur support papier ou support informatique et sont
maîtrisés. Le système qualité
génère des enregistrements relatifs à la
qualité. Ces enregistrements constituent la preuve que
le système qualité prévu est bien mis en
oeuvre, que les activités ont été
effectuées et les résultats attendus ont
été obtenus. Les informations enregistrées
sont des sources de réflexion pour la mise en oeuvre
éventuelle d'actions préventives ou
correctives.
f) Auto-évaluation :
L'auto-évaluation est un examen
détaillé et périodique des conditions et
procédures de travail en usage en vue de vérifier
leur niveau d'application. Elle est effectuée par le
responsable de la structure évaluée ou par une
équipe appartenant à cette structure.
L'auto-évaluation fait l'objet de compte-rendu
enregistré.
g) Audit interne : L'audit interne est un
examen méthodique et indépendant effectué
en vue de déterminer si les activités et les
résultats obtenus satisfont à la politique
qualité de l'établissement, si les dispositions
adéquates sont mises en úuvre de façon
effective et si elles sont aptes à atteindre les
objectifs définis.
L'audit interne est effectué conformément
à des procédures documentées. Il est
programmé, d'une part, en fonction de la nature et de
l'importance de l'activité et, d'autre part, des
résultats des audits précédents.
L'audit interne est conduit par des personnes
compétentes, n'ayant pas d'implication directe dans les
secteurs à auditer et en coopération avec le
personnel de ces secteurs. Le véritable esprit d'audit
est un esprit de coopération, permettant de mettre
à jour des faits qui échappent à
l'observation courante et de déceler des causes
potentielles d'anomalie.
L'audit interne fait l'objet d'un rapport écrit. Le
responsable de l'activité auditée présente
ses observations, l'auditeur conclut dans un rapport final et
propose des actions correctives.
Retour sommaire
3.1.2. Documentation : Des écrits
clairs, utiles et exploitables dans le temps évitent les
erreurs inhérentes aux communications verbales. La
documentation est un outil de transmission et de conservation de
l'information. Tous les documents nécessaires et suffisants
au fonctionnement efficace du service biomédical et du
système qualité sont gérés de
manière cohérente selon des procédures
appropriées. Les informations qui permettent de suivre un
produit, une prestation ou une opération, d'en assurer la
traçabilité et de participer aux systèmes de
vigilance sont enregistrées. Les documents se
présentent en fonction des textes réglementaires en
vigueur sur tout support approprié.
a) Maîtrise de la documentation :
Une procédure définit tout le système
documentaire. Tout document est :
- créé, référencé,
daté (la date est la date d'approbation, si elle est
différente, la date d'application est
également mentionnée).
- signé par chacune des personnes
compétentes qui l'ont rédigé,
validé et approuvé.
- connu, compris et accessible à chaque personne
qui l'utilise.
- modifié en tant que de besoin par les personnes
compétentes et autorisées, il porte alors une
nouvelle référence et fait l'objet du
même plan de diffusion que le document
précédent qui est systématiquement
retiré et archivé.
- la traçabilité de la diffusion des
documents, essentielle pour le maintien de la
qualité, fait l'objet d'une particulière
attention. La liste des destinataires, l'enregistrement de
la réception ou du rendu du document font partie de
la traçabilité.
b) Différents types de documents : Les
différents types de documents sont
hiérarchisés selon l'organisation ci-dessous
définie.
- Manuel qualité : Le manuel qualité
énonce la politique qualité et décrit
le système qualité. Il peut porter sur la
totalité des activités ou seulement sur une
partie de celles-ci. Le titre et l'objet du manuel indiquent
le champ d'application. Il est mis à jour en fonction
des évolutions du système qualité. Il
comporte au minimum :
- l'exposé de la politique qualité
- l'organigramme, les responsabilités et les
relations entre les personnes qui dirigent, effectuent et
vérifient les travaux qui ont une incidence sur la
qualité
- l'organisation du système qualité mis
en place avec le sommaire des procédures
- Procédures écrites : Une
procédure écrite comporte pour une
activité, l'objet et le domaine d'application. Elle
indique qui fait quoi, quand, où et comment, avec
quel matériel, quel document et comment ce qui est
fait est maîtrisé et enregistré. Sa
réelle mise en oeuvre est démontrée par
des enregistrements adaptés et pertinents. La
procédure est rédigée et
présentée afin de s'adapter à la
complexité des tâches et méthodes
utilisées, ainsi qu'aux compétences et
à la formation du personnel. Elle est à la
fois la mémoire de l'organisation, un outil de
formation et la référence interne sur laquelle
s'appuient les auto-évaluations et les audits.
- Documents opérationnels : Le détail
de l'action à accomplir peut être défini
par un document opérationnel ou un mode
opératoire lorsque la procédure le
nécessite et le prévoit.
- Documents d'enregistrement : Les documents
d'enregistrement permettent de prouver que le produit ou
l'opération est conforme aux exigences
spécifiées.
Retour
sommaire
c) Maîtrise des documents
- Création et modification : La
procédure de maîtrise des documents permet de
s'assurer que lors de leur création, les documents
comportent toutes les mentions définies. Les
documents à modifier suivent la même
procédure. Une liste indiquant les versions en
vigueur des documents est établie.
- Gestion et diffusion : La procédure de
maîtrise des documents indique également :
- les modalités de diffusion des documents afin
qu'ils soient connus, compris et accessibles et que seule
la version en vigueur soit utilisée.
- le nombre de copies diffusées ainsi que leur
localisation, leurs destinataires et leurs
utilisateurs.
- le mode d'identification, de conservation, de
localisation et de classement des originaux.
- le mode de retrait des documents
périmés.
- Archivage : La procédure de maîtrise
des documents concernant le système qualité
décrit :
- les documents à archiver
- le responsable de l'archivage
- la durée de l'archivage
- les modalités pratiques de l'archivage
Retour sommaire
3.2.
Gestion des risques-Matériovigilance
3.2.1. Maîtrise des non
conformités : Lorsque les prestations ou les
produits fabriqués ne sont pas conformes aux exigences, les
procédures de maîtrise de non conformité
s'appliquent. La maîtrise de la non conformité
comporte :
- son identification
- sa documentation
- l'évaluation de ses conséquences
- son traitement par une action corrective
- sa notification aux personnes concernées
La maîtrise de la non conformité comprend, si
nécessaire, la suspension du service ou de la prestation
non conforme ainsi que le retrait et l'isolement du produit non
conforme. Les actions préventives consistent à
éliminer les causes d'une non conformité ou d'un
défaut et de tout autre événement
indésirable potentiel pour éviter qu'ils ne se
produisent. Pour ce faire, toutes les sources d'informations
relatives à la qualité (réglementation,
enregistrements, ...) sont prises en compte.
Les actions correctives visent à empêcher le
renouvellement des non conformités en éliminant
leurs causes. Les actions préventives et correctives
permettent de réduire progressivement ou de limiter les
conséquences organisationnelles, financières et
humaines de la non qualité, elles sont
enregistrées.
3.2.2. Matériovigilance : La
matériovigilance est une des plus récentes des
vigilances sanitaires. Elle était prévue par les
directives européennes relatives à la mise sur le
marché des dispositifs médicaux sur le territoire de
la CEE.
a) Champ de la matériovigilance :
La matériovigilance est une conséquence directe
de l'obligation, pour tous les fournisseurs de dispositifs
médicaux agissant dans la Communauté
Européenne, d'obtenir préalablement à la
mise sur le marché le marquage CE de leurs dispositifs.
La matériovigilance s'applique à tous les
dispositifs médicaux. La définition
précise des dispositifs médicaux est fixée
dans l'article L.665-3 du Code de la Santé Publique (loi
94-43). Concrètement, il s'agit:
- de tous les appareils médicaux, y compris les
appareils d'imagerie et de diagnostic, à l'exception
des appareils d'analyse utilisés dans les
laboratoires.
- de tous les produits consommables à usage unique
délivrés par la pharmacie (tubulures, cordons
capteurs).
- des dispositifs médicaux qui sont conçus
pour être implantés en totalité ou en
partie dans le corps humain ou placés dans un orifice
naturel et qui dépendent pour leur bon fonctionnement
d'une source d'énergie autre que celle du corps
humain.
Il existe des "produits frontières" pour lesquels
l'appellation dispositifs médicaux doit être
appréciée en fonction de l'usage et des risques
associés.
L' objectif de la matériovigilance est de
vérifier que les objectifs de sécurité
visés par le marquage CE sont bien atteints. En cas de
survenue d'un incident, tout doit être fait pour
éviter la récidive. La matériovigilance
s'exerce aussi bien sur un incident avéré, qu'en
cas de découverte potentielle.
Retour sommaire
b) Le signalement des incidents :
c) Qui déclare ? : Toute personne,
utilisateur, fabricant ou tiers, ayant connaissance d'un
accident ou d'un incident mettant en cause un dispositif
médical doit le déclarer. La non
déclaration est passible de 4 ans de prison et 500 000
francs d'amende.
d) Quand déclarer ? : Le décret
96-32 impose une déclaration sans délai pour les
incidents majeurs. Les incidents mineurs, à signalement
facultatif, doivent être déclarés
trimestriellement.
e) A qui déclarer ? : La
déclaration se fait auprès du correspondant local
de la matériovigilance désigné par le
directeur après avis de la commission médicale
d'établissement pour les établissements de
santé publique. Il peut être du personnel
administratif technique, médical ou paramédical.
Il doit faire acte de candidature volontaire après avoir
pris connaissance de la consistance et des obligations de sa
mission. Un ou plusieurs suppléants sont
désignés afin d'assurer une continuité de
la fonction.
f) Organigramme de déclaration
d'incidents
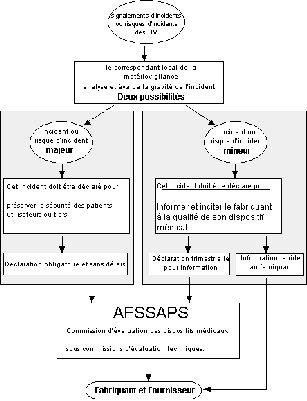
Retour sommaire
CONCLUSION
La réalisation d'un tel projet est très enrichissant
aussi bien professionnellement que personnellement. La prise de
contact avec de nombreux ingénieurs et techniciens
biomédicaux a approfondi nos connaissances sur le
fonctionnement et la gestion des services biomédicaux. De
plus, elle nous a apporté une vision moins théorique
mais beaucoup plus concrète et pratique.
L'objectif principal du projet a été atteint
à l'issue des délais réglementaires. Toutefois,
un tel sujet nécessite de nombreuses discussions, de nombreux
échanges d'informations et le recueil de l'avis de la
communauté biomédicale.
Nous avons donc, comme nouvel objectif, la diffusion du rapport
aux services biomédicaux ayant répondu aux
différentes enquêtes, afin d'obtenir une première
analyse et ainsi, passer du stade de réflexions sur des Bonnes
Pratiques de l'Ingénierie Biomédicale au stade de
principes des Bonnes Pratiques de l'Ingénierie
Biomédicale.
A plus long terme, ce document est amené à
être diffusé à l'ensemble de la communauté
biomédicale pour une validation par les pairs et aboutir, dans
ce cas, à un guide des Bonnes Pratiques de
l'Ingénierie Biomédicale.
L'avenir de ce document dépend donc de vos commentaires,
analyses et critiques. Nous restons à la disposition de toutes
celles ou tous ceux qui souhaiteraient nous transmettre des
renseignements complémentaires.
Ghislaine MANIBAL : gmanibal@yahoo.com
& Christophe RONCALLI :
chrisroncalli@aol.com
Retour sommaire
BIBLIOGRAPHIE
Livres et revues
- · Guide de bonnes pratiques pour la gestion du parc
biomédical, Elaboré par la
société PCS à la demande de la
Direction des Hôpitaux
- · Nordic Guidelines for Good Clinical Engineering
Practice, NORMEDTEK (Nordic Coopérative Group for Medical
Technology) Version 2, November 1998, Complies with ISO 9001
- · Bonnes pratiques de pharmacie hospitalière,
Ministère de l'Emploi et de la Solidarité -
Direction des Hôpitaux, Enquête Publique - Juin
2000
- · Normes ISO 9000 version 2000, Editions AFNOR
- · Assurance qualité dans les laboratoires
d'analyses et d'essais, Gilles REVOIL - 3ème tirage 1999 -
AFNOR
- · Bonnes pratiques de laboratoire (BPL), Fascicule
spécial n° 84/17 bis, Ministère des Affaires
Sociales et de la Solidarité Nationale, Secrétaire
d'Etat chargé de la Santé
- · Table des Références
Réglementaires en fonction des Sujets, A. Jaborska,
Ingénieur Biomédical au CH de DOUAI
Rapports de stage et de
projet
- Création d'un service biomédical au Centre
Hospitalier de Valence, Y. Rochais, Stage DESS "TBH", UTC, 1999,
pp 41
- · Optimisation de la politique de maintenance
biomédicale des Hôpitaux du Mont-Blanc, N. Mocquet,
Stage DESS "TBH", UTC, 1999, pp 69
- · Audit de la maintenance biomédicale :
méthodologie et application, H. Dion, Stage DESS "TBH",
UTC, 2000, pp 47
- · Habilitation des Techniciens Biomédicaux, F.
Kieliger, B. Uguen, Projet SPIBH, UTC, 1997, pp 31
- · Guide méthodologique pour l'avancement de la
qualité, S. Pierrefitte, J. Mescam, Projet DESS "TBH", UTC,
1998, pp 56
- · Qualité et Rentabilité, C. Delagneau, C.
Ladislas, Projet DESS "TBH", UTC, 1997, pp 34
- · L'analyse du chapitre 4.6 de la norme ISO 9002 pour un
Service biomédical dans un Etablissement public de
santé, G. Fernandes, Y.Rochais, DESS "TBH", UV OMQM, UTC,
1998, pp 30
- · Vivre la qualité dans un service
biomédical certifié ISO 9002, M. Gandon, Stage
SPIBH, UTC, 1999-2000, pp 43
- · Appel d'Offres Européen en monitoring et
matériovigilance, C. Maliges, Stage DESS "TBH", UTC,
1999, pp 49
- · Maintenance : Faire ou Faire faire ?, G. Fernandes, D.
Bouvet, Projet DESS "TBH", UTC, 1998, pp 30
- · La Matério-Vigilance : de l'amont à
l'aval, N. Everaerts, A. Jabour, Projet DESS "TBH", UTC, 1997, pp
17
- · Les vigilances, P. Arnault, J-P. Gorre, Projet SPIBH,
UTC, 1999-2000
- · Définition des éléments essentiels
de l'outil GMAO face au contexte réglementaire et à
l'attente des services biomédicaux
, D. Dugor, L. Forcadell, S. Geysens, Projet DESS "TBH", UTC,
1999, pp 90
Retour sommaire
REFERENCES
NORMATIVES ET REGLEMENTAIRES
Relatives à la réalisation des
Réflexions sur des Bonnes Pratiques de l'Ingénierie
Biomédicale
Directives européennes
- · Directive 1999/11/CE de la commission du 8 mars 1999
portant adaptation au progrès technique des principes de
bonnes pratiques de laboratoire visés dans la directive
87/18CEE du Conseil concernant le rapprochement des dispositions
législatives, réglementaires et administratives
relatives à l'application des principes de bonnes pratiques
de laboratoire et au contrôle de leur application pour les
essais sur les substances chimiques.
- · Directive 1999/12/CE de la commission du 8 mars 1999
portant deuxième adaptation au progrès technique de
l'annexe de la directive 88/320/CEE du Conseil concernant
l'inspection et la vérification des bonnes pratiques de
laboratoire (BPL).
Concernant les critères relatifs
à l'organisation
Directives européennes
- · Directive 89/655/CEE du 30 Novembre 1989 concernant les
équipements de travail à risque spécifique
ainsi que les prescriptions minimales de sécurité et
de santé pour l'utilisation par les travailleurs
d'Equipements de travail (formation des travailleurs).
- · Directive 90/385/CE du 20 juillet 1990 relative au
marquage CE.
- · Directive 93/42/CEE du 14 juin 1993 relative aux
dispositifs médicaux (J.O. du 12 juillet 1993).
- · Directive 97/43 du 30 juin 1997 relative à la
protection des personnes contre les rayonnements.
- · Directive 98/79/CEE du 27 octobre 1998 relative aux
dispositifs médicaux de diagnostic in vitro.
Loi : · Loi du 1 juillet 1998 relative à
l'exploitation et au droit de s'assurer du maintien des performances
et la maintenance des dispositifs médicaux.
Retour sommaire
Décrets
- · Décret n°86-1103 du 2 octobre 1986 relatif
à la protection des travailleurs contre les dangers des
rayonnements ionisants (J.O. du 12 octobre 1986).
- · Décret n°88-1056 du 14 novembre 1988
relatif à la sécurité électrique (J.O.
du 24 novembre 1988).
- · Décret n°95-292 du 16 mars 1995 relatif au
marquage C.E.
- · Projet de décret D. 665-5 relatif à la
maintenance, à la sécurité et au
contrôle qualité des dispositifs médicaux
(élaboration de registres).
Arrêtés
- · Arrêté du 20 décembre 1988 fixant
la périodicité, l'objet et l'étendue des
vérifications des installations électriques ainsi
que le contenu des rapports relatifs aux dites
vérifications (J.O. du 30 décembre 1988).
- · Arrêté du 21 décembre 1988 relatif
aux conditions et aux modalités d'agrément des
personnes ou organismes pour la vérification des
installations électriques (J.O. du 1 février
1989).
- · Arrêté du 2 octobre 1990 fixant la
périodicité des contrôles des sources
scellées, des installations des appareils
générateurs électriques de rayonnements
ionisants et de leurs dispositifs de protection (J.O. du 13
octobre 1990).
- · Arrêté du 10 janvier 1992 modifiant
l'arrêté du 20 décembre 1988 fixant la
périodicité, l'objet et l'étendue des
vérifications des installations électriques ainsi
que le contenu des rapports relatifs aux dites
vérifications (J.O. du 17 janvier 1992).
- · Arrêté du 23 décembre 1992
modifiant l'arrêté du 21 décembre 1988 relatif
aux conditions et aux modalités d'agrément des
personnes ou organismes pour la vérification des
installations électriques (J.O. du 3 janvier
1993).
- · Arrêté du 4 juin 1993 complétant
l'arrêté du 5 mars 1993 soumettant certains
équipements de travail à l'obligation de faire
l'objet des vérifications générales
périodiques prévues à l'article R.233-11 du
Code du Travail (J.O. du 15 juin 1993).
- · Arrêté du 2 novembre 1994 applicable
à l'ensemble des laboratoires d'analyses médicales
(structures publiques et privées) depuis le 1 janvier 1995
- GBEA.
- · Arrêté du 3 octobre 1995 relatif aux
modalités d'utilisations et de contrôle des
matériels et dispositifs médicaux assurant les
fonctions et actes cités aux articles D.712-43 et D.712-47
du code de la santé publique (J.O. du 13 octobre
1995) - (maintenance interne / externe).
- · Arrêté du 10 octobre 1997 concernant
l'homologation de divers dispositifs médicaux. (J.O. du 21
décembre 1997).
Lettres circulaires
- · Lettre circulaire n° 971770 du 1er mars 1997 ayant
pour objet la sécurité d'utilisation des dispositifs
médicaux.
- · Lettre circulaire n° 974448 du 2 juin 1997
relative à la sécurité d'utilisation des
dispositifs médicaux.
- · Lettre circulaire n° 976922 du 18 août 1997
ayant pour objet la sécurité d'utilisation de
dispositifs médicaux.
- · Lettre Circulaire n° 987262 du 15 juillet 1998
relative à la Sécurité d'utilisation des
dispositifs médicaux.
- · Lettre-circulaire n°993315 du 19 mars 1999 ayant
pour objet la Sécurité des dispositifs
médicaux.
Normes
- · NF EN 60 601 relatif à la sécurité
électrique.
- · NF EN ISO 9002 relative au modèle d'assurance
qualité en production, installation et prestations
associées (formation du personnel).
- · NF X 60-010 relative à la maintenance, concepts
et définition de la maintenance.
Retour sommaire
Concernant les critères relatifs
à la qualité et à la
prévention
Directives européennes
- Directive 89/391/CEE du 12 Juin 1989 concernant la mise en
oeuvre des mesures visant à promouvoir
l'amélioration de la sécurité et de la
santé des travailleurs au travail.
Lois
- · Loi 94-43 du 18 janvier 1994 relative à la
Santé Publique et à la protection sociale.
- · Loi n°98-535 du 1 juillet 1998 relative au
renforcement de la sécurité sanitaire (J.O. du 2
juillet 1998).
Décrets
- · Décret n°95-292 du 16 mars 1995 relatif aux
dispositifs médicaux.
- · Décret n°96-32 du 15 janvier 1996 relatif
à la matériovigilance exercée sur les
dispositifs médicaux et modifiant le Code de la
Santé Publique (J.O. du 17 janvier 1996).
- · Décret n°99-145 du 4 mars 1999 relatif aux
transferts de compétences en matière de dispositifs
médicaux et modifiant le livre V du Code de la Santé
Publique.
Arrêtés
- · Arrêté du 2 septembre 1996
précisant les modalités de regroupement des
établissement en vue de désigner un correspondant de
matériovigilance commun.
- · Arrêté du 10 février 1997 portant
sur la délimitation du champ de compétences des
sous-commissions techniques de la Commission Nationale de
Matériovigilance.
- · Arrêté du 24 mars 1997 relatif à la
forme et au contenu des signalements d'incidents ou risque
d'incidents dans le cadre de la matériovigilance.
- · Arrêté du 3 juillet 1998 relatif aux
associations distribuant des dispositifs médicaux à
domicile devant désigner un correspondant local de
matériovigilance et au regroupement de ces associations en
vue de désigner un correspondant commun .
Lettres circulaires
- · Lettre circulaire DH/EM1 95-2498 du 10 mai 1995 relatif
à l'organisation de la matériovigilance.
- · Lettre circulaire n° 973573 du 16 mai 1997 ayant
pour objet la mise en place du système national de
matériovigilance.
Normes
- · Norme ISO 9004 relative au Management de la
qualité et éléments de système
qualité.
Retour sommaire