|
Référence à rappeler : |
|
|
|
|
|
Avertissement |
|
Si vous arrivez directement sur cette page, sachez que ce travail est un rapport d'étudiants et doit être pris comme tel. Il peut donc comporter des imperfections ou des imprécisions que le lecteur doit admettre et donc supporter. Il a été réalisé pendant la période de formation et constitue avant-tout un travail de compilation bibliographique, d'initiation et d'analyse sur des thématiques associées aux technologies biomédicales. Nous ne faisons aucun usage commercial et la duplication est libre. Si vous avez des raisons de contester ce droit d'usage, merci de nous en faire part . L'objectif de la présentation sur le Web est de permettre l'accès à l'information et d'augmenter ainsi les échanges professionnels. En cas d'usage du document, n'oubliez pas de le citer comme source bibliographique. Bonne lecture... |
|
Université de Technologie de Compiègne |
|
Référence à rappeler : |
|
|
|
|
|
Résumé La maladie de Legg-Perthes-Calvé est une pathologie infantile touchant la tête du fémur lors de la croissance de la hanche de l’enfant. Elle évolue en quatre stades que l'on peut suivre par différentes modalités d’imagerie. Dans ce rapport sont détaillés les différents aspects de la maladie, les modalités d’imagerie utilisées pour son diagnostic et son pronostic, ainsi qu’un état des lieux des protocoles employés par les chirurgiens, en 2002, dans les quatre centres pédiatriques parisiens (Trousseau, Saint Vincent de Paul, Necker et Robert Debré) pour diagnostiquer et effectuer le suivi d'une ostéochondrite de hanche. Mots clefs : ostéochondrite, hanche, modalités d'imagerie, IRM, protocole, orthopédie, diagnostic, pronostic, radiographie. |
|
Abstract The illness of Legg-Perthes-Calvé is a childish pathology that affects the head of the thighbone during the growth of the child’s hip. It develops in four stages that we can follow it up in different modalities of imagery. In this report are detailed the different aspects of the disease, the imagery’s modalities used for the diagnosis and the prognostic of a hip’s osteochondritis, as well as the protocols employed by the surgeons, in 2002, in the four parisians pediatrics centers (Trousseau, Saint Vincent de Paul, Necker and Robert Debré) for the case of an osteochondritis. Key words : osteochondritis, hip, imagery methods, MRI, protocol, diagnosis, forecast, orthopedics, radiography. |
Remerciements
Nous tenons particulièrement à remercier notre coordinatrice projet, Isabelle Claude, pour sa disponibilité et son suivi efficace ainsi que Renaud Wintzenrieth pour son aide.
Merci également à M. Georges Chevallier et M. Gilbert Farges pour leur attention et les moyens mis à notre disposition.
Nous remercions M. François Langevin pour nous avoir donné accès au Centre d'Imagerie Médicale Avancée.
Nous remercions enfin chaleureusement les chirurgiens qui ont pris de leur temps pour nous répondre :
Pierre Mary, de l'hôpital Trousseau (30/11/02)
Raphaël Seringe, hôpital Saint Vincent de Paul (13/01/03)
Stéphanie Pannier, hôpital Necker (24/01/03)
Keyvan Mazda, hôpital R. Debré (24/01/03)
La maladie de Legg-Perthes-Calvé
II.3.1 - Phase de condensation
II.3.2 - Phase de fragmentation
II.3.3 - Phase de reconstruction ou d'ossification
III.1 - Classification de Caterall
III.2 - Classification de Salter
III.3 - Classification de Herring
III.4 - Classification fondée sur l'IRM
III.5 - Classification de Stulberg
III.6 - Classification de Green (subluxation)
III.7 - Classification de Salles de Gauzy
V.1 - Traitements orthopédiques
V.1.2 - L'immobilisation plâtrée
V.1.3 - Les méthodes déambulatoires
V.2.1 - Chirurgie de varisation
Les modalités d'imageries utilisées
I - La radiologie conventionnelle
I.1 - Définition et principe physique
I.2 - Phases évolutives : signes radiographiques
I.2.1 - Phase de densification de la tête fémorale (durée 6 à 8 mois)
I.2.2 - Phase de fragmentation de l'épiphyse
I.2.3 - Phase de reconstruction
I.3 - Avantages de la radiologie conventionnelle
I.4 - Inconvénients de la radiologie conventionnelle
II.1 - Définition et principe physique
II.2 - Avantages de l’arthrographie
II.3 - Inconvénient de l’arthrographie
II.4 - Images arthrographiques
III.1 - Définition et principe physique
III.4 - Images scintigraphiques de l’ostéochondrite primitive de la hanche
IV - L’imagerie par résonance magnétique
IV.1 - Définition et principes physiques
VI - Synthèse sur les modalités d'imagerie utilisées pour l'ostéochondrite primitive de hanche
Questionnaire utilisé pour les entretiens
I.1.1 - Les différentes modalités
I.1.2 - Statistiques-Traitement
I.2 - Synthèse du protocole suivi en cas d'ostéochondrite
II - Hôpital St Vincent de Paul
II.1.1 - Les différentes modalités
II.1.2 - Traitement - Statistiques
II.2 - Synthèse du protocole suivi en cas d'ostéochondrite
III.1.1 - Les différentes modalités
III.1.2 - Traitement - Statistiques
III.2 - Synthèse du protocole suivi en cas d'ostéochondrite
IV.1.1 - Les différentes modalités
Connue sous le nom de maladie de Legg-Perthes-Calvé (LPC), l'ostéochondrite primitive infantile de hanche est une pathologie quelque peu répandue : on dénombre un cas sur 2000 naissances en Europe (cf. [1], page 16) et un cas sur 5000 sur le continent africain. C'est une maladie à caractère essentiellement masculin : un cas sur 500 naissances en Europe. Cette maladie qui touche la hanche en croissance évolue selon quatre stades bien définis : condensation, fragmentation, reconstruction, évolution séquellaire. Même si on connaît avec précision ces phases évolutives, il n'y a à l'heure actuelle que peu de consensus sur les protocoles de diagnostic et de suivi d'une LPC, même si systématiquement, une modalité d'imagerie médicale vient compléter le bilan clinique
L'objectif de cette étude est de faire l'état des lieux des protocoles actuellement utilisés par les chirurgiens orthopédiques face à une ostéochondrite de hanche ainsi que la place que tient l'IRM dans ces protocoles.
Dans l'optique de la réalisation de ces objectifs, nous avons mis au point un questionnaire-type que nous avons soumis à l'un des chirurgiens orthopédiques de chacun des quatre centres pédiatriques parisiens ( Trousseau, Saint Vincent de Paul, Necker and Robert Debré ) durant un entretien. L'exploitation des résultats des questionnaires nous a permis de mieux connaître la place de l'IRM dans le diagnostic et le pronostic de la maladie de LPC.
Ce rapport est composé d'une première partie où nous détaillerons les différents aspects de la maladie suivi d'un chapitre sur les principes physique et l'intérêt des différentes modalités d'imagerie (radiologie, échographie, arthrographie, scintigraphie, IRM) cloturé par une synthèse sur ces modalités. Suite à ces deux chapitres bibliographiques, nous avons reportés le questionnaire utilisé lors des entretiens suivi des synthèses des protocoles utilisés. Notre travail s'achèvera sur une synthèse générale des entretiens.
Une ostéochondrite infantile primitive de la hanche est définie comme une nécrose de la tête du fémur en période de croissance. Waldenstrom, Legg, Perthes et Calvé dissocient pour la première fois en 1909 l'ostéochondrite de hanche de la tuberculose de hanche, atteinte beaucoup plus grave. Elles étaient jusque là confondues, avant que l'on ne commence à utiliser la radiologie en diagnostic. Dès 1913, les troubles histologiques de l'ostéochondrite sont décrits : ossification ralentie, zones du tissu épiphysaire nécrosées, épaississement du cartilage de l'épiphyse fémorale. Waldenstrom propose en 1922 une première classification (les différentes classifications actuelles sont décrites page 11) basée sur les images radiologiques des hanches de 22 enfants qu'il a suivis jusqu'à la fin de leur croissance. Il distingue ainsi plusieurs formes de gravité selon l'étendue de la nécrose épiphysaire.
Une ostéochondrite de hanche peut être révélée par la pratique sportive et se traduit par des douleurs à l'articulation de la hanche, douleurs souvent projetées au niveau du genou et qui s'estompent par une activité réduite. Legg et Waldenstrom, devant le caractère bénin d'une ostéochondrite primitive à la hanche, préconisent un traitement minimum, c'est à dire symptomatique de la maladie : en respectant une période de repos, la maladie de LPC évoluera toujours vers la guérison.
On semble connaître beaucoup de facettes sur la maladie de LPC, mais il n'existe finalement que peu de consensus parmi les spécialistes tant sur le traitement à appliquer que sur l'origine de la maladie. Voici donc un aperçu des connaissances actuelles touchant à l'origine de la maladie, son évolution, les différentes formes connues, les classifications actuellement utilisées et finalement sur les principaux traitements appliqués.
cf. [1], page 13.
Elle est plurifactorielle. L'origine de la maladie semble être vasculaire : un défaut de vascularisation (infarctus) au niveau de la tête du fémur entraînerait une nécrose de celle-ci; mais aujourd'hui encore cette explication est controversée. Les micro-traumatismes (présents chez les sujets hyper-actifs et sportifs) seraient aussi des facteurs déclenchant l'apparition d'une maladie de LPC. La répartition des sujets atteints selon les continents (cf. paragraphe suivant), très inégale, amène à penser que les conditions de vie et d'alimentation seraient également à prendre en considération dans les causes d'une ostéochondrite chez l'enfant (cf. [2]). Par contre, la recherche de facteurs endocriniens ou génétiques est toujours restée vaine. L'examen biologique est donc tout à fait normal : l'atteinte porte uniquement sur l'os en croissance et n'a pas de caractère infectieux ou inflammatoire.
La maladie de Legg-Perthes-Calvé touche une population précise : 4 cas sur 5 sont des garçons, avec un âge moyen de 7 ans (les extremums sont 2 et 12 ans). La plupart des enfants touchés sont hyperactifs, ce qui corrobore l'hypothèse des micro-traumatismes favorisant l'apparition d'une ostéochondrite. Les atteintes, moins fréquentes chez la fille, y sont très souvent plus sévères. En Europe, cette maladie atteint en moyenne un enfant sur 2000 (cf. [1], p.16) (un garçon sur 500); mais les chiffres sont très variables selon les origines de l'enfant : sur le continent africain, on dénombre un cas sur 5000 naissances. La différence de rapidité de la maturation osseuse serait à l'origine de ces différences de répartition.
Les enfants atteints par la maladie de Legg-Perthes-Calvé sont souvent de petite taille. Ce retard osseux n'a aucune conséquence sur la taille finale et serait même un avantage puisque la tête fémorale possède encore, dans ce cas, un fort potentiel de croissance, et donc une capacité de remodelage importante. Les atteintes survenues avant l'âge de 6 ans sont de fait de meilleur pronostic à long terme.
La maladie évolue en quatre étapes :
Illustration 2 : Phases évolutives de la LPC (d'après [3]).
Nécrose due à un déficit de vascularisation.
Durant cette première phase, le noyau d'ossification présente un défaut de croissance et le cartilage épiphysaire s'épaissit : il en résulte un élargissement de l'espace articulaire (le cotyle, où se loge l'épiphyse). Le noyau se condense, s'aplatit et on observe une fracture sous-chondrale dite en “ coup d'ongle ” (cf. Image p.22). Celle-ci permettrait de déterminer exactement la zone de nécrose (Selon Salter : cf.[1], p.57).
On observe, durant cette phase, un fort contraste entre des zones nécrosées hypodenses et des zones hyperdenses où la revascularisation a débuté. Les zones hyperdenses peuvent correspondre aux lieux de formation du nouvel os.
C'est une phase de cicatrisation qui peut se prolonger sur plusieurs années : l'os réapparaît par plages, le noyau reprend sa place dans le cotyle (il reprend de la hauteur), la tête se reconstruit. Cette phase est déterminante pour un bon remodelage de l'épiphyse : il peut en effet y avoir incongruence de la tête du fémur et du cotyle (cf schéma ci-dessus) si la tête n'est pas idéalement placée dans le cotyle lors de sa reconstruction. Si ça n'est pas le cas, les contraintes asymétriques pourront contribuer dans une certaine mesure à la déformation de la tête fémorale. Une fermeture prématurée de la plaque de croissance lors de la phase de cicatrisation peut aussi jouer dans la déformation de l'épiphyse.
Une guérison complète reste très longue : entre 2 et 4 ans. La partie nécrosée se résorbe d'elle même : elle est progressivement remplacée de la périphérie vers le centre par les tissus osseux sains qui se développent sans problème de vascularisation.
La maladie de LPC, si elle évolue ainsi toujours vers la guérison, n'est jamais sans séquelles au niveau de la tête fémorale : 10% d'entre elles se déformeront progressivement après la période de réossification, 50% resteront stables et 30% s'amélioreront. Les déformations les plus couramment rencontrées sont les suivantes :
Illustration 3 : coxa magna gauche (d'après [3]).
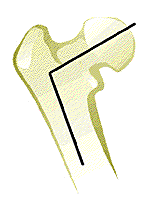
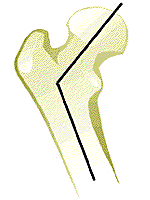
Angle normal (120~135°) coxa vara (angle < 120°) (d'après [11])
Une déformation de la tête du fémur n'est pas la seule séquelle possible : l'arthrose survient chez l'adulte suite à une ostéochondrite de hanche dans 20 à 25% des cas. Plus la déformation est importante et plus le risque d'arthrose est élevé. Les atteintes survenues avant l'âge de 6 ans sont de meilleur pronostic vis à vis de l'arthrose que celles plus tardives.
Ces considérations, associées aux stades de la maladie et aux différentes techniques d'imagerie, ont donné naissance à plusieurs classifications de gravité de la maladie dont voici les principales.
Sources : [1], [4].
Elle est basée sur l'évolution de la nécrose, visible en radio et IRM. Caterall la propose en 1971 à partir de clichés radiologiques.
Stade I : atteinte antérieure exclusive sans collapsus et sans séquestre.
Stade II : atteinte plus étendue avec séquestre ou collapsus mais conservation des secteurs médians et latéraux et conservation de la hauteur du noyau.
Stade III : séquestre central large avec collapsus mais aspect normal du secteur postérieur, secteurs médian et latéral moins atteints.
Stade IV : atteinte totale ou sub-totale avec collapsus et résorption de toute l’épiphyse.
Cette classification pose deux problèmes majeurs :
Si elle est réalisée trop tôt, elle risque de ne plus être valide : 40% des patients changent de catégorie au cours de l'évolution de la maladie.
La reproductibilité est discutable : elle dépend de l'opérateur.
Basée sur la fracture sous-chondrale (coup d'ongle). Proposé par Salter et Thompson en 1984.
Groupe A : trait de fracture sous chondrale inférieur à la moitié de la circonférence de la tête fémorale.
Groupe B : trait supérieur à la moitié.
Plus simple que les précédentes et utilisable plus précocement, elle présente le désavantage de se fonder sur la fracture sous-chondrale qui n'est présente que dans 30% des cas d'ostéochondrite. De plus, elle est aussi dépendante de l'observateur.
Basée sur la division de la tête fémorale. Proposée par Herring en 1991.
La variable est la hauteur du pilier latéral le plus atteint, le pilier étant pris à partir du séquestre central jusqu'au bord de la zone nécrosée.
Groupe A : Le pilier latéral est indemne (15 à 30 % de la surface épiphysaire est nécrosée) : l'évolution est favorable.
Groupe B : Le pilier latéral conserve plus de 50% de sa hauteur. Deux évolutions possibles : si l'enfant à moins de 9 ans, le pronostic est bon, s'il est plus âgé, le pronostic est plus réservé.
Groupe C : moins de 50% de hauteur du pilier est préservé. Le pronostic est significativement plus sévère que dans les deux premier cas et la tête fémorale sera toujours déformée.
Cette classification simple semble être fiable, reproductible et est de ce fait de plus en plus utilisée.
Elle se fonde sur l'étendue de la nécrose, visualisable avec précision à l'IRM.
|
Séquence pondérée en T1 |
Séquence pondérée en T2 |
Prise de contraste (PC) |
Stade de la maladie |
Zone dite : |
|---|---|---|---|---|
|
- |
- |
- |
Nécrose |
A |
|
0 |
+ |
+ |
Régénération |
B |
|
0 |
+ |
- |
Fibrocartilage |
C |
|
+ |
0 |
+ |
Os normal |
D |
(d'après [1], p.51)
+ signifie hypersignal
- signifie hyposignal
0 signifie signal intermédiaire
D'après [1], p.67.
Valable au stade des séquelles.
1 : hanche normale, congruence sphérique
2 : tête sphérique, anomalie du col, coxa magna, angle de Sharp élevé (cotyle adapté aux déformations céphaliques)
3 : tête non sphérique mais non plate, anomalie du col.
4 : tête plate avec anomalie du col.
5 : tête plate sans anomalie du col.
Pronostic :
1 et 2 : bon pronostic, pas de séquelles, congruence sphérique
3 et 4 : risque d’arthrose à partir de 40 ans mais bien tolérée, la réaction du cotyle vient contenir la déformation : congruence asphérique.
5 : rapidement symptomatique : arthrose précoce et douloureuse, incongruence asphérique.
Une subluxation se caractérise par un déplacement partiel des deux extrémités d'un os dans une articulation. La classification de Green pondère négativement la classification de Catterall. Une subluxation de plus de 20% est toujours de mauvais pronostic.
C'est une transposition de la classification de Green à l’IRM. Le rapport entre la largeur de tête (y compris la partie cartilagineuse) couverte par le cotyle et le labrum, et la largeur totale de la tête (os et cartilage) doit être supérieure à 77%. En deçà de cette valeur une ostéotomie de Salter semble à envisager (Chirurgies : cf. p.17).
Elles représentent 1/5 des formes rencontrées et correspondent aux classes suivantes :
I et II Caterall
A Salter
A Herring
L'atteinte de l'épiphyse est dans tous ces cas inférieure à 50%. Le risque
que la tête fémorale se reconstruise en s'excentrant
est inférieur à 10%.
Elles représentent 4/5 des formes rencontrées et correspondent aux classes suivantes :
III et IV Caterall
B Salter
B et C Herring
L'atteinte de l'épiphyse est dans tous ces cas supérieure à 50%. Le risque que la tête fémorale se reconstruise en s'excentrant est supérieur à 80%.
Les atteintes sont bilatérales dans 10% des cas environ (d'après [2]), (les deux côtés sont touchés). Elles sont environ à 80% Caterall III ou IV, c'est à dire sévères. Mais les travaux sont trop peu nombreux pour déboucher sur des statistiques valables. Dans le cas d'une atteinte bilatérale, il y a souvent asymétrie de l'atteinte, avec un décalage dans le temps qui peut atteindre plusieurs années.
Ces classifications sont utilisées comme critère (parmi d'autres) vis à vis du traitement à appliquer, comme expliqué ci-après.
Il existe deux types de traitement : orthopédique et chirurgical. Notons que dans plus de la moitié des cas (57 %), aucun traitement n'est justifié, soit parce qu'il s'agit d'une forme localisée bénigne, soit parce qu'il s'agit d'une forme déjà cicatrisée plus tardivement. 88 % des formes classées I ou II dans la classification de Caterall guérissent sans traitement. Toutefois, les atteintes survenues après 8 ans, même si elles sont II, devront être surveillées du fait qu'à cet âge la potentialité de croissance, et donc de reconstruction, est déjà amoindrie.
Le traitement choisi dans le cas d'une ostéochondrite dépend principalement de (cf. [3]) :
l'âge de l'enfant (potentiel de croissance)
le stade de l'atteinte,
la raideur articulaire,
l'étendue de la nécrose,
le contexte psychologique, social, scolaire et familial de l'enfant.
Ils ont pour visée de diriger la reconstruction de la tête fémorale afin de limiter les déformations séquellaires (Cf § II.3.4 p.10). Ils permettent le centrage de la tête fémorale dans le cotyle afin d'uniformiser les pressions subies par l'épiphyse et de profiter ainsi de l'action remodelante du cotyle pendant la reconstruction. Il s'agit également de décharger la hanche pour éviter la perte de sphéricité de la tête fémorale, ce qui diminuerait la mobilité articulaire. Il existe trois types de traitement orthopédique.
Le décubictus consiste en une simple décharge, c'est à dire en une diminution des pressions exercées par le cotyle sur l'épiphyse. C'est le traitement orthopédique le plus contraignant. Pour permettre une moindre pression, il est en effet nécessaire d'immobiliser totalement la tête fémorale en reconstruction dans le cotyle. On peut à cet effet maintenir l'enfant au repos au lit, avec un corset pour maintenir l'épiphyse dans une position favorable. Cette solution n'est bien évidemment pas des plus évidente pour l'enfant, souvent très actif. Pour améliorer la décharge, on peut aussi utiliser des systèmes de traction qui tirent sur les jambes de l'enfant, ce qui impose bien sûr encore l'immobilisation, mais aussi une surveillance rapprochée de l'enfant en raison d'apparition de problèmes liés à l'immobilisation (enraidissement, stase urinaire, hypertension artérielle). Enfin, on peut associer appareil de décharge et fauteuil roulant, ce qui permet à l'enfant de se déplacer mais cette méthode n'est pas des plus efficaces car l'enfant est tenté de se lever et l'immobilité de la tête fémorale dans le cotyle est toute relative.
C'est la méthode la plus ancienne. Il existe deux types de plâtres, celui pelvi-pédieux, qui immobilise totalement la hanche, et celui bi-cruro-jambier qui laisse une certaine liberté de mouvement à l'enfant.
Le premier plâtre permet le recentrage idéal mais est très contraignant : l'enfant ne peut plus s'asseoir (il ne va donc plus à l'école) et est dépendant pour son hygiène. De plus les contrôles radiographiques à travers le plâtre sont d'interprétation difficile.
Le deuxième plâtre, n'englobant pas la hanche, permet une scolarité normale (si ce n'est les déplacements en fauteuil roulant) et évite le problèmes d'enraidissement car il laisse une certaine liberté de rotation. Le seul désavantage est qu'il autorise un appui dissymétrique sur la hanche et donc une position critique de la tête du fémur dans le cotyle.
Méthodes plus récentes, elles consistent à faire porter à l'enfant des orthèses qui maintiennent (théoriquement) les jambes fixes par rapport à la hanche. Ces appareils ne sont toutefois pas efficaces, l'enfant pouvant se déplacer normalement et même faire du vélo avec l'orthèse. N'étant presque plus utilisées, nous ne détaillerons pas les différentes orthèses qui existent.
Une opération ne se justifie que dans les formes les plus sévères, survenues après l'âge de six ans. L'intervention chirurgicale ne peut survenir après un traitement orthopédique : l'opération doit être précoce, avant le 8ème mois de maladie. La hanche doit toujours être assouplie préalablement par une période de traction d'une durée de trois semaines ou plus.
Le traitement chirurgical d'une ostéochondrite vise à diminuer au maximum les séquelles d'une ostéochondrite. On distingue principalement deux ostéotomies relatives à l'ostéochondrite de hanche : l'ostéotomie de varisation et l'ostéotomie du bassin triple (Salter).
La première chirurgie est une ostéotomie de recentrage de la tête fémorale dans le cotyle qui était indiquée dans les cas où la déformation de la tête fémorale était peu importante et quand la hanche avait tendance à se recentrer. Elle a pour désavantage d'augmenter la coxa vara, surtout pour les atteintes les plus sévères, et est de ce fait maintenant presque complètement supplantée par la deuxième technique chirurgicale.
L'ostéotomie du bassin de Salter n'est indiquée que dans les cas graves (atteinte épiphysaire dépassant 50% : Caterall III ou IV), et vise l'obtention d'une meilleure couverture du cotyle sur la tête fémorale. Elle doit être suivie d'une longue période de décharge et d'immobilisation postopératoire après une période de plâtre la plus courte possible.
Il n'y a à l'heure actuelle aucun consensus thérapeutique pour traiter l'ostéochondrite infantile de la hanche. Voici les pratiques les plus courantes (cf. [4]) :
Jusqu’à 5 ans : Abstention thérapeutique pour les groupes I-II et traitement orthopédique pour le groupe III sans signe de tête à risque (déformation, débord, signes scintigraphiques ou IRM). Dans les autres cas : chirurgie.
De 6 à 9 ans : Traitement orthopédique. La chirurgie est souvent nécessaire dès l’apparition de signes de tête à risques (décelés par radiographie, scintigraphie et IRM).
Après 9 ans : c'est la chirurgie qui prime, elle permettra de minimiser la survenue des séquelles.
La décision thérapeutique pour une ostéochondrite est dépendante d'un diagnostic clinique et d'un diagnostic effectué par une ou plusieurs modalités d'imagerie, que nous allons maintenant détailler.
La radiologie conventionnelle est la modalité d’imagerie qui consiste à envoyer un faisceau homogène de rayon X sur la partie à examiner du patient et de récupérer les rayons verticaux sur un couple détecteur-film tout en éliminant les rayonnements diffusés.
Cette modalité demeure une méthode de choix pour l'examen des os et des articulations. Les appareillages et la technique générale d'examen des os et articulations sont bien connus. Il est toujours judicieux de disposer de films comparatifs, d'étudier l'os et les parties molles, d'utiliser chaque fois que possible le foyer le plus fin pour améliorer la résolution spatiale.
En ce qui concerne l’ostéochondrite de hanche, la radiographie de face et de profil permet de reconnaître la lésion (signes discrets au début puis signes de gravité: excentration et aplatissement de la tête du fémur...), d'en préciser l'étendue et d'apprécier les stades évolutifs (successivement): phase de nécrose du noyau épiphysaire; phase de résorption (fragmentation); phase de reconstruction; phase de remodelage.
Il faut analyser la taille de l'épiphyse par rapport à l'autre coté : elle
est plus petite et plus dense. Les cellules cartilagineuses périphériques
continuant de fonctionner et de fabriquer du matériel cartilagineux entraînent un pseudo élargissement de l'interligne articulaire.
Il faut toujours demander un profil de hanche, c'est sur le profil que
l'on voit mieux les premiers signes radiographiques. L'un des signes les
plus classiques est une image linéaire sous-chondrale, image "en coquille
d'oeuf" (cf. image p.4). Si on a des doutes diagnostiques ou si la radio
n'est pas trop facile à interpréter, on peut demander une scintigraphie au
Technétium marqué en précisant bien que l'on veut
voir la vascularisation de l'épiphyse : le diagnostic
est affirmé sur un trou de fixation.
L' épiphyse va se morceler de façon plus ou moins importante traduisant
la revascularisation de l'épiphyse. Certaines images traduisent un risque
évolutif (écrasement du mur externe, géodes métaphysaires, excentration épiphysaire).
C'est à ce stade que la tête fémorale est la plus fragile. Elle risque de
s'écraser, de devenir plate. C'est donc à ce stade qu'il faut être prudent
sur le plan thérapeutique.
Arthrographie, scanner ou IRM peuvent être nécessaires pour analyser au
mieux la morphologie céphalique avant une éventuelle chirurgie.
La tête va se reformer, plus ou moins arrondie, en fonction des thérapeutiques
qui auront été proposées.
Ces trois stades : densification, fragmentation et reconstruction s'étalent
sur un temps moyen de 2 à 4 ans. L'enfant devra donc être surveillé de façon
extrêmement précise pendant cette période.
La radiographie est :
L’examen dont les techniques sont très bien connues.
L’examen le plus simple et le plus rapide à effectuer.
L’examen qui donne une image non compliquée et donc simple à interpréter.
Une modalité d’imagerie qui permet de comparer les deux hanches à la fois (et de suivre l’ostéochondrite à plusieurs stade).
La radiographie:
Est un examen irradiant puisqu’elle est basé sur les rayons X .
Est négative au stade précoce de la maladie, tandis que d’autres modalités (IRM-scintigraphie) montre l’anomalie.
Donne seulement accès à la visualisation de l'os, elle ne permet pas de visualiser le cartilage.
Illustration 4 : Évolution radiologique de l'ostéochondrite (d'après [3])
Illustration 5 : Signes radiologiques initiaux de l'ostéochondrite (d'après [3])
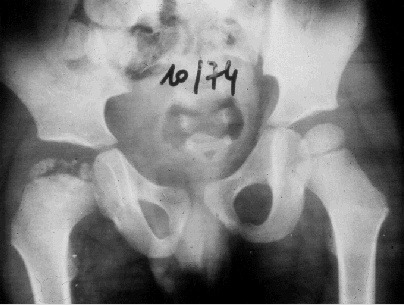
Illustration 6 : Stade très avancée : fragmentation de l'épiphyse droite (d'après [3]).
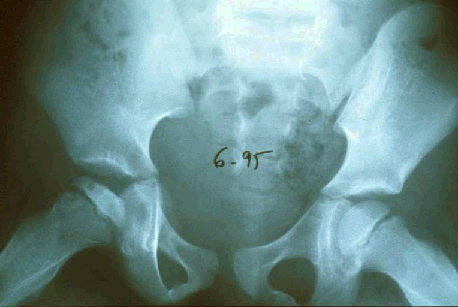
Illustration 7 : Coxa plana à droite.
L'arthrographie est un examen qui consiste à injecter dans l'articulation un produit opaque iodé, puis à prendre des clichés radiographiques (rayons X) qui permettront de visualiser l'intérieur de l'articulation, et d’étudier le contenu. Les articulations les plus fréquemment explorées sont le genou, l'épaule et la hanche.
Cette technique tient une place particulière pour la maladie de LPC. Elle permet une étude de la morphologie de la tête fémorale et une recherche possible de la position idéale de la tête avant chirurgie. Une étude dynamique peut être aussi réalisée, à la recherche d’une subluxation externe de la tête fémorale à la mise en abduction traduisant un effet “came” dont la valeur pronostique est négative.
L'image arthrographique est pertinente dans le cas d'une maladie de LPC mais les médecins aimeraient remplacer cette modalité (par l’IRM si elle disponible) étant donné son irradiation et son invasivité.
L’arthrographie permet :
De visualiser l'intérieur des articulations.
De faire des études dynamiques .
De diagnostiquer l’ostéochondrite à tous les stades.
De comparer les deux hanches à la fois.
L’arthrographie :
Utilise les rayons X et donc elle est irradiante.
Est invasive.
Nécessite une anesthésie générale.
Une fois finie il est conseillé de laisser l’articulation au repos pendant 3-4 heures.
Cause des problèmes pour les sujets allergiques (à cause du produit de contraste).
Illustration 8 : Point de ponction de l'arthrographie de hanche (d'après [9]).
Illustration 9 : image arthrographique d'une hanche saine (d'après [10]).
La scintigraphie est l'obtention de l'image d'un organe après injection au patient d'une solution radioactive (Tec99m en scintigraphie osseuse). On visualise par détection externe la répartition d'atomes radioactifs émetteurs gamma, éventuellement couplés à une molécule spécifique.
Dans notre projet on s'intéresse à la scintigraphie osseuse ou le produit radioactif se fixe de façon privilégiée et importante sur une zone osseuse anormale. Le rayonnement émis par l’os après injection du produit radioactif est enregistré par une caméra spéciale et visualisé sur un écran.
Cet examen, dit de "médecine nucléaire", reste celui du diagnostic précoce de l'ostéochondrite à la hanche. En effet la scintigraphie est perturbée et montre un trou de fixation (hypofixation), alors même que les signes radiologiques sont encore absents. Pour certains auteurs, elle est également un instrument de surveillance de l’évolution et de l’évaluation pronostique en fonction du mode de revascularisation.
La scintigraphie permet :
de visualiser de façon simple des organes non accessibles à la radiologie conventionnelle.
de réaliser des images non seulement morphologiques mais aussi fonctionnelles; seules les zones physiologiquement actives captent la molécule marquée, l'intensité de la captation étant liée à l'activité physiologique ou métabolique à visualiser. Pour la même dose d'irradiation, on peut réaliser plusieurs vues de l'organe sous plusieurs incidences.
de suivre au cours du temps les variations de l'activité détectée dans chacune des régions de l'organe.
De faire des diagnostics précoces de l'ostéochondrite de hanche.
La scintigraphie :
fait partie de la médecine nucléaire, et est donc irradiante (utilisant des noyaux radioactifs), même si l’irradiation est minime.
montre des faux positifs et négatifs en ostéochondrite primitive de la hanche.
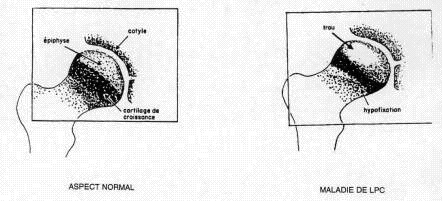
Illustration 10 : Aspect scintigraphique
de l'ostéochondrite (d'après [3]).
Illustration 11 : Scintigraphie : trou de fixation à gauche (d'après [3]).
Illustration 12 : Scintigraphie : trou de fixation à gauche.
Source : [5], [6].
L’imagerie par résonance magnétique (IRM) est une modalité d’exploration universelle et en continuelle évolution.
L’IRM dérive d'une application de la technique d'analyse chimique par résonance magnétique nucléaire (RMN). L'appareil ressemble à un scanner, à la différence près que ce n'est pas un bloc d'irradiation mais de résonance magnétique qui est utilisé. À l'intérieur se trouve un aimant en forme de fer à cheval, qui produit un champ magnétique, et une bobine émettant une onde radio d'une fréquence précise.
Le principe de l'IRM repose sur le fait que certains atomes peuvent entrer en résonance dans certaines conditions: c'est le cas de l'atome d'hydrogène, qui, étant l'un des éléments de la molécule d'eau, est présent en grande quantité dans le corps humain . De plus, la quantité d'eau varie d'un tissu à un autre, mais aussi à l'intérieur d'un même tissu selon son état physiologique
Quand les atomes d'hydrogène entrent en résonance, ils absorbent de l'énergie: plus il y a d'hydrogène, plus il y a absorption d'énergie. À l'arrêt du phénomène de résonance, l'énergie est restituée, puis récupérée sous forme d'informations, qui servent à la synthèse d'une image.
La RMN concerne différents atomes. Nous nous intéressons à l’1H, qui est, ainsi qu'on l'a dit plus haut, l'élément le plus abondant dans l'organisme. Les atomes, possédant un moment angulaire intrinsèque (ou spin) auquel est lié un moment magnétique, peuvent être assimilés à des aimants. Sans perturbation extérieure, ces aimants élémentaires sont orientés dans toutes les directions, de façon aléatoire. Si on applique un champ magnétique B0 constant et homogène (0,02 à 2,0 T), ils s'orientent selon des directions privilégiées. Si on superpose au champ B0 un champ magnétique tournant B1, perpendiculaire à B0 et fourni par une onde radiofréquence, un phénomène de résonance des noyaux de l'échantillon étudié intervient. Lorsque l'excitation par le champ B1 est supprimée, le proton retourne à son état initial en émettant un signal qui permet d'appréhender: la densité des protons, les temps de relaxation spin-réseau (T1) et spin-spin (T2) qui sont caractéristiques de la structure chimique et de la composition du matériau étudié. À un instant déterminé, seuls quelques points bien localisés peuvent entrer en résonance. Les gradients de champ varient au cours du temps afin d'explorer une ligne, un plan ou un volume du patient.
Les aimants utilisés pour créer le champ magnétique B sont des aimants résistifs ou supraconducteurs.
Plusieurs séquences sont appliquées en IRM (pondérées en T1, T2 et ), on se contentera d’ énumérer les séquences des grandes familles sans étudier leurs principes physiques:
La famille Echo de spin (SE) qui donne des images en vrai T2.
La famille écho de gradient (GE) qui donne des images dépendant de T2* (T2*=T2 + inhomogénéités du champ magnétique).
L'association écho de spin et écho de gradient constitue la famille des séquences hybrides (très rapides).
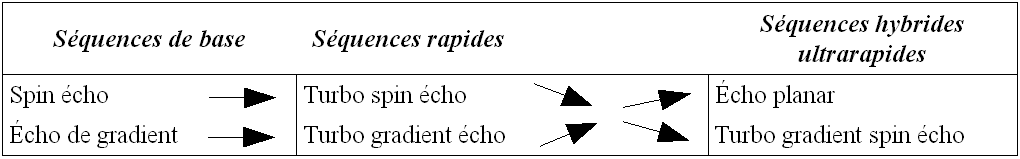
(D'après [12]).
En ce qui concerne l’ostéochondrite de hanche, L’IRM permet de bien visualiser l’étendue de la nécrose et est très utile avant de prendre une éventuelle décision chirurgicale. Elle permet également d'étudier les modifications de la morphologie de la hanche,et donne une excellente visualisation du cartilage articulaire (son épaisseur, la couverture de la tête fémorale). Notons en plus que l’IRM peut suivre la maladie à tous ses stades et donc permet de confirmer le diagnostic au stade précoce et d'établir un pronostic au fur et à mesure de l’avancement de la maladie.
On obtient une excellente appréciation de l’étendue de la nécrose à l’IRM
semi précoce entre le 3 ème et le 6 ème mois. Elle
prend donc là un intérêt prédictif.
Les signes précurseurs sont les suivants :
hyposignal atteignant plus des 2/3 de l’épiphyse.
hyposignal d’oedème réactionnel sur le col fémoral et la métaphyse.
la réapparition d’un hypersignal T1 sur le pilier externe indique qu’il n’y a plus de risque de décentration progressive.
ponts osseux trans physaires indiquant de probables troubles de croissance ultérieurs.
L’IRM n’est ni irradiante ni invasive.
C’est une modalité d’imagerie qui permet de comparer les deux hanches à la fois (et de suivre l’ostéochondrite à plusieurs stade).
Elle fourni des images très riches en informations (étendue de la nécrose, cartilage...).
l'IRM coûte très cher, et ce pour deux raisons:
les travaux d'installation sont onéreux, car il est nécessaire d'isoler la pièce d'examen, le champ magnétique risquant de déplacer n'importe quel objet métallique et les ondes radio pouvant interférer avec d'autres ondes («bip» des alarmes portatives individuelles, sirène des ambulances...).
la seconde raison vient de l'obligation de maintenir l'aimant à une température très basse (- 193 °C, dans de l'azote liquide).
L'IRM n'est donc pas applicable à des personnes qui portent des appareils métalliques (prothèses de valvules cardiaques, pacemaker, etc...).
Vu le nombre d’informations qu’elle contient, l’image de l’IRM est nettement plus dure a interpréter que beaucoup d’autres modalités (arthrographie, radiographie…).
Illustration 14 : Séquence T2. On note une fracture sous-chondrale et une excentration de la tête fémorale gauche. L'épanchement apparaît en blanc entre le cotyle et la tête.(source : hôpital Robert Debré)
Illustration 15 : Séquence dynamique avec injection de gadolinium. La tête gauche se reconstruit. On visualise la vascularisation de la tête gauche en noir. La ligne de démarcation entre le fémur et la tête du fémur n'est pas nette : la revascularisation se fait par le fémur ce qui est de très mauvais pronostic.(source : hôpital Robert Debré).
Le principe physique de l'échographie repose sur l'émission et la réception d'ondes ultrasonores.
Les ultrasons sont imperceptibles à l’oreille humaine. Comme toutes les ondes sonores, les ultrasons sont absorbés ou réfléchis par les substances qu’ils rencontrent. Les liquides par exemple les absorbent tous. Ils peuvent être émis par une sonde en direction d’un objet solide à atteindre. Le temps qu’ils mettent à revenir à la sonde qui les a émis (écho) est fonction de la distance à laquelle se trouve l’objet. Dans l’échographie, la mesure de l’écho est analysée par un ordinateur et restituée en temps réel sur l'écran sous forme de points plus ou moins noirs délimitant les différentes structures. En pratique, la sonde est dirigée et "promenée" sur la région à examiner après avoir appliqué un gel ou une pâte afin de permettre la transmission des ultrasons (faute de quoi ils seraient arrêtés par l’air).
Nous ne détaillerons pas cette modalité comme les précédentes car elle permet seulement de confirmer un épanchement articulaire et de le quantifier; mais cela n'est pas spécifique d'une ostéochondrite.
|
Modalités |
Principe physique |
Avantages (pour l'ostéochondrite) |
Inconvénients ( pour l'ostéochondrite ) |
Dangers |
Coût 1 (€) |
|---|---|---|---|---|---|
|
Radiographie |
Faisceaux de rayons X |
Suivi complet Répandue |
Phase muette |
Rayonnement ionisant |
25 à 300 |
|
Arthrographie |
Faisceaux de rayons X |
Suivi complet Image contrastée |
Phase muette |
Rayonnement ionisant + injection de produits iodés (invasivité) |
50 à 350 |
|
Scintigraphie osseuse |
Injection de solution radioactive : Tc99. Photons γ. |
Précoce |
Faux positifs et négatifs |
Rayonnement ionisant + invasivité |
120 à 320 |
|
Échographie |
Émissions d'ultrasons |
Montre un épanchement |
Pas de spécificité |
Pas de danger |
30 à 137 |
|
IRM |
Résonance magnétique (B0, radio fréquence) |
Nombreuses informations : cartilage, étendue... |
Limite physique de l'appareil (séquence dynamique) |
Champ magnétique intense : pacemaker, clips vasculaires... |
380 à 500 |
1Il s'agit d'un coût moyen, non spécifique à une ostéochondrite. cf. [7].
Ces connaissances sur les modalités et sur la maladie (première partie), ont été la base des entretiens effectués dans les centres pédiatriques de l'APHP, dont voici les compte-rendu.
Questionnaire utilisé pour les entretiens
Quelles sont les infos importantes pour diagnostiquer une ostéochondrite primitive de la hanche?
Quelle(s) modalité(s) d'imagerie utilisez-vous pour un premier diagnostic?
Si l'ostéochondrite est confirmée, utiliseriez-vous d'autres modalités d'imageries pour réaliser un diagnostic plus avancé?
Que pouvez-vous visualiser avec les modalités choisies? Quelles sont leurs lacunes?
Ce type d'examen est t-il adapté à tous les stades de la maladie?
En travaillant au projet, nous avons rencontré plusieurs modalités pour le diagnostic de la maladie : écho, radiologie ordinaire, scanner, IRM, arthrographie, scintigraphie. Si toutes les modalités sont accessibles, laquelle choisiriez-vous au stade précoce de la maladie ? Au stade avancé?
Avez-vous déjà utilisé l'IRM pour l'ostéochondrite?
A- Si oui :
Que permet de visualiser cette méthode, et à quel stade?
Suivez-vous un protocole particulier? Existent ils des séquences spécifiques à l'ostéochondrite de la hanche? Que permet chaque séquence?
Utiliseriez-vous des séquences dynamiques, avec injection de gadolinium?
L'IRM permet de visualiser le cartilage : cela permet-il un diagnostic plus précoce de la maladie?
B- Si non :
Pour quelle(s) raison(s)?
L'IRM permet de visualiser le cartilage : cela permet-il un diagnostic plus précoce de la maladie?
Statistiques
-La modalité choisie influence-t-elle la façon de traiter la maladie? (chirugie ou orthopédie)
-Nb cas/an
BILAN : protocole complet pour une ostéochondrite primitive.
Ce questionnaire a été soumis à quatre chirurgiens orthopédiques appartenant aux quatre centres pédiatriques de l'APHP. Le contenu des entretiens est donc spécifique à chaque chirurgien : ce sont uniquement ses propos qui ont été résumé.
Date : 30 novembre 2002
Lieu : Hôpital Trousseau (12ème)
Chirurgien : Dr. Pierre Mary
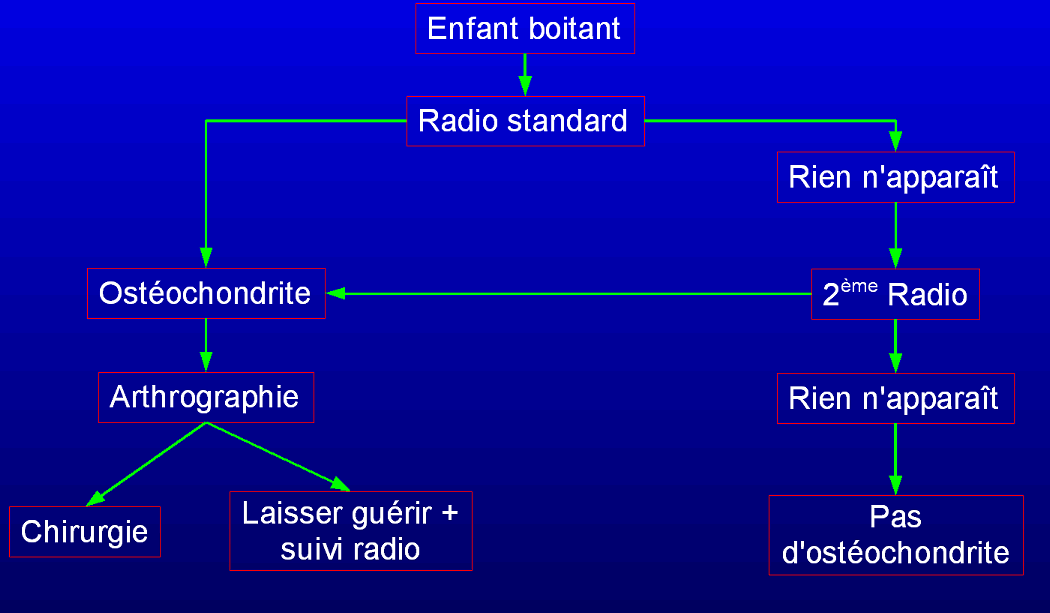
Lorsque on soupçonne un problème à la hanche, l’enfant est directement transmis à la radiologie. Si rien n'apparaît, il s'agit soit de la phase muette de la maladie (les deux premier mois qui suivent l'accident vasculaire); soit d'une autre pathologie. Il n'existe pas de traitement pour l'ostéochondrite durant la phase muette, c'est pourquoi aucune modalité n'est utilisée pour un diagnostic plus avancé. Cependant, une scintigraphie peut à ce stade confirmer l'ostéochondrite si les parents désirent le savoir. Une arthrographie dynamique permet de voir si la tête fémorale reste bien emboîtée dans le cotyle, quelque soit la position de la jambe par rapport à la hanche. C'est la modalité la plus utile après la radio. Elle est utilisée avant toute décision d'orthopédie ou de chirurgie. Elle permet également de voir si la tête est cabossée ou non.
Pour le chirurgien, l'imagerie est un outil permettant d'effectuer un diagnostic et de déterminer le traitement approprié. Toutes informations supplémentaires données par des modalités plus avancées n'influenceront pas le traitement choisi mais pourront intéresser le radiologue. En ce qui concerne l'IRM, cette modalité n'apporterait rien de plus dans l'état actuel de la technique malgré la possibilité de visualiser le cartilage. Ses avantages sont de mieux visualiser l'étendue et la position de la nécrose (par rapport à la radiologie). Cependant, étant donné sa disponibilité limitée, la complexité de l’exploitation de l’image, l’IRM n’est pas utilisée à Trousseau pour un cas d’ostéochondrite courant. La radiologie associée à l’arthrographie est de toute façon suffisante pour un diagnostic ainsi que pour décider du traitement approprié : l’avantage de l’IRM n’est donc pas pour l’instant suffisant pour justifier qu’elle supplante la radiologie. Toutefois, si une IRM était disponible et avait les mêmes possibilités dynamiques que l'arthrographie, elle remplacerait cette dernière.
La radiologie conventionnelle
Si on diagnostique l'ostéochondrite, la radio reste la modalité de référence pour le suivi; en effet elle permet de bien visualiser l'avancement de la maladie.
L'échographie
Elle montre un épanchement qui peut ne pas être dû à une ostéochondrite. De plus, cet épanchement est aussi visible avec la radio.
La scintigraphie
Elle confirme l'ostéochondrite au stade précoce si les parents le désirent. Elle n'est pas utile pour le diagnostic, car la radio est suffisante. Elle n'a pas non plus d'utilité pour le suivi de la maladie.
L'IRM
Pas d'IRM à Trousseau (ils utilisent celle de R. Debré). L'IRM n'est donc pas utilisée car non disponible. Si elle l'était, son étroitesse et les antennes actuelles (rigides) rendraient quasiment impossible l'utilisation en dynamique. Par contre, elle donne une idée précoce et précise de l'étendue et de la position de la nécrose et permet ainsi de réaliser un pronostic : opération ou non (en fonction de l'étendue). Son utilisation ne change pas le traitement (orthopédie ou chirurgie). De toute façon, l'immobilisation est abandonnée à Trousseau. L'IRM ne permet pas de bien distinguer un oedème d'une nécrose. L'utilité de l'IRM pour visualiser le cartilage reste limitée car le cartilage n'est pas touché par la nécrose dans le cas d'une ostéochondrite, il est seulement déformé, information déjà donnée par la radiologie et l'arthrographie.
L'arthrographie
C'est la modalité la plus utilisée après la radio à Trousseau. Elle donne des images très précises et permet des examens dynamiques.
A l'hôpital Trousseau, on opère 50 à 60 enfants par an pour une ostéochondrite de hanche. Ces 50 cas représentent 1/5 des cas. Les 4/5 restant ne sont pas opérés. Ils ne sont pas non plus immobilisés en chariot à cause du préjudice social pour l’enfant. Mais ils seront régulièrement suivis (1 fois par mois) par radio pour vérifier que la tête fémorale reste bien emboîtée dans le cotyle.
Date : 13 janvier 2003
Lieu : Hôpital St Vincent de Paul (14ème)
Chirurgien : Pr. SERINGE
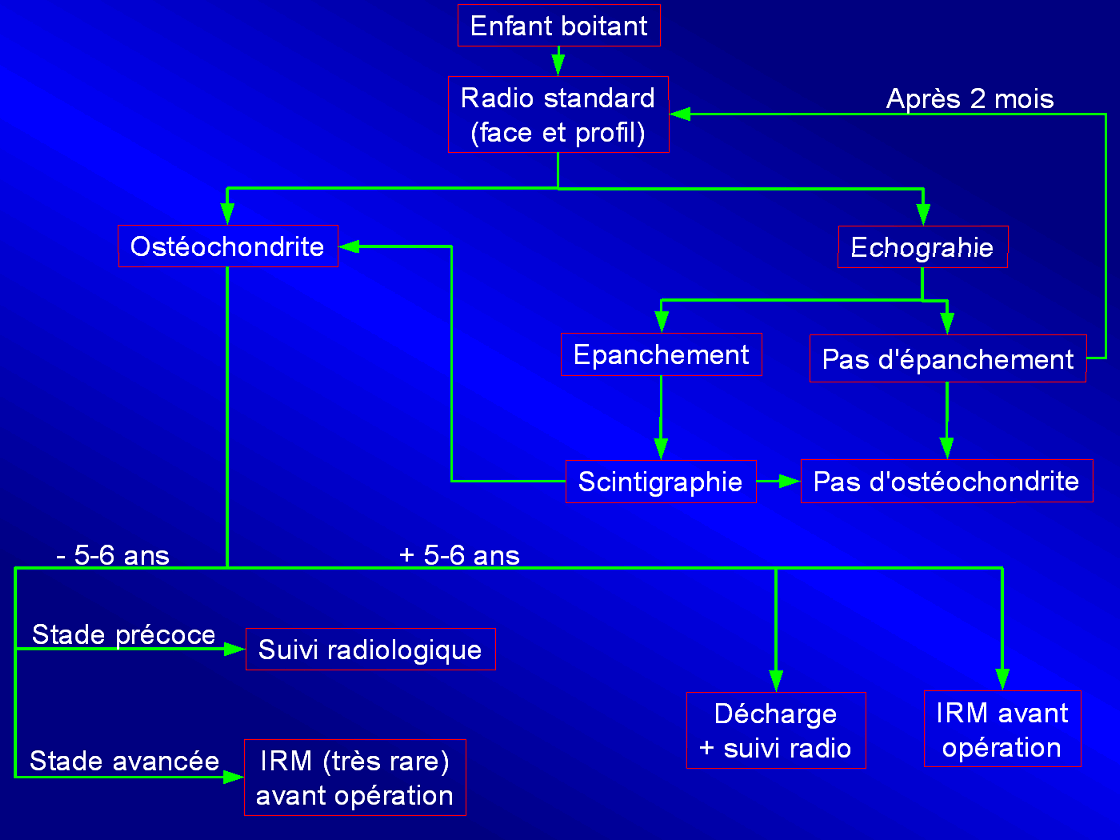
Dans le cas d'une douleur à la hanche, une radio standard est réalisée. Si elle ne montre rien, on effectue une échographie pour rechercher une anomalie qui sera confirmée par un épanchement. La scintigraphie permettra alors de diagnostiquer ou non la présence d'une ostéochondrite. Ce sont les seules modalités utilisées à St Vincent de Paul, exceptée l'IRM dans les cas les plus sévères et les plus avancés (avant une décision de traitement).
Le Pr. Seringe utilise plusieurs radios successives qu'il compare pour suivre l'évolution de la maladie. Ce suivi radiologique expose l'enfant aux radiations, qui seront diminuées d'un facteur dix grâce à l'emploi de la chambre à fils (invention de Charpak). La radiologie reste la modalité de référence pour l'ostéochondrite : en effet, c'est par la radio que Waldenstorm a découvert l'ostéochondrite et a établi une classification chronologique de cette maladie.
Radio standard
Elle est utilisée de face (méthode comparative : les deux côtés) et de profil (montre bien l'écart inter articulaire).
La radio n'est pas l'examen le plus précoce, mais permet de voir la forme, la taille, l'écartement, le coup d'ongle qui sont des signes suffisamment précoces pour diagnostiquer une ostéochondrite. En effet, il n'est pas nécessaire de diagnostiquer une ostéochondrite plus tôt car le traitement n'est pas encore possible.
Échographie
Elle montre seulement un épanchement : n'est pas spécifique à une maladie. Elle sert aussi si on cherche une autre atteinte.
Scintigraphie
C'est l'examen le plus précoce. Toutefois il présente l'inconvénient de donner des faux positifs (on voit des trous vasculaires qui n'existent pas). Elle est utilisée systématiquement pour un diagnostic quand la radio ne montre rien.
L'IRM
Pas d'IRM à St Vincent de Paul. Examen très précoce. Elle est amenée à remplacer dans une certaine mesure l'arthrographie. Elle a de grands avantages : elle montre la forme réelle de la tête du fémur (le cartilage), ses éventuelles déformations. Une image IRM réalisée après une opération permet de valider un traitement en comparant l'image IRM avec une image radio réalisée à l'âge de seize ans.
L'IRM n'est utilisée que dans les formes les plus sévères, à un stade très avancée, avant opération. Ou bien si on cherche autre chose : tumeurs dans les parties molles, etc...
L'Arthrographie
Elle était utilisée par le Pr. Seringe au stade décisionnel (avant traitement) car elle donne les meilleures images. Toutefois elle est très irradiante autant pour l'enfant que pour les mains du chirurgien et a donc été abandonnée.
On ne pratique plus la mise en traction prolongée depuis 1979 à St Vincent de Paul. On n'envoie plus du tout les enfants en centre orthopédique. Dans le cas d'une atteinte sévère, l'enfant est opéré. Il y a une dizaine d'opération pour l'ostéochondrite par an à St Vincent de Paul. Quand il n'est pas nécessaire d'opérer l'enfant, on effectue simplement un suivi radiologique associé à une décharge.
Date : vendredi 24 janvier 2003
Lieu : Hôpital Necker Enfants Malades (15ème)
Chirurgien : Dr. Stéphanie Pannier
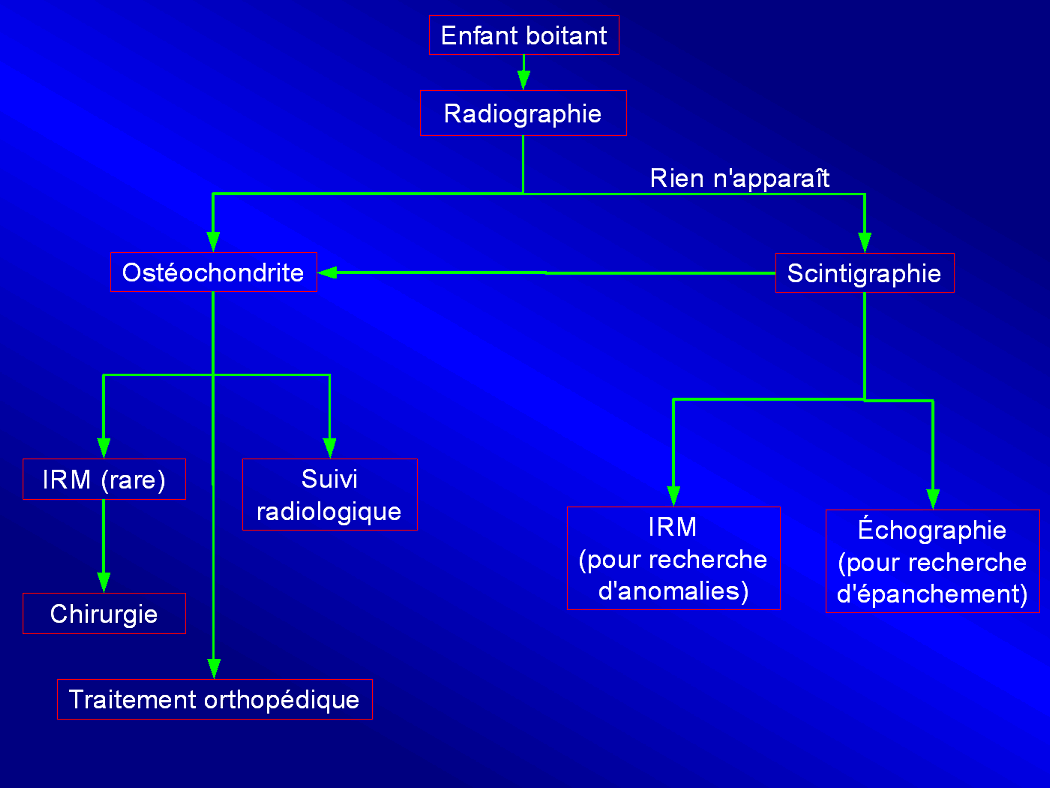
Dans le cas d'un enfant avec une douleur à la hanche, un examen clinique oriente le choix de la modalité et le plus souvent la radiographie est celle du premier diagnostic. Si cet examen est positif, l'enfant sera suivi par cette même modalité jusqu'à la guérison (y compris avant opération ou traitement orthopédique). Si la radio est normale, la scintigraphie est systématique : elle permet le diagnostic d'une ostéochondrite. Une fois la maladie confirmée, on revient à un suivi radiologique.
La scintigraphie a toujours été préférée à l'IRM (malgré sa disponibilité à Necker) étant donné le coût d'une IRM relativement trop élevée et les temps d'attentes qui sont deux à trois mois du rendez-vous à l'examen. L'IRM est éventuellement utilisée avant une opération chirurgicale pour déterminer, avec plus de précisions que la radio, la couverture de l'épiphyse par le cotyle (morphologie de l'articulation).
Radiologie
C'est la modalité la plus utilisée pour un problème osseux, notamment pour l'ostéochondrite de hanche pour laquelle elle permet un suivi complet de la maladie (jusqu'à à la guérison).
Échographie
Utilisée en diagnostic différentiel (comparaison des deux côtés) si on
cherche une autre pathologie.
Scintigraphie
Elle est systématiquement utilisée au stade précoce de la maladie, lorsque la radio est muette. Elle permet de visualiser les défauts de perfusion dans la tête fémorale
IRM
Examen autant précoce que la scintigraphie, elle permet la visualisation des défauts de perfusion, la morphologie de la tête ainsi que l'étendue de la nécrose, c'est à dire tout ce que permet de visualiser l'ensemble des autres examens. Dans certains cas, la radiologie montre une tête excentrée, alors que l'IRM la montre centrée (position exacte).
Arthrographie
N'est pas utilisée car implique trop de risques liés à l'anesthésie générale et à l'irradiation
L'hôpital Necker pratique la traction prolongée (12 à 18 mois) dans les cas suivants :
enfant déjà “ âgé ” (peu de potentiel de croissance),
nécrose étendue,
hanche déjà raide.
La modalité d'imagerie utilisée n'influence pas le traitement choisi. Celui-ci est généralement orthopédique et, dans le cas d'une excentration de la tête du fémur, on pratique soit une varisation fémorale, soit une ostéotomie pour améliorer la couverture de la tête par le cotyle. L'opération a lieu après 3 à 4 mois d'immobilisation. Les orthèses ne sont plus utilisées, mais on immobilise les enfants avec des plâtres.
Il y a 30 cas d'ostéochondrite en tout et pour tout par an à Necker.
Date : vendredi 24 janvier 2003
Lieu : Hôpital Robert Debré (19ème)
Chirurgien : Pr. Keyvan Mazda
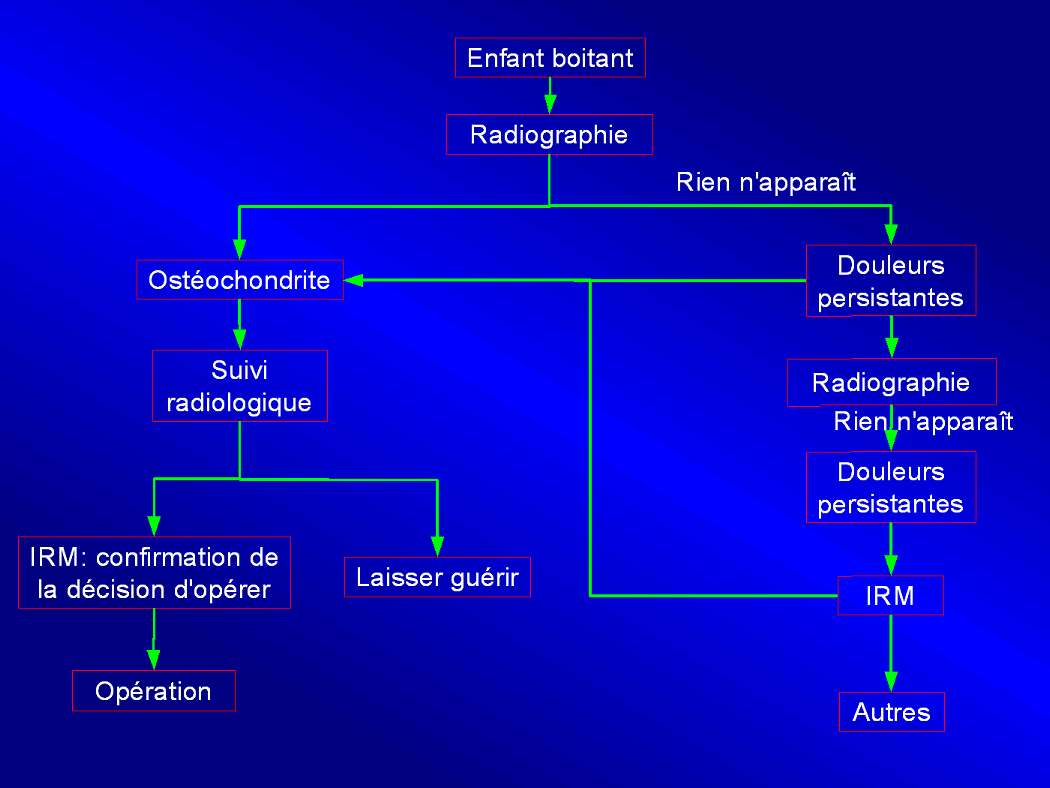
À l'hôpital R. Debré, on n'utilise que deux modalités d'imagerie pour le diagnostic et le suivi d'une LPC. Dans un premier temps, une radio permet de diagnostiquer et de suivre l'évolution de la maladie jusqu'à l'éventuelle décision d'opérer. Dans ce cas, l'IRM permet une étude morphologique et dynamique de la couverture de la tête fémorale par le cotyle ainsi qu'une visualisation précise de l'étendue de la nécrose. Si la première radio ne montre rien, on ne réalise pas d'autres examens, excepté une deuxième radio, si les douleurs persistent. La scintigraphie n'est plus utilisée à cause des trop nombreux faux positifs et négatifs et étant donné la disponibilité d'une IRM à R. Debré.
La façon de traiter la maladie conditionne la modalité choisie.
Radiologie
La radio standard est la modalité la plus utilisée pour le diagnostic et le suivi d'une ostéochondrite de hanche. En effet elle n'est remplacé par aucune autre modalité si elle permet de visualiser l'ostéochondrite dès la première fois. Si les douleurs persistent et si la radio ne montre toujours rien, elle est à ce moment là remplacé par une autre modalité.
L'IRM
Elle tient une place très importante à Robert Debré : on l'utilise systématiquement au stade décisionnel dans le cas d'une ostéochondrite à la hanche. Elle remplace tout autre modalité du fait des nombreuses informations qu'elle permet de visualiser. Son seul inconvénient reste son utilisation en dynamique : la relative étroitesse du tube empêche de couvrir toute les possibilités de positionnement de l'épiphyse dans le cotyle. Une étude réalisée au sein de l'hôpital Robert Debré a montré que l'on perd 40% de l'information concernant la couverture de la tête fémorale par le cotyle en utilisant l'IRM.
Notre questionnaire élaboré au mois de novembre 2002 avait pour objet de mettre en évidence la place particulière que tient l'IRM parmi les modalités d'imagerie utilisées par les chirurgiens pour le diagnostic et le pronostic d'une LPC.
À l'heure actuelle, seulement la moitié des centres pédiatriques parisiens possèdent une IRM sur place; ce qui explique en partie la position modeste que tient cette modalité dans les protocoles suivis en cas d'ostéochondrite : lorsqu'elle est disponible, elle n'est utilisée qu'au stade décisionnel, avant une opération. N'étant ni invasive, ni irradiante, elle est tout naturellement préférée à la scintigraphie et à l'arthrographie lorsque son utilisation est possible dans des délais raisonnables. D'autre part, ses possibilités lui permettent de remplacer les autres modalités, exceptée la radio qui reste l'examen standard dans le cas d'une douleur osseuse. Toutefois, son inconvénient majeur dans le cas d'une ostéochondrite de hanche est l'utilisation limitée en dynamique : on perd de l'information sur la couverture de la tête par le cotyle par rapport à une arthrographie dynamique.
Étant donné sa disponibilité limitée, l'IRM est remplacée par l'arthrographie, la scintigraphie et la radiologie, selon les habitudes de chaque chirurgien et leurs convictions personnelles. Il n'existe donc pas de protocole de référence en cas d'ostéochondrite et il n'y a pas de consensus sur la marche à suivre entre les différents spécialistes des centres pédiatriques parisiens.
Toutefois, l'utilisation de la radio est commune à chaque équipe questionnée en tant que modalité de base pour le diagnostic et le suivi de la maladie. Dans certains centres, on lui associe une arthrographie pour ses qualités dynamiques et sa bonne visualisation des articulations; tandis que dans d'autres, on associe radiographie et scintigraphie sans arthrographie car celle-ci est jugé trop invasive et irradiante.
L'IRM est attendue dans les centres qui n'en possèdent pas car elle permettrait de simplifier les protocoles et remplacerait les modalités irradiantes et/ou invasive, tout en étant associée à la radiologie. Nous pensons, d'autre part, qu'elle permettrait aussi d'harmoniser les protocoles dans le sens de celui de R. Debré.
Grâce aux entretiens effectués avec les chirurgiens orthopédiques, ce projet nous a permis d'appréhender les approches complémentaires des chirurgiens et des chercheurs. Il était, pour nous, notre premier contact avec le milieu hospitalier.
Nous avons été surpris de constater que, pour une maladie relativement courante, les équipes cliniques de l'APHP n'ont pas de protocoles communs. Apparemment, cela est dû, d'une part, à l'équipement disparate d'un centre à un autre en appareillage d'imagerie médicale et d'autre part, à l'importance des habitudes, des convictions personnelles et des formations initiales différentes des chirurgiens orthopédiques. Il n'y a pas, de façon visible, de prise en compte du patient en tant qu'individu, mais plutôt une prise en charge d'une maladie; mais ce problème est complexe et il n'y a pas de solution évidente.
La nature du projet nous a également permis d'approfondir nos connaissances sur les modalités d'imagerie (principe physique, avantages, inconvénients...), connaissances fondamentales pour l'ingénieur biomédical.
Ce travail a consisté à faire l'état des lieux des protocoles actuellement utilisés par les chirurgiens orthopédiques face à une ostéochondrite de hanche ainsi que mettre en relief la place que tient l'IRM dans ces protocoles.
Il s'avère qu'actuellement, dans les hôpitaux parisiens, la disponibilité de l'IRM et la force des habitudes, ne positionne pas cette modalité prioritairement dans les protocoles cliniques liés à cette maladie. Par contre, la radiologie conventionnelle reste la plus utilisé en diagnostic et suivi de la maladie de LPC.
L'autorisation d'achat d'IRM récemment décidé amènera peut être une harmonisation et une simplification des protocoles liés à l'ostéochondrite. Celle-ci, combiné à la radiographie, permettra le diagnostic et le suivi complet d'une ostéochondrite.
Ouvrages
[1] : A. Diméglio, Ch. Hérisson, L. Simon; La maladie de Legg-Perthes-Calvé, 1999
[2] : YOCHUM & ROWE; Essentials of Skeletal Radiology, 1996
[5] : B. Kastler, D. Vetter, Z. Patay, P. Germain; Comprendre l'IRM, 1994
Sites internet
[3] : http://www.univ-st-etienne.fr/facmed/finit/cottalor/osteoch.html,
[4] : http://www.bmlweb.org/chir_ped_osteochondrite0300.html,
[6] : http://fr.encyclopedia.yahoo.com/article/so/so_302_p0.html,
[7] : http://www.frm.org/upload/dossier/imageriemed.edf,
[8] : http://www.scoi.com/hipanat.html,
[9] : http://www.med.univ-rennes1.fr/cerf/edicerf/RADIOANATOMIE/024.html,
[10] : http://radiography.gulfcoast.edu/rte1613/week51.htm,
[11] : http://www.echo.uqam.ca/mednet/francais/hermes_f/hanche/hanc_06.html,
[12] : http://menbers.aol.com/radiochd/irm/sequences.htm,
Illustration 1 : Hanche et tête du fémur (d'après [7])
Illustration 2 : Phases évolutives de la LPC (d'après [3])
Illustration 3 : coxa magna gauche (d'après [3])
Illustration 4 : Évolution radiologique de l'ostéochondrite (d'après [3])
Illustration 5 : Signes radiologiques initiaux de l'ostéochondrite (d'après [3])
Illustration 6 : Stade très avancée : fragmentation de l'épiphyse droite (d'après [3])
Illustration 7 : Coxa plana à droite
Illustration 8 : Point de ponction de l'arthrographie de hanche (d'après [8])
Illustration 9 : image arthrographique d'une hanche saine (d'après [9])
Illustration 10 : Aspect scintigraphique de l'ostéochondrite (d'après [3])
Illustration 11 : Scintigraphie : trou de fixation à gauche (d'après [3])
Illustration 12 : Scintigraphie : trou de fixation à gauche
Illustration 13 : Séquence T1. Fragmentation et coxa plana à gauche
Illustration 14 : Séquence T2. Fracture sous-chondrale et excentration de la tête fémorale gauche
Illustration 15 : Séquence dynamique avec injection de gadolinium