|
Avertissement
|
| Si vous arrivez directement sur cette page sachez que
ce travail est un rapport d'étudiant(e)s et doit être pris
comme tel. Il peut donc comporter des imperfections ou des imprécisions
que le lecteur doit admettre et donc supporter. Il a été
réalisé pendant la période de formation et constitue
avant-tout un travail de compilation bibliographique,
d'initiation et d'analyse sur des thématiques associées aux
technologies biomédicales. Nous ne
faisons aucun usage commercial et la duplication est libre. Si vous avez
des raisons de contester ce droit d'usage, merci
de nous en faire part. L'objectif de la présentation
sur le Web est de permettre l'accès à l'information et d'augmenter
ainsi les échanges professionnels. En cas d'usage du document, n'oubliez
pas de le citer comme source bibliographique. Bonne lecture... |
Référence à rappeler :
ISO 9000 en santé : bilan
Accréditation et certification au service biomédical
Projet DESS "TBH", UTC, 2000, pp 30
URL : https://www.utc.fr/~farges/DESS_TBH/99-00/Projets/bilan_ce/bilan_ce.htm
|
ISO 9000 en santé :
bilan
Accréditation et certification
au service biomédical
|

|

|
|
Hervé MIGNARDOT
|
Hervé DION
|
Remerciements
Nous tenons tout d'abord à
remercier Monsieur Georges CHEVALLIER, responsable du DESS "Technologies
Biomédicales Hospitalières" ainsi que Monsieur Gilbert FARGES,
co-animateur du DESS pour les conseils qu'il a pu nous apporter pour mener
à bien ce projet.
Nos remerciements vont aussi à
Monsieur François THIBAULT, Université d'Angers, pour toutes
les connaissances qu'il nous a fait partager tout au long de la formation.
Remerciements enfin à l'ensemble
des services biomédicaux qui ont participé à l'enquête
portant sur le bilan de la certification ISO 9002.
Introduction
Qualité, tracabilité,
conformité, certification, · sont autant de termes qui sont de plus
en plus employés dans le secteur hospitalier français.
La volonté de mettre en place
une amélioration continue de la qualité des soins par l'introduction
de l'ordonnance du 24 avril 1996 portant sur la réforme hospitalière,
incite les établissements de soins à mettre en pace des actions
"qualité" pour répondre aux exigences réglementaires.
L'objectif de ce rapport est d'effectuer
un état des lieux de la qualité en santé.
Les normes ISO 9000, bien connues
dans le monde industriel, sont-elles aussi répandues dans le secteur
hospitalier ? Un bilan réalisé à la fin de l'année
1999 apportera la réponse.
En parallèle, le service
biomédical prend conscience des nouveaux enjeux générés
par le nombre croissant des textes réglementaires.
Sa mission de prestataire de service,
le place dans une position stratégique entre le monde industriel
et le secteur de la santé. Cette position l'incite à entamer
une démarche qualité. Plusieurs d'entre eux sont déjà
allés jusqu'à la certification.
Une enquête, réalisée
en décembre 1999, permet à la communauté biomédicale
de bénéficier de cette expérience.
Enfin, une réflexion a été
menée pour évaluer l'apport de la certification ISO 9000
du service biomédical dans la démarche d'accréditation.
Sommaire
Chapitre
I
La
démarche qualité dans les établissements de santé
I.1.
Pourquoi une démarche qualité ?
I.1.1.
La qualité dans un établissement de santé
I.1.2. La réglementation dans un établissement de santé
I.2.
La qualité dans le cadre réglementaire : l'accréditation
hospitalière
I.2.1. L'A.N.A.E.S.
I.2.2. Définition de l'accréditation
I.2.3. Les objectifs
I.2.4. Description du référentiel d'accréditation
I.2.5. La procédure d'accréditation
I.3.
La qualité dans le cadre volontaire : la certification
I.3.1. Définition de la certification
I.3.2. Les normes de la série ISO 9000
I.3.2.1. Présentation
I.3.2.2. Application de la norme ISO 9000 dans un établissement
de santé
I.3.3. La certification
I.3.3.1. Le COFRAC
I.3.3.2. Les organismes certificateurs
I.3.3.3. La procédure de certification
I.4.
Comparatif entre la certification et l'accréditation hospitalière
I.4.1. Similitudes
I.4.2. Différences
Chapitre
II
Bilan
de la certification ISO 9000 dans les établissements de santé
II.1.
Bilan des structures de santé certifiées en Europe
II.2.
Bilan des structures de santé certifiées en France
II.2.1. Méthodologie
II.2.2. Les organismes certificateurs
II.2.3. Les structures certifiées
II.2.4. Les activités certifiées
II.3.
Bilan des services biomédicaux certifiés et en cours de certification
II.3.1. Etat des lieux
II.3.2. Enquête
II.3.3. Résultat et interprétation
Chapitre
III
Apport
de la norme ISO 9000 pour le service biomédical dans la démarche
d'accréditation
III.1.
Pourquoi aller jusqu'à la certification ?
III.2.
Comparatif entre l'accréditation et la certification
III.3.
Quelle activité certifier ?
III.3.1. Les missions du service biomédical
III.3.2. L'activité à certifier
CONCLUSION
BIBLIOGRAPHIE
ANNEXE
A : Organismes certificateurs de systèmes accrédités
par le COFRAC pour la certification selon les normes ISO 9000 dans le secteur
de la santé
ANNEXE
B : Liste des établissements de santé français
certifiés par la norme ISO 9000
ANNEXE
C : Résultats du questionnaire des services biomédicaux
certifiés ISO 9002 et ceux en cours
ANNEXE
D : Tableau de comparaison entre les exigences de l'accréditation
et la norme ISO 9000
I.1.
Pourquoi
une démarche qualité ? [2] [3]
I.1.1. La qualité dans un établissement de santé
Les établissements de santé ont pour objectifs de prendre
en charge des malades pour les soigner. Ils se différencient d'une
unité de production conventionnelle, comme une usine, par un certains
nombres de points :
-
Les décideurs sont multiples :
Il n'y a pas une seule Direction, mais plusieurs qui sont plus ou
moins bien formalisées et qui, selon le caractère privé
ou public de l'établissement de santé, jouent des rôles
d'importance différente.
Ces Directions peuvent être la Direction administrative, la Commission
Médicale d'Equipement (C.M.E.), une Direction de soins infirmiers,
un conseil d'administration, ·
-
L'importance des services et leurs spécificités :
Dans les établissements de santé, la prestation de soins,
incluant un diagnostic et un traitement, est l'activité dominante.
Cette prestation de soins est faite directement sur le malade, ce qui rend
l'erreur difficilement admissible. Ce risque d'erreur doit donc être
supprimé, car il peut parfois être irrémédiable.
La prévention du risque revêt toute son importance.
La démarche qualité doit aider à fédérer
tous les métiers exercés dans l'établissement dans
un objectif commun qui est celui de satisfaire le patient au moindre coût.
-
La multiplicité des interfaces :
Pour un service rendu directement à un malade, il existe de
nombreux acteurs impliqués dans la structure d'accueil, de soins,
de sortie et de suivi après la sortie. Mais, il existe aussi des
acteurs impliqués dans les structures médico-techniques (laboratoire,
imagerie médicale et bloc opératoire).
Une attention particulière doit être portée à
la gestion efficace de ces interfaces.
I.1.2.
La réglementation dans un établissement de santé
De nombreuses contraintes réglementaires sont apparues ces
dernières années dans le secteur de la santé.
D'une part l'ordonnance n° 96346 du 24 avril 1996
portant sur la réforme de l'hospitalisation publique et privée
permettra aux établissements de comparer leurs performances en matière
de coût des fonctionnements, mais aussi de qualité. La législation
est venue structurer les initiatives qualité en créant un
cadre juridique approprié ; c'est la raison pour laquelle, les pouvoirs
publiques ont initié le lancement d'une démarche d'accréditation
fondée sur l'assurance qualité en milieu hospitalier.
D'autre part, les textes portant sur la qualité des soins et
la sécurité des patients se multiplient, parmi les plus importants
:
-
L'arrêté du 3 octobre 1995 relatif aux modalités
d'utilisation et de contrôle des dispositifs médicaux d'anesthésie
implique une démarche d'assurance qualité pour les dispositifs
concernés. Sa rédaction s'inspire largement des concepts
liés à l'assurance qualité où l'on demande
de décrire l'organisation et la formalisation des pratiques.
-
Le marquage CE en vigueur depuis le 14 juin 1998, oblige tout fabricant
de dispositifs médicaux, qui veut mettre ses produits sur le marché
de l'Espace Economique Européen, à apposer le marquage CE
après avoir établi la conformité des dispositifs concernés
aux exigences réglementaires qui découlent des directives
européennes 90/385/CEE (20 juin 1990) et 93/42/CEE (14 juin 1993).Pour
les établissements de soins, ce marquage introduit une notion de
surveillance des dispositifs médicaux : la matériovigilance.
-
La politique des vigilances constitue une veille sanitaire permanente
dont les objectifs sont le signalement, l'enregistrement, le traitement
et l'investigation des évènements indésirables et
des incidents liés à l'utilisation de produits thérapeutiques,
ainsi que leur traçabilité et la réponse aux réponses
sanitaires. Ce dispositif doit être au service des responsables de
santé publique qui sont les garants d'un fonctionnement optimal
du système de santé. Le principe de vigilance qui consiste
à assurer une surveillance attentive sans défaillance s'applique
à plusieurs domaines des activités de soins des hôpitaux
et cliniques. Il existe cinq types de vigilances :
· la matériovigilance
: elle a pour objet la surveillance des incidents ou des risques d'incidents
résultant de l'utilisation des dispositifs médicaux.
La matériovigilance comporte :
-
le signalement et l'enregistrement des incidents ou des risques d'incidents
;
-
L'enregistrement, l'évaluation et l'exploitation de ces informations
dans un but de prévention ;
-
la réalisation de toutes les études ou travaux concernant
la sécurité d'utilisation des dispositifs médicaux
;
-
la réalisation et le suivi des actions correctives décidées.
· l'hémovigilance
: ensemble des procédures de surveillance organisées depuis
la collecte du sang et de ses composants jusqu'au suivi des receveurs,
en vue de recueillir et d'évaluer les informations sur les effets
inattendus ou indésirables résultant de l'utilisation thérapeutique
des produits sanguins labiles et d'en prévenir l'apparition.
· la pharmacovigilance : elle
a pour objet la surveillance du risque d'effets indésirables résultant
des médicaments, des produits à usage humain et des produits
contraceptifs.
· la biovigilance : elle a
pour but d'assurer une attention sur les éléments et produits
du corps humain, sur les produits, autres que les médicaments qui
en dérivent, ainsi que les dispositifs médicaux les incorporant,
et en particulier en ceux concernant les informations sur ces produits.
· la toxiciovigilance : elle
se définit comme la détection et l'étude des effets
néfastes pour la santé, d'expositions chimiques non médicamenteuses.
-
La lutte contre les infections nosocomiales : La réduction
des infections nosocomiales à l'hôpital est une priorité
de santé publique définie par la conférence nationale
de santé depuis 1996. Les Infections Nosocomiales (IN) sont les
infections acquises par le patient dans un établissement de santé,
que celles ci soient directement liées aux soins ou qu'elles surviennent
indépendamment de tout acte médical ; les IN représentent
donc un véritable indicateur de non-qualité. Des Comités
de Lutte contre les infections nosocomiales (CLIN) ont été
institués dans les établissements de santé publics
en 1988 puis dans les cliniques privées par la loi du 1er
juillet 1998 relative au renforcement de la sécurité sanitaire.
-
le Guide de bonne exécution des analyses (GBEA) (deuxième
version - 26 novembre 1999, J.O. du 11 décembre 1999) stipule que
tout laboratoire, réalisant des analyses de biologie médicale,
doit disposer d'un système d'assurance qualité basé
sur des procédures opératoires écrites concernant
l'analyse proprement dite, l'organisation générale du laboratoire
et de la traçabilité des contrôles. Il touche l'activité
du service biomédical car il exige le suivi de la maintenance des
appareils de laboratoire.
-
La Loi du 1er juillet 1998 N° 98-535 (J.O. Numéro
151 du 2 juillet 1998) relative au renforcement de
la veille sanitaire et du contrôle de la sécurité sanitaire
des produits destinés à l'homme stipule que :
"Pour les dispositifs médicaux dont la liste est fixée
par le ministre chargé de la santé après avis de l'Agence
Française de Sécurité SAnitaire des Produits de Santé,
l'exploitant est tenu de s'assurer du maintien de ces performances et de
la maintenance du dispositif médical.
Cette obligation donne lieu, le cas échéant, à
un contrôle de qualité dont les modalités sont définies
par décret et dont le coût est pris en charge par les exploitants
des dispositifs.
Pour les dispositifs médicaux dont la liste est fixée
par le ministre chargé de la santé après avis de l'Agence
Française de Sécurité SAnitaire des Produits de Santé,
la personne morale ou physique responsable d'une nouvelle mise sur le marché
fait établir préalablement une attestation technique, dont
les modalités sont définies par décret, garantissant
que le dispositif médical concerné est toujours conforme
aux exigences essentielles".
Les décrets d'application devraient paraître dans le courant
de l'année 2000.
-
La réglementation en dehors des soins : les établissements
doivent garantir :
· la sécurité alimentaire
des repas qu'ils servent aux malades hospitalisés,
· la sécurité des systèmes d'information,
· la sécurité incendie
· ·
La description des ces réglementations parle de tracabilité,
de contrôle, de client, termes de langage qualité. La mise
en place d'un système qualité peut donc répondre d'une
manière plus ou moins complète à leurs exigences.
Les professionnels de la santé, dans leur prise en compte de
la qualité sont donc face à des contraintes de type réglementaire
: l'accréditation. Ils peuvent s'ils le désirent, compléter
par une démarche volontaire : la certification.
(Retour au sommaire)
I.2.
La
qualité dans le cadre réglementaire : l'accréditation
hospitalière
I.2.1. L'A.N.A.E.S.[1](aller
sur le site web de l'A.N.A.E.S.)
L'A.N.A.E.S. (Agence Nationale d'Accréditation et d'Evaluation
en Santé) est la structure compétente pour gérer la
procédure d'accréditation prévue par l'ordonnance
du 24 avril 1996 (Cf. chapitre I.1.2.).
L'A.N.A.E.S. a un statut d'établissement public administratif
de l'Etat. Le conseil d'administration est composé de 32 membres
titulaires : personnels médicaux, paramédicaux, techniques
et administratifs, des représentants de l'Etat et des organismes
de maladie.
I.2.2. Définition
de l'accréditation [2] [16]
Il s'agit selon le manuel de l'A.N.A.E.S. "d'une procédure
d'évaluation externe à un établissement de santé,
effectuée par des professionnels, indépendante de l'établissement
et de ses organismes de tutelle, évaluant l'ensemble de son fonctionnement
et de ses pratiques. Elle vise à assurer la sécurité
et la qualité des soins donnés au patient et à promouvoir
une politique d'amélioration continue de la qualité au sein
des établissements".
L'accréditation concerne tous les établissements de santé
publics, privés ainsi que les établissements militaires de
santé. Elle concerne également les groupements de coopération
sanitaire entre établissements de santé et les réseaux
de soins.
Elle ne s'applique pas actuellement aux activités médico-sociales
même lorsque celles-ci s'exercent au sein d'un établissement
de santé.
L'accréditation s'applique à l'établissement de
santé au sens juridique du terme. Cela revient à dire que
l'accréditation concerne simultanément l'ensemble des structures
(services, départements...) et des activités, en raison des
interrelations existantes entre elles.
Dans le cas d'un établissement de santé installé
sur plusieurs sites, l'A.N.A.E.S. peut mettre en þuvre une procédure
par site.
Près de 4 000 établissements sont concernés par
l'accréditation hospitalière.
I.2.3. Les objectifs[16]
L'accréditation s'inscrit dans une logique de progrès
d'un établissement de santé. Elle accorde une place centrale
au patient, à son parcours, à la coordination des soins qui
lui sont apportés, à sa satisfaction.
L'accréditation a 6 objectifs principaux :
- L'appréciation de la qualité et de la sécurité
des soins, qui constituent une attente principale des patients vis-à-vis
du système de santé,
- L'appréciation de la capacité de l'établissement
à améliorer de façon continue la qualité des
soins et la prise en charge globale du patient, grâce à la
mise en þuvre d'un système reconnu de gestion de la qualité,
- La formulation de recommandations explicites,
- L'implication des professionnels à tous les stades de la
démarche qualité, afin qu'ils acceptent et s'approprient
les changements,
- La reconnaissance externe de la qualité des soins dans les
établissements de santé,
- L'amélioration continue de la confiance du public.
I.2.4.
Description du référentiel d'accréditation
[16]
L'A.N.A.E.S. a bâti un référentiel qui s'inspire
largement du modèle canadien. Il comprend trois chapitres, eux même
déclinés en onze sous-chapitres :
I - Le patient et sa prise en charge
-
Droit et information du patient (DIP)
-
Dossier du patient (DPA)
-
Organisation de la prise en charge des patients (OST)
-
La prise en charge hôtelière (PCH)
II - Management et gestion au service du patient
-
Management de l'établissement et des secteurs d'activités
(MEA)
-
Gestion des ressources humaines (GRH)
-
Gestion des fonctions logistiques (GFL)
-
Gestion du système d'information (GSI)
III - Qualité et prévention
-
Gestion de la qualité et prévention des risques (QPR)
-
Vigilances sanitaires et sécurité transfusionnelle (VST)
-
Surveillance, prévention et contrôle du risque infectieux
(SPI)
I.2.5. La procédure
d'accréditation [16]
La procédure d'accréditation s'effectue en huit étapes
:
- 1. La procédure d'accréditation est engagée
sur l'initiative du directeur de l'établissement. Il adresse une
demande d'engagement à l'ANAES, accompagnée d'un dossier
de présentation de l'établissement décrivant ses activités,
son organisation générale et sa stratégie qualité.
L'Agence peut ainsi déterminer le déroulement et le planning
de la procédure.
- 2. L'A.N.A.E.S. propose un contrat d'accréditation
rappelant les engagements à tenir puis envoie les documents d'analyse
nécessaires à la phase d'auto-évaluation.
- 3. L'établissement effectue son auto-évaluation
et en transmet les résultats à l'A.N.A.E.S.
- 4. Après réception des résultats de l'auto-évaluation,
la visite d'accréditation est effectuée par une équipe
d'experts-visiteurs, qui rédige le rapport des experts, lequel s'appuie
sur les résultats de l'auto-évaluation.
- 5. Le rapport des experts est communiqué à l'établissement
pour qu'il formule ses observations.
- 6. Le rapport des experts sur les observations de l'établissement
est communiqué au Collège de l'accréditation de l'A.N.A.E.S.,
qui examine le déroulement de la procédure, valide le rapport
d'accréditation qui comporte des recommandations, fixe les modalités
de suivi et arrête le délai au bout duquel une nouvelle procédure
devra être engagée.
Les appréciations du Collège de l'Accréditation
seront formulées sous une forme graduée pouvant se résumer
ainsi :
|
Appréciation
|
Modalités de suivi par
|
Délai d'engagement entre
deux procédures
|
|
Sans recommandations
|
Par l'établissement |
5 ans
|
|
Avec recommandations
|
L'établissement de santé réalise
un bilan de suivi des recommandations en perspective de la prochaine procédure |
5 ans
|
|
Avec réserves
|
L'établissement de santé réalise
un bilan de suivi et le transfert à l'A.N.A.E.S. à échéance
déterminée |
Moins de 5 ans
|
|
Avec réserves majeures
|
L'A.N.A.E.S. demande que l'établissement
de santé apporte des solutions aux questions ayant fait l'objet
de réserves majeures à échéance donnée |
Moins de 5 ans et visite ciblée à échéance
fixée sur les questions ayant fait l'objet de réserves majeures
|
- 7. Le rapport d'accréditation est transmis par l'Agence
au directeur de l'établissement de santé, ainsi qu'au directeur
de l'Agence Régionale de l'Hospitalisation (ARH) compétente.
- 8. Un compte-rendu de la procédure d'accréditation
est transmis par l'A.N.A.E.S. à l'établissement. Il est consultable
sur demande par le public et les professionnels de santé intéressés.
(Retour au sommaire)
I.3.
La
qualité dans le cadre volontaire : la certification
I.3.1. Définition
de la certification [10]
La certification est le fruit d'un travail reconnu par un organisme
officiel suivant un référentiel international. C'est la satisfaction
de voir déclaré atteint, un objectif fixé par une
entité compétente. Mais c'est aussi la garantie de la mise
en þuvre d'une organisation adaptée qui formalise les relations
internes du type "client/fournisseur".
La certification est la concrétisation d'une démarche
qui prouve la qualité d'un service vis à vis de ses partenaires
externes, qui, eux-mêmes, ont été validés sur
le même référentiel. Les actions de partenariat, de
ce fait, devraient se développer puisqu'elles reposent sur les mêmes
préoccupations organisationnelles. Pour le service biomédical,
la certification peut être aussi, et surtout, un outil de management
et d'amélioration des pratiques.
I.3.2. Les normes
de la série ISO 9000
I.3.2.1.
Présentation
C'est en 1979 que l'ISO (International Organisation for Standardisation)
met en place le Comité Technique (TC 176) qui prend en charge l'élaboration
des normes sur le management et l'assurance qualité. L'objectif
de ces normes était essentiellement de facilité les relations
contractuelles client/fournisseur par l'élaboration d'un référentiel
international.
La première publication de la série des normes ISO 9000
de base (ISO 8402, ISO 9000, ISO 9004 et ISO 9001/2/3) date de 1987. En
1994, elles connaissent leur première évolution et s'acheminent
pour l'an 2000 vers leur deuxième révision.
La structure des normes ISO 9000 version 2000 évolue vers la
simplification comme le montre le tableau suivant :
|
ISO 9000 version 1994
|
ISO 9000 version 2000
|
Concept, sélection et terminologie
ISO 9000-1; ISO 8402
|
Concept et vocabulaire
ISO 9000
|
Management de la qualité - lignes directrices
ISO 9004-1; ISO 9004-2
ISO 9004-3; ISO 9004-4
|
Conseils pour l'amélioration des performances
ISO 9004
|
Assurance de la qualité
ISO 9001; ISO 9002; ISO 9003
|
Système de management de la qualité - exigences
ISO 9001
|
Audit qualité - lignes directrices
ISO 10011-1; ISO 10011-2; ISO 10011-3
|
Audit du système de management de la qualité et de
l'environnement
ISO 19011
|
Les trois normes ISO 9001/ 2 /3 ne feront plus qu'une, ainsi le service
souhaitant entrer dans la démarche de certification ne répondra
qu'aux chapitres qui concernent le champ d'activité qu'il souhaite
certifier. Malgré tout, si une entreprise a un service de conception
ou de recherche et développement, il devra obligatoirement le faire
certifier.
Par rapport à la norme ISO 9002 de 1994, quatre évolutions
principales sont constatées :
- la responsabilité de la Direction (chapitre 5 du projet
de norme),
- la prise en compte plus importante du client (tous les chapitres),
- une meilleure gestion des ressources (chapitre 6),
- une approche en processus de l'activité (principalement
le chapitre 7).
I.3.2.2.
Application de la norme ISO 9000 dans un établissement de santé
L'objectif est de "traduire" les chapitres de la norme ISO 9000 en
l'appliquant, de façon très générale, à
un établissement de santé.
4.1 Responsabilité de la direction
4.1.1 Politique qualité
La mise en place d'un système qualité ne peut se réaliser
que si la direction en accepte le principe et met toute son autorité
pour que la démarche réussisse.
-
Organisation
4.1.2.1 Responsabilité et autorité
La définition écrite des missions évite les conflits
et les erreurs. Cette clarté facilite la réactivité
face à des situations d'urgence.
-
Moyens
Outre le risque potentiel sur l'état de santé du patient,
les moyens peu adaptés sont sclérosants et générateurs
de difficultés qui compliquent le processus de traitement et augmentent
les coûts de fourniture de services rendus.
-
Représentant de la direction du système
qualité
Pour qu'un système puisse fonctionner efficacement et progresser,
il est indispensable qu'une personne s'en occupe régulièrement,
avec l'autorité et l'attribution des moyens nécessaires.
4.1.3 Revue de la direction
De telles réunions permettent au directeur du système
qualité de vérifier que les objectifs fixés sont toujours
d'actualité et qu'ils sont atteints. Elles permettent également
d'ajuster les moyens et de définir les priorités.
4.2 Système qualité
4.2.2 Généralités
4.2.2 Procédures du système
qualité
4.2.3 Planification de la qualité
Le système qualité formalisé sans excès
est un outil particulièrement intéressant.
Pour maintenir une dynamique d'amélioration, il conviendra de
s'appuyer sur des revues de direction, des revues de contrats - sans négliger
:
-
la fixation d'objectif
-
les audits qualité
-
les actions correctives tant sur le produit ou le service que le système
qualité
-
les actions préventives, les enregistrements exploités au
cours de la revue de Direction
4.3 Revue de contrat
Une revue de contrat permet d'évaluer et de formaliser l'ensemble
des besoins du patient, et mettre les moyens nécessaires pour satisfaire
ses besoins. Elle permet également de déterminer si l'établissement
de santé, ou le service concerné, a les moyens réels
pour obtenir les résultats attendus par le patient.
4.5 Maîtrise des documents et des données
La maîtrise des documents et des données permet de formaliser
le savoir-faire des acteurs hospitaliers, de faciliter l'adaptation au
poste de travail et la polyvalence dans le respect des compétences
réglementaires.
La bonne gestion de la documentation est le gage de l'assurance de
la bonne maîtrise de l'information, en particulier concernant la
transmission des données médicales lors des changements d'équipe.
Elle constitue donc un des maillons de la chaîne de maîtrise
du risque au sein de l'établissement de santé.
4.6 Achats
La maîtrise des achats en fonction de leur influence sur la qualité
du produit de l'établissement de santé est une condition
nécessaire pour obtenir la qualité au moindre coût
et en toute sécurité.
4.7 Maîtrise du produit fourni par le
client
Le dossier médical préalable à l'admission apporte
des informations précieuses qui s'intègrent aux données
qui permettront le bon diagnostic et assureront la fiabilité des
informations fournies.
4.8 Identification et traçabilité
du produit
Les établissements de santé sont tenus réglementairement
d'assurer la traçabilité d'un certain nombre de produits,
en particulier tous ceux qui sont concernés par la sécurité
transfusionnelle, les dispositifs implantables, et les lots de certains
médicaments.
4.9 Maîtrise des processus
Une bonne connaissance et un suivi permanent des processus et procédés
utilisés pour réaliser directement ou indirectement les soins
aux patients, sont nécessaires pour assurer une production de qualité
constante, et conforme aux exigences fixées.
Tous les processus susceptibles d'avoir une influence sur le service
fourni au patient doivent être pris en compte.
4.10 Contrôles et essais
A la réception, un meilleur suivi de la qualité des fournitures
a pour conséquence une réduction des produits ou services
non conformes permettant un gain de temps, une sécurité accrue,
et un dialogue facilité et constructif avec les fournisseurs internes
et externes.
La bonne exécution des contrôles et essais est une assurance
de la qualité pour le malade dont la sécurité est
l'une des composantes importantes.
4.11 Maîtrise des équipements
de contrôle, mesure et d'essai
Cette maîtrise permet de connaître tous les appareils réellement
utiles, et leurs véritables applications.
4.12 Etat des contrôles et des essais
Le but est de s'assurer que seul un produit ou un service rendu conforme
aux exigences spécifiées a été distribué
ou réalisé.
4.13 Maîtrise du produit non conforme
Les établissements de santé doivent tenir à jour
des procédures écrites garantissant la maîtrise de
ses produits ou services non conformes.
La non-conformité doit être signifiée au patient
dans le respect de la déontologie médicale (infections nosocomiales
par exemple).
4.14 Actions correctives et préventives
La notion de prévention revêt un caractère particulièrement
important dans le domaine de la santé où les risques encourus
sont importants pour beaucoup de partenaires, et où la maîtrise
du risque est primordiale. L'action de prévention permet également
de limiter les coûts de la non-qualité.
4.15 Manutention, stockage, conditionnement,
préservation, livraison
Une bonne gestion des stocks, en particulier des produits à
usage médical stérile, médicaments, dérivés
du sang, etc. ·, supprime les risques encourus à l'utilisation et
permet de diminuer les coûts financiers.
4.16 Maîtrise des enregistrements relatifs
à la qualité
Outre qu'ils permettent de prouver que le produit ou le service est
conforme aux exigences spécifiées et que le système
qualité fonctionne comme prévu, les enregistrements permettent
de tirer un certain nombre d'enseignements conduisant à des améliorations
de la qualité.
4.17 Audits qualité internes
Ils sont de toute première importance pour assurer la progression
permanente de la qualité de la prestation au sein des établissements
de santé
4.18 Formation
L'intérêt est d'identifier les besoins de formation pour
apporter au personnel les compétences nécessaires à
l'activité de l'entité sous assurance qualité.
4.19 Prestations associées
La bonne organisation de ces prestations vient renforcer l'image de
qualité globale donnée par l'établissement et accentue
la sensation de confort du patient, de sa famille, fragilisés par
la maladie.
4.20 Techniques statistiques
Il n'y a pas d'améliorations possibles de la qualité
du service ou du procédé sans définition de critères
quantitatifs par des mesures aussi exactes ou par des évaluations
aussi objectives que possible.
I.3.3. La certification
I.3.3.1. Le COFRAC [17](aller
sur le site web du COFRAC)
Mis en place en avril 1994 par les pouvoirs publics à l'initiative
de l'ensemble des opérateurs économiques. Conçu en
tous points conforme aux exigences européennes et internationales,
le COFRAC (COmité FRançais d'ACcréditation) permet
aux laboratoires et organismes qu'il accrédite, d'apporter la preuve
de leur compétence et de leur impartialité. Il offre ainsi
aux entreprises, aux consommateurs et aux pouvoirs publics, une réelle
garantie de confiance dans les prestations effectuées par les entités
accréditées. Le COFRAC est une association sans but lucratif
déclarée selon la loi du 1er juillet 1901. Ses
membres peuvent être toutes personnes intéressées par
son activité.
I.3.3.2. Les
organismes certificateurs [1]
A la date du 1er juin 1999, il existe dix organismes certificateurs
de systèmes accrédités par le COFRAC pour la certification
selon les normes ISO 9000 dans le secteur de la santé.
L'annexe A dresse la liste de ces dix organismes.
I.3.3.3.
La procédure de certification [5]
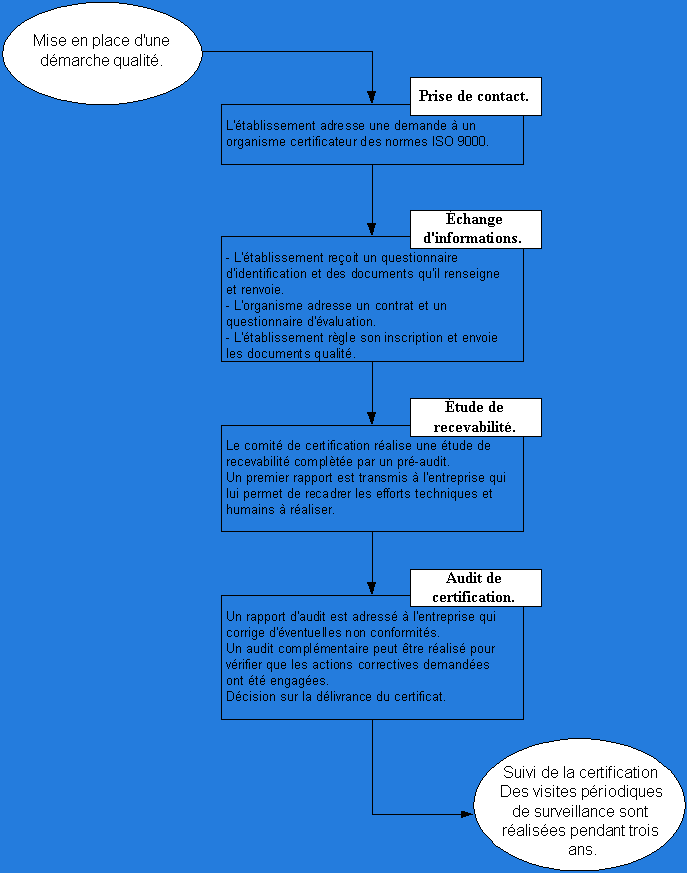
(Retour au sommaire)
I.4.
Comparatif
entre la certification et l'accréditation hospitalière[5]
La certification et l'accréditation hospitalière sont
deux démarches qualité présentent dans les établissements
de santé. Il est donc intéressant de les comparer pour déterminer
l'intérêt de mettre en place une démarche volontaire,
pour répondre à une démarche réglementaire.
I.4.1. Simillitudes
Dans les deux cas, un organisme apporte la preuve que l'établissement
satisfait à un certain nombre d'exigences préalablement établies
Chacune de ces procédures se base sur un référentiel
écrit : manuel qualité pour l'accréditation et norme
ISO 9002 pour la certification. Par ailleurs, la mise en place d'un système
qualité est nécessaire pour répondre aux exigences
du référentiel. Celles-ci ont été élaborées
en consensus avec des professionnels, et sont rédigées sous
forme de textes structurés en référentiels ou chapitres.
Chaque démarche qualité est centrée sur l'organisation
et les pratiques, et non sur le produit fini.
Chaque procédure est mise en place pour satisfaire son client.
L'acte délivré est valable pour une durée limitée
par l'organisme en question, il est renouvelable et peut être sujet
à suspension ou retrait.
Le certificat est donné après audit d'évaluation
réalisé par des experts de l'organisme.
I.4.2. Différences
Les exigences du manuel d'accréditation sont beaucoup plus
détaillées, spécifiques à l'hôpital et
rigides, tandis que la nomme ISO 9002 est applicable à tout secteur
d'activité. Par ailleurs la notion de client est différente
: il s'agit du patient pour l'un, et des services cliniques, économiques
et médico-techniques pour l'autre.
La certification est une démarche volontaire, non obligatoire
et ne concernant qu'une partie de l'établissement, tandis que l'accréditation
revêt l'aspect réglementaire et obligatoire (bien que dans
un premier temps, elle reste encore volontaire jusqu'en avril 2001).
L'accréditation revêt l'aspect national, alors que la
certification est internationale.
Il existe divers degrés d'accréditations tandis que la
certification est accordée ou pas.
La norme ISO 9000 ne fixe aucune règle en ce qui concerne la
gestion des risques alors que le manuel y consacre tout un chapitre : cela
est dû au fait que l'approche ISO 9000 est plus souple. La gestion
des risques existe tout de même à travers la réforme
du matériel et la déclaration des incidents au ministère
(programme de matériovigilance par exemple).
(Retour au sommaire)
II.1.
Bilan
des structures de santé certifiées en Europe
La réalisation d'un bilan des structures de santé certifiées
ISO 9000 en Europe a été effectuée en contactant les
bureaux accréditeurs (équivalent COFRAC) dans dix pays (Espagne,
Allemagne, Suisse, Norvège, Belgique, Pays bas, Angleterre, Italie,
Portugal et Suède).
Trois pays (Espagne, Allemagne, Suisse) ont fourni une liste complète
des organismes certificateur de la norme ISO 9000 dans le secteur de la
santé. Chaque organisme certificateur a alors été
contacté. La moitié des organismes n'ont pas répondu,
ce
bilan donc est loin d'être exhaustif.
La recherche a été arrêtée le 15 décembre
1999.
Bilan en Espagne
Le bureau accréditeur s'appelle ENAC (Entitad Nacional
de Accréditaction), il a accrédité quatre organismes
certifiant la norme ISO 9000 dans le secteur de la santé.
Sur les quatre organismes contactés, un seul a répondu.
Il apparaît que cet organisme a certifié 28 structures
de santé (12 structures privées et 16 structures publiques).
Un certificat couvre souvent plusieurs activités et les services
de soins représentent les activités les plus certifiées.
Par ailleurs, quatre services médicalisés d'urgence et
de réanimation (l'équivalent français du SMUR) ont
été certifiés ISO 9001.
Bilan en Allemagne
Le bureau accréditeur s'appelle TGA (Trägergermeinschaft
für Akkreditierumg Gmgh), il a accrédité 29 organismes
certificateurs. Seul l'organisme DEKRA s'est manifesté. Sur les
43 structures de santé qu'il a certifiées, aucun service
biomédical n'est recensé.
Bilan en Suisse
Le bureau SAS (Suisse Accréditation Service) a accrédité
14 organismes certificateurs.
Ce bureau est le seul en Europe à tenir à jour la liste
des structures certifiées par ses organismes (pourtant cette liste
est obligatoire). D'après le bureau SAS, 109 structures de santé
sont certifiées ISO 9000; aucune ne concerne les services biomédicaux.
Par ailleurs, un organisme certificateur a certifié 2 structures
de santé Hongroise.
Bilan en Italie
Le bureau accréditeur SINCERT (Ente Nazionale Italiabo Di Unlfazione)
n'a pas répondu. Cependant l'association des ingénieurs biomédicaux
Italiens indique qu'il n'y a que le service des ingénieurs de l'hôpital
de Bolzano qui serait certifié ISO 9002.
La Norvège, la Belgique, et les Pays Bas n'ont pas de structures
de santé certifiées ISO 9000. Ces informations ont été
fournies par chaque bureau accréditeur des trois pays.
Les recherches menées pour l'Angleterre, la Suède et
le Portugal n'ont pas abouti.
(Retour au sommaire)
II.2.
Bilan
des structures de santé certifiées en France
II.2.1. Méthodologie
Pour recenser les bureaux certificateurs Français, le COFRAC
a été contacté pour fournir la liste des organismes
certificateurs français de la norme ISO 9000 dans le secteur de
la santé.
Ces organismes ont fourni la liste des structures de santé qu'ils
ont certifiées.
Cette recherche a été arrêtée le 1er
décembre 1999.
L'annexe B dresse la liste de l'ensemble de
ces structures certifiées ISO 9001/2/3
II.2.2. Les organismes
certificateurs
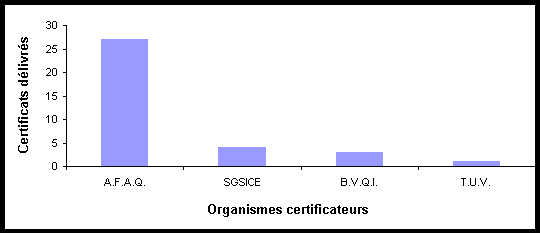
Les organismes certificateurs ont délivrés 35 certificats
ISO 9000 dans le secteur de la santé ; 4 pour la norme
ISO
9001 et 31 pour la norme ISO 9002.
Ce graphique montre que le plus grand nombre de certificats a été
délivré par l'A.F.A.Q. Ceci est certainement dû au
fait qu'il a été le premier bureau certificateur Français.
Il a été délivré 14000 certificats ISO
9000 dont 12000 par l'AFAQ depuis l'adoption par la France des normes ISO
9000.
Aujourd'hui la concurrence s'est organisée et des bureaux, comme
BVQI par exemple, sont de plus en plus sollicités.
II.2.3. Les structures
certifiées
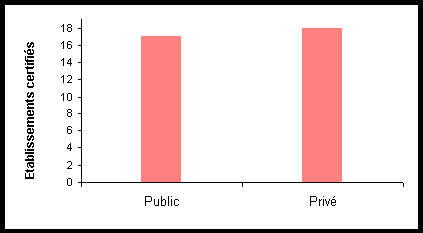
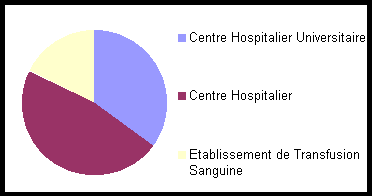
La répartition entre le secteur privé (18 établissements)
et le secteur public (17 établissements) est équitable.
Parmis les 17 établisements publics certifiés ISO 9000,
la taille de la structure n'a pas d'influence.
Par contre, 3 établissements de transfusion sanguine sont certifiés;
ce nombre devrait augmenter dans les années à venir car le
cadre réglementaire les y incite de plus en plus (Cf. chapitre
II.2.4.).
II.2.4. Les activités
certifiées
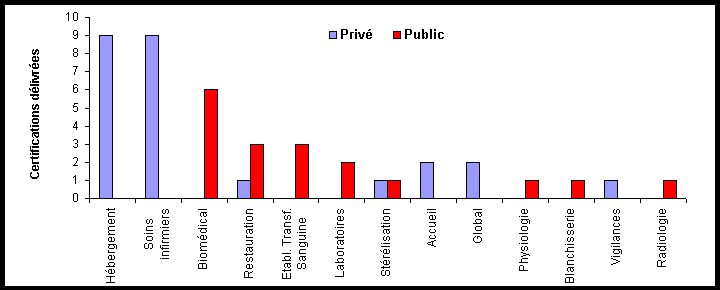
Le secteur privé regroupe souvent plusieurs activités
dans un seul certificat alors que les établissements publics ne
certifient qu'une seule activité. Cela explique que 40% des activités
ont été certifiées dans le secteur public et 60% dans
le secteur privé, alors qu'en fait, le nombre des certificats délivrés
est quasiment le même.
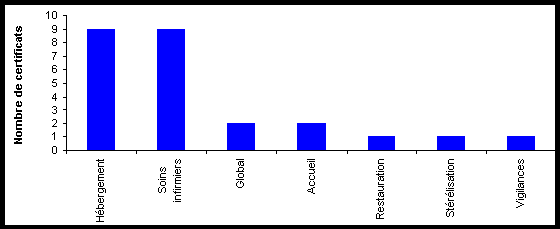
Services certifiés dans les établissements privés
Le secteur privé a principalement certifié des activités
d'hébergement, d'accueil des patients, et d'actes infirmiers. Cela
montre qu'ils ont effectué leur démarche qualité sur
la prise en charge des patients. Comme dans l'industrie, les établissements
de santé privé, utilisent la certification ISO 9000 comme
un argument commercial.
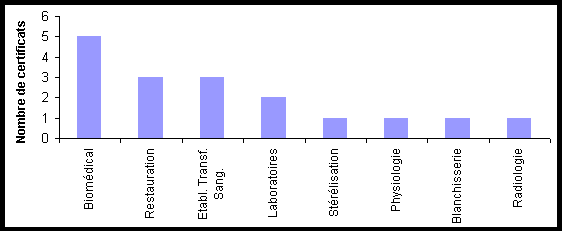
Services certifiés dans les établissements publics
En ce qui concerne le secteur public, ce sont les fonctions logistiques
(biomédical; restauration; stérélisation; blanchisserie)
qui ont été les plus certifiées avec 52% des certificats
(les services Biomédicaux représentent 55% des certificats).
Ceci s'explique par le fait que les services logistiques, notamment
les services biomédicaux sont soumis à la concurrence d'une
part des sociétés de tierce maintenance et d'autre par les
services après vente des fournisseurs, eux même certifiés
ISO 9000. Ainsi, pour qu'un service biomédical réalise une
maintenance sur un dispositif médical fabriqué par un fournisseur
certifié ISO 9000, il s'avère important que le service biomédical
soit lui aussi certifié pour ne pas casser la chaîne de la
qualité.
De plus, les nombreuses contraintes réglementaires apparues
ces dernières années, dans le secteur de la santé,
accentuent la volonté des services biomédicaux à se
faire certifier.
Par ailleurs, trois établissements de transfusion sanguine ont
été certifiés. Cela vient du fait que le législateur
impose au moyen d'une réglementation (loi du 4 janvier 1993), la
mise en þuvre et la formalisation d'une démarche qualité
au sein des établissements de transfusion sanguine. Ces textes sont
largement inspirés des normes ISO 9000.
(Retour au sommaire)
II.3.
Bilan des services Biomédicaux français certifiés
et en cours de certification
II.3.1. Etat des lieux
Au 31 décembre 1999, il y avait six services biomédicaux
certifiés ISO 9002.
|
Centre hospitalier
|
Activité certifiée ISO 9002
|
|
CHU d'Angers
|
Maintenance de dispositifs médicaux non stériles,
tenus en inventaire au service
Biomédical, vérifications de sécurité
et formation des usagers.
|
|
CH de Bourg en bresse
|
Maintenance de dispositifs médicaux non stériles,
tenus en inventaire au service Biomédical, vérifications
de sécurité et formation des usagers.
|
CHU Robert Debré
(AP-HP) Paris
|
Maintenance de dispositifs médicaux non stériles,
tenus en inventaire au service Biomédical, vérifications
de sécurité et formation des usagers.
|
|
CHU de Poitiers
|
Maintenance de dispositifs médicaux non stériles,
tenus en inventaire au service Biomédical, vérifications
de sécurité et formation des usagers.
|
|
CHU de Rouen
|
Maintenance, formation, contrôles électriques
et des générateurs de rayons X
|
|
CH de Versailles
|
L'unité Biomédicale pour ses activités
de maintenance des équipements biomédicaux et la matériovigilance
s'y référant.
|
Les services biomédicaux d'Angers, Bourg en Bresse, Robert Debré
(Paris) et Poitiers se sont lancés la démarche de certification
ISO 9002 dans le cadre d'un Programme Hospitalier de Recherche Clinique
(PHRC) proposé par le ministère de la santé.
De plus, plusieurs services biomédicaux sont en cours de
certification ISO 9002, ce sont:
- CHR de Metz-Thionville
- CH de Béziers
- CH du Havre
- CH de Pau
- CHU de Lariboisière, Paris (AP-HP)
II.3.2. Enquête
|
Objectifs de cette enquête
|
- faire le bilan quantitatif et qualitatif des
services biomédicaux certifiés ISO 9002 et ceux en cours
de certification |
|
Echantillon
|
- les six services biomédicaux certifiés
- les cinq services biomédicaux en cours de certification |
|
Thèmes abordés
|
- Pourquoi une démarche qualité
certifiée ?
- Pré-requis à la démarche
- Sensibilisation investissement
- Mise en place
- Bilan sur la certification
- Point sur la norme ISO 9002 |
|
Type de questionnaire
|
- 1questionnaire rédigé sur feuille
A4 pour les services certifiés
- 1 questionnaire rédigé sur feuille A4 pour les services
en cours de certification
- pour chaque questionnaire : cases à cocher et/ou réflexion
à apporter |
|
Déroulement de l'enquête
|
- envoie des questionnaires le 15 novembre 1999
- date limite pour répondre : 15 décembre 1999
- relance jusqu'au 31 janvier 2000 en cas de non-réponse |
Le résultat de l'enquête est située en annexe
C
II.3.3. Résultat
et interprétation
- Cinq services biomédicaux certifiés sur six
ont répondu.
- Trois services biomédicaux en cours de certification
sur
cinq ont répondu.
Ä Le taux de réponse total
est de 72 %
Voici la synthèse de l'enquête située en annexe
C
|
Thèmes abordés
|
Résultats de l'enquête
|
Pourquoi une
Démarche qualité
certifiée ?
|
La volonté de mettre en
place un système d'assurance qualité certifié vient
uniquement des services biomédicaux. Jamais elle n'est venue de
la direction de l'hôpital. Cette situation est contraire au monde
industriel, où la direction est souvent à la base de la mise
en place d'une certification.
Par ailleurs, les deux principales motivations évoquées
sont d'une part, l'amélioration de l'organisation du travail, et
d'autre part, l'image de marque apportée par la certification ISO
9000.
Cette reconnaissance vise à la fois "les clients"
du service biomédical (service clinique, plateau technique, Direction
...) et les fournisseurs. Ces derniers sont certifiés, cela permet
donc, vis à vis d'eux, une reconnaissance des capacités du
service biomédical (lors des maintenances en contrats partagés
par exemple).
Enfin, les textes réglementaires n'ont pas été
déterminants, mais ont plutôt favorisé la volonté
d'engager une procédure de certification. |
Pré-requis
à la
démarche
|
Aucun service Biomédical
n'avait de système qualité avant de se lancer dans la démarche
de certification. Pourtant la mise en place d'une démarche qualité
devrait être un pré-requis pour démarrer une certification.
Malgré tout, sous la pression réglementaire
et notamment l'arrêté du 03 octobre 1995 sur l'Anesthésie,
les services biomédicaux ont du s'organiser pour mettre en place
des procédures qualité. |
Sensibilisation
Investissement
|
Les équipes biomédicales
se sont investies car la démarche de certification est partie du
service biomédical lui-même, et non de la direction.
De plus, la culture des techniciens leur a permis de comprendre
les intérêts d'une telle démarche. Il est intéressant
de noter qu'une des raisons qui a fait s'intégrer la plupart des
techniciens à la démarche, est que ceux ci auront plus de
responsabilités dans leur travail quotidien. |
Mise en place
|
Les services biomédicaux
certifiés et en cours de certification ont répondu que la
mise en place de la démarche qualité demande "moyennement"
ou "beaucoup" de temps, mais seul un service biomédical l'a quantifié
:
Un service biomédical a placé 0,75 équivalent
temps plein (ETP) technicien pendant 4 mois et 0,5 ETP technicien sur 2
ans.
Dans le cadre du (PHRC) il y a eu 0,5 ETP de technicien
pour coordonner et communiquer les idées des uns et des autres. |
Bilan
sur la
Certification
|
Le retour d'expérience
des services biomédicaux certifiés met en évidence
que le suivi de la certification demande du temps. Mais comme ils en ont
gagné par une meilleure organisation cela ne pénalise pas
leur activité.
Pour les services certifiés la principale amélioration
obtenue est l'organisation (reproductibilié des actes, gestion des
documents, ·). Par contre les objectifs visés concernant la traçabilité
et les indicateurs qualité sont difficiles à obtenir ou à
atteindre.
Aucun service n'a rencontré les mêmes difficultés.
Cela s'explique probablement par le fait que chacun a sa propre organisation
liée à son histoire et à celle de l'établissement
Il est intéressant de remarquer qu'il n'y a pas
de "décalage" entre les attentes des services en cours de certification,
et les résultats obtenus par les structures déjà certifiées. |
Le point
sur la
norme ISO 9000
|
Tous les services estiment que
la norme ISO 9002 est la mieux adaptées et la plus applicable aux
activités biomédicales.
Les points négatifs évoqués à
la démarche ISO 9002 sont identiques à ceux qui sont cités
dans le monde industriel (système rigide et un peu lourd, grand
consommateur de temps, ·). |
Le résultat complet de l'enquête est situé en
annexe
C
(Retour au sommaire)
III.1.
Pourquoi aller jusqu'à la certification ?
La mise en place d'un système qualité au sein du service
biomédical ne doit pas seulement être le résultat des
obligations réglementaires (cf. chapitre
I.1.). En effet, elle doit être motivée par l'ambition
de mettre en place une organisation rigoureuse permettant la reproductibilité
des services rendus aux clients, la traçabilité, ·.
L'assurance qualité permet donc d'assurer la crédibilité
du service biomédical auprès de son établissement,
mais aussi auprès des industriels car il reste une entité
récente et mal définie dans la législation. Le service
met donc en valeur ses activités, ses compétences et sa méthodologie
de travail.
Le service biomédical, par son activité principale qui
est la maintenance, peut être comparé à une société
de prestation de services (comme celles de tierce maintenance), mais en
même temps, elle joue un rôle dans l'amélioration de
la qualité des soins, en s'assurant de la pérennisation de
la conformité des dispositifs médicaux utilisés par
les services cliniques.
Ainsi, La certification du service biomédical est une démarche
pertinente pour l'accréditation de l'établissement, car son
activité est située à l'intersection de ces deux domaines.
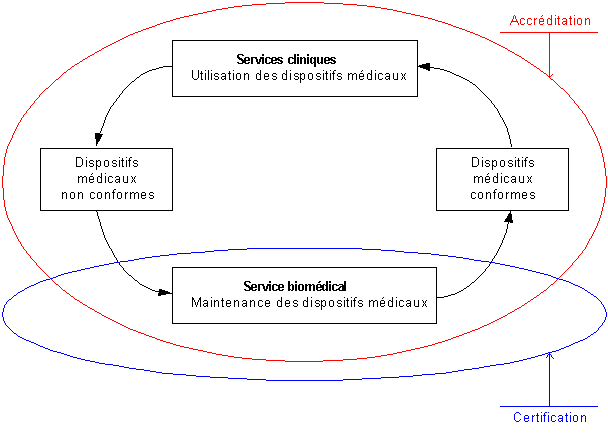
Figure III.1. Intersection entre les domaines d'accréditation
et de certification
La certification est la garantie de la mise en þuvre d'une organisation
adaptée qui formalise les relations internes du type client/fournisseur.
C'est aussi la concrétisation d'une démarche qui prouve la
qualité d'un service vis-à-vis de ses partenaires externes
qui, eux-mêmes, ont été certifié sur le même
référentiel. Les actions de partenariat, de ce fait, devraient
se développer, puisqu'elles reposent sur les mêmes préoccupations
organisationnelles.
Enfin, pour répondre à l'aspect juridique, la certification
apporte une preuve extérieure de la mise en þuvre de moyens pour
répondre à l'obligation de moyens dont sont soumis les centres
hospitaliers.
La certification ISO 9000 semble la mieux adaptée aux activités
biomédicales. Celle ci est applicable dans le domaine de la santé
(cf. chapitre
II) et plus particulièrement pour les services biomédicaux
comme le démontre les acteurs qui se sont lancés dans cette
démarche (Cf. chapitre
III.3.).
(Retour au sommaire)
III.2.
Comparatif entre l'accréditation et la certification
L'objectif consiste à évaluer de façon quantitative
et qualitative l'apport de la norme ISO 9000, pour le service biomédical,
dans la démarche d'accréditation hospitalière.
Un premier travail aura permis de dresser la liste des exigences du
manuel d'accréditation impliquant directement la maintenance biomédicale.
Cette liste a été réalisée en s'appuyant sur
les travaux[11] effectués par Monsieur François
THIBAULT ESTHUA - Angers) et Monsieur Gilbert FARGES (Université
de technologie de Compiègne).
Le manuel d'accréditation n'implique la fonction maintenance que
de manière ponctuelle et parfois à mots cachés. ces
approches ne prennent pas en compte la transversalité de la démarche
d'accréditation qui vise une amélioration qualitative réelle
et continue. Les exigences sur la continuité des soins ou sur l'organisation
des présences ne citent pas la fonction maintenance, alors que cette
activité est essentielle. Cependant, elle est concernée par
de nombreuses de références (cf. annexe
D, un quart implique la maintenance et le plus souvent, elle est l'acteur
principal).
L'ensemble des exigences obtenues a été classé
selon quatre domaines relatifs à l'activité maintenance biomédicale.
Il s'agit :
-
De la maintenance,
-
De la compétence et la formation,
-
De l'analyse des risques,
-
Du système qualité
|
Chapitres
|
Exigences
|
|
Organisation de la maintenance
|
- Coordination de travaux
- Gestion de l'activité, planification, budget
- Maîtrise des achats
- sécurité, implication de la maintenance |
|
Compétence et formation
|
- Description des compétences et des
responsabilités
- Gestion des ressources
- Formation |
|
Analyse des risques
|
- Maîtrise du programme d'analyse des
risques
- Analyse des pratiques et traitement
- Formation en analyse des risques |
|
Système qualité
|
- Description des activités et des liens
- Système d'information et fonction maintenance
- Analyse de la satisfaction du clients et évaluation |
Le second travail a consisté à associer, lorsque cela
était possible, chaque exigences de l'accréditation à
un ou plusieurs chapitres de la norme ISO 9000 (version 1994 et 2000).
L'annexe D présente le tableau
du comparatif réalisé
L'accréditation est plus directive et laisse moins de liberté
d'action que la certification. De ce fait, la souplesse de la démarche
de certification peut amener certains écarts par rapport aux exigences
de l'accréditation. Les notions de matériovigilance, projet
d'établissement, CLIN, ... n'apparaissent évidemment jamais
dans la norme ISO 9000.
L'analyse des exigences de la norme ISO 9000 (version 1994) avec les
exigences du manuel d'accréditation de l'A.N.A.E.S. montre que ces
deux procédures sont en phases et complémentaires. En effet,
peu d'exigences de l'accréditation n'ont pas trouvé d'équivalence
avec la norme ISO 9000. De plus la révision des normes ISO 9000
prévue pour la fin de l'année 2000 réduit encore cet
écart.
Voici un tableau des exigences où l'équivalence a été
difficile à trouver :
|
Exigences de l'accréditation pour le service
biomédical
|
Norme ISO 9000
(version 1994)
|
| Références MEA3 a et b:
L'établissement a une politique de communication interne et externe.
Les orientations du projet d'établissement sont portées à
la connaissance du public et des professionnels |
Aucun chapitre n'aborde cette question. Par
contre la norme ISO 9000 version 2000 l'intègre. |
| Les exigences relatives à la matériovigilance:
Comment doivent-elles être prise en compte pour l'adaptation à
la norme ISO 9000?
- L'incident sur le dispositif médical doit être traité
par une procédure du chapitre 4.9 (maîtrise du processus)
ou
- L'incident est traité par une procédure du chapitre
4.13 (maîtrise du produit fourni par le client) |
- Si l'incident consiste une erreur d'utilisation
d'un dispositif médical, il faut le traiter par une procédure
de non-conformité (chapitre 4.13). La formation à l'utilisation
ou l'évaluation n'a pas été bien faite ou assimilée.
- Si l'incident est dû au dispositif médical lui
même, c'est une procédure de déclaration d'incident
(chapitre 4.9), qui doit être appliquée.
Si la matériovigilance fait partie du champ de certification,
le responsable biomédical devra utiliser ces deux chapitres pour
répondre aux exigences de l'accréditation. |
La fonction maintenance n'est impliquée que de manière
ponctuelle
|
C'est pourquoi les chapitres:
- 4.10 (Contrôle et Essais)
- 4.11 (Maîtrise des équipements de contrôle, de
mesure et d'essai)
n'apparaissent pas. Pourtant ces deux points sont des composantes essentielles
du fonctionnement d'un service biomédical. |
Pas d'équivalence
|
Le chapitre 4.7 (maîtrise du produit fourni
par le client) et le chapitre 4.15 (manutention, stockage, conditionnement,
prévention et livraison) sont, pour un service biomédical,
très liés. Les seuls produits confiés par les clients,
sont les dispositifs médicaux en panne dont la prise en charge est
prévue par le chapitre 4.15. |
(Retour au sommaire)
III.3.
Quelle activité certifier ?
III.3.1.
Les missions d'un services biomédical
Le rôle du service biomédical vis à vis des services
médicaux est de répondre à trois principales demandes
:
· La maintenance des dispositifs
médicaux,
· Lâachat, ou le conseil de
lâachat, des dispositifs médicaux, dâaccessoires et de consommables,
· La formation sur lâutilisation
des dispositifs médicaux,
Pour répondre aux besoins des services cliniques et du plateau
technique, le service biomédical doit quotidiennement être
en relation avec des fournisseurs. Cette relation doit permettre au service
biomédical d'acheter :
-
Des dispositifs médicaux neufs,
-
Des pièces détachées,
-
Des accessoires,
Mais aussi, de bénéficier de prestations de maintenance.
Afin de coordonner les relations avec les services de son établissement
et les fournisseurs, le service biomédical doit sâorganiser autour
de quatre activités :
· La maintenance :
La maintenance biomédicale des dispositifs médicaux fait
généralement appel à deux types de maintenances :
-
La maintenance curative qui est réalisée après
une défaillance,
-
La maintenance préventive qui est effectuée selon
des critères prédéterminés.
Ces deux maintenances peuvent être :
-
Internes, câest à dire faites par le service biomédical
lui-même,
-
Externes, le service biomédical co-traite la maintenance
à une société prestataire de services.
· Les achats :
Le rôle est ici de conseiller et dâeffectuer des achats de dispositifs
médicaux, d'accessoires et de consommables.
· La formation :
Elle doit permettre aux utilisateurs de dispositifs médicaux
d'assurer une bonne utilisation, mais aussi d'entretenir, les dispositifs.
· Le prêt :
L'activité prêt doit permettre au services médicaux
de disposer temporairement d'un dispositif médical, soit pour remplacer
un dispositif qui est immobilisé lors d'une maintenance, soit pour
répondre à une augmentation d'activité.
(Retour au sommaire)
III.3.2. Activité
à certifier
Les six services biomédicaux français ont été
certifiés ISO 9000 pour trois champs d'application différents:
Ä Un domaine technique particulier
qui est :
"Maintenance, formation, contrôles électriques et des générateurs
de rayons X".
Ä La fonction maintenance du
service biomédical vu de deux façons :
- " Maintenance de dispositifs médicaux non stériles,
tenus en inventaire au service Biomédical, vérifications
de sécurité et formation des usagers."
- "L'unité Biomédicale pour ses activités de maintenance
des équipements biomédicaux et la matériovigilance
s'y référant."
Pour répondre aux exigences de l'accréditation, le choix
du domaine d'activité à certifier est important. Ainsi, elle
doit au moins couvrir les deux activités les plus importantes à
savoir la maintenance des dispositifs médicaux et la formation
des
utilisateurs.
L'idéal serait d'inclure toutes les activités c'est à
dire l'achat, la formation, la maintenance, la gestion des prêts,
et la matériovigilance.
Malgré tout, une monté en charge progressive est préconisée.
En effet la certification bouscule les habitudes, de ce fait il faut laisser
le temps aux équipes de s'approprier la démarche pour envisager
une certification couvrant l'ensemble des activités du service biomédical.
Ainsi une première certification pourrait être : " Maintenance
de dispositifs médicaux non stériles, tenus en inventaire
au service Biomédical, vérifications de sécurité
et formation des usagers"
Le rôle de la certification étant l'amélioration
continue, il suffira aux services biomédicaux certifiés d'intégrer
ces missions dans leurs champs d'application :
"achat des dispositifs médicaux non stériles, maintenance
de ces dispositifs, vérification de sécurité, formation
des usagers, matériovigilance et suivi des dispositifs médicaux
en prêt."
Enfin, comme il a été vu au chapitre
III.1., la certification répond à l'obligation de moyen
dont est soumis le centre hospitalier. La description du domaine d'activité
à certifier doit être suffisamment précise pour éviter
toute approximation ou interprétation.
(Retour au sommaire)
CONCLUSION
Les établissements de santé se différencient du
secteur industriel dans leur prise en compte de la qualité.
Les acteurs du domaine de la santé sont face à des contraintes
réglementaires (l'accréditation et de nombreux textes réglementaires).
Cette démarche qualité peut être complétée
par des démarches volontaires pouvant aboutir à la certification.
Le bilan réalisé en novembre 1999 portant sur la certification
ISO 9000 en santé apporte la preuve que cette démarche est
applicable aux établissements de santé quelque soit leur
nature (public ou privé) et leur taille. En effet, 35 certificats
ont été délivrés aussi bien dans le secteur
public que privé.
Cependant, les établissements privés ont principalement
orienté leur certification sur l'accueil et sur l'hébergement
du patient. Comme dans l'industrie, les établissements de santé
utilisent la certification comme un argument commercial.
Dans le secteur public, les fonctions logistiques (biomédicale
-la plus représentée-, restauration, blanchisserie, ·) sont
les plus certifiés. Celles-ci sont soumises à une forte concurrence
externe, elle-même souvent certifiée.
A la différence du secteur industriel, la volonté d'engager
une démarche de certification en santé, part le plus souvent
des services eux-mêmes, et plus rarement de la Direction.
L'enquête menée en décembre 1999 sur la certification
ISO 9000 dans les services biomédicaux a mis en évidence
que six sont certifiés, et qu'au moins cinq sont lancés dans
cette démarche.
Les résultats montrent que ce sont les services eux-mêmes
qui ont voulu mettre en place la certification en vue d'améliorer
leur organisation, et de gagner en crédibilité au sein de
leur établissement et de leurs fournisseurs.
Les équipes biomédicales se sont bien investies malgré
le travail supplémentaire demandé. La principale retombée
est l'amélioration de l'organisation.
L'accréditation ainsi que les nombreux textes réglementaires
incitent les services biomédicaux à démarrer une démarche
qualité. La norme ISO 9000 semble être une réponse
adaptée au service biomédical qui peut être considéré
à l'intersection du domaine de l'accréditation et celui de
la certification. Cependant, cette norme universelle ne peut répondre
entièrement aux exigences très spécifiques de l'accréditation,
de ce fait le service biomédical devra, par ailleurs, s'assurer
de la pertinence du champ de certification.
(Retour au sommaire)
BIBLIOGRAPHIE
[1]
[2]
[3]
[4]
[5]
[6]
[7]
8]
[9]
[10]
[11]
[12]
[13]
[14]
[15]
[16]
[17]
[18]
|
Ouvrages
Mémento pratique de la qualité dans la santé
Quali thème Santé
Editions dpe
Qualité en mouvement
N° 42, novembre et décembre 1999
L'hôpital à l'heure du tournant (p 16 à 39)
E. BALLERY
Les droits du patient à l'hôpital
Que sais-je ?
F. PONCHON
L'assurance Qualité appliquée au domaine biomédical
hospitalier
A.F.I.B. numéro 41
Septembre 1996
Apport d'une démarche qualité de type ISO 9002 au service
biomédical dans le cadre de l'accréditation
DESS "T.B.H.", U.T.C. promotion 1999 - rapport de stage
S. NENNIG
Apport de la certification ISO 9000 d'un service biomédical,
dans la démarche d'accréditation d'un établissement
Mastère "Equipements biomédicaux", U.T.C. promotion 1994
- thèse professionnelle
P. FINET
Manuel d'accréditation des établissements de santé
Version de février 1999
Editions de l'A.N.A.E.S.
Préparer et conduire votre démarche d'accréditation
Guide pratique
Version provisoire - juin 1999
Editions de l'A.N.A.E.S.
Articles "RBM"
Pourquoi et comment se faire certifier ISO 9002 ?
Application à un service biomédical
Première partie (avril 1999, p 48 à 53)
Deuxième partie (juillet 1999, p98 à 110)
M. POMMIER
Apport de la certification ISO 9002 d'un service biomédical,
dans la démarche d'accréditation d'un établissement
Avril 1998, p 37 à 41
P. FINET, Y. DERENNE, C. GROSS, J. JEGU
Accréditation et maintenance biomédicale : outil de
diagnostic
Novembre 1999, p 6 à 8
F. THIBAULT, G. FARGES
Normes
Normes ISO 9000 version 1994
Editions AFNOR
ISO 9001, ISO 9002 et ISO 9003
Normes ISO 9000 version 2000
Editions AFNOR
Avant projet n°2 : Commitee Draft 2
Sites Internet
-
AFNOR : Association Française de NORmalisation
Http://www.afnor.fr
-
AFAQ : Association Française d'Assurance Qualité
Http://www.afaq.org
-
A.N.A.E.S. : Agence Nationale d'Accréditation et d'Evaluation
en Santé
Http://www.anaes.fr
-
COFRAC : COmité FRançais d'ACcréditation
Http://www.cofrac.fr
A.F.S.S.A.P.S. : Agence Française de Sécurité
SAnitaire des Produits de Santé
Http://www.agmed.sante.gouv.fr |
(Retour au sommaire)
ANNEXE A
Organismes certificateurs de systèmes
accrédités par le COFRAC pour la certification selon les
normes ISO 9000 dans le secteur de la santé
AFAQ - Association Française pour l'Assurance
Qualité
116 avenue Aristide Briand
BP 40
92224 Bagneux Cedex
Tél. : 01 46 11 37 37
Fax : 01 46 11 37 77
AFAQ ASCERT INTERNATIONAL
BP 83
92225 Bagneux Cedex
Tél. : 01 46 15 70 60
Fax : 01 46 15 70 69
AOQC MOODY France
89, rue Damrémont
75018 Paris
Tél. : 01 42 54 01 21
Fax : 01 42 54 42 03
ASCII QUALITEM
Cap Vaise
14, rue Gorge de Loup
69009 Lyon
Tél. : 04 78 83 90 00
Fax : 04 78 64 66 30
BVQI FRANCE SA - VERITAS
Le Guillomet
94406 PARIS La Défense cedex
Tél. : 01 41 97 00 60
Fax : 01 41 97 00 65
DNV Certification France
79, rue Jean-Jacques Rousseau
92158 SURESNES cedex
Tél. : 01 42 04 31 31
Fax :01 42 04 07 47
EURO QUALITY SYSTEM France
4, rue de lâAbreuvoir
92415 COURBEVOIE
Tél. : 01 42 42 96 55
Fax :01 47 84 02 74
LCIE - Direction certification
33, avenue du général Leclerc - BP 8
92266 FONTENAY AUX ROSES Cedex
Tél : 01 40 95 60 60
Fax : 01 40 95 86 56
LRQA France SA
Le Danica - 17/19, avenue G. Pompidou
69486 LYON cedex 03
Tél : 04 72 13 31 41
Fax : 04 72 13 31 40
SCGS / ICS SA
6, square Lamartine
94234 CACHAN cedex
Tél. : 01 41 24 87 75
Fax : 01 41 24 86 63
(Retour au sommaire)
ANNEXE B
Liste des établissements de santé
français certifiés par la norme ISO 9000
(à la date du 1er
décembre 1999)
Organisme certificateur : A.F.A.Q.
|
Nom de lâétablissement de santé
certifié
|
Type
dâétablissement
|
Norme
|
Service certifié
|
Description de lâactivité certifiée
|
|
Hôpital Edouard Herriot (LYON)
|
Public
|
9001
|
Laboratoire
|
Recherche sur les tissus cutanés, production
de feuillet épidermique pour le traitement des plaies difficiles.
Réalisation de tests sur des substituts cutanés
|
|
Le Marquisat (SAINT JEAN-31240)
|
Privé
|
9001
|
Soins infirmiers
|
Amélioration et optimisation des processus
hospitaliers. Prestation de soins médicaux chirurgicaux, infirmiers
et rééducation
|
|
Nouvelle clinique de lâUnion (SAINT JEAN-31240)
|
Privé
|
9001
|
Soins infirmiers
|
Amélioration et optimisation des processus
hospitaliers. Prestation de soins médicaux chirurgicaux, infirmiers
et rééducation
|
|
C.H.R. dâOrléans
|
Public
|
9002
|
Laboratoire
|
Réalisation dâanalyses de biologie médicale
par techniques dâimmunologie, de radios immunologie et de biologie moléculaire
(PCR), aide au diagnostic et à la thérapeutique avec à
la disposition de résultats
|
|
E.T.S. de Berry Touraine (TOURS)
|
Public
|
9002
|
E.T.S.
|
Collecte, préparation qualification, contrôle
et distribution de produits sanguins labiles. Réalisation dâanalyses
biologiques, érythrocytaires, leucoplaquettaires et sérologies
virales. Gestion dâune banque de tissus et dâune unité de thérapie
cellulaire. Activité de centre de soins (prélèvements
et transfusion de produits sanguins)
|
|
C.H.U. de Rouen
|
Public
|
9002
|
Restauration
|
Unité de production, distribution et suivi
hôtelier de repas de liaison froide destiné aux services de
soins du C.H.U. et aux hôpitaux de Rouen
|
|
C.H.U. Saint Antoine (PARIS)
|
Public
|
9002
|
Physiologie
|
Exécution dâE.F.R., spirographie, test breucomoteurs,
analyse des gaz du sang, mécanique ventilatoire, capacité
de diffusion du CO, test de marche
|
|
Hôpital Robert Debré (PARIS)
|
Public
|
9002
|
Biomédical
|
Maintenance des dispositifs médicaux non stériles
tenus en inventaire au S.B.M. Vérification de sécurité
et formation des usagers
|
|
C.H. de LENS
|
Public
|
9002
|
Stérilisation
|
Stérilisation et mise à disposition
de linge à usage médical, collecte, stérilisation
et mise à disposition dâinstrumentations réutilisables à
usages médicaux chirurgicales
|
|
C.H.U. dâANGERS
|
Public
|
9002
|
Biomédical
|
Maintenance des dispositifs médicaux non stériles
tenus en inventaire au S.B.M. Vérification de sécurité
et formation des usagers
|
|
C.H.U. dâANGERS
|
Public
|
9002
|
Restauration
|
Elaboration session interne et livraison de repas
à destination du secteur hospitalier. Prestation associée
(Suivi hôtelier)
|
|
C.H.U. de POITIER
|
Public
|
9002
|
Biomédical
|
Maintenance des dispositifs médicaux non stériles
tenus en inventaire au S.B.M. Vérification de sécurité
et formation des usagers
|
|
C.H. de BOURG EN BRESSE
|
Public
|
9002
|
Biomédical
|
Maintenance des dispositifs médicaux non stériles
tenus en inventaire au S.B.M. Vérification de sécurité
et formation des usagers
|
|
E.T.S. (LE MANS)
|
Public
|
9002
|
E.T.S.
|
Collecte, préparation qualification, contrôle
et distribution de produits sanguins labiles. Réalisation dâanalyses
biologiques, érythrocytaires, leucoplaquettaires et sérologies
virales. Gestion dâune banque de tissus et dâune unité de thérapie
cellulaire. Activité de centre de soins (prélèvements
et transfusion de produits sanguins)
|
|
C.H. de MAUX
|
Public
|
9002
|
Blanchisserie
|
Réalisation de prestation de service de la
blanchisserie hospitalière
|
|
Polyclinique Jeanne dâArc (GIEN)
|
Privé
|
9002
|
Hébergement et soins
|
Réalisation de service de soins infirmiers
dâaccueil et dâhotelerie
|
|
Clinique du Parc (CROIX-59000)
|
Privé
|
9002
|
Hébergement et soins
|
Réalisation de service de soins infirmiers
dâaccueil et dâhotelerie
|
|
Centre de Convalescence du Val de Cygne (LABARTHE
SUR LEZE-31860)
|
Privé
|
9002
|
Hébergement et soins
|
Réalisation de service de soins infirmiers
dâaccueil et dâhotelerie
|
|
Le Centre dâHémodialyse Serena (FIGANIERES-83830)
|
Privé
|
9002
|
Hébergement et soins
|
Réalisation de service de soins infirmiers
dâaccueil et dâhotelerie
|
|
Clinique de Sourdille (NANTES)
|
Privé
|
9002
|
Hébergement
|
Prestation de prise en charge de lâentrée
à la sortie du patient le jour de lâintervention au laser Excimer
|
|
Hôpital Américain de PARIS
|
Privé
|
9002
|
Restauration
|
Fabrication, assemblage et vente de plateau de rampas
pour la restauration hospitalière
|
|
Institut Calot (BERCK SUR MER ö 62608)
|
Privé
|
9002
|
Accueil et interprétation
|
Réalisation de prestation de services pour
les actes dâimagerie médicale, diagnostic et interventionel pour
les pathologies de lâappareil locomoteur : prise de rendez-vous, accueil
des patients, réalisation et interprétation et diffusion
|
|
Etablissement Heliot-Marin (BERCK ö 62600)
|
Privé
|
9002
|
Accueil et interprétation
|
Réalisation de prestation de service pour
les actes de scanner : prise de rendez-vous, accueil et réalisation
et interprétation et diffusion des résultats
|
|
Centre médical, chirurgical de la Côte
dâOpal (BOULOGNE 62222)
|
Privé
|
9002
|
Vigilance
|
Sécurité anesthésique, hémovigialnce,
sécurité transfusionnel et gestion du dépôt
de sang, pharmacovigilance et gestion de la pharmacie, matériovigilance,
maintenance et mise à disposition de D.M. et techniques. Décontamination,
nettoyage et stérilisation des matériels de soins et de bloc
opératoire
|
|
Centre de réadaptation cardio vasculaire,
W. Harvey (SAINT MARTIN DâAUBIGNY ö 50190)
|
Privé
|
9002
|
Globale
|
Réalisations de prestation : Animation, accueil,
gestion des séjours, hôtellerie et restauration, maintenance
des locaux, aménagement et entretient des espaces verts, pharmacie,
consultation médicale, actes médicaux ; rééducation
fonctionnelle, soins infirmiers, unité de nutrtion et diététique,
service social
|
|
Clinique Saint Charles (LA ROCHE SUR YON ö 85016)
|
Privé
|
9002
|
Globale
|
Réalisations de prestation de : prise en charge
globale du patient en services de soins (chirurgie, maternité, urgence
et convalescence), service médical technique, hôtellerie et
prestation associées
|
|
Clique Florimond Robertet (BLOIS ö 4100)
|
Privé
|
9002
|
Stérilisation
|
Stérilisation du matériel chirurgical
|
Organisme certificateur : B.V.Q.I.
|
Nom de lâétablissement de santé
certifié
|
Type
dâétablissement
|
Norme
|
Service certifié
|
Description de lâactivité certifiée
|
|
Clinique des Cèdres (GRENOBLE ö38000)
|
Privé
|
9002
|
Soins et herbergement
|
Prestation de soins médicaux(chirurgie, médecine,
obstétrique). Prestations de soins paramédicaux, prestations
associées (pharmacie, restauration, entretien, hotelerie)
|
|
Clinique du Parc (LYON -69006
|
Privé
|
9002
|
Soins et herbergement
|
Prestation de soins médicaux(chirurgie, médecine,
radiologie). Prestations de soins paramédicaux, prestations associées
(pharmacie, restauration, entretien, hotelerie)
|
|
E.T.S. de BLOIS
|
Public
|
9002
|
E.T.S.
|
Examen de laboratoire immuno-hématologique
et distribution de produits sanguins labiles, prélevement, préparation
qualification des dons
|
Organisme certificateur : SGS Internationale certification
|
Nom de lâétablissement de santé
certifié
|
Type
dâétablissement
|
Norme
|
Service certifié
|
Description de lâactivité certifiée
|
|
C.H.U. de RENNES
|
Public
|
9001
|
Radiologie
|
Conception et production dâacte dâimagerie, recherche
appliquée et enseignement
|
|
Centre Chirurgical Saint Gérard (CARPENTRAS
ö 84200)
|
Privé
|
9002
|
Hébergement et soins
|
Accueil, prise en charge du patient (consultation
et admission), herbergement et soins infirmiers, coordinantion de soins
en chirurgie, anesthésie et réanimation
|
|
Polyclinique du Plateau (BEZON ö 95870)
|
Privé
|
9002
|
Hébergement
|
Activité de prise en charge des patients traités
au centre dâhémodialyse
|
|
C.H. V. Dupouy
|
Public
|
9002
|
Restauration
|
Elaboration et livraison de repas en liaison froide
en C.H. et maison de retraite
|
Organisme certificateur : T.U.V.
|
Nom de lâétablissement de santé
certifié
|
Type
dâétablissement
|
Norme
|
Service certifié
|
Description de lâactivité certifiée
|
|
C.H. VERSAILLE
|
Public
|
9002
|
Biomédical
|
Maintenance des équipements biomédicaux
et la maintenance sây référent
|
(Retour au sommaire)
ANNEXE
C
Résultats du questionnaire des services
biomédicaux
certifiés ISO 9002 et ceux en cours
Pourquoi une démarche qualité certifiée
?
(Q1) Qui a eu l'initiative de la démarche
ISO 9002 ?
-
[La direction : 0 réponse]
-
Le service biomédical : 8 réponses
(Q2) Quelles ont été les trois principales
motivations pour mettre en place cette démarche ?
- Amélioration de la façon de travailler
- Meilleure image de marque
- Organisation optimisée
(Q3) La réglementation (accréditation,
...) a constitué un élément :
- [Très important : 0 réponse]
- Plutôt important : 5 réponses
- Peu important : 2 réponses
- Pas du tout important : 1 réponse
Pré-requis à la démarche
(Q4) Avant de décider la mise en route
d'une démarche ISO 9002, aviez vous un système qualité
?
- [OUI : 0 réponse]
- NON : 8 réponses
Sensibilisation et investissement
(Q5) Comment l'équipe Biomédicale
a-t-elle accueilli cette démarche ?
- Très bien : 2 réponses
- Plutôt bien : 6 réponses
- [Plutôt mal : 0 réponse]
- [Très mal : 0 réponse]
(Q6) A l'état actuel d'avancement, l'équipe
s'est-elle investie en totalité ?
- OUI : 5 réponses
- NON : 3 réponses
Si non pensez-vous pouvoir faire s'investir
toute l'équipe ?
- OUI : 2 réponses
- NON : 1 réponse (il reste à convaincre 2 personnes
sur 6)
Mise en place
(Q7) Le temps consacré à la mise
en place de la démarche ISO 9002 pénalise-t-il l'activité
Biomédicale ?
- beaucoup : 2 réponses
- Moyennement : 4 réponses
- Très peu : 2 réponses
- [Pas du tout : 0 réponse]
Quantifier le temps de mise en place :
Un service biomédical a placé 0,75 équivalent
temps plein (ETP) technicien pendant 4 mois et 0,5 ETP technicien sur 2
ans.
Dans le cadre du (PHRC) il y a eu 0,5 ETP de technicien pour coordonner
et communiquer les idées des uns et des autres.
Estimez si possible le temps perdu ou gagné
en routine ?
(seulement pour les services biomédicaux
certifiés)
- Gagné : 1 réponse
- Pas de perte de temps : 5 réponses
(Q8) quels chapitres de l'adaptation ISO 9002
ont posé des problèmes ?
(seulement pour les services biomédicaux
certifiés)
- Maîtrise du produit fourni par le client - Revue de contrat
- Action corrective et préventive - Contrôles et essais
- Audit qualité interne - Formation
- Responsabilité de la direction - Enregistrement des non-conformités
- Relation client/fournisseur
Bilan sur la certification
Questions posées seulement aux services
biomédicaux en cours de certification :
(Q8) Quelles sont les trois principales améliorations
souhaitées grâce à la certification ISO 9002 ?
- Meilleure organisation
- Traçabilité
- Maîtrise des coûts
(Q9) Pensez-vous que cette norme améliorera
la qualité du travail ?
- OUI : 2 réponses
- NON : 1 réponse
(Q10) Pensez-vous que cette norme améliorera
l'organisation du service biomédical ?
- OUI : 3 réponses
- [NON : 0 réponse]
Questions seulement pour les services biomédicaux
certifiés :
(Q9) Quelles sont les trois principales améliorations
obtenues grâce à la certification ?
- Meilleure traçabilité
- Meilleure image du service
- Amélioration de l'organisation
(Q10) La certification a-t-elle répondu
à vos attentes ?
-Très bien : 2 réponses
- Plutôt bien : 3 réponses
- [Plutôt mal : 0 réponse]
- [Très mal : 0 réponse]
Citez trois améliorations attendues qui
n'ont pas été atteintes
- Les objectifs et les priorités restent très difficile à
respecter
- La traçabilité est moyenne malgré la G.M.A.O.
- Les indicateurs d'amélioration de la satisfaction des clients
sont difficiles à trouver
(Q11) Cette norme a-t-elle amélioré
la qualité du travail ?
- OUI : 5 réponses
- [NON : 0 réponse]
(Q12) Cette norme a-t-elle amélioré
l'organisation du service biomédical ?
- OUI : 5 réponses
- [NON : 0 réponse]
Point sur la norme ISO 9002
(Q11) L'ISO 9002 est elle la norme la mieux adaptée
au service biomédical ?
OUI : 8 réponses
[NON : 0 réponse]
(Q12) connaissez-vous d'autres normes adaptées
au service biomédical ?
[OUI : 0 réponse]
NON : 8réponses
(Q13) Avez-vous envisagé l'adaptation de
la norme ISO 9000 version 2000 ?
OUI : 7 réponses
NON : 1 réponse
(Q14) Si vous deviez donner au moins trois points
négatifs à la démarche ISO 9002 lesquels seraient-ils
?
- Le système mis en place est rigide et un peu lourd
- La certification ISO 9002 est un grand consommateur de temps ingénieur
- La notion de "toujours plus" n'est pas évidente à gérer
avec les contraintes (réglementaires, économiques, ...) quotidiennes.
(Retour au sommaire)
ANNEXE D
Tableau de comparaison entre
les exigences de l'accréditation
et la norme ISO 9000
Organisation de la maintenance
|
Référence
|
Manuel d'accréditation
(Version de février 1999)
|
Norme ISO 9000
(version de 1994)
|
N°
Chapitre
|
|
OPC 7e
|
La continuité des soins est assurée
entre secteurs dâactivité.
|
Le système d'information sera la colonne vertébrale
de la continuité des soins
|
4.2
4.1.2
|
|
OPC 7b
|
Des règles de présence, de concertation
et de délégation, ainsi quâun système de gardes et
astreintes sont mis en place afin dâassurer la permanence 24 h/24 h.
|
Un système de garde par secteur d'activité
est en place et tous les personnels concernés y participe
|
4.2
|
|
MEA 6a
|
Les objectifs et les types de prestations fournies
par chaque secteur dâactivité sont clairement définis en
cohérence avec le projet dâétablissement et font lâobjet
dâun suivi et dâun bilan annuel
|
Définir les relations entre les différents
services client / fournisseur
|
4.1.1
4.20
|
|
MEA 6b
|
Un mode de concertation entre les professionnels
est en place dans chaque secteur dâactivité en vue de favoriser
lâexpression et la recherche de solutions aux problèmes posés
|
La définition écrite des missions de
chacun évite conflit, perte de temps, erreurs
|
4.17
4.1.2
|
|
MEA 6c
|
Chaque secteur dâactivité sâorganise pour
assurer une prise en charge continue du patient. Des règles de présence
de tous les professionnels, de concertation et de délégation,
sont élaborées et un système de gardes et dâastreintes
est mis en place
|
Des profils et fiches de poste doivent être
rédigé et connu de tous les personnels
|
4.12
|
|
MEA 8a
|
Le responsable du secteur dâactivité connaît
les coûts de fonctionnement de son secteur dâactivité et sa
situation par rapport aux ressources allouées
|
Pas de correspondance
|
|
|
MEA 5
|
Lâétablissement a des outils de pilotage de
sa gestion permettant lâimplication des secteurs dâactivité
|
Pas de correspondance
|
|
|
GFL 2b
|
Une politique de maintenance est définie
|
La politique sera en accord avec les objectifs défini
dans la politique qualité
|
4.1.1
|
|
GFL 2c
|
Une maintenance préventive est assurée
|
Toutes les procédures ayant une influence
sur la qualité finale du service doivent être identifiées,
mise en þuvre dans des conditions maîtrisées et conformes
à la réglementation en vigueur
|
4.9
|
|
GFL 2d
|
Une maintenance curative est assurée
(lire : maintenance corrective)
|
Toutes les procédures ayant une influence
sur la qualité finale du service doivent être identifiées,
mise en þuvre dans des conditions maîtrisées et conformes
à la réglementation en vigueur
|
4.9
|
|
QPR 3c
|
Les secteurs dâactivité élaborent des
protocoles dans les domaines où ils sont utiles
|
Procédures pour les pratiques qui sont susceptible
d'entraîner une incidence néfaste pour la qualité du
service
|
4.9
|
|
QPR 3f
|
La gestion des documents internes (procédures,
protocoles) et externes (textes réglementaires, recommandations
professionnelles, etc.) est organisée
|
Les documents seront répertoriés et
gérés de manière cohérente selon des procédures
appropriées
|
4.5
|
|
GFL 2e
|
Des protocoles dâalerte et dâintervention sont écrits
et connus des personnels concernés
|
Une procédure de demande d'intervention est
réalisée.
Elle est évaluée
|
4.9
|
|
GFL 1b
|
Les personnels utilisateurs sont associés
aux procédures dâachat
|
Les achats doivent tenir compte des exigences des
utilisateurs
|
4.6
|
|
GFL 1a
|
Les besoins (équipements, consommables..)
sont évalués sur le plan quantitatif et sur le plan qualitatif
|
Le consommable, le matériel nécessaire,
les logiciels, la maintenance sont étudiés sur tous les plans
à l'achat
|
4.6
|
|
VST 2c
|
La traçabilité des produits et dispositifs
médicaux est assurée
|
Une procédure est écrite pour la tracabilité
de la réception à la réforme de l'équipement
|
4.16
4.8
4.15
|
|
GRH 10a
|
Les conditions de travail sont évaluées
à périodicité définie
|
Les audits tiennent compte des moyens et des conditions
de travail
|
4.1.2.2
4.17
|
|
GRH 10b
|
Un plan annuel dâamélioration des conditions
de travail est mis en þuvre, suivi et évalué
|
Les actions correctives et leur suivi y répond
|
4.1.2.2
4.14
|
Compétence et formation
|
Référence
|
Manuel d'accréditation
(Version de février 1999)
|
Norme ISO 9000
(version de 1994)
|
N°
Chapitre
|
|
MEA 2a
|
Lâorganigramme fonctionnel de la direction est défini
et connu des professionnels.
|
L'organigramme existe et est communiqué
Le manuel d'assurance qualité l'intègre
|
4.1.2.1
4.2
|
|
MEA 7a
|
La structure organisationnelle des secteurs dâactivité
est connue des professionnels
|
Elle existe et elle est communiquée
Le manuel d'assurance qualité l'intègre
|
4.1.2.1
4.2
|
|
MEA 7b
|
Les compétences et les domaines de responsabilité
des responsables des secteurs dâactivité et de lâencadrement sont
clairement définis et écrits
|
L'organigramme est complété par les
profils et fiches de postes
|
4.1.2.1
|
|
GRH 4c
|
Une description actualisée des fiches de fonction
et des profils de poste est effectuée. Les responsabilités
et les exigences de tout poste font lâobjet dâun document écrit
et communiqué
|
L'organigramme est complété par les
profils et fiches de postes
|
4.1.2
|
|
GRH 4a
|
Lâétablissement met en þuvre une gestion prévisionnelle
des ressources humaines
|
Les audits qualité intègrent l'adéquation
de compétences
|
4.1.2.2
4.17
4.1.3
|
|
MEA 8b
|
Le responsable du secteur dâactivité connaît
les compétences de son personnel et utilise ces informations pour
une gestion prévisionnelle
|
Les audits qualité intègrent l'adéquation
de compétences
|
4.1.2.2
4.17
4.1.3
|
|
GRH 4b
|
La gestion prévisionnelle des ressources humaines
permet dâassurer les prestations de soins selon les exigences des postes,
lâévaluation de la charge de travail, les nécessités
de remplacement et les compétences du personnel
|
Les audits qualité intègrent l'adéquation
de compétences
|
4.1.2.2
4.17
4.1.3
|
|
GRH 7b
|
Les besoins individuels en formation sont identifiés
|
L'identification des besoins individuels est faite
|
4.18
|
|
GRH 7c
|
Des objectifs sont fixés pour lâannée
suivante (pour la gestion des ressources humaines)
|
Des actions correctives sont mises en évidences
à la suite d'audit interne
|
4.1.2.2
4.1.3
4.17
|
|
GRH 5a
|
Le recrutement est effectué sur la base des
profils de poste
|
Les fiches de postes existantes servent de base au
recrutement
|
4.1.2
|
|
GRH 6a
|
La mission, le plan stratégique, les secteurs
dâactivité, lâorganisation, le fonctionnement et la gestion de lâinformation
de lâétablissement sont présentés à tout professionnel
ou stagiaire
|
Une journée des nouveaux agents est organisée
trimestriellement
|
4.2
|
|
GRH 6b
|
Dans chaque secteur, une information dâadaptation
au poste est fournie à tout professionnel, concernant les exigences
en matière de sécurité, le contrôle et la prévention
du risque infectieux et les stratégies dâamélioration de
la qualité des soins
|
Le service biomédical est formé au
risque infectieux par le CLIN
|
4.18
|
|
GFL 7b
|
Le personnel chargé de lâélimination
des déchets est formé
|
Le service biomédical est formé au
risque infectieux par le CLIN
|
4.18
|
|
VST 3b
|
Les professionnels sont formés sur les conduites
à tenir en cas dâincident (risques infectieux et transfusionnels)
|
Le personnel biomédical est formé et
applique les procédures en cas d'incident
|
4.18
4.9
|
|
GRH 8a
|
Les besoins des personnels en matière de formation
continue sont identifiés
|
Le responsable biomédical applique les procédures
d'identification des besoins en formation
|
4.18
|
|
GRH 8b
|
Un programme de maintien et dâamélioration
du niveau de compétence adapté aux besoins identifiés
des personnels de lâétablissement est mis en place
|
La direction donne les moyens d'appliquer le plan
de formation basé sur le chapitre 4.18
|
4.1.2.2
|
Analyse des risques
|
Référence
|
Manuel d'accréditation
(Version de février 1999)
|
Norme ISO 9000
(version de 1994)
|
N°
Chapitre
|
|
SPI 2b
|
Les modalités de mise en þuvre du programme
de lutte contre le risque infectieux permettent de garantir la coordination
des actions menées par les professionnels ou secteurs dâactivité.
Une définition des responsabilités, connue de tous, est élaborée
|
Le personnel biomédical connaît et applique
les procédures contre les risques infectieux
|
4.9
|
|
VST 2b
|
Les procédures à mettre en þuvre en
cas dâincident sont en place et connues des professionnels (pour le
risque infectieux)
|
Le personnel biomédical connaît et applique
les procédures contre les risques infectieux
|
4.9
|
|
SPI 5a
|
Des protocoles visant à maîtriser le
risque infectieux sont utilisés
|
Le personnel biomédical connaît et applique
les procédures contre les risques infectieux
|
4.9
|
|
VST 2d
|
Une organisation permettant de répondre à
une alerte sanitaire concernant les produits et dispositifs médicaux
à usage thérapeutique est en place.
|
Les procédures relatives à la matériovigilance
sont appliquées
|
4.9
|
|
VST 2e
|
Le système de vigilance alimente une réflexion
permettant lâamélioration des pratiques professionnelles quant à
lâusage des produits et dispositifs médicaux.
|
Les procédures de matériovigilance
intègrent l'expertise des incidents et la formation des utilisateurs
|
4.9
4.18
|
|
GFL 9d
|
Les protocoles dâalerte et les mesures à prendre
en cas dâincendie sont écrits et connus de tous les professionnels
|
Le personnel biomédical est formé
|
4.18
|
|
GFL 7a
|
Chaque catégorie de déchet est traitée
de façon adaptée
|
Le personnel biomédical connaît les
procédures et les applique
|
4.9
|
|
GFL 7c
|
Lâélimination des déchets est évaluée
à périodicité définie
|
Des audits qualité interne le vérifie
|
4.17
|
|
QPR 4d
|
Les secteurs, pratiques, actes ou processus à
risque sont identifiés et font lâobjet dâactions prioritaires dans
le programme de prévention des risques
|
Le service biomédical réalise des procédures
d'analyse des risques sur les dispositifs médicaux
|
4.13
4.16
4.9
|
|
QPR 4a
|
Les informations disponibles relatives aux risques
et aux événements indésirables sont rassemblées
|
Enregistrement de non conformité
|
4.16
|
|
QPR 4b
|
Un système de signalement des événements
indésirables est en place
|
Procédure matériovigilance
Traitement des non conformités
|
4.9
4.13
|
|
SPI 8b
|
Des procédures dâentretien (nettoyage, désinfection)
des équipements et dispositifs médicaux non stérilisables
sont écrites, validées et mises en þ uvre par du personnel
formé. Leurs respect et pertinence sont évalués à
périodicité définie
|
Le personnel biomédical les appliquent et
les audits internes les évalues
|
4.9
4.17
|
|
SPI 7c
|
Lâensemble des professionnels est immunisé
contre certains risques spécifiques liés à lâexercice
en établissement de santé
|
Pas de correspondance
|
|
|
SPI 7d
|
Des actions sont menées pour prévenir
les risques de contamination liés à lâexercice professionnel
|
Le personnel biomédical applique les procédures
|
4.9
|
|
QPR 1f
|
La formation des professionnels de lâétablissement
et lâassistance méthodologique sont assurées pour la prévention
des risques
|
Le personnel biomédical est formé
|
4.18
|
|
SPI 2d
|
Une formation en hygiène est dispensée
à tout professionnel temporaire ou permanent lors de son arrivée
|
Les stagiaires et intérimaires y participe
|
4.18
|
|
SPI 2e
|
Les actions de formation continue en hygiène
concernent lâensemble des professionnels, notamment lors de la diffusion
de nouvelles procédures
|
Le personnel y participe
|
4.18
|
|
SPI 9b
|
Les procédures font lâobjet dâune formation
des professionnels (maîtrise du risque infectieux)
|
Le personnel y participe
|
4.18
|
|
GFL 5b
|
Le personnel chargé du nettoyage des locaux
et des équipements est formé
|
Le personnel biomédical est formé et
applique les procédures
|
4.18
4.9
|
|
GFL 9c
|
Les professionnels bénéficient dâune
formation incendie actualisée
|
Le personnel biomédical est formé et
applique les procédures
|
4.18
4.9
|
Système qualité
|
Référence
|
Manuel d'accréditation
(Version de février 1999)
|
Norme ISO 9000
(version de 1994)
|
N°
Chapitre
|
|
QPR 1a
|
La politique qualité par la direction en concertation
avec la CME, la DSSI ou le responsable du service de soins infirmiers,
le CTE, ou structure équivalente, et le personnel
|
Le directeur est signataire de l'engagement et des
objectifs de la qualité au service biomédical
Ils sont connus du personnel biomédical
|
4.1
|
|
QPR 1b
|
La politique qualité comporte des objectifs
précis, mesurables dans le temps, traduits dans le programme de
gestion de la qualité et de prévention des risques.
|
Le service biomédical connaît les objectifs
et participe à la définition de ceux ci
|
4.1.1
4.20
|
|
QPR 1b
|
La politique qualité comporte des objectifs
précis, mesurables dans le temps, traduits dans le programme de
gestion de la qualité et de prévention des risques.
|
Le service biomédical connaît les objectifs
et participe à la définition de ceux ci
|
4.1.1
4.20
|
|
QPR 1e
|
Les responsabilités concernant la gestion
de la qualité et la prévention des risques sont identifiées
|
Les fiches de poste précisent tous ses éléments
|
4.1.2.3
|
|
QPR 3b
|
Des démarches qualités sont en cours
sur des thèmes prioritaires
|
Pas de correspondance
|
|
|
QPR 3b
|
Les actions (qualité) sont conduites
par les professionnels de manière multidisciplinaire
|
Chaque membre du service biomédical peut y
être impliqué
|
4.2
|
|
QPR3d
|
Les secteurs dâactivité évaluent lâutilisation
des protocoles de gestion des plaintes et des réclamations
|
Audit interne en liaison avec le traitement des non
conformités
|
4.17
4.13
|
|
QPR 3e
|
Des indicateurs de résultats sâintégrant
dans la démarche dâamélioration continue de la qualité
sont élaborés
|
Le service biomédical suit les indicateurs
en place
|
4.20
|
|
MEA 3a
|
Lâétablissement a une politique de communication
interne et externe.
|
Pas de correspondance
|
|
|
MEA 3b
|
Les orientations du projet dâétablissement
sont portées à la connaissance du public et des professionnels.
|
Pas de correspondance
|
|
|
GSI 1a
|
Le système d'information et l'informatisation
de lâétablissement sont fondés sur un schéma directeur,
cohérent avec le projet dâétablissement et élaboré
de manière participative
|
Pas de correspondance
|
|
|
GSI 1b
|
Le système dâinformation couvre lâensemble
des activités de lâétablissement et favorise une approche
et une utilisation coordonnées et efficaces de lâinformation, notamment
pour la politique dâévaluation
|
Pas de correspondance
|
|
|
GSI 1c
|
Les instances concernées sont impliquées
dans le suivi du schéma directeur de lâinformation
|
Pas de correspondance
|
|
|
MEA 9a
|
Des objectifs quantifiables sont définis et
font lâobjet dâune actualisation annuelle
|
La direction de la qualité définit
et écrit sa politique qualité
|
4.1.1
|
|
MEA 9b
|
Le suivi des objectifs fait lâobjet dâune communication
à lâétablissement et aux secteurs dâactivité concernés
|
La revue de direction est effectuée et la
direction communique
|
4.1.3
|
|
QPR 2d
|
Un système de gestion des réclamations
et/ou plaintes est en place et permet leur analyse et la mise en þuvre
des mesures dâamélioration appropriées
|
Les procédures de traitement des non conformités
sont mise en þuvre
|
4.13
|
|
DIP 8c
|
Toutes les plaintes des patients sont analysées
et ont une réponse.
|
Des procédures de traitement de non conformité
existent
|
4.13
|
|
DIP 8d
|
Les secteurs dâactivité concernés sont
tenus informés de tout contentieux avec un patient.
|
Des procédures de traitement de non conformité
existent
|
4.13
|
|
MEA 7c
|
Les responsables des secteurs dâactivité sâassurent
de la mesure, de lâévaluation et de lâamélioration de lâensemble
des activités, et en particulier du bon déroulement des démarches
dâamélioration continue de la qualité
|
Le responsable du service biomédical est un
animateur de la qualité pour le service
|
4.1.2.3.
|
|
GSI 4b
|
Les dysfonctionnements du système dâinformation
sont recensés, analysés et traités
|
Pas de correspondance
|
|
|
GSI 4c
|
Un plan dâamélioration de la qualité
du système dâinformation, aux priorités hiérarchisées
et auquel participent les professionnels utilisateurs, est en place
|
Pas de correspondance
|
|
|
QPR 2c
|
Les informations recueillies sont exploitées
et utilisées pour définir ou adapter le programme de gestion
de la qualité dans lâobjectif dâune amélioration du service
rendu
|
La revue de Direction les appliquera pour améliorer
le service rendu
|
4.1.3
|
| QPR 2b |
Les informations recueillies sont diffusées
aux professionnels (concernant la satisfaction clients)
|
Les résultats des revues de contrats sont
communiqués à tous les professionnels
|
4.3
|
|
QPR 5a
|
Lâefficacité du programme de gestion de la
qualité est évaluée
|
C'est le rôle de la revue de direction
|
4.1.3
|
|
QPR 5b
|
Lâefficacité du programme de prévention
des risques est évaluée
|
C'est le rôle de la revue de direction
|
4.1.3
|
|
GFL 10
|
Une évaluation des prestations logistiques
est réalisée auprès des secteurs dâactivité
utilisateurs
|
Régulièrement, il faut vérifier
que le service offert est toujours en adéquation avec les besoins
du client
|
4.3
|
|
QPR 5c
|
Le fonctionnement du système de signalement
des événements indésirables est évalué
|
Un audit interne est effectué pour évaluer
les procédures de matériovigilance
|
4.17
|
(Retour au sommaire)
(Retour au début de la présentation)











