CONCLUSION
BIBLIOGRAPHIE
-
Devant l'augmentation des dépenses de
santé, l'hôpital est considéré comme
une structure de production soumise à des règles de
gestion strictes. L'objectif est d'éviter de rationner la
santé et de produire des soins à un coût
moindre. En matière de gestion globale des
équipements hospitaliers, l'ingénieur
biomédical doit de façon urgente optimiser tous les
aspects liés à ces investissements de la
planification à la mise en service en passant par la
fonction maintenance. L'intégration de
l'électronique dans les équipements
biomédicaux entraîne un besoin urgent de
fiabilité. Il lui faudra essayer de trouver un compromis
entre innovation et rigueur en adaptant de nombreux concepts,
règles et méthodes de maintenance industrielle en
milieu hospitalier.
Dans cette optique, nous vous présenterons un
outil de la qualité "la méthode
d'échantillonnage" jusqu'à lors méconnue des
services biomédicaux malgré son intérêt
suite à une bonne exploitation.
Notre travail apportera les premiers
éléments indispensable de base pour mettre en
application cette méthodologie au sein d'un service
biomédical. Cependant, compte tenu du temps imparti pour
réfléchir sur ce sujet, nous ne pourrons pas
approfondir les applications mathématiques et statistiques
(ce qui fera l'objet d'une prochaine étude).
(retour sommaire)
|
I) L'échantillonnage : outil de la
qualité
|
1)
Définition:
On appelle échantillonnage le
prélèvement d'échantillons. Un
échantillon de taille n est une liste de n individus
(X1,...,Xn) extraits de la
population-mère.
Le rapport t de l'effectif n de l'échantillon
à l'effectif N de la population, dans laquelle il a
été prélevé, est appelé taux
d'échantillonnage ou fraction de sondage: t = n/N
L'échantillonnage est une technique
d'amélioration de la qualité au même titre que
les 7 outils de la qualité (le diagramme causes-effets, les
graphiques, les histogrammes, les feuilles de relevées de
données....), les méthodes statistiques (essais et
estimation, analyse de la corrélation...) et bien
d'autres.
ý Cette
technique peut être performante si elle est utilisée
dans un but précis afin de pouvoir analyser correctement
les informations qu'elle génère et tirer des
conclusions objectives
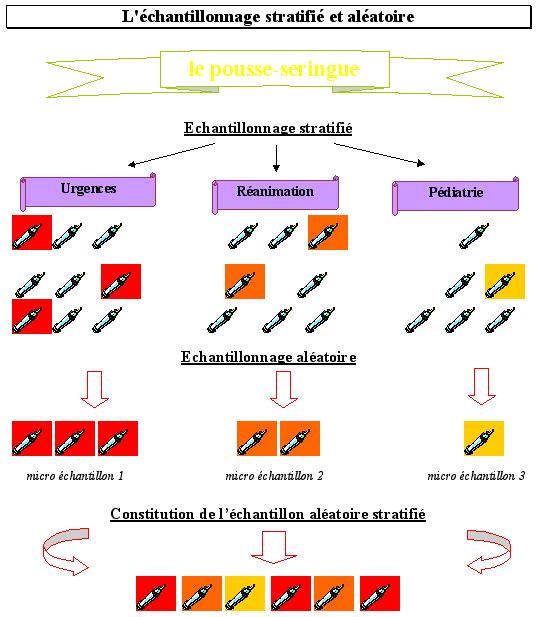
2) Domaine
d'application
A l'hôpital, on s'intéressera aux
équipements présents en grand nombre. Il s'agira
d'équipements électroniques ou informatiques peu
complexes ( pousse-seringues, manomètres,....).
3)
Intérêt du procédé dans un service
biomédical
L'une des fonctions de l'ingénieur
biomédical est d'assurer pour chaque dispositif
médical un niveau de sécurité et de
fonctionnalité pendant la phase d'utilisation avec la
meilleure disponibilité. Dans le cadre d'un contrôle
qualité, l'idéal serait de suivre les prescriptions
du constructeur en matière de maintenance préventive
pour chaque dispositif. Cependant, dans beaucoup de
problèmes pratiques, il n'est pas possible d'analyser
l'ensemble de la population pour connaître le comportement
des variables étudiées. Il suffira de
l'étudier à partir d'un échantillon
représentatif. L'utilisateur, qui veut un coût
raisonnable, mais aussi une disponibilité et des
performances élevées, devra donc accepter un
compromis technico-économique.
Le rôle de l'ingénieur biomédical
consistera à faire une estimation à partir des
résultats obtenus sur un échantillon
d'équipements suivant un niveau de qualité
acceptable et d'extrapoler sur l'ensemble de la population
d'équipements dans laquelle a été
prélevé l'échantillon.
(retour sommaire)
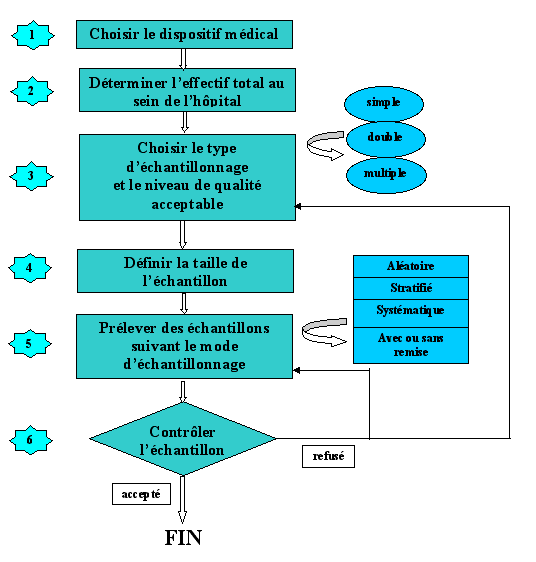
4)
La méthode d'échantillonnage
- 4.1) Les
différentes étapes
(retour
sommaire)
-
4.2)
Constitution et taille de l'échantillon à
prélever
- 4.2.1)
La taille de l'échantillon
La taille de l'échantillon sera d'autant
plus grande que la population manque
d'homogénéité.
Pour déterminer la taille de
l'échantillon, on pourra adopter une méthode
utilisée dans l'industrie.
Il suffira simplement de suivre la
procédure suivante:
Le principe consiste à
déterminer:
- - l'effectif total N de la population que l'on
souhaite échantillonner
- le niveau de criticité du dispositif
médical (I faible, II normal ou III
élevée) : c'est l'attention qu'il
convient d'accorder à une défaillance
donnée considérant sa probabilité
d'apparition et la gravité de ses
conséquences ( l'objectif est de garantir la
sécurité des patients, d'éviter les
dommages ou les pertes indirectes, et de garantir la
disponibilité du service).
Quelques exemples :
-
|
Niveau
I
:
criticité
faible
|
Niveau
II
:
criticité
normale
|
Niveau
III
:
criticité
élevée
|
|
Tensiomètres
|
Monitorings
|
Pousse-seringues
|
- Criticité faible : Pas d'interaction
sur le patient
- Criticité normale : Interaction
sur la qualité du service mais pas sur le
patient
- Criticité élevée :
Interaction directe sur le patient
- (retour sommaire)
-
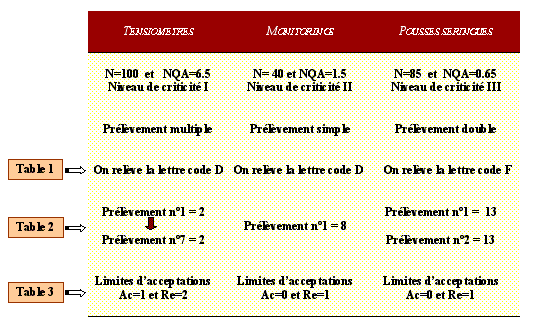
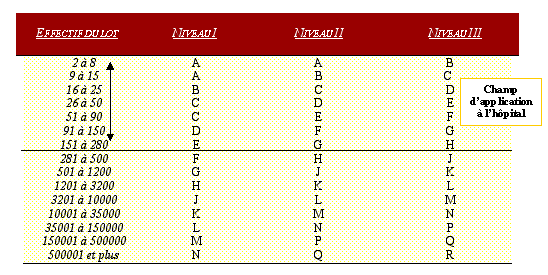
Suivant l'effectif du lot et le niveau de
criticité du dispositif médical, on
déterminera (via la table 1) une lettre
code :
Table 1:
(utilisable pour les
dispositifs médicaux et les
consommables)
[1]
(retour
sommaire)
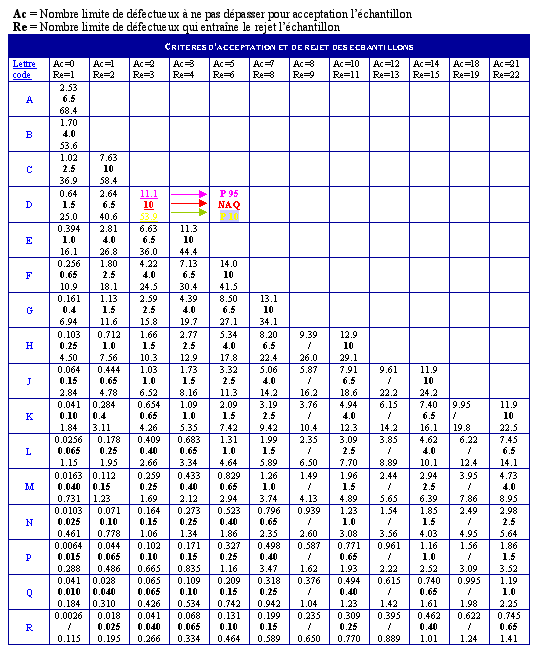
Cette lettre code donnera ensuite la
possibilité à l'ingénieur
biomédical de choisir la taille des
échantillons (via la table 2) suivant les trois
types de procédés d'échantillonnage
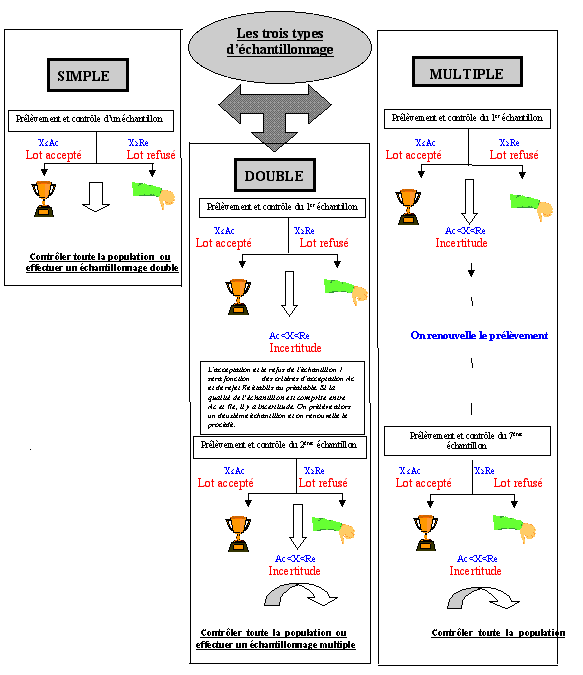
(simple, double et multiple).
Table 2
: [1]
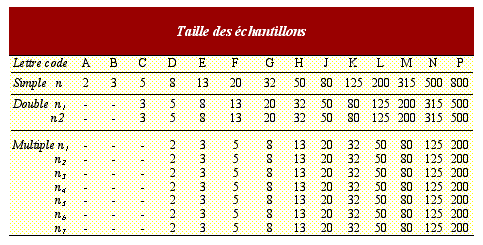
- échantillonnage simple
: On prélève un
échantillon de taille n et on le
contrôle.
- échantillonnage double
: On prélève un
échantillon n1 et éventuellement
un deuxième n2 de même
taille.
- échantillonnage multiple
: Le principe est le même
que pour l'échantillonnage double. Dans
le cas de l'échantillonnage multiple, le
nombre de prélèvements
consécutifs est
répété si nécessaire
jusqu'à sept fois. Pour chaque
prélèvement d'échantillon,
on conserve le même effectif.
-
- (retour
sommaire)
-
Le choix du type
d'échantillonnage :
Les trois types d'échantillonnage
présentent des avantages et des
inconvénients. En fonction du parc de
dispositifs médicaux étudiés,
l'ingénieur biomédical choisira la
méthode la plus appropriée.
- L'échantillonnage simple sera
préconisé lorsque l'effectif des
dispositifs est très réduit
(c'est-à-dire s'il est compris entre 2 et
15).
|
Effectif
du lot
|
Criticité
faible
|
Criticité
normale
|
Criticité
élevée
|
|
2 à
8
|
- Echantillonnage
simple
- Taille des
prélèvements =
2
|
- Echantillonnage
simple
- Taille des
prélèvements =
2
|
- Echantillonnage
simple
- Taille des
prélèvements =
2
|
|
9 à
15
|
-
Echantillonnage
simple
- Taille des
prélèvements =
2
|
-
Echantillonnage
simple
- Taille des
prélèvements =
3
|
- Echantillonnage
simple
- Taille des
prélèvements =
5
- Possibilité de faire
un
- échantillonnage double
- Taille des
prélèvements =
3
|
(retour sommaire)
Þ
Tout dispositif médical dont l'effectif
total est compris entre 2 et 8 sera soumis
obligatoirement à un échantillonnage
simple quelque soit son niveau de criticité.
Si l'échantillon est rejeté à
l'issue de ce contrôle, l'ingénieur
n'aura pas d'autres alternatives que d'engager une
procédure générale de
contrôle pour l'ensemble de la
population.
Þ
En ce qui concerne les dispositifs compris dans
la deuxième catégorie (9 à
15), l'ingénieur biomédical aura la
possibilité de procéder à un
double échantillonnage pour ceux dont la
criticité est élevée (si les
résultats sont médiocres,
l'ingénieur devra contrôler l'ensemble
de la population).
L'échantillonnage double
est un contrôle plus économique
que l'échantillonnage simple. Si
l'échantillon est excellent dès le
premier prélèvement, on aboutira
à l'acceptation et à la fin du
contrôle. Le gain de temps sera ainsi
considérable. Si l'échantillon est
médiocre, l'échantillon sera
refusé, l'ingénieur devra renouveler
l'application en prélevant un
échantillon de même taille.
Le double échantillonnage
paraît ainsi adapté au Service
Biomédical, il est le meilleur compromis
entre le coût du contrôle, son
efficacité et sa facilité de mise en
úuvre.
|
Effectif
du lot
|
Criticité
faible
|
Criticité
normale
|
Criticité
élevée
|
|
16 à
25
|
- Echantillonnage
simple
- Taille des
prélèvements =
3
|
- Echantillonnage
simple
- Taille des
prélèvements =
5
Possibilité de faire un
échantillonnage double
Taille des
prélèvements =
3
|
- Echantillonnage simple
- Taille des
prélèvements =
8
- Possibilité de faire un
échantillonnage double
- Taille des
prélèvements =
5
- Possibilité de faire un
échantillonnage multiple
- Taille des
prélèvements =
2
|
Þ
Pour étudier un dispositif
médical dont l'effectif total est compris
entre 16 et 25, l'ingénieur choisira le type
d'échantillonnage à adopter en
fonction du niveau de criticité
attribuée au dispositif en question.
Par exemple, si le dispositif a une
criticité élevée,
l'ingénieur peut utiliser
l'échantillonnage simple, double ou
multiple.
L'échantillonnage multiple est un
procédé de contrôle plus lourd
à mettre en úuvre dans la mesure
où les prélèvements
consécutifs peuvent aller jusqu'à
sept. Il est cependant fortement conseillé
pour des raisons économiques (à
condition que ce contrôle des
échantillons par étapes donne des
résultats positifs dès les
premières séries de
prélèvements).
A l'issue d'un rejet consécutif
des sept prélèvements,
l'ingénieur biomédical peut
prévoir un contrôle de ces dispositifs
pour le bon fonctionnement de son parc.
La taille de l'échantillon
prélevée sera donc fonction du type
d'échantillonnage privilégié
par l'ingénieur biomédical
(retour
sommaire)