|
Référence à rappeler
: |
|
|
MISE EN PLACE D'UNE UNITE TEP-SCANNER AU CHU DE CAEN |
 Julien MOUCHEL |
|
|
|
Si vous arrivez
directement sur cette page, sachez que ce travail est un rapport
d'étudiants et doit être pris comme tel. Il peut donc comporter des
imperfections ou des imprécisions que le lecteur doit admettre et donc
supporter. Il a été réalisé pendant la période de formation et constitue
avant-tout un travail de compilation bibliographique, d'initiation et
d'analyse sur des thématiques associées aux technologies biomédicales.
Nous ne faisons aucun usage commercial et la
duplication est libre. Si vous avez des raisons de contester ce droit
d'usage, merci de nous en faire
part . L'objectif de la présentation sur le Web est de
permettre l'accès à l'information et d'augmenter ainsi les échanges
professionnels. En cas d'usage du document, n'oubliez pas de le citer
comme source bibliographique. Bonne
lecture... |
|
|
|
Référence à rappeler
: |
|
|
MISE EN PLACE D'UNE UNITE TEP-SCANNER AU CHU DE CAEN |
 Julien MOUCHEL |
REMERCIEMENTS
Je tiens tout dabord à remercier mon maître de stage Monsieur Pierre LACOMBE, pour mavoir accueilli dans son service et mavoir donné lopportunité de travailler sur un projet important et très intéressant.
Je remercie également Madame Aurélie MAILLARD pour les conseils en Radioprotection quelle ma apportés ainsi que Monsieur Hervé GONCALVES et Monsieur Jacques DALLET pour mavoir fait partagé leur expérience dIngénieur Biomédical.
Pour terminer, je tiens à remercier les techniciens du service Biomédical : Monsieur Jean Jacques MARY, Monsieur Joachim CARREL, Monsieur Serge SACCO, Monsieur Philippe FERCHAUD, Monsieur Jean Jacques BELLENGER, Monsieur Jean Luc VASNIER, Monsieur Alain MENAGER, Monsieur Gérard BLIN, Mademoiselle Katie HELIE ,Monsieur Jean Marie CATHERINE, Monsieur Denis BLAISON, Madame Séverine ROUSSEL, Monsieur Pascal COUVERT, Monsieur Pascal LE MENAGER, Monsieur Fabien DAUFY, pour mavoir fait partager leur travail ainsi que Madame Françoise DUVAL et Madame Odile PETTIER.
|
Lobjectif de ce rapport est de tenter daider toute personne ayant comme projet la création dune unité TEP-Scanner. En effet, pour les personnes ne connaissant pas cette modalité dimagerie, ce rapport décrit globalement cette technologie. Il sera question ensuite des différentes contraintes quil est possible de rencontrer vis-à-vis du dispositif médical mais également vis-à-vis du produit radioactif utilisé lors dun examen. En effet, le 18FDG, qui est le traceur employé, engendre beaucoup de problèmes de radioprotection. Des solutions seront alors apportées afin dêtre en conformité avec la DGSNR. Il sera question également de lacquisition du dispositif médical et du matériel de radioprotection.
|
|
The goal of this report is to try to help any person having like project the creation of a unit PET-Scan. Indeed, for the people not knowing this method of imagery, this report describes this technology overall. It will be a question thereafter various constraints which it is possible to meet with respect to the medical device but also with respect to the radioactive product used at the time of an examination. Indeed, the 18FDG, which is the tracer employed, generates much problem of protection against radiation. Solutions will then be brought so being in conformity with the DGSNR. It will be a question also of the acquisition of the medical device and the material of protection against radiation.
|
I. Présentation du Centre Hospitalier Universitaire de Caen
3. Le service de Médecine Nucléaire
II. Contexte socio-économique et technologique dune implantation dun TEP-Scanner
2. Aspects technologiques du TEP-Scanner
III. Mise en place dune unité TEP-Scanner
1. Contraintes liées à la partie TEP
2. Contraintes liées à la partie Scanner
3. Contraintes liées à léquipement par lui-même
4. Contraintes liées au 18Fluoro-DéoxyGlucose
5. Contraintes liées à limplantation au CHU de Caen
IV. Acquisition dun TEP-Scanner et des équipements nécessaires au fonctionnement de cette unité
1. Cahier des charges du TEP-Scanner
2. Cahier des charges du matériel de radioprotection
b. Autres matériels de radioprotection
Introduction. Retour Sommaire
Limagerie médicale regroupe lensemble des techniques utilisées par la médecine pour le diagnostic mais aussi le traitement de pathologies. Elle a révolutionné la médecine en donnant un accès immédiat et fiable à des informations jusqualors invisibles au diagnostic clinique.
Depuis quelques années, limagerie médicale ne cesse de se développer et cela dans la plupart des modalités. Limagerie par résonance magnétique devient de plus en plus performante. Les systèmes de détection et dacquisition sur les scanners sont de plus en plus rapides et limagerie en Médecine Nucléaire se voit être associée à dautres modalités. En effet, sur le marché, les constructeurs commence à proposer dans leur gamme des γ caméras couplées à un scanner. Mais ce qui nous intéresse actuellement, cest le couplage dune caméra de Tomographie par Emission de Positons (TEP) à un Scanner. Ce dispositif médical est appelé TEP-Scanner.
La Tomographie par Emission de Positons est apparue dans les années 1990. Elle permet dobtenir une imagerie métabolique en oncologie. Développée au départ pour la recherche en cardiologie et en neurologie, La TEP deviendra un outil médical à part entière en oncologie. Cest à partir des années 2000 que le TEP-Scanner fait son apparition. Ce couplage de deux modalités différentes, permet dobtenir un repérage anatomique de bonne qualité sur une image fonctionnelle.
A lheure actuelle, une soixantaine dautorisations dimplantation déquipement lourd [1] pour un TEP-Scanner ont été délivrées sur le territoire français. Ces autorisations sont le reflet de la politique de lutte contre le cancer.
Le TEP-Scanner est donc un dispositif médical pouvant apporter énormément sur le diagnostic en oncologie mais également au niveau du traitement car les images peuvent servir à effectuer un repérage pour une éventuelle intervention chirurgicale mais aussi peuvent être utilisées pour évaluer la réponse à une chimiothérapie.
En contrepartie, linstallation dun tel équipement est à étudier sérieusement. En effet, de nombreuses contraintes liées aux deux modalités viennent se greffer lors de lacquisition dun TEP-Scanner et sont à prendre en compte. De plus, le choix du dispositif est également délicat avec une technologie de pointe. Cest pour ces raisons, quau long de ce rapport, nous tenterons de répertorier les difficultés pouvant être rencontrées lors de limplantation dun TEP-Scanner.
Nous verrons tout dabord, dans quel contexte le TEP-Scanner du CHU de Caen sera implanté. Nous verrons dans un deuxième temps, quelles peuvent être les différentes contraintes dimplantation quil est possible de rencontrer. Nous tenterons dans une dernière partie de dégager les caractéristiques les plus importantes que doit offrir un TEP-Scanner ainsi que le matériel de radioprotection pour la manipulation du 18FDG. Cette dernière partie a comme finalité, laide à la rédaction du Cahier des Clauses Techniques Particulières (CCTP).
I. Présentation du Centre Hospitalier Universitaire de Caen.
Le Centre Hospitalier Universitaire de Caen est constitué de trois établissements :
Lhôpital Côte de Nacre, mis en service en 1975, est une structure monobloc. Il comprend 1137 lits, 32 services, 12 blocs opératoires, 1 plateau technique dimagerie (2 Scanner,2 IRM, 3 Gamma Caméras, ) Son activité est particulièrement orientée vers la médecine et la chirurgie adulte.
Lhôpital Clemenceau, mis en service au début du 20ème siècle, est une structure pavillonnaire traditionnelle de 396 lits. Cet hôpital est particulièrement orienté autour du pôle mère-enfant (pédiatrie, gynécologie obstétrique, néonatalogie, ...).
Le centre pour personne âgées dispose de 270 lits répartis en unités de soins de longue durée, soins de suite et réadaptation et maison de retraite.
Lavenir du CHU de Caen est basé sur un plan directeur. En effet, celui-ci a pour but la création de 8 pôles médico-chirurgicaux et de 4 ensembles dactivités. Cela a pour objectif de regrouper les disciplines afin doptimiser les performances du CHU. Lhôpital Côte de Nacre sera le site où le regroupement seffectuera.
Dans les années à venir, lun des premier regroupement à seffectuer sera celui du pôle mère-enfant.
Fig.1 Projet dimplantation de nouveaux bâtiments
Aujourdhui, cette activité est en partie sur le site de Clemenceau mais devra donc rejoindre le site de Côte de Nacre. Ce pôle mère-enfant comprendra la Pédiatrie médicale, la Chirurgie Pédiatrique, la Néonatalogie, la Gynécologie Obstétrique. Pour la construction de ce pôle mère-enfant, le CHU de Caen met en place un projet PPP (Partenariat Public Privé). Ce projet est le premier sur le plan national au niveau des structures hospitalières. En effet, le CHU de Caen a décidé de confier à un opérateur privé la conception, la réalisation, lentretien et le financement de cette nouvelle infrastructure. Le CHU sera alors locataire de ces bâtiments.
Le service Biomédical, localisé sur le site de Côte de Nacre au 22ème étage, a en charge la maintenance des différents dispositifs médicaux ainsi que lachat de nouveaux équipements.
Le service est composé de 21 personnes :
Les techniciens sont répartis majoritairement sur le site Côte de Nacre mais également sur le site Clemenceau. Ils sont organisés par équipe avec différentes spécialités (Imagerie, Laboratoire, Monitorage, Réanimation, Chirurgie, Hémodialyse, ). Ils soccupent notamment de la maintenance corrective et préventive et du suivi des équipements sous contrat.
Les ingénieurs travaillent en étroite collaboration avec les services économiques pour toutes les procédures dachats déquipement.
Les projets actuels du service biomédical sont lacquisition dun scanner multibarrette, la mise en place dun système de pré analytique, le remplacement dun IRM, la mise en place dune unité TEP-Scanner et la préparation du projet visant à accueillir le pôle mère-enfant sur le site Côte de Nacre.
3. Le Service de Médecine Nucléaire.
Actuellement, le service de Médecine Nucléaire sétend sur une surface denviron 600 m² et accueille trois Gamma Caméras afin de réaliser les examens de scintigraphies classiques de Médecine Nucléaire. Le service se compose également dun laboratoire chaud, dune salle dinjection et dune salle de marquage.
La nouvelle technologie dimagerie médicale qui va être mise en place, sera implantée dans le service actuel de Médecine Nucléaire. Pour cela, le service se verra être remodelé afin de trouver la place nécessaire à limplantation dune unité TEP-Scanner ainsi quà la mise en place des règles de conformité dun tel équipement.
Lors de limplantation de lunité TEP-Scanner, diverses modifications devront avoir lieux :
Après la présentation des différents services nous intéressant dans le cadre de ce rapport, nous allons étudier dans quel contexte lunité TEP-Scanner se mettra en place.
II. Contexte socio-économique et technologique dune implantation dun TEP-Scanner.
1. Aspects socio-économiques [3, 4, 5].
Tous cancers confondus, la France comptaient 280000 nouveaux cas en 2000, contre 150000 en 1980, soit une progression de lincidence de 63%. Cette augmentation sexplique notamment par les techniques de dépistages qui deviennent plus sensibles
Les chiffres des décès par tumeurs en Basse-Normandie sont les suivants :
|
Tumeurs (localisation) |
Hommes |
Femmes |
Total |
% Basse-Normandie |
% France |
|
Trachée, bronches, poumon |
502 |
79 |
580 |
15 |
16.9 |
|
Colon, rectum |
200 |
211 |
411 |
10.6 |
11 |
|
Sein |
3 |
282 |
285 |
7.4 |
7.5 |
|
Prostate |
256 |
- |
256 |
6.6 |
6.3 |
|
Foie, voies biliaires intrahépatiques |
154 |
31 |
186 |
4.8 |
4.6 |
|
Estomac |
109 |
73 |
183 |
4.7 |
3.7 |
|
Oesophage |
144 |
20 |
164 |
4.2 |
3 |
|
Lèvres, cavité buccale, pharynx |
130 |
13 |
143 |
3.7 |
3.3 |
|
Vessie |
85 |
28 |
113 |
2.9 |
3.1 |
|
Leucémies |
56 |
49 |
105 |
2.7 |
3.3 |
|
Ovaires, annexes de l'utérus |
- |
98 |
98 |
2.5 |
2.2 |
|
Utérus |
- |
79 |
79 |
2 |
2 |
|
Larynx |
64 |
4 |
68 |
1.7 |
1.5 |
|
Peau |
28 |
21 |
49 |
1.3 |
1.1 |
|
Autres tumeurs |
643 |
506 |
1149 |
29.7 |
30.4 |
| TOTAL |
2372 |
1495 |
3867 |
100 |
100 |
Nous pouvons constater que lun des cancers les plus meurtriers est le cancer du poumon qui représente en France, 27000 nouveaux cas par an. Globalement, les différents types de cancer font énormément de victimes par an. Il est donc urgent de trouver des solutions afin de diminuer ces chiffres au maximum.
La TEP apparaît aujourdhui comme une technique incontournable en oncologie. Son association à une autre modalité dimagerie permettra des bilans précis pour caractériser lavancée du cancer ou les possibles récidives. Elle a donc un rôle à la fois dans la stratégie diagnostique mais également dans la stratégie thérapeutique.
Mais, étant donné les coûts dinvestissement et de fonctionnement, limplantation dun tel équipement doit être analysée afin de connaître les apports sur le plan médical qui justifieraient un tel investissement. En effet, au niveau du coût dinvestissement, il faut prévoir environ 3 millions deuros. Il faut rajouter à ce prix, un budget de fonctionnement qui sélève à 2 millions deuros par an. Dans le budget de fonctionnement, il faut penser à inclure le personnel dédié à lunité TEP-Scanner. Un tel investissement est difficilement gérable pour un seul établissement. Par conséquent, comme dans la plupart des implantations de TEP-Scanner en France, le CHU de Caen va créer, avec le Centre Régional de Lutte Contre le Cancer François Baclesse, un partenariat financier afin dacquérir un tel équipement. Ce partenariat est un Groupement de Coopération Sanitaire (GCS). Ce GCS précise les modalités de fonctionnement du centre TEP-Scanner, la part respective de lactivité de chaque partenaire, le rôle et la responsabilité de chaque acteur, ainsi que les modalités de financement.
Lunité TEP-Scanner de Caen aura pour vocation daccueillir les patients de Basse-Normandie mais également, dans une proportion moindre, des patients de départements voisins. Le nombre dhabitants en Basse-Normandie est aux alentours de 1.400.000 habitants ce qui est en accord avec lindice spécifique de besoins propre aux TEP [6]. Après les premières années de mise en place, le nombre dexamen envisagé sélève à 8 examens par jour, correspondant à 2000 patients par an.
2. Aspects technologiques du TEP-Scanner.
Le TEP-Scanner est un couplage de deux technologies dimagerie. Nous avons à la fois un scanner qui va donner une image anatomique et une caméra TEP qui utilise un produit radioactif, donnant une image métabolique
La caméra TEP est une technique dimagerie nécessitant un produit radioactif, émetteur de positons. Au niveau des examens cliniques, lémetteur de positons est le 18FDG. Cette molécule est un analogue du glucose marqué par le fluor 18 [7].
Pour effectuer un examen TEP, il faut avant tout que le patient reçoive une injection de 18FDG. Cette molécule étant un analogue du glucose, elle se fixera dans les cellules consommant fortement du glucose. Cette fixation peut être physiologique (cerveau, cur, reins, vessie, ) ou bien pathologique (cellules cancéreuses, inflammation diverses, ). En effet, les cellules cancéreuses sont fortement consommatrices de glucose. Par conséquent, le 18FDG, lors de linjection, se fixera préférentiellement sur ces cellules cancéreuses et seront donc visualisées au cours de ces examens.
La visualisation est possible grâce à la détection des phénomènes dannihilation.
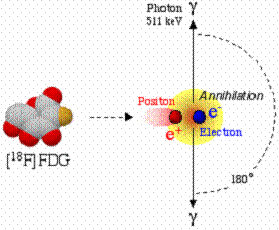
Figure 3 - Phénomène dannihilation
En effet, lorsque le 18FDG est injecté, puis diffusé dans les tissus consommateurs de glucose, il émettra des positons β+. Ces positons vont interagir avec les électrons de la matière pour créer au final, un phénomène dannihilation. Ce phénomène dannihilation se traduit par lémission de deux photons γ, de 511 keV chacun, émis à 180° lun de lautre. La caméra TEP détectera lémission de ces photons seulement si celle-ci est en coïncidence. Par conséquent, là où il y aura des cellules cancéreuses, il y aura consécutivement accumulation de 18FDG, phénomène dannihilation et émissions de photons γ. On pourra alors détecter les tissus cancéreux par la caméra TEP.
Cette modalité dimagerie permet notamment, de repérer les cellules cancéreuses en fonction de leur activité métabolique. Par contre, la résolution dune caméra TEP reste relativement modérée. Il est alors difficile deffectuer un repérage anatomique de la zone à traiter.
Cette modalité dimagerie ne nécessite pas de produit radioactif comme la caméra TEP. Le scanner est constitué principalement de deux parties. Le générateur de rayons X et le système de détecteurs.
Le générateur va donc produire des rayons X qui vont traverser le patient pour arriver ensuite sur les détecteurs. Ces rayons seront atténués en fonction des tissus traversés. Grâce à lélectronique associée, il sera possible dobtenir pour chaque coupe, une carte datténuation caractérisant les tissus traversés.
Grâce au scanner, il sera donc possible dobtenir une imagerie anatomique très précise du corps humain.
Par contre, nous navons pas dinformation métabolique et il est parfois difficile de différencier certains types de tissus de même densité.
Il a été développé un dispositif médical qui associe les deux modalités. Ceci permet dobtenir une imagerie anatomique et une imagerie métabolique. De plus, étant donné que nous navons plus quun seul équipement, le patient reste exactement dans la même position au cours des deux examens qui senchaînent. La fusion des images peut seffectuer sans aucun problème de recalage et nous avons sur un même examen, une information métabolique et une information anatomique. Cela permettra entre autre, de reconnaître les cellules cancéreuses et doptimiser les limites dun geste chirurgical ou bien de préciser le volume cible pour la radiothérapie.
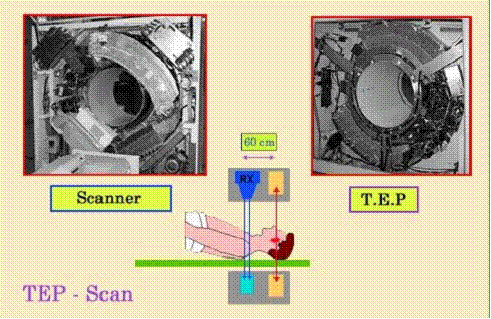
Figure 4 - Statif de la partie Scanner et de la partie TEP
Lautre atout de ce type déquipement, est lacquisition dune carte de transmission précise, obtenue grâce à la partie scanner. Cette carte de transmission représente les coefficients datténuation pour une énergie de 511 keV ce qui rend possible une correction de latténuation de meilleur qualité que celle obtenue avec les sources radioactives. Egalement, la superposition directe des images démission et de transmission se traduit également par un gain de temps lors de lacquisition.
Après
avoir pris connaissance du contexte dans lequel lunité TEP Scanner sera
implantée, nous allons maintenant tenter de recenser les différentes contraintes
pouvant se poser à cette implantation.
III. Mise en place dune unité TEP-Scanner.
La mise en place dun tel équipement engendre beaucoup de contraintes. Celles-ci sont de différents ordres : radioprotection, environnement, agencement de la future unité.
Cest pour cela que nous allons tenter de répertorier les principales contraintes quil est susceptible de rencontrer dans linstallation dun TEP-Scanner
1. Contraintes liées à la partie TEP.
Les contraintes liées à la partie TEP sont les plus contraignantes car elles impliquent un aspect radioactif pour cet équipement. En effet, lors dun examen TEP-Scanner, il est nécessaire dinjecter au patient un produit radioactif. Ce produit radioactif va entraîner de nombreuses contraintes liées aux rayonnements ionisants quil produit. Dautre part, des textes officiels, provenant notamment de la DGSNR (Direction Générale de Sûreté Nucléaire et de Radioprotection), vont établir les règles à respecter pour limplantation dun tel dispositif.
Nous pouvons citer en exemple, quelques textes ou décrets qui devront être appliqués lors de la mise en place dun TEP-Scanner :
De ces textes, plusieurs points importants sont à mettre en avant :
Au niveau de linfrastructure, il est nécessaire de prévoir une salle dexamen ayant des dimensions suffisantes afin de pouvoir recevoir le TEP-Scanner. En effet, les différents équipements proposés par les constructeurs ont une longueur importante. Si nous ne voulons pas faire le choix de léquipement par rapport aux contraintes dinstallation, il est donc important davoir une salle suffisamment grande.
De plus, une salle dinjection dédiée à lunité TEP-Scanner sera nécessaire. Cette salle dinjection devra être individualisée en boxes. En effet, suite à linjection, chaque patient va émettre des rayonnements ionisants. Par conséquent, afin de minimiser lexposition dun patient par un autre ainsi que lexposition des manipulateurs par plusieurs patients à la fois, chaque patient sera placé dans un box. Par ailleurs, une réflexion sur le nombre de boxes à mettre en place devra avoir lieux. Cette réflexion sera basée sur les estimations du nombre dexamens quotidiens.
Dautre part, lexistence dun sas avant le labo chaud apparaît nécessaire pour être en accord avec les contraintes de radioprotection et les contraintes de radiopharmacie. En effet, selon les contraintes de radioprotection, le labo chaud doit être en dépression par rapport à lextérieur. Selon la radiopharmacie, cest le contraire afin que le labo chaud reste une zone propre. Par conséquent, le sas permettrait aux deux contraintes de sappliquer et serait une zone de transition où les manipulateurs séquiperaient de « survêtements » afin de ne pas contaminer le labo chaud.
En ce qui concerne le laboratoire chaud, il nest pas nécessaire de lindividualiser du labo chaud de Médecine Nucléaire. Ce qui est obligatoire par contre, cest dindividualiser les enceintes blindées. En effet, il est nécessaire de séquiper dune enceinte spécifique FDG car lénergie de ce radioélément est beaucoup plus importante que les radioéléments classiques de Médecine Nucléaire. Ce type denceinte a ses parois renforcées par des épaisseurs supplémentaires de plomb. Ceci permet dêtre en conformité avec la notice de la DGSNR au niveau des débits de dose aux parois de lenceinte (<25μSv.h-1 à 5cm des parois) [9]. Il sera possible de demander aux constructeurs un justificatif sur ces valeurs à ne pas dépasser.
Pour conclure sur ces contraintes liées aux rayonnements ionisants, nous allons nous intéresser aux épaisseurs des murs pour une unité TEP-Scanner. En effet, afin de minimiser lexposition aux alentours de la salle dexamen et de la salle dinjection, il est demandé par la DGSNR de calculer les épaisseurs de murs nécessaires pour la protection du personnel et du public. Pour cela, la notice de la DGSNR précise sous quelles conditions les calculs doivent être faits (Annexe 1 & 2). De ces calculs nous pouvons tirer plusieurs conclusions :
Afin de respecter les épaisseurs nécessaires, différentes solutions peuvent être apportées pour renforcer les murs. Il est possible par exemple de rajouter ou de remplacer certains murs par des parpaings pleins qui ont comme caractéristique darrêter plus efficacement les rayonnements ionisants. Il est possible également de mettre en place des panneaux de placoplâtre plombé. Dautre part, dans le cas où le plafond serait à renforcer, il existe du faux plafond plombé qui permettrait darrêter une partie du rayonnement.
Par ailleurs, la salle devra également avoir tous les aménagements habituels dune salle de caméra à scintillation (revêtement du sol, des murs, ventilation en dépression, )
2. Contraintes liées à la partie Scanner.
En ce qui concerne la partie scanner, les contraintes pouvant exister, sont liées à laménagement de la salle dexamen mais également à la radioprotection.
En effet, le scanner est également une source de rayonnements ionisants. Mais en comparaison avec le rayonnement dû au produit radioactif de la partie TEP, lexposition due au scanner est très inférieure. Par conséquent, au niveau de la radioprotection, si lunité TEP-Scanner est mise aux normes vis-à-vis de la partie TEP, elle sera également aux normes vis-à-vis de la partie scanner. Il nest donc pas nécessaire deffectuer dautres modifications liées à ce type de contraintes.
Par contre, les autres contraintes sont régies par la norme NFC 15-161 [10]. Certains points de cette norme sont à mettre en avant :
3. Contraintes liées à léquipement par lui-même.
Dautres contraintes existent également mais celles-ci sont liées à léquipement par lui-même et non pas à la modalité dimagerie. En effet, limplantation dun tel équipement imposent quelques règles :
Par conséquent, dans le but de prévoir ces contraintes dimplantation et dacheminement, il est important denvoyer les plans des futurs locaux aux différentes sociétés commercialisant ce type déquipement. Cela permettra deffectuer des études dacheminement et dimplantation.
4. Contraintes liées au 18Fluoro-DéoxyGlucose [11].
Le 18FDG, en utilisant essentiellement les caractéristiques métaboliques des tissus, permet de différencier un processus bénin dune pathologie maligne. Analogue dun sucre, le déoxyglucose est devenu radioactif émetteur de positons par marquage avec du Fluor 18. Il permet également la visualisation des tumeurs à un stade précoce de développement ainsi que de détecter des métastases.
Comme tous les émetteurs de positons, le fluor 18 nexiste pas à létat naturel. Cest une substance artificielle que lon peut fabriquer dans un cyclotron. Mais le fluor 18 a la particularité davoir une demi-vie courte de 109 minutes. Cette dernière caractéristique signifie quen moins de deux heures, la radioactivité initialement disponible a diminué de moitié. De nombreuses conséquences pratiques en découlent :
En effet, lors de létude dimplantation dun TEP-Scanner, il est important détudier lapprovisionnement en 18FDG. Plusieurs cas de figure peuvent se présenter :
Il est donc nécessaire de sinformer au préalable sur les possibilités dapprovisionnement de 18FDG afin que cela ne pose pas de problèmes par la suite.
5. Contraintes liées à limplantation au CHU de Caen.
Les problèmes rencontrés par le CHU de Caen, dans la mise en place de ce projet, sont liés principalement au fait que lunité TEP-Scanner simplante dans un service déjà existant. En effet, il faut sadapter aux locaux actuels et par conséquent les normes à respecter le sont plus difficilement.
Le premier problème qui a été rencontré, fut de trouver la surface nécessaire pour implanter lunité TEP-Scanner. En effet, le service de Médecine Nucléaire actuel ne possède pas de surface supplémentaire. Dans ce cas, une extension dans la cour intérieure accolée au service a été proposée. Cette extension accueillera tous les bureaux ainsi que la salle dinterprétation commune. Cette extension libèrera la place nécessaire pour pouvoir implanter la salle dexamen, la salle dinjection et le nouveau labo chaud.
Mais lun des problèmes majeurs rencontré par le CHU de Caen, est la conformité vis-à-vis des contraintes de radioprotection pour les épaisseurs des murs. En effet, différentes zones posent problèmes :
Dans le cas du CHU, il faut également sinterroger sur les épaisseurs existantes avec les étages supérieur et inférieur :
Dautre part, en ce qui concerne lapprovisionnement en 18FDG, le cas du CHU de Caen est assez particulier. En effet, la ville de Caen dispose dun cyclotron sur le site du GANIL. Celui-ci produit actuellement le 18FDG pour les caméras TEP du centre Cycéron. Mais des problèmes dAMM et de commercialisation viendront compromettre la livraison du 18FDG par le GANIL. Pour pouvoir commercialiser le 18FDG au CHU de Caen, le GANIL devrait être une industrie pharmaceutique responsable de la fabrication et de la distribution du produit, ce qui nest pas le cas. Il faudra donc envisager dautres solutions et notamment lapprovisionnement par dautres cyclotrons. Dans le cas de Caen, deux possibilités peuvent être proposées :
Nous avons tenté de répertorier les principales contraintes dimplantation dun tel équipement. Nous allons maintenant parler de lacquisition dun TEP-Scanner et du matériel de radioprotection correspondant.
IV. Acquisition dun TEP-Scanner et des équipements nécessaires au fonctionnement de cette unité.
Au cours de cette partie, nos allons développer une étape de lacquisition dun TEP-Scanner qui est la rédaction du cahier des charges ou CCTP (Cahier des Clauses Techniques Particulières). Nous verrons également quels sont les différents équipements de radioprotection pouvant être utilisés.
1. Cahier des charges du TEP Scanner [12].
Le cahier des charges dun tel équipement va permettre à la fois de recenser les besoins vis-à-vis du dispositif médical mais également sera lobjet dun comparatif entre les différents constructeurs de TEP-Scanner. En effet, celui-ci nous permettra dévaluer les offres de chaque société commercialisant ce type déquipement. Cela passera notamment, par le comparatif des questionnaires techniques qui permet de caractériser les différents équipements.
Différentes étapes peuvent être utile à la rédaction dun cahier des charges:
Lors de la rédaction du cahier des charges, il faudra mettre en avant les caractéristiques de léquipement qui nous semblent les plus importantes. En effet, il faut dans un premier temps définir les besoins au niveau des principaux points suivants :
Lorsque loffre de base a bien été définie, il faut sintéresser aux options qui pourraient être utiles à acquérir. En effet, de nombreuses options sont proposées. Il existe entre autre des options au niveau de la radiothérapie notamment au niveau des systèmes de centrage du patient qui permet un replacement lors du traitement en radiothérapie. Egalement, lacquisition dun plateau plat peut savérer utile. Il est donc nécessaire de sentretenir avec les acteurs spécialisés dans le traitement du cancer afin de connaître leurs besoins. Dautres options peuvent être demandées comme par exemple une console supplémentaire afin de connaître le prix dans le cas où cela savèrerait utile.
Après avoir défini loffre de base ainsi que les options, il est important également dans le CCTP, de demander aux soumissionnaires, tous les documents certifiant la conformité du dispositif médical et le respect de certains textes officiels sur la maintenance et la radioprotection. Il sera aussi demandé aux soumissionnaires de remplir le questionnaire technique qui permettra de comparer plusieurs aspects de léquipement. Dans ce questionnaire, plusieurs points peuvent être demandés :
Ceci nest quune partie des questions que nous pouvons trouver dans un questionnaire technique. Ce questionnaire pourra alors nous aider à choisir léquipement correspondant au mieux à nos besoins. Pour conclure, nous classerons les offres des constructeurs selon les critères de choix suivants:
Après avoir choisi léquipement qui correspond à nos besoins, nous allons maintenant nous intéresser aux équipements de radioprotection utilisés lors de la manipulation du 18FDG.
2. Cahier des charges du matériel de radioprotection [13].
Lutilisation de produit radioactif tel que le 18FDG engendre lachat de matériels spécifiques aux rayonnements ionisants de haute énergie. Comme cela est souligné dans la notice de la DGSNR, il est nécessaire dacquérir une enceinte spécifique au fluor 18. De même, le matériel habituel de Médecine Nucléaire tel que les protèges seringues, les valisettes devront être également spécifiques pour ce type dénergie. Nous allons donc voir quels sont les différents équipements pouvant être utilisés dans une unité TEP-Scanner.
Ce type déquipement a pour but de minimiser au maximum lexposition des manipulateurs lors de la préparation des seringues pour linjection du 18FDG. Il est donc important de faire un choix correct sur le produit pour quil puisse convenir au mieux aux utilisateurs.
Tout dabord, sur le plan réglementaire, les enceintes proposées par les sociétés pour la manipulation de 18FDG, doivent répondre aux exigences de la DGSNR (Débit de dose équivalente ne dépassant pas 25μSv.h-1 à 5 cm des parois de lenceinte). Donc dun point de vue radioprotection, les épaisseurs de plomb de ces enceintes sont suffisantes. Il faut également sassurer que lemplacement dédié à lactivimètre réponde également à cette exigence. Lactivimètre, quant à lui, doit être conçu afin dassurer un bon fonctionnement pour une large gamme dénergie et des activités importantes. De plus, celui-ci doit être précis, rapide et fiable. Un système de gestion des sources peut y être associé. Lenceinte devra aussi être équipée dun système de ventilation en dépression.

Dautre part, sur ce type déquipement, il est nécessaire dévaluer en priorité lergonomie et la fonctionnalité. Il est donc important dans le questionnaire technique du CCTP de sinformer sur le nombre douvertures latérales, sur les dimensions du plan de travail. Il également intéressant de savoir si lenceinte est réglable en hauteur. Cette option a un coup financier mais permet aux manipulateurs de travailler dans de meilleures conditions.
Comme pour le TEP-Scanner, il peut être utile denvoyer les plans aux différentes sociétés commercialisant des enceintes. En effet, une étude dacheminement peut être demandée afin de sassurer du bon déroulement de linstallation de celle-ci.
b. Autres matériels de radioprotection.
Suite à la préparation du 18FDG dans lenceinte blindée, il faudra transporter la seringue jusquau patient afin dinjecter le produit. Afin de minimiser lexposition, plusieurs solutions sont possibles.
La première est lutilisation de protèges seringues, spécifiques aux hautes énergies. Le nombre de protèges seringues est à étudier et dépendra de lactivité prévisionnelle et du nombre de salles dinjection. Ces protèges seringues permettent de réduire lexposition aux rayonnements ionisants lors des étapes de manipulation de la seringue à lextérieur de lenceinte.
Dautre part, afin de transporter la seringue sans sexposer, il existe des chariots de transport avec des protections en plomb suffisantes.
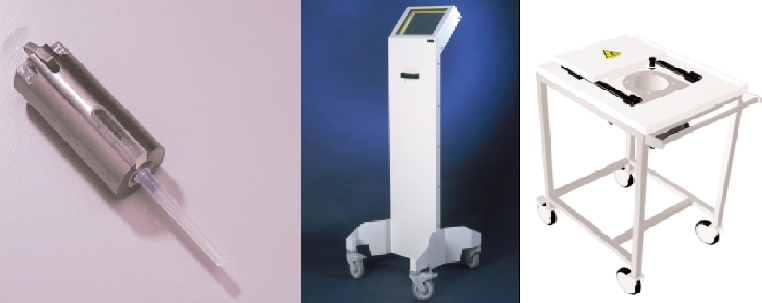
Figure 6 Protège seringue, Paravent plombé, Chariot de transport
Lors de linjection, lutilisation dun paravent plombé est nécessaire. En efet, lorsque linjection a lieu, le patient devient une source de rayonnements ionisants et par conséquent, le manipulateur doit se protéger.
Pour conclure sur les moyens de protection, une autre solution peut être proposée. Il sagit dun injecteur automatique qui remplace à la fois le chariot roulant et le paravent. En effet, après la préparation dans lenceinte, la seringue est placée dans un compartiment protégé de linjecteur automatique. Nous pouvons donc transporter la seringue sans risque dexposition aux rayonnements jusquà la salle dinjection. Dans celle-ci, le patient est relié par cathéter à la seringue et il est possible dinjecter le patient à distance. De plus, les protections de linjecteur ont été calculées afin de réduire au maximum lexposition.

Figure 7 – Injecteur Automatique
Etant donné la situation actuelle, où les chiffres du cancer ne sont pas favorables, nous avons tenté au cours de ce rapport de mettre en avant cette nouvelle technologie en plein essor qui est le TEP-Scanner. Ce dispositif médical permet dacquérir en un seul examen, une image fonctionnelle et une image anatomique afin dobtenir un meilleur dépistage et une meilleur localisation pour de futurs traitements.
Ce rapport a donc pour finalité de répertorier le maximum de contraintes dinstallation afin que les établissements souhaitant se doter de cette technique dimagerie puissent être au mieux préparés. Nous avons également répertorié les différents points importants pour le choix de léquipement ainsi que de lenvironnement de travail. Les principaux problèmes qui peuvent être rencontrés et qui ressortent de ce document sont les contraintes de radioprotection et particulièrement dans le cas où les locaux existent déjà. Dans ce dernier cas, il faudra sadapter à lenvironnement préexistant, ce qui nest pas toujours facile à mettre en place.
Au cours de cette étude, nous avons pris contact avec des établissements qui se sont ou qui sont actuellement en train de se doter de ce type déquipement médical. Nous avons pu recueillir de nombreux témoignages avec des recommandations sur des points pouvant posés problèmes. Il savère en fait que chaque établissement et chaque implantation sont un cas particulier. Etant donné la situation géographique de la future unité et de bien dautres critères, nous nous apercevons que la création de cette unité pose bien dautres problèmes qui sont découverts au fur et à mesure de lavancée du projet. Il faudra alors trouver les solutions les plus adaptées pour réaliser à bien cette unité TEP-Scanner.
Annexe 1 : Formules permettant de calculer les épaisseurs de murs à mettre en place
Après quelques recherches pour obtenir la formule du débit de dose, il a été proposé une formule intégrant les épaisseurs des matériaux déjà existants. La formule est la suivante :
![]()
![]()
Constante de Kerma 18F égale à 0.135 μGy.h-1.MBq-1.m².
d : distance entre la source 18F et le mur à étudier.
E : Epaisseur de mur selon le matériau (BO : Béton ordinaire ; BB : Béton Baryté ; F : Fer ; Pb : Plomb).
CDA : Couche de Demi Atténuation.
Lorsque nous avons le débit de dose et la dose limite à atteindre, il est alors possible de calculer lépaisseur dun matériau nécessaire afin de ne pas avoir un débit de dose supérieur aux limites :
![]()
Avec ces formules , il est maintenant possible de calculer les épaisseurs des différents murs qui seront susceptibles dêtre dans lunité TEP-Scanner. Pour les calculs, il est nécessaire de prendre une source de 600 MBq et de la positionner à une hauteur de 1m.
Annexe 2 : Notice DGSNR/SD9 L/04-V2
DIRECTION GÉNÉRALE DE LA SÛRETÉ NUCLÉAIRE ET DE LA RADIOPROTECTION Sous-direction activités radiologiques et biomédicalesNotice DGSNR/SD9 L/04-V2 |
 |
CONTRAINTES DE RADIOPROTECTION LIEES A L'UTILISATION DE 18FDG DANS UNE UNITE DE MEDECINE NUCLEAIRE
L'emploi de fluor 18, actuellement sous forme de 18FGD, associé à la mise en uvre des caméras TEP dans les unités de médecine nucléaire implique des dispositions particulières sur le plan de la radioprotection, du fait des caractéristiques de ce radioélément et de ses conditions dutilisation. La présente fiche précise les principales dispositions, sous langle de la radioprotection, à prévoir en vue du fonctionnement dune unité TEP.
La mise en uvre de fluor 18 et dune unité TEP ne peuvent s'envisager que dans un service de médecine nucléaire respectant l'ensemble des règles daménagement et déquipement en vigueur fixées notamment dans l'arrêté du 30 octobre 1981. Tout en bénéficiant de linfrastructure du service de médecine nucléaire, il ny a que des avantages à individualiser nettement lunité TEP au sein du service, compte tenu en particulier des émissions photoniques de 511 keV du 18F et du blindage des caméras conventionnelles adapté pour le 99mTc.
En complément des aménagements et équipements habituels dune unité de médecine nucléaire, il y a lieu de prévoir pour lunité TEP:
¨ Une pièce spécifique pour la caméra TEP, dont le poste de commande devra être situé à lextérieur mais permettant de surveiller en permanence le patient. Les parois, y compris si besoin est, les dalles de plafond et de plancher de la pièce doivent être renforcées pour des raisons de radioprotection. En cas de fenêtre en verre plombé entre les 2 pièces, on veillera à ce que lépaisseur du verre soit adaptée à lénergie de 511 keV. Dans le cas où la caméra TEP est couplée à un scanner (TEPSCAN), la salle devra également répondre aux critères daménagement des installations de scannographie, fixés dans la norme NFC 15-161 additif 2. En particulier, la surface minimale de la salle doit être dans ce cas dau moins 20 m², avec aucune dimension linéaire inférieure à 4 m. Les aménagements habituels dune salle de caméra à scintillation sont également à réaliser (revêtements des sol, des murs, ventilation en dépression ).
¨ Une salle dinjection pouvant servir également de salle de repos et dattente des patients avant leur examen. Cette salle, à situer à proximité de la pièce TEP et du laboratoire chaud, doit être pourvue de boxes individuels pour recevoir simultanément au moins deux patients. Les parois de ces boxes doivent être renforcées pour des raisons de radioprotection.
¨ Linstallation dans le laboratoire chaud, dune enceinte blindée ventilée en dépression sous filtre dédiée aux opérations de stockage, de préparation et de mesure des sources de fluor 18. Elle est obligatoirement distincte de celle affectée aux autres radioéléments utilisés à des fins de diagnostic, par contre elle pourra être utilisée pour liode 131. Cette enceinte devra être équipée dun activimètre, adapté à la mesure de lactivité de sources de fluor 18.
¨ Du matériel de manipulation, de transport et de collecte des déchets marqués par du fluor 18. Le choix des matériels devra seffectuer à partir détudes de poste avec comme objectif de maintenir les expositions des personnels aussi bas quil est raisonnablement possible (principe doptimisation). Dans ce but, outre les critères liés à lergonomie, il conviendra détudier la possibilité davoir recours à des dispositifs de préparation et dadministration des solutions radioactives semi automatisés permettant de réduire lexposition des mains des opérateurs.
¨ La protection des parois, y compris les dalles de planchers et de plafonds doit être déterminée sur la base dune source de référence de fluor 18 de 600 MBq positionnée au centre du lit dexamen de lappareil TEP, dans son emplacement définitif, ou des lits ou fauteuils dinjection des boxes de la salle dinjection et dattente. Ces protections doivent permettre de respecter les débits de dose équivalente maximaux admissibles au sein de zones contrôlées ou surveillées.
¨ Lenceinte blindée de manipulation des sources de fluor 18 et les containers de collecte des déchets doivent être conçus de façon que, pour lactivité maximale pouvant y être détenue et manipulée, le débit de dose équivalente ne dépasse pas, à 5 cm des parois et en tout point, 25 mSv/h, y compris à hauteur de la chambre de mesure de lactivimètre de lenceinte. Il conviendra dobtenir des fabricants de ces matériels les attestations et/ou justificatifs garantissant le respect de ces critères.
¨ La protection radiologique des containers de transport dans le service et des protèges seringues devra être également être adaptée à l'énergie du 18FDG. Le débit de dose équivalente à 5 cm de leur paroi ne dépassera pas 100 µSv/h, pour lactivité maximale que peut recevoir le dispositif.
Les règles générales visant à assurer la protection des personnels fixées dans le code du travail sont bien entendu applicables au cas des services de médecine nucléaire et de leur unités TEP, en particulier :
¨ Désignation par le chef détablissement d'une personne compétente en radioprotection (PCR). A noter que dans le cas détablissement doté une installation soumise au moins à déclaration au titre du code de lenvironnement (cas des services de médecine nucléaire), il doit exister un service compétent en radioprotection dont leffectif comprend des salariés de létablissement ayant suivi avec succès la formation de personne compétente en radioprotection ;
¨ Analyse des postes de travail en tenant compte notamment des procédures mises en uvre, de lactivité et de la nature des sources radioactives manipulées pour identifier et quantifier le risque encouru. A partir de cette analyse, seront définis puis mis en place les moyens de protection adaptés ;
¨ Délimitation des zones contrôlées ou surveillées, après évaluation des risques par la PCR ;
¨ Classement des personnels exposés en catégorie A ou B, par le chef détablissement après avis du médecin du travail ;
¨ Surveillance médicale du personnel exposé comprenant un suivi dosimétrique de lexposition externe et interne ;
¨ Formation et information des personnels du service de médecine nucléaire. A noter que cette formation doit être faite lors de la prise de fonction puis renouvelée régulièrement et au moins une fois tous les 3 ans.
Lutilisation de sources de fluor 18 nécessitera de modifier les consignes de travail et de sécurité précisant les dispositions à respecter pour :
- La réception, lentreposage et la manipulation des radionucléides ;
- La collecte, le tri, lentreposage et lélimination des déchets et des effluents radioactifs ou non produits dans linstallation de médecine nucléaire ;
- Les contrôles de contamination des surfaces et des locaux et notamment la fréquence, lemplacement, le matériel à utiliser et le mode opératoire ;
- Les vérifications du bon fonctionnement des équipements de lunité de médecine nucléaire concourrant à la radioprotection tels que les systèmes de ventilation et les matériels destinés à lentreposage et à la manipulation des radionucléides.
- Lintervention en zones surveillées ou contrôlées de personnels qui ny sont pas normalement en poste.
Les caractéristiques du fluor 18 et ces conditions dutilisation conduisent à privilégier le risque dexposition externe à distance ou au contact des sources par rapport à celui dexposition interne. Le suivi dosimétrique du personnel de lunité TEP est donc à adapter en conséquence :
¨ Dosimétrie passive mensuelle ;
¨ Dosimétrie des mains (à considérer comme impérative avec le port de bagues thermoluminescentes) ;
¨ Dosimétrie opérationnelle, si poste en zone contrôlée.
Pour le seul fluor 18, en conditions normales de travail, un suivi de lexposition interne nest pas pertinent (utilisation uniquement sous forme liquide à température ambiante, période de 110 mn et descendant stable (18O), radioélément peu radiotoxique 5,7 10-11 Sv/Bq en inhalation et 4,9 10-11
Sv/Bq en ingestion) dautant que du fait de la très courte période du radioélément, ce suivi par examen radiotoxicologique ou anthropogammamétrie par des laboratoires spécialisé (IRSN) est matériellement très difficile. En revanche, si les personnels en poste dans lunité TEP exercent dans le reste du service de médecine nucléaire, le suivi de leur exposition interne doit demeurer.
Compte tenu des modifications de lunité de médecine quentraîne lemploi de fluor 18, il est nécessaire de procéder à une actualisation de lautorisation, prise au titre de larticle R.1333-24 du code de la santé publique, qui est délivrée au médecin nucléaire responsable de lunité. En conséquence, il appartient à ce responsable de constituer le dossier correspondant en temps utile[1] à transmettre à :
Autorité de sûreté nucléaire
DGSNR / SD9
6 place du colonel Bourgoin 75572 Paris cedex 12
Le formulaire à utiliser suivant les indications de la notice explicative, peut être obtenu sur simple demande à cette adresse, par courriel à SD9.DGSNR@asn.minefi.gouv.fr ou par téléphone (01 44 59 47 85).
Après réception et vérification du dossier, lASN peut délivrer une autorisation provisoire valable quelques mois pour permettre au service dapprovisionner des sources de fluor 18 et les sources scellées détalonnage et de correction datténuation de la caméra TEP et ainsi procéder à la mise au point de son linstallation avant son démarrage en routine. Durant cette période, lASN effectuera le contrôle de lunité TEP qui conditionnera la délivrance de lautorisation définitive couvrant le fonctionnement du service de médecine nucléaire et de son unité TEP. A noter que si lappareil est un modèle de type TEPSCAN, létablissement devra également faire procéder à la vérification du scanner par un organisme agréé pour le contrôle des installations de radiologie, le rapport de contrôle correspondant devant être transmis à lASN.
Le fluor 18 est un radioélément émetteur de positons qui s'annihile avec un électron du milieu pour donner deux photons de 511 keV. Sa période radioactive est de 110 mn et son descendant est loxygène 18 qui est un élément stable.
Pour les calculs de radioprotection les valeurs de Couche de Demi Atténuation (CDA) et d'épaisseur dixième (C 1/10ème ) pour les matériaux les plus courants à utiliser sont :
|
|
CDA |
C 1/10ème |
|
Plomb |
4 mm |
16 mm |
|
Acier |
19 mm |
64 mm |
|
Béton ordinaire (ou parpaings pleins) |
51 mm |
170 mm |
Rappel : Le débit de Kerma dans lair pour le Fluor 18 est de 135 mGy.m2.GBq-1.h-1
[1] Il importe que ce dossier soit déposé suffisamment tôt à la DGSNR/SD9 par rapport à la date prévisionnelle douverture de lunité TEP (au moins 1,5 mois) pour faciliter, si besoin est sa finalisation, et permettre son instruction dans de bonnes conditions, faute de quoi lapprovisionnement en fluor 18 ne pourrait être autorisée aux échéances envisagées.
[1] Le Journal Officiel ; Article L. 6122-14 ; Liste des équipements considérés comme matériels lourds.
[2] www.chu-caen.fr ; Informations sur le CHU de Caen.
[3] Circulaire DGS/DH/AFS n° 98-213 du 24 mars 1998 ; NOR : MESP9830149C « relative à lorganisation des soins en cancérologie dans les établissements dhospitalisation publics et privés ».
[4] CEDIT, Les recommandations référence 02.06.1 « La Tomographie par Emission de Positions couplée à la Tomodensitométrie (TEP-TDM).
[5] Circulaire DHOS/SDO/O 4 n°2002-242 du 22 avril 2002 ; NOR : MESH0230213C « relative aux modalités dimplantation des tomographes à émission de positons (TEP) et des caméras à scintillation munies dun détecteur démission de positons (TEDC) ».
[6] Arrêté du 18 décembre 2001 ; NOR : MESH0124368A « fixant lindice de besoins afférent aux appareil de diagnostic utilisant lémission de radioéléments artificiels (caméra à scintillation munie de détecteur d émission de positons en coïncidence, tomographe à émission, caméra à positons) ».
[7] Revue Médecine Nucléaire-Imagerie fonctionnelle et métabolique-2004-vol.28-n°11, P.J. Lamy ; J.Grenier « Tomographie par Emission de Positons au 18Fluorodeoxyglucose et Marqueurs Tumoraux ».
[8] Décret du 31 mars 2003 « relatif à la protection des travailleurs contre les dangers des rayonnements ionisants ».
[9] Notice DGSNR/SD9 L/04-V3 « contraintes de radioprotection liées à lutilisation de 18FDG dans une unité de Médecine Nucléaire ».
[10] Norme NC 15-161 « relative à laménagement dune salle qui accueillera un appareil de radiodiagnostic médical ou dentaire ».
[11] Revue de lACOMEN, 1999, vol 5, n°2 « Lenvironnement dune caméra TEP ».
[12] Revue Médecine Nucléaire-Imagerie fonctionnelle et métabolique-2004-vol.28-n°5, J. Pasquier ; I. Brenot-Rossi ; N. Hassan Sebbag ; R.Sauvan « Installation dun TEP-TDM : réglementation, cahier des charges, locaux matériels ».
[13] Revue Médecine Nucléaire-Imagerie fonctionnelle et métabolique-2004-vol.28-n°5, H. Visseaux ; J.P. Vuillez ; J.Y. Giraud « Etude dosimétrique et optimisation de la radioprotection en scintigraphie au [18-F]-FDG ».
![]() Figure 1 :
www.chu-caen.fr.
Figure 1 :
www.chu-caen.fr.
![]() Figure 2 :
www.ancelots.net.
Figure 2 :
www.ancelots.net.
![]() Figure 3 :
www.cermep.fr/activite/acti3.htm.
Figure 3 :
www.cermep.fr/activite/acti3.htm.
![]() Figure 5,6 et 7 : Brochure commerciale Lemer Pax.
Figure 5,6 et 7 : Brochure commerciale Lemer Pax.