Bonnes Pratiques de
Réalisation adaptées au contexte africaine
|
|
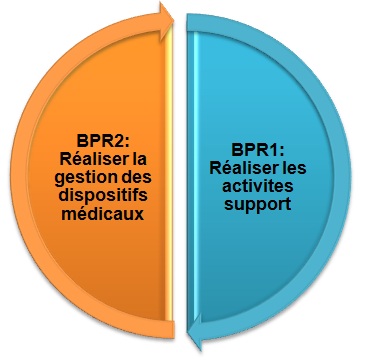
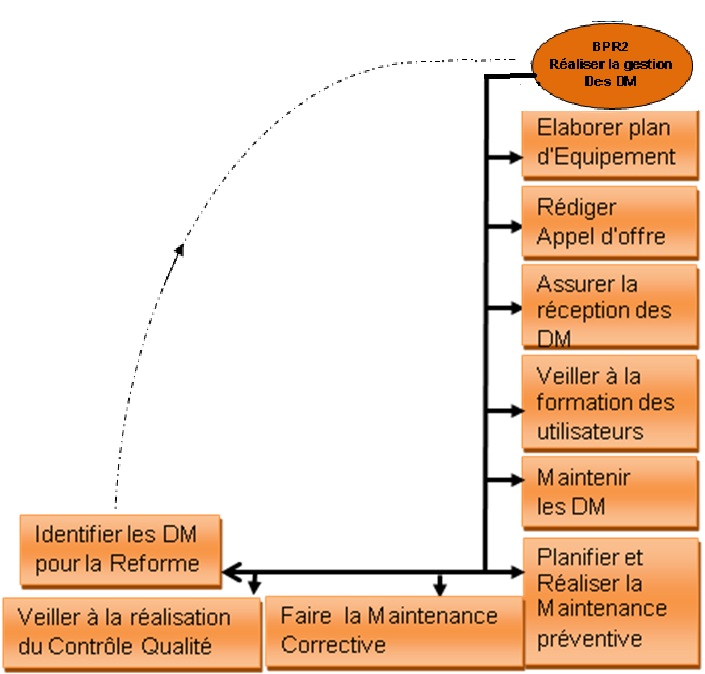
BPR2
Réaliser
la
gestion
des
dispositifs
médicaux
|
Critères
associés
|
|
BPR-2-01
Elaborer
le
plan
d'équipements
:
Le service biomédical en collaboration avec le service de
Finance élaborent des plans d'équipements pluriannuels
|
Ils conseillent, identifient et
élaborent, avec les services de soins, médico-techniques
ou utilisateurs des technologies, et les directions, les besoins, les
priorités, les justifications et les caractéristiques
essentielles souhaitées dans l'exploitation des dispositifs
médicaux à court, moyen et long terme.
|
Ils proposent à la
direction des plans stratégiques d'investissement de nouveaux
dispositifs médicaux et de remplacement des plus vétustes
ou critiques (éventuellement selon la fréquence de pannes
et la durée de vie de l’équipement donne par le
fabriquant) en présentant les implications et effets induits de
leur exploitation.
|
Ils gardent une trace
écrite des différentes phases du processus ayant conduit
à la décision de financement par la direction…
|
|
BPR-2-02
Rédiger l'appel d'offre:
Le service biomédical en collaboration avec le service
d’approvisionnement gèrent les processus d'acquisition des
dispositifs médicaux.
|
Ils hiérarchisent les
acquisitions potentielles avec les services de soins et les directions,
en fonction des impacts cliniques, techniques, logistiques et
financiers qu'elles auront en exploitation, et contribue au bon
déroulement du processus d'achat.
|
Ils négocient dès
l'achat les contrats de garantie à court terme et, le cas
échéant, de maintenance à moyen terme visant
à obtenir le maximum de performances des dispositifs
médicaux sur toute leur durée de vie
prévisionnelle.
|
|
BPR-2-03
Assurer la
réception de DM :
Le service biomédical s'assure de la mise en fonctionnement
correcte des nouveaux dispositifs médicaux.
|
Il s'assure que les aspects
réglementaires et les contraintes d'implantation sont
respectés dans l'aménagement des lieux d'exploitation
prévus pour l'installation des dispositifs médicaux,
qu'ils soient fixes ou mobiles, dans l'établissement de
santé ou, quand cela fait partie de ses missions, au domicile du
patient.
|
Il enregistre les informations
permettant de s'assurer de la conformité de ce qui est
reçu par rapport à la commande dans un document de
réception de dispositif médical.
|
Il procède si
nécessaire à des essais de fonctionnalité et des
mesures des caractéristiques initiales des performances
appelés "tests de recette" ou "qualifications" (qualification
d'installation, qualification fonctionnelle, qualification des
performances), utiles en cas de dérives ou de
réclamations ultérieures.
|
En cas de non-conformité
mise en évidence lors de la réception, des mesures
adaptées sont engagées. L’enregistrement des
non-conformités et le suivi des moyens et solutions
apportées pour une remise en conformité sont
réalisés
|
Il gère le bon de
réception signé par les parties, documente l'inventaire,
identifie et marque de manière univoque les dispositifs et
informe les services de soins et les directions concernés…
|
|
BPR-2-04
Veiller à la formation
des utilisateurs :
Le service biomédical s'assure des aptitudes à l'usage
des dispositifs médicaux.
|
Il planifie, ou aide les
services de soins et médico-techniques ou utilisateurs des
technologies à planifier les formations des utilisateurs
prévues lors de l'achat des dispositifs médicaux, et
celles devenues nécessaires au cours de leur exploitation suite
aux rotations ou changements du personnel, ainsi que la
réactualisation des connaissances du fait du temps ou de
modifications apportées à l’équipement au cours de
son exploitation.
|
Il s'assure à la mise en
service de l’équipement que les guides d'emploi, les manuels
d'instruction, de nettoyage et d'utilisation, rédigés
dans la langue usuelle du pays et/ou de l'utilisateur, sont fournis et
mis à disposition du personnel utilisateur.
|
Il s'assure à la
première mise à disposition de l’équipement que
les documentations d'entretien périodique, de calibration et de
mise en service sont disponibles et accessibles pour tout utilisateur
ou autre personnel impliqué.
|
Il veille à ce que les
formations aux utilisateurs soient délivrées par des
personnes qualifiées et compétentes par rapport aux
dispositifs médicaux concernés. Il s'assure que les
formations réglementaires, quand elles existent, sont
réalisées
|
Il enregistre dans un document
d'aptitude à l'usage que les utilisateurs médicaux et
responsables de services de soins et médico-techniques ou
utilisateurs des technologies ont été formés,
suivant les besoins, à la mise en service et à la
manipulation du dispositif médical et qu’ils disposent des
documentations utiles à leur fonctionnement et des protocoles de
vérification avant leur emploi sur les patients...
|
|
BPR-2-05
Maintenir
les
DM
:
Le service biomédical gère l'exploitation des dispositifs
médicaux dont il a la charge.
|
Il dresse une liste des
dispositifs critiques, vis-à-vis du patient et de l'utilisateur,
en cohérence avec les règlements ou exigences pouvant
existe.
|
La criticité est
qualifiée (formulée) mais aussi quantifiée sur une
échelle homogène entre
0% et 100% afin d'en permettre la comparaison entre services et
inter-établissements.
|
Il prévoit, avec les
services de soins, médico-techniques ou utilisateurs des
technologies, et techniques de l'établissement, un processus
spécifique d'exploitation des dispositifs médicaux
critiques et des alternatives ou « modes dégradés
» en cas de problème d'exploitation des dispositifs
médicaux critiques et des alternatives ou « modes
dégradés » en cas de problème.
|
Il veille à la
qualité et conformité des accessoires, consommables et
fluides associés au fonctionnement des dispositifs
médicaux.
|
Il contribue au processus de
vigilance au sein de l'établissement pour tout danger potentiel
ou risque en exploitation qui pourrait être identifié.
|
Il s'assure que les formations
sont délivrées et que les moyens techniques
spécifiques et nécessaires au maintient des performances
sont accessibles au personnel du service biomédical.
|
Il entretient une communication
active avec les services de soins sur l'exploitation des dispositifs
médicaux et leurs critères de succès en usage.
|
Il renseigne l'inventaire et le
suivi des dispositifs médicaux avec les observations
d'exploitation et les indicateurs de suivi du succès en usage.
|
Il vérifie que les
matériels prêtés, mis à disposition ou
loués sont tracés et gérés selon la
réglementation en vigueur.
|
|
BPR-2-06
Planifier
et
réaliser
la
Maintenance
Préventive
:
Le service biomédical gère la maintenance
préventive des dispositifs médicaux dont il a la charge.
|
Il élabore les programmes
de maintenance préventive en fonction des données des
constructeurs (incluant d’éventuelles modifications à
faire, demandées ou proposées par le constructeur), mais
aussi en tenant compte de la criticité du dispositif
médical, de la réglementation, des conditions d'emploi et
de son intensité d'usage, et de la politique de maintenance de
l’établissement validée par les instances.
|
Il planifie avec les services de
soins et médico-techniques ou utilisateurs des technologies la
disponibilité d'accès aux dispositifs médicaux et
propose éventuellement des alternatives d'usage.
|
Il réalise, ou fait
réaliser, la maintenance préventive au minimum selon les
recommandations du constructeur, les accords contractualisés ou
des procédures internes validées.
|
Une fois la maintenance
préventive achevée, il effectue un contrôle
qualité complet de toutes les fonctionnalités, autant
qualitatif (acceptable, bon, excellent..) que quantitatif sur les
caractéristiques essentielles (valeurs et incertitudes des
mesures).
|
Il remet en exploitation les
dispositifs médicaux conformes au contrôle qualité
en informant l’utilisateur de l'activité réalisée
et de la période prévisionnelle pour la prochaine
maintenance préventive (éventuellement avec une
étiquette du type "maintenance effectuée le : … ",
"prochaine maintenance prévue le : ...").
|
|
BPO-2-07
Faire
la
maintenance
Corrective:
Le service biomédical gère la maintenance corrective des
dispositifs médicaux dont il a la charge.
|
Il veille à ce que tout
utilisateur connaisse et utilise la procédure prévue mise
en place en cas de panne d'un dispositif médical.
|
Il planifie avec les services de
soins la disponibilité d'accès aux dispositifs
médicaux en panne et propose éventuellement des
alternatives d'usage.
|
Il adresse une personne
compétente du service biomédical pour réaliser
systématiquement un diagnostic de panne et identifier les
actions correctives à mener, le cas échéant en
s’appuyant sur les contrats de maintenance couvrant les dispositifs.
|
Il s'assure de l'application des
protocoles de décontamination ou désinfection ou de
stérilisation des dispositifs avant maintenance.
|
Il met à disposition du
personnel utilisateur toute information sur l'avancement dans le
processus de maintenance corrective.
|
Une fois la maintenance
corrective achevée, il effectue un contrôle qualité
complet de toutes les fonctionnalités, autant qualitatif
(acceptable, bon, excellent..) que quantitatif sur les
caractéristiques essentielles (valeurs et incertitudes des
mesures).
|
Il remet en exploitation les
dispositifs médicaux conformes au contrôle qualité
en informant l’utilisateur de la source de la panne et de
l'activité réalisée.
|
Il documente et rend facilement
accessible à toute personne autorisée un rapport
d'intervention en maintenance corrective comportant les informations
pertinentes (dates et intervenants, identification des dispositifs
médicaux, activités techniques réalisées,
pièces changées et temps de main d'œuvre, les
écarts, les défauts, les dysfonctionnements
corrigés, les tests et contrôles effectués et leurs
conformités, origines probables de la défaillance,
propositions éventuelles d'actions de prévention..).
|
Il veille au respect
réglementaire de conservation des données techniques sur
les dispositifs médicaux.
|
Il s'assure du respect de la
confidentialité sur les données concernant les
prestataires…
|
|
BPR-2-08
Veiller à la
réalisation du Contrôle Qualité :
Le service biomédical travail en collaboration avec le service
de contrôle Qualité National pour gère le
contrôle qualité des dispositifs médicaux dont il a
la charge.
|
Il conçoit et planifie
les opérations de contrôle qualité.
|
Il communique sa planification
aux services en charge de la qualité (Service National de
Contrôle Qualité).
|
Le dispositif est
immédiatement étiqueté "conforme" ou
"non-conforme" suivant les résultats. Une non-conformité
est due à une exigence spécifiée non
respectée.
|
Il remet en exploitation les
dispositifs médicaux déclarés conformes au
contrôle qualité en informant l’utilisateur des
résultats obtenus et de la période prévisionnelle
pour le prochain contrôle qualité. Il renvoie en
maintenance les dispositifs médicaux déclarés "non
conformes" au contrôle qualité.
|
Il documente et rend facilement
accessible à toute personne autorisée un rapport de
contrôle qualité comportant les informations pertinentes
(date de contrôle réalisé et date du
précédent contrôle, intervenant et habilitation,
dispositif médical concerné, ECME utilisé et
période de validité, méthode ou norme
utilisée (si nécessaire), résultats qualitatifs et
quantitatifs des contrôles effectués, déclaration
de conformité ou non, suivi des non conformités, date ou
période prévisionnelle du prochain contrôle
qualité...)
|
|
BPR-2-09
Identifier les DM pour la Réforme :
Le service biomédical en collaboration avec le commuté de
direction de la structure sanitaire gèrent la réforme
(déclassement ou mise hors service) des dispositifs
médicaux dont il a la charge.
|
Ils élaborent et valident
la planification de réforme (déclassement ou mise
hors-service) avec les services de soins, médico-techniques ou
utilisateurs des technologies, et les directions, en s'assurant de la
continuité des soins.
|
Ils prévoient en
partenariat avec les services de soins ou médico-techniques ou
utilisateurs des technologies une procédure de réforme
inopinée en cas de problème incurable ou de coût de
réparation trop élevé.
|
Le dispositif médical
réformé (déclassé), ses accessoires et
éventuellement ses consommables spécifiques sont
marqués de manière visible et explicite et stockés
dans un lieu identifié, garantissant leur non-usage, en
attendant leur retrait physique effectif.
|
La documentation associée
est retirée physiquement ou archivée dans un endroit
spécifié.
|