Cartographies
des risques liés aux dispositifs ci-dessus analysés (voir
Annexe 1)
Quelques exemples d’une analyse des risques liés au service
d’endoscopie :
Clic ici pour telécharger ces
exemples
Commentaire des résultats
et actions à mener:
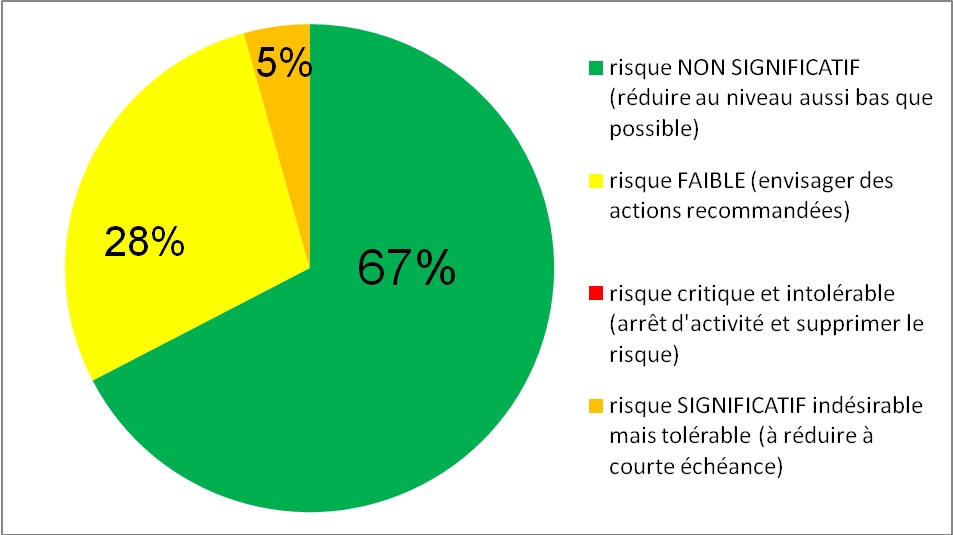
Sur l’ensemble des 46
catégories des DM analysés, nous remarquons que environ
67% représentent l’ensemble des dispositifs médicaux
à criticité non significative c.à.d. que les
risques liés à ces dispositifs restent toujours
tolérable mais par contre doivent faire l’objet
d’engagement des actions optionnelles donc la maintenance
préventive doit être régulière.
28% des dispositifs analysés
font l’objet d’une criticité à risque
tolérable ce qui conduit à réduire le risque
à un niveau aussi bas que raisonnablement possible mais
sans caractère d’urgence et à un coût
limité (à 5 ans selon le Centre Médical de
Bligny) et de plus il faut prendre une mise en garde dans le document
d’accompagnement de chaque dispositif médical
5% des équipements
médicaux analysés peuvent faire l’objet d’un risque
significatif et indésirable si jamais ils ne sont pas bien
suivis. Il faut donc apporter toutes solutions pour la réduction
du risque à un niveau aussi bas que raisonnablement possible et
à courte échéance (6 mois à 1 an) ou
a supprimer.
⇒ mise en garde sur le
dispositif lui-même dans la mesure du possible et / ou formation
III.4 Les
enseignements
• Assurer la
mise à jour et le suivi régulier de la criticité
des DM et des fiches de sécurité
• Besoin des ECME
pour le suivi de la démarche Qualité des DM.
• Etendre le
calcul de criticité à tous les services et sur l’ensemble
des DM.
• Organiser
régulièrement des réunions d’informations et
d’échanges entre les services des soins, du biomédical et
qualité sur l’analyse des risques liées au DM.
•
Paramétrer la formule de criticité dans la GMAO pour
avoir un calcul sur chaque DM
III.5 Les
propositions
1. Un diagramme en arbre (Suivi des recommandations par rapport
à la HAS – critère 8K)
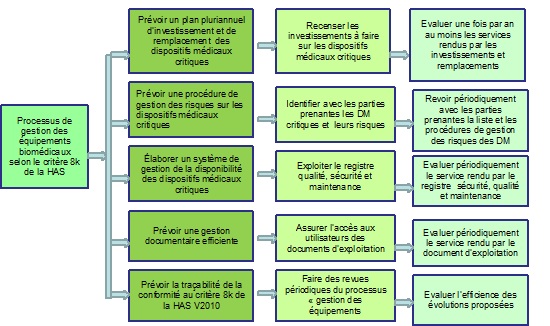 fig.17
fig.17 diagramme en arbre selon le critère
8k de la HAS
2. Proposition d’une
procédure pour cartographier les autres services
Pour telécharger cette procédure
d’analyse
de
criticite
d’un
dispositif
médical
clic
ici.
3.
Proposition
d’une
méthode
d’évaluation
de
la
criticité,
alternative
à
la
méthode
AMDEC
(la
méthode
PIEU)
La méthode PIEU présente quatre paramètres qui,
associés permettent de déterminer la criticité de
chaque catégorie d’appareil. Ces quatre critères sont
pondérés pour chaque type d'équipement par des
valeurs allant de 0.01 à 3 (0.01 étant le
paramètre ayant le plus d'importance, et 3 le moins critique)
Cette méthode PIEU présente certains avantages
parce qu’en retenant les quatre paramètres i haut
mentionnés dans le tableau en bas, on intègre
indirectement les autres facteurs vus dans le diagramme de Hishikawa
comme par exemple :
• La nature du service utilisateur car une
désignation précise du dispositif médical permet
de s’en dispenser. (Exemple : respirateur d’anesthésie).
• L’âge du matériel
• L’impact du dysfonctionnement sur
l’activité du service car en prenant en compte l’importance de
l’équipement « I » on intègre
déjà cette notion, en effet si un DM est unique dans
l’établissement, en cas de panne, il en résulte
automatiquement un arrêt de l’activité du service.
A -
GRILLE DE CALCUL
DE CRITICITE AVEC LA METHODE PIEU (Fig. 18)
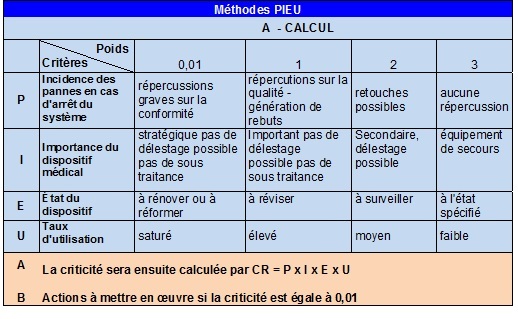
Il en
résulte que selon la formule PIEU= P x I x E x U, plus la valeur est petite, plus le
dispositif est critique
En fonction de cette méthode, le classement des DM
imposé est le suivant :
PIEU < 1 : Très critique
1≤ PIEU ≤ 10 Moyennement critique
PIEU > 10 Moins critique
La détermination de cette criticité va
permettre de mettre en évidence les équipements sur
lesquels doit être axée en priorité la maintenance
préventive et de prioriser les actions à mettre en œuvre
Par exemple, les équipements sensibles, très
utilisés et non remplaçables facilement seront les plus
surveillés en terme de maintenance. Un type d’équipement
disponible en grand nombre dans le Centre et peu critique sera moins
sensible ...
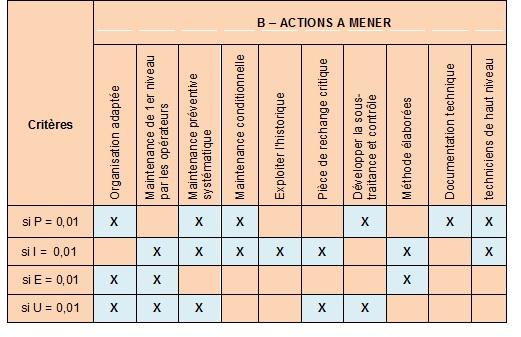
B –
ACTIONS A MENER (Fig. 19)
Conclusion
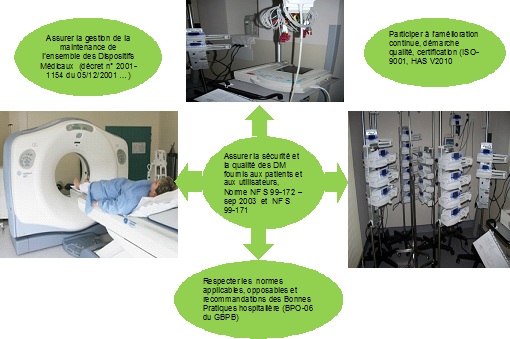
La qualité et la
sécurité des dispositifs médicaux, la gestion des
risques liés à leur exploitation, la satisfaction du
patient, c’est l’affaire de tous et c’est une volonté de
chacun
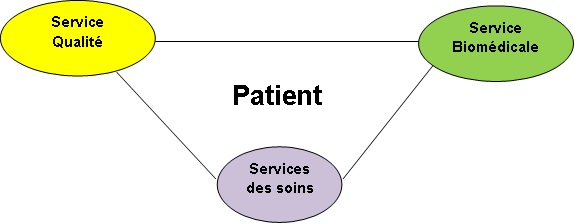
 Fig 20
Fig 20 : les services qualité ,
biomédicale et des soins
au service de la sécurité du patient et des DM.
Au
terme
de
ces
onze
semaines
passées
au
sein
du
Centre
Médical
de
Bligny,
il
en
ressort
un
bilan
plus
que
satisfaisant
autant
pour moi que pour le Centre Médical de
Bligny.
Ma principale mission a porté
sur l’analyse de la criticité des DM effectuée dans
certains services (USI, Radiologie, endoscopie), à l’issue de
laquelle j’ai eu à établir une cartographie des
différents types de dispositifs médicaux analysés
par niveau de criticité en fonction des recommandations des
bonnes pratiques de la Haute Autorité de Santé, ce qui
m’a conduit à définir les actions à mener afin de
réduire les risques.
Cette étude va donc permettre
d’établir les bases de ce que va permettre d’établir les
bases de ce qui constitue la politique de maintenance de
l’établissement en priorisant les maintenances
préventives et curatives des dispositifs les plus critiques.
Comme atouts personnel,
ce stage m’aura permis de me plonger dans l’univers des normes et
des exigences en matière de management des dispositifs
médicaux dans un établissement de santé, un
univers qui m’était complètement étranger compte
tenu de ma formation antérieure en tant que technicien en
maintenance des équipements biomédicaux.
Les connaissances qualité et
gestion des risques qui viennent donc renforcer mes compétences
techniques me serviront avec beaucoup d’utilité dans mes futures
responsabilités.
Accréditation :
procédure externe à un établissement volontaire,
qui permet de lui conférer de façon publiquement accessible une reconnaissance de
qualité au regard de références
préalablement établies.
Action
corrective
: action
entreprise pour éliminer les causes d’une non-conformité,
d’un défaut ou de tout autre événement
indésirable existant pour empêcher leur renouvellement
(ISO 9000 : 2000).
Action
préventive
: action
entreprise pour éliminer les causes d’une non-conformité,
d’un défaut et de tout autre événement
indésirable potentiel pour empêcher qu’ils ne se
produisent (ISO 9000 : 2000).
Afnor
: Association française
de normalisation
Afssaps
: Agence française de
sécurité sanitaire des produits de santé
Amdec
: Analyse des modes de
défaillance, leurs effets et leurs criticités
Anaes
: Agence nationale
d’accréditation et d’évaluation en santé.
Assurance
de
la
qualité :
partie du management de la qualité visant à donner
confiance dans la satisfaction des exigences pour la qualité
(voir série des normes ISO 9000 : 2000, Éd Afnor).
Bonnes
pratiques
fonctionnelles :
actions de management à mettre en oeuvre afin d’avoir une
organisation robuste et efficiente.
Bonnes
pratiques
opérationnelles
: actions à mettre en œuvre afin
de
réaliser des activités pertinentes et optimales au sein
du service biomédical.
Certification
: procédure par
laquelle une tierce partie donne une assurance écrite qu’un
produit, un processus, une
organisation ou un service sont
conformes à des exigences spécifiées.
CMB
: Centre Médical de Bligny
Conformité
: satisfaction
d’une exigence (ISO 9000 : 2000).
Contrôle
qualité :
activités telles que mesurer, examiner, essayer ou passer au
crible une ou plusieurs caractéristiques d’une entité,et
comparer les résultats aux exigences spécifiées en
vue de déterminer si la conformité est obtenue pour
chacune de ces caractéristiques (ISO 9000). Ensemble des
opérations destinées à évaluer le maintien
des performances revendiquées par le fournisseur ou, le cas
échéant, fixées par le directeur
général de l’Agence française de
sécurité sanitaire des produits de santé
(décret no 2001-1154).
Critère
:
énoncé d’un moyen ou d’un élément plus
précis permettant de satisfaire la référence
d’accréditation.
Décret
: décision,
ordre émanant du pouvoir exécutif.
Démarche
qualité :
ensemble des dispositifs mis en place par une structure en vue de
répondre aux objectifs et aux conditions de
l’accréditation ou à des exigences de qualité
librement adoptées. Ce programme rend nécessaire une
évaluation régulière et permanente des
activités concernées, et la fourniture des preuves
correspondantes.
Dispositif
médical : tout
instrument, appareil, équipement, matière ou autre
article, utilisé seul ou en association, y compris le logiciel
nécessaire à son bon fonctionnement, destiné par
le fournisseur à être utilisé chez l’homme à
des fins :
– de diagnostic, de
prévention, de contrôle, de traitement ou
d’atténuation d’une maladie ;
– de diagnostic, de contrôle,
de traitement, d’atténuation ou de compensation d’une blessure
ou d’un handicap ;
– d’étude, de remplacement ou
modification de l’anatomie ou d’un processus physiologique ;
– de maîtrise de la conception
;
– et dont l’action principale voulue
dans ou sur le corps humain n’est pas obtenue par des moyens
pharmacologiques ou immunologiques ni par métabolisme, mais dont
la fonction peut être assistée par de tels moyens
(directive 93/42/CEE, JOCE du 12/7/93, no L 169/1)
Documentation
qualité
:
ensemble des documents inhérents à la mise en place d’une
démarche qualité.
ECME
: équipement de
contrôle, de mesure et d’essai.
Exigence
: besoin ou attente qui
peut être formulé, habituellement implicite, ou
imposé (ISO 9000 : 2000).
Formation
des
utilisateurs : phase
d’apprentissage, pendant laquelle le personnel médical et
paramédical acquiert les connaissances indispensables pour faire
fonctionner correctement le dispositif médical récemment
acquis.
Fournisseur
: organisme ou personne
qui procure un produit (ISO 9000 : 2000).
Gestion
des
dispositifs
médicaux : différentes actions mises en oeuvre
depuis
l’achat d’un dispositif médical jusqu’à sa réforme.
Gestion
des
matériels
et
ECME
: gestion de l’ensemble des outils et appareils électriques
divers (tels que perceuse, soudeuse, multimètre…) qui permet au
service biomédical de mener ses missions de maintenance et de
contrôle à bien.
Gestion
de
la
qualité :
processus par lequel le service biomédical organise sa
démarche qualité et la met en oeuvre.
Gestion
des
risques : application
systématique des politiques de gestion, des procédures et
des pratiques à des tâches d’analyse, d’évaluation
et de maîtrise des risques (NF EN ISO 14 971).
GMAO
: gestion de la maintenance
assistée par ordinateur.
Habilitation
: action de donner
l’aptitude légale à faire quelque chose
Indicateur
: donnée objective
décrivant une situation d’un point de vue quantitatif.
Infection
nosocomiale : Infection
acquise dans un établissement de soins, qui se déclare 48
à 72h après l’admission (tenir compte du délai
d’incubation de la maladie car peut avoir été
contractée avant l’hospitalisation =infection communautaire)
Maintenance
: ensemble des
activités destinées à maintenir ou rétablir
un bien dans un état ou dans des conditions données de
sûreté de fonctionnement, pour accomplir une fonction
requise (NF X 60-000). Ensemble des activités destinées
à maintenir ou à rétablir un dispositif
médical dans un état ou dans des conditions
données de sûreté de fonctionnement pour accomplir
une fonction requise (décret no 2001-1154).
Maintenance
corrective : maintenance
effectuée après défaillance (NF X 60-010).
Maintenance
préventive :
maintenance effectuée selon des critères
prédéterminés, dans l’intention de réduire
la probabilité de
défaillance d’un bien ou de
dégradation d’un service rendu (NF X 60-010).
Maîtrise
de
la
qualité
: partie du management de la qualité axée sur la
satisfaction des exigences pour la qualité (ISO 9000 : 2000).
Mise
en
service : installation et
mise en marche d’un matériel médical dans le service
utilisateur en présence des utilisateurs, du service
biomédical et/ou du fournisseur.
Non-qualité
: écart
entre la qualité visée et la qualité effectivement
obtenue.
Norme
: accord documenté
contenant des spécifications techniques ou autres
critères précis destinés à être
utilisés systématiquement en tant que règles,
lignes directrices ou définitions de caractéristiques
pour assurer que des matériaux, produits, processus et services
sont aptes à leur emploi.
Norme
opposable : norme
spécifiée dans un texte réglementaire comme une
directive européenne, un décret ou un arrêté
ministériel en charge d’une activité. Ses
responsabilités, objectifs mesurables et moyens sont
définis.
Planification
: action d’organiser
les activités.
Pieu
: Incidence des pannes ,
importance de l’équipement, état de l’équipement,
taux d’utilisation de l’équipement.
Processus
: système
d’activités utilisant des ressources pour transformer des
éléments d’entrée en éléments de
sortie (ISO 9000 : 2000).
Procédure
: manière
spécifiée d’effectuer une activité ou un processus
(ISO 9000 : 2000).
Qualification
: ensemble de ce qui
constitue le niveau de capacité, de formation, reconnu à
un employé.
Qualité
: aptitude d’un
ensemble de caractéristiques intrinsèques d’un produit,
d’un système ou d’un processus à satisfaire
les exigences des clients et autres parties
intéressées (ISO 9000 : 2000).
Réforme
: retrait du parc de
dispositifs médicaux.
RSQM
: registre
sécurité, qualité et maintenance.
Stock
: ensemble des articles
stockés, nécessaire à la réalisation
optimale de la fonction, c’est-à-dire dans les meilleurs
délais, avec un minimum de coûts et un maximum de
sécurité.
Système
de
management
de
la
qualité : système permettant d’établir la
politique qualité et les objectifs qualité et d’atteindre ces objectifs (ISO 9000 : 2000).
Textes
opposables
(droit
français) : Les décrets et arrêtés
sont
opposables : ils s’imposent aux établissements de santé,
publics et privés. Les circulaires, qui précisent
l’interprétation correcte de ces textes ou explicitent les
procédures administratives utiles à leur application,
n’apportent pas d’obligations supplémentaires et n’ont pas de
fait de valeur juridique en tant que telle. Les « recommandations
» ou « guides de bonne pratique » n’ont pas de force
obligatoire, sauf quand ils font l’objet d’un arrêté (par
exemple : GBEA, bonnes pratiques de pharmacie hospitalières,
bonnes pratiques cliniques et biologiques de l’AMP) ; cependant, ils
lient les agents publics chargés du contrôle et de
l’inspection qui doivent s’y référer pour
apprécier les situations qu’ils sont amenés à
constater.
Traçabilité
: aptitude
à retrouver l’historique, l’utilisation ou la localisation d’une
entité au moyen d’identifications enregistrées.
UTC
: Université de
Technologie de Compiègne
Bibliographie
et
Références
[1]
Site web Visite le 28/04/2011
http://www.cm-bligny.com
[2] Site
web
visite
le
28/04/2011
http://www.cm-bligny.com/IMG/pdf/Bligny_historique_2008_web_size.pdf
[3]
Site web
visite le 29/04/2011
http://www.cm-bligny.com/-Poles-d-activites-.html
[4]
Site web
visite le04/05/2011
http://www.has-sante.fr/portail/upload/docs/application/pdf/2008-12/20081217_manuel_v2010_nouvelle_maquette.pdf
[5]
Site web visite le02/05/2011
http://www.sante.gouv.fr/adm/dagpb/bo/2001/01-49/a0493242.htm
Décret n° 2001-1154 du 5 décembre 2001 relatif
à l'obligation de maintenance et au contrôle de
qualité des dispositifs médicaux.
http://www.infirmiers.com/pdf/maintenance_DM.pdf
Maintenance
des
dispositifs
médicaux:
Obligation
et
recommandations
http://www.legifrance.gouv.fr/WAspad/UnTexteDeJorf?numjo=SANP0320928A
Arrêté du 3 mars 2003 fixant les listes des dispositifs
médicaux soumis à l'obligation de maintenance et au
contrôle de qualité.
[6a] Site
web visite le02/05/2011
http://www.boutique.afnor.fr/Boutique.asp?lang=French&aff=1530&url=NRM%5Fn%5Fhome%2Easp
a) La norme NF S99-172 spécifie un processus pour permettre aux
établissements de mettre en œuvre un système de
management des risques et d'identifier les phénomènes
dangereux associés aux dispositifs médicaux et à
leurs accessoires, y compris les dispositifs médicaux de
diagnostic in vitro, d'estimer et d'évaluer les risques, de
maîtriser ces risques et de surveiller l'efficacité de
cette maîtrise. Les exigences de la présente norme
s'appliquent à tous les stades du cycle de vie d'un dispositif
médical et en particulier dans sa phase d'exploitation.
[6b] Site web visite le02/05/2011
http://www.boutique.afnor.fr/Boutique.asp?lang=French&aff=1530&url=NRM%5Fn%5Fhome%2Easp
b) La norme NF EN 1441 spécifie une procédure qui permet
au fabricant d'examiner, en utilisant des informations disponibles, la
sécurité d'un dispositif médical, y compris les
dispositifs ou accessoires de diagnostic in vitro, en identifiant les
dangers et en estimant les risques qui sont associés au
dispositif.
[7]
Méthodologie AMDEC
http://erwan.neau.free.fr/Toolbox/AMDEC.htm
:
Methode
AMDEC
http://www.cyber.uhp-nancy.fr/demos/MAIN-003/chap_deux : Methode AMDEC
Norme NF S99-171 : Modèles et
définition pour l'établissement et la gestion du registre
sécurité, qualité et maintenance d’un dispositif
médical. NF EN ISO 14971 : Dispositifs médicaux –
Application de la gestion des risques aux dispositifs médicaux.
Édition Afnor. Mai 2001. Indice de classement : S99-211. Statut
: Norme homologuée.
NF
ISO 9001 version 2000 :
Systèmes de management de la qualité-exigence.
Édition Afnor,
NF
EN ISO 9004 : Systèmes de
management de la qualité – Lignes directrices pour
l’amélioration des performances. Édition Afnor,
décembre 2000. Indice de classement : X50-122. Statut : Norme
homologuée.
NF
EN ISO 13485 : Systèmes
qualité – Dispositifs médicaux – Exigences
particulières relatives à l’application de l’EN ISO 9001.
Édition Afnor, février 2001. Indice de classement :
S99-101. Statut : Norme homologuée.
NF
EN 45502-1 : Dispositifs
médicaux implantables actifs
– Partie 1 : règles
générales de sécurité, marquage et
informations fournies par le fabricant. Édition Afnor, novembre
1998.
Indice de classement : C74-502-1.
Statut : Norme homologuée. Norme harmonisée dans le cadre
d’une Directive européenne :
DI 90-385 01/06/1990 Directive
concernant le rapprochement des législations des États
membres relatives aux dispositifs médicaux implantables actifs.
Afnor
: Association française
de normalisation http : //www.afnor.fr
Afssaps
: Agence française de
sécurité sanitaire des produits de santé
http : //agmed.sante.gouv.fr
Anaes
: Agence nationale
d’accréditation et d’évaluation en santé http :
//www.anaes.fr
Site
Biomédical
de
l'Université
Technologique
de
Compiègne
(UTC)
http://www.utc.fr/~farges
UTC : Université de
Technologie de Compiègne http ://www.utc.fr
Analyse de risque
http://www.saq.ch/fachzeitschriften/mq_2_03.pdf : Management et
qualité.
http://www.a3p.asso.fr/even/pdf/donnon1.pdf : Analyse de risque de
Dispositif Médical
http://www.minefi.gouv.fr/daj/guide/gpem/dispositifs_medicaux/princip.pdf
Références figures:
Figure 1 : situation
géographique du Centre Médical de
Bligny
Source : Centre Médical de
Bligny
Figure 2: Ancien
bâtiment du CMB – source Centre Médical de Bligny
http://www.cm-bligny.com/IMG/pdf/Bligny_historique_2008_web_size.pdf
Figure 3 :
Organigramme
Source
:
Centre
Médical de Bligny
Figure 4 : maintenance
préventive dans les services, atelier et stock du service
biomédical
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
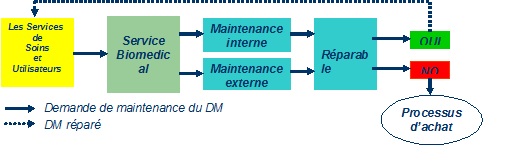
Figure 5 : Fonctionnement
actuelle du service biomédical
Source :
service biomédical – CMB
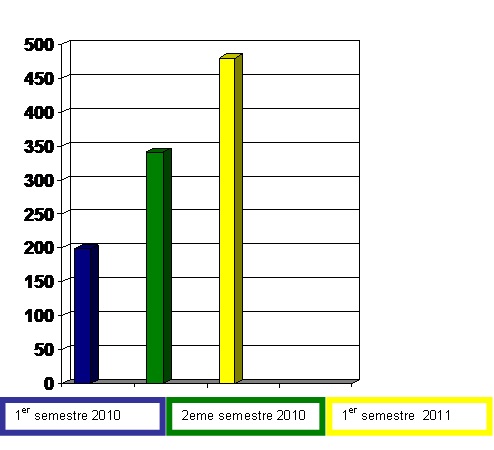
Figure 6 :
Interventions du service biomédical
Source GMAO : service biomédical – CMB
Figure 7 : Les enjeux
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
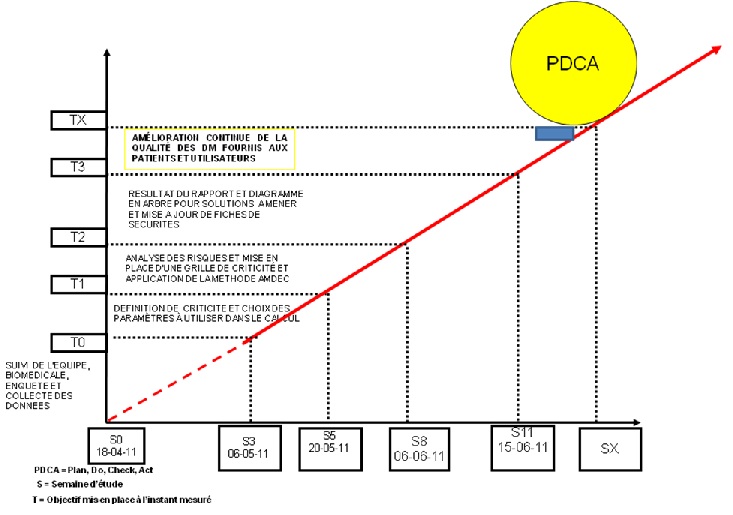
Figure 8 : Les
objectifs mis en place
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
Figure 9 : Organisation
des services à T0
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
Figure 10
:Evaluation du service biomédical sur la garantie de la
maîtrise des équipements biomédicaux selon le
critère 8k de la Haute Autorité de Santé
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
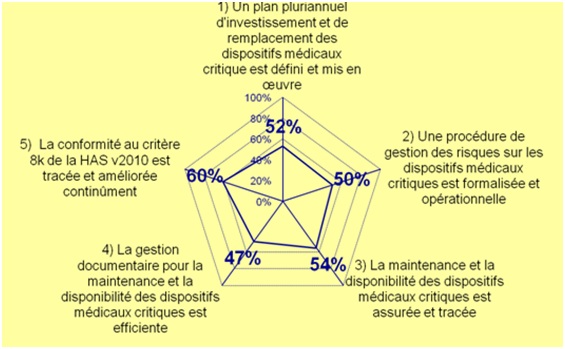
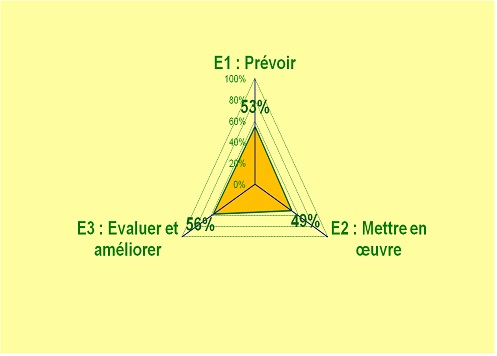
Figure 11: Evaluation du
service biomédical sur la conformité au
critère 8k de la HAS V2010
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
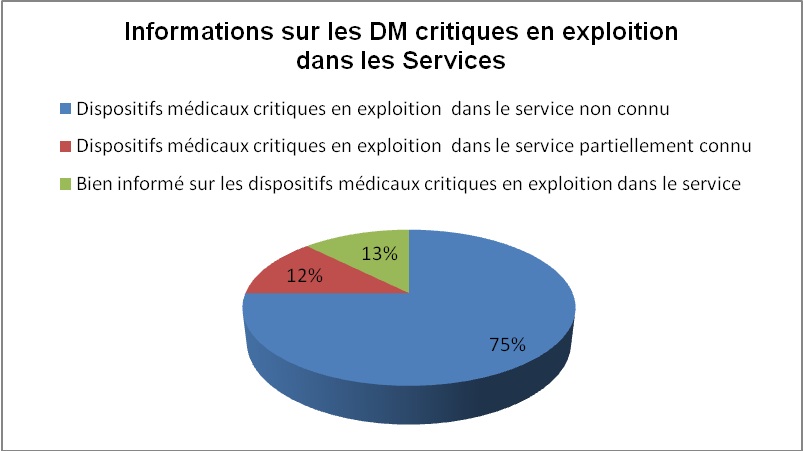
Figure 12 : Graphique
sur le niveau de connaissance de la criticité des DM au CMB
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
Figure 13 : Graphique
sur le niveau de formation à la manipulation des DM
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
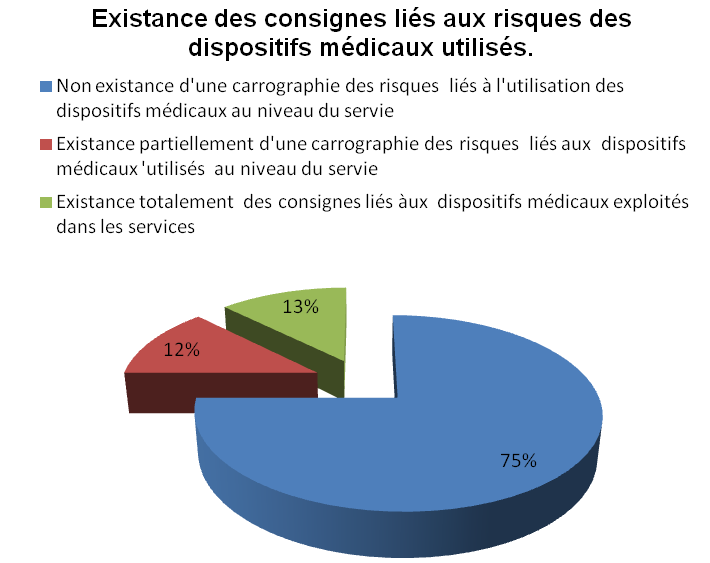
Figure 14 :
Graphique sur les mesures préventives des risques
engendrés par les DM
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
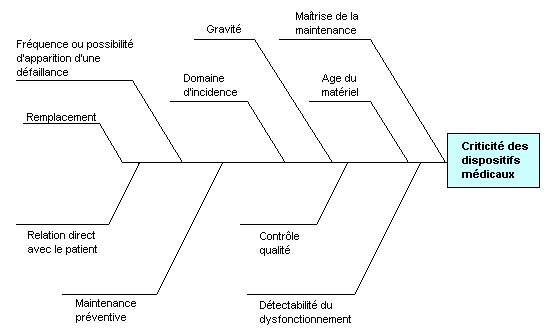
Figure 15 : Utilisation
de l’outil de qualité Ishikawa pour l'analyse des faits et
des causes racines de la criticité
http://www.utc.fr/tsibh/public/spibh/03-04/Stages/archier/archier.html
Figure 16:
Resultat du taux de criticité de l'ensemble des
différents types des DM analysés
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
Figure 17:Proposition
d'un
diagramme
en
arbre pour suivi des recommandations par rapport
à la HAS – critère 8K
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
Figure 18:Grille
de calcul de criticité avec la méthode PIEU
http://www-inst.utc.fr/tsibh/public/tsibh/09/projet/groupe3/index.html#pieu
Figure 19:Tableau
des actions à mener avec la méthode PIEU
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
Figure 20 : les
services qualité , biomédicale et des soins au service de
la sécurité du patient et des DM.
http://www.utc.fr/tsibh/extranets/etudiants/rapport_HTML/nsabimana/index.html
Annexes
Annexe-1
Cartographie des risques liés aux dispositifs médicaux
critiques analysés en général pour les trois
services qualité, biomédicale et des soins et une
cartographie des risques pour le groupe particulier du service
d’endoscopie.
Clic
ici
pour
telecharger
annexe1.a
Clic
ici
pour
telecharger
annexe1.b
Annexe-2
Quelques réponses d’une enquête de diagnostic sur la
connaissance de la criticité des DM au Centre Médical de
Bligny
Clic ici pour
telechargement
Annexe-3
Divers correspondances et réunions sur le sujet du stage Clic
ici pour les telecharger
Clic ici pour
telechargement
Annexe-4