4. Autres besoins
Criticité
La criticité va permettre de définir des priorités
d’intervention en maintenance. Le laboratoire définit une
criticité interne liée à l’impact du mauvais fonctionnement
d’équipement sur la qualité des analyses biologiques.
Un tri doit être fait entre les équipements critiques à
soumettre à l’accréditation COFRAC, et les autres à soumettre au
contrôle qualité.
Une autre criticité intervient : c’est la criticité d’un DM,
normée ou pas qui l’associe au risque de son utilisation. Le
laboratoire devra en être informé.
Disponibilité des équipements
Le laboratoire doit savoir à tout instant si des appareils
ne sont pas disponibles.
L’idéal serait que le laboratoire dispose d’un tableau de bord
concernant ses équipements, issu des informations de la Gestion
de Maintenance Assistée par Ordinateur du Service biomédical.
Temps de dépannage : plusieurs durées peuvent être
mesurées (temps pour avoir un diagnostic, temps de réception des
pièces détachées, temps de remise en fonction…). Ils peuvent
être de bons indicateurs de performance du SBM.
Hygiène et sécurité : le personnel qui intervient au
laboratoire doit respecter les consignes d’hygiène et de
sécurité.
Mode de fonctionnement dégradé : le SBM doit donner des
procédures dégradées de fonctionnement d’équipements, pour que
le LBM puisse continuer de travailler en mode dépannage.
Visites des sous-traitants : dans le cas où la
maintenance est partagée entre SBM et sous-traitant, les
techniciens du SBM auraient grand intérêt à être présents lors
de la visite de fournisseurs, pour une prise d’informations,
voire pour un complément de formation.
Respect de réglementations : Le référentiel NFS
99-170 concernant la maintenance s’adresse aussi aux
laboratoires. La sécurité des équipements médicaux est décrite
dans les normes IEC 60601.1, la maintenance dans la
norme IEE 62353.
5. Apports des visites et des contacts en
Centre Hospitalier
Nos visites au Centre Hospitalier de Compiègne et nos contacts
en milieu hospitalier nous ont conforté dans l’idée que nous
nous faisions de la situation des laboratoires à la suite
de nos lectures d’articles récents, dont des
mémoires de master de l’Université de Technologie de Compiègne.
Les laboratoires de biologie contactés, bien conscients de
l’urgence et de l’importance cruciale de la situation,
sont bien en phase d’accréditation, dans une démarche qualité en
cours, avec un réel besoin d’appui pour l’entretien de leurs
équipements, la formation du personnel, de l’organisation, et
qui pourrait leur faire gagner du temps.
Nous avons également constaté quelques pratiques courantes.
6. Pratiques courantes observées entre LBM
et SBM
Nous avons essayé de savoir comment étaient organisées les
interactions entre un SBM et un LBM non encore accrédité.
Quand il existe un service biomédical en établissement de santé,
les équipes sont souvent réparties en spécialités. On constate
pourtant souvent une volonté de conserver une certaine
polyvalence. Celle-ci est toutefois discutée parce qu’une
spécialisation des techniciens permettrait d’alléger des
contrats de maintenance des fournisseurs en prenant certaines
tâches en interne.
Pour assurer un service continu, une organisation classique peut
être
-
Un technicien de permanence affecté au curatif
-
Les autres techniciens ayant la charge des maintenances
préventives, des contrôles qualité, et des tests de sécurité
électrique.
Pour une part non négligeable de leurs activités, les
fournisseurs de consommables mettent à disposition des automates
pour les analyses. Ils en assurent aussi les maintenances, si
bien que ces équipements sortent du champ du SBM.
La technicité des automates utilisés dans les laboratoires étant
parfois élevée, les techniciens de maintenance se limitent
souvent au diagnostic ou au dépannage de premier niveau
(intervention interne). S’ils ne peuvent pas résoudre le
problème, le SBM fait appel au fournisseur ou à une société de
tierce maintenance (intervenant externe).
Quand le LBM fait appel au SBM pour un dépannage ou une
maintenance, il peut laisser le SBM décider des choix techniques
pour résoudre le problème. Il peut même aller jusqu’à ne pas
intervenir dans le choix d’une intervention interne.
Afin de garantir une disponibilité maximale des équipements, les
plannings d’intervention en interne et faisant appel à la
sous-traitance sont établis conjointement entre le LBM et
le SBM, et entre le LBM et les sous-traitants
Les accords de principe LBM SBM sont souvent implicites, et il
serait préférable de les formaliser pour définir les limites et
domaines d’intervention de chacun.
Le laboratoire a des besoins d’expertise technique sur ses
appareils, mais il doit aussi s’assurer que les équipes qui
interviennent aient une reconnaissance professionnelle.
Synthèse des besoins et attentes
Les paragraphes précédents nous ont permis de connaître les
besoins et attentes d’un laboratoire. Nous pouvons les résumer
dans le tableau ci-dessous :
Les attentes explicites d’un LBM devront être clarifiées, les
attentes implicites précisées. On pourrait citer
-
L’autonomie, la polyvalence des intervenants
-
La connaissance et le respect, par les techniciens, des
normes appliquées au laboratoire
-
Le temps d’intervention souhaité pour un diagnostic de
premier niveau
-
Le délai maximum de résolution du problème
-
Le règlement du dysfonctionnement en une seule fois
retour
sommaire
III.
COMPETENCES D’UN SERVICE BIOMEDICAL
1. Le savoir faire
Un service biomédical pouvant se réduire à un seul technicien,
nous allons étudier ses compétences et savoirs faire.
Les techniciens remplissant la fonction biomédicale ou bien
travaillant dans un service biomédical peuvent avoir des
formations initiales et des parcours professionnels bien
différents.
Nous pouvons rencontrer des ouvriers qualifiés, des techniciens
et des techniciens supérieurs. Dans le secteur public, l’accès
au poste de technicien se fait par voie interne ou externe. Le
niveau requis est un diplôme niveau III (bac +2/3 ans)
Le code Rome
[13] associé à ce métier est
I1305, et le code métier est 20O30.
D’après le répertoire des métiers de la fonction publique
hospitalière, un technicien(ne) de maintenance des équipements
biomédicaux a les missions :
- d’installer, maintenir, effectuer le
contrôle qualité et assurer la traçabilité des
interventions, dispositifs ou équipements biomédicaux
- d’informer sur l'utilisation des
équipements biomédicaux.
retour
sommaire
Participer à la gestion des risques et au suivi des dossiers de
matériovigilance.
Le technicien doit avoir des connaissances détaillées en
anatomie, physiologie, anglais technique, automatisme, fluides
médicaux, logiciel dédié de gestion de maintenance biomédicale
et des connaissances approfondies en biomédical et en
électronique.
Le métier de technicien biomédical demande
- des compétences techniques liées à la
technologie des équipements (mécanique, fluides médicaux,
électricité, automatisme, électronique, informatique)
- des capacités à diagnostiquer un
dysfonctionnement, une panne, le défaut d'un matériel, d'un
équipement, une anomalie d'un système. Il peut par exemple
intervenir dans le cas d’interactions entre machines ou
entre machines et environnement (température, compatibilité
électromagnétique…)
- des capacités à en identifier la cause,
à réparer l’élément défectueux, à vérifier la remise en
fonction de la partie défectueuse. Il devra pouvoir
renseigner le registre de sécurité, qualité et
maintenance (RSQM[14])
- de savoir utiliser des matériels, des
outils de dépannage, de réparation ou de maintenance.
Le technicien biomédical sera en mesure de
-
réaliser des actions curatives pour éliminer les causes
profondes du dysfonctionnement
-
réaliser des actions préventives pour éliminer les problèmes
potentiels de l’équipement
-
Évaluer la conformité d'un produit, d'un matériel, d'une
prestation au regard des normes internes et externes
-
Réaliser la métrologie de certains appareils
-
Réaliser le contrôle qualité des équipements
-
Réaliser les contrôles de sécurité électrique des
équipements
-
Evaluer les performances du matériel.
retour
sommaire
Le technicien sera en mesure d’intervenir dans toute la vie des
équipements, de sa réception, son installation, sa mise en
service.
Le technicien biomédical pourra d’intervenir dans la
détermination de la criticité d’un dispositif médical,
indispensable à la décision de sa réforme en fin de vie.
Cependant, un matériel en bon état ne
garantit pas que les fonctions que l’on attend de lui sont
satisfaites.
Le technicien biomédical devra faire des actions d’information,
de formation pour s’assurer qu’il est correctement utilisé, dans
le but que l’on s’est fixé. En effet, une grande part des
problèmes rencontrés vient d’une mauvaise utilisation des
équipements.
Un technicien ou un service biomédical n’a en
général pas le temps de prendre en charge toutes les
interventions qu’on lui demande.
Il peut alors intervenir dans le choix d’un prestataire
extérieur qui viendra dans l’établissement de santé, ou bien qui
réalisera des réparations dans son établissement.
Nous voyons que son expertise technique peut
aider les décideurs, du conseil à l’achat jusqu'à la réforme de
l’équipement.
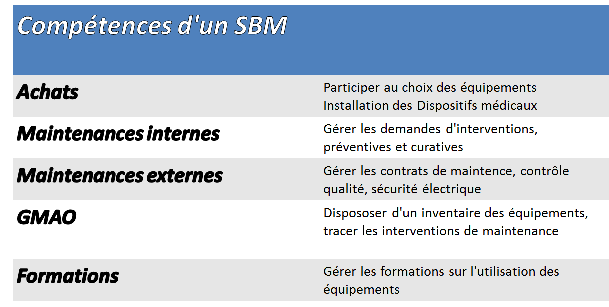
Synthèse des compétences d’un SBM
Nous pouvons résumer les compétences d’un SBM dans le tableau
ci-après.
Les besoins d’un laboratoire et les compétences d’un service
biomédical étant précisées, quels services ce dernier pourra
proposer au laboratoire ?
2. Prestations possibles d’un service
biomédical
Après l’approfondissement des besoins d’un laboratoire et
des compétences d’un service biomédical, au cours d’un atelier
de brainstorming, notre équipe a décidé de retenir quatre
prestations principales pour l’étude: la maintenance, la
métrologie, la formation et l’audit.
a.Prestations de maintenance
Le but de ces prestations est d’assurer au laboratoire la
continuité d’exécution des analyses, par l’entretien des
équipements. Dans le biomédical, le matériel est couramment
remplacé au bout de huit à dix ans. L’objectif est aussi de
limiter les pannes, les arrêts, d’augmenter la disponibilité, de
réaliser la maintenance préventive, de maîtriser les coûts
d’intervention, de diminuer les coûts de stock.
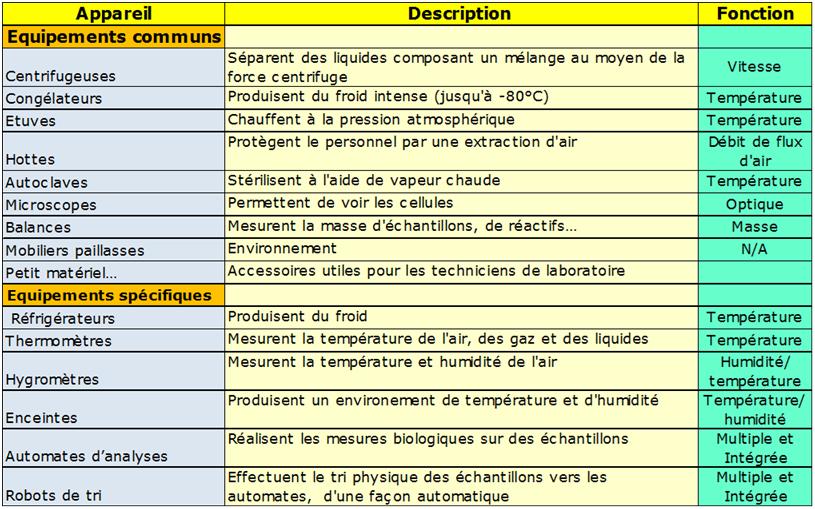
Ces prestations vont s’adresser aux équipements essentiels,
utilisés « en première intention », mais également au matériel
de secours souvent appelé « backup ». Les réparations
peuvent porter sur les centrifugeuses, les balances, les
réfrigérateurs, les microscopes…
Les opérations de maintenance peuvent être réalisées en interne
ou en externe. Le diagnostic de premier niveau peut être pris en
charge par la personne ou la structure qui remplit la fonction
biomédicale. Elle peut faire appel à un prestataire externe si
nécessaire. C’est le cas des gros équipements comme les
automates, les robots de tri…
-
L’intervention va consister à remettre l’équipement en état
de fonctionnement exempt de danger. Cela doit inclure
l’analyse de la sécurité électrique, des dispositifs d’arrêt
d’urgence (s’ils existent)
-
D’après la norme ISO 15189, si un matériel se révèle
défectueux, il doit être mis hors service et clairement
identifié. Le laboratoire doit garantir que le matériel
défectueux n’est pas utilisé tant qu’il n’a pas été réparé
et montré, par vérification, qu’il répondait aux critères
d’acceptation spécifiés.
-
Son but est de concourir à l’entretien des équipements, au
maintien de la sécurité, à la réduction des risques, à la
réduction des interventions de maintenance curative. La
maintenance systématique, selon un calendrier, est la plus
utilisée. La maintenance prévisionnelle, selon une
surveillance de la dégradation, est moins courante.
- Contrôles qualité sur appareils
-
Ils vont prouver que l’appareil respecte les
caractéristiques du constructeur. Ces contrôles
interviennent dans l’évaluation de la performance.
- Contrôles de sécurité électrique
- Ils
sont primordiaux pour garantir le fonctionnement des
appareils avec un risque maîtrisé.
retour
sommaire
b. Prestations de métrologie
Le but de la métrologie est de prouver que le matériel est
capable d’atteindre les performances requises. La métrologie va
permettre de relier l’appareil aux étalons de mesure
internationaux, et donc de garantir que les exigences
métrologiques sont satisfaites.
Les Equipements de Contrôle de Mesure et d’Essais (ECME,
appareils étalons) permettent de vérifier les
caractéristiques du matériel.
La preuve de la bonne mesure sera fournie par un constat
de vérification ou un certificat d’étalonnage.
La figure ci-après présente le principe du contrôle
métrologique.
Afin d’écrire une procédure de contrôle métrologique ou de
décrire une prestation de métrologie à un sous-traitant, on
s’aidera de la norme ISO 10012 relative à la mesure. Elle
fournit des exigences génériques et des guides d'application
pour le management des processus de mesure. Elle permet
d’élaborer la procédure documentée d’étalonnage exigée par la
norme ISO 15189 pour les équipements susceptibles d’affecter
directement ou indirectement les résultats d’examens.
-
La vérification est une opération qui énonce un
jugement émis sur des
valeurs spécifiées : le résultat est conforme ou non aux
tolérances d’acceptation qui seront, par défaut, celles du
constructeur.
-
L’étalonnage est la comparaison à un étalon dans des
conditions spécifiées, aboutissant à des résultats de
mesures associés à des incertitudes.
La métrologie concernera
Pour garantir les mesures des équipements et leur traçabilité,
les sous-traitants en métrologie devront être accrédités COFRAC.
Afin d’éviter un contrôle métrologique systématique sur tous les
appareils, et ainsi éviter de la sur-qualité, on peut tout de
même envisager un contrôle ciblé, élaboré avec
l’utilisateur, à condition de bien préciser l’étendue des
mesures souhaitées. Une analyse de risque peut être envisagée.
c. Prestations de formation
Un équipement, qu’il soit simple ou complexe, n’a pas beaucoup
d’utilité si l’on ne sait pas s’en servir. Le rôle de la
formation est de transmettre à un futur usager, les
informations qui lui seront utiles pour l’exploiter au mieux.
Elle vise à garantir l’aptitude à l’usage d’un appareil, à
l’aide de notices par exemple. L’apprenant pourra ainsi
comprendre le fonctionnement du DM, l’exploiter au mieux,
diagnostiquer le dysfonctionnement au plus vite, être capable de
le maintenir en état.
- Formation dispensée par les
fournisseurs à l’équipe biomédicale :
Le fabricant d’un matériel est le mieux placé pour enseigner son
utilisation complète et optimum.
En principe, plus l’équipement sera complexe, plus la formation
sera longue. On admet généralement qu’il faut un an pour
maitriser un nouvel équipement complexe (un automate de
biochimie par exemple)
Pour ces raisons, il est souhaitable que les techniciens
biomédicaux profitent de la venue des fournisseurs pour
compléter leur formation.
La formation des techniciens sur des équipements complexes
démarrent souvent quelques mois avant la fin de la période de
garantie de l’appareil.
Cela peut être le cas d’un fournisseur d’automate qui peut
former les techniciens à l’utilisation et au diagnostic de
premier niveau, et aux démarches à entreprendre en cas de panne
importante.
- Formation dispensée par le SBM au
laboratoire :
-
De par sa connaissance du fonctionnement interne des DM, le
technicien biomédical peut donner les explications
concernant le bon usage d’un DM. Dans beaucoup de cas,
il les aura apprises auprès du fournisseur. Le SBM
peut aussi rappeler aux opérateurs le mode opératoire d’un
automate.
-
Une attention particulière devra être portée à
l’interprétation des alertes des dispositifs médicaux.
- Formation dispensée par le LBM à
l’équipe biomédicale
-
Comme pour tous les DM, les opérateurs du laboratoire
connaissent mieux l’utilisation des équipements que les
techniciens qui les réparent ou même que le fabricant !
Leurs informations seront précieuses à l’équipe chargée du
dépannage. Les opérateurs formeront donc les techniciens aux
manipulations de base qui vont les concerner. Les opérateurs
formeront donc les techniciens aux manipulations de base
(navigation dans les menus du logiciel, entrée des mots de
passe utilisateurs), qui leur serviront lors des dépannages
- Des certificats de formation peuvent
attester la présence d’une personne à une session de
formation, mais ils peuvent aussi, si un contrôle de
connaissance y est associé, prouver l’acquisition du nouveau
savoir ou du savoir-faire.
- La formation SPILAB (Stage de
perfectionnement en Ingénierie du Laboratoire) de l’UTC
prépare à exercer dans le domaine du laboratoire.
Une formation courte y associant la norme ISO 15189 pourrait
avoir un intérêt pour des techniciens destinés à travailler dans
un laboratoire accrédité.
d. Prestations d’audits
D'après la norme 15189,
(4.14 Audits internes)
Afin de vérifier que les opérations soient
conformes aux exigences du système de management de la qualité,
des audits internes de tous les éléments du système, la
direction et les services techniques, doivent être effectués à
des intervalles définis par le système lui-même. L’audit interne
doit progressivement aborder ces éléments et souligner les
domaines revêtant une importance déterminante pour la qualité
des analyses pour le patient.
Les audits doivent être planifiés, organisés
et réalisés de façon formelle, par le responsable qualité ou le
personnel qualifié désigné. Le personnel ne doit pas auditer ses
propres activités. Les procédures des audits internes doivent
être définies et documentées et indiquer les types d’audit
réalisés, les fréquences, les méthodologies et la documentation
requises. Si des défauts ou des possibilités d’amélioration sont
notés, le laboratoire doit procéder aux actions préventives ou
correctives appropriées. Ces actions doivent être documentées et
réalisées dans un délai convenu.
Il convient normalement que les éléments principaux du système
de management de la qualité fassent l’objet d’un audit interne
annuel.
Les résultats des audits internes doivent être soumis à la
direction du laboratoire pour revue.
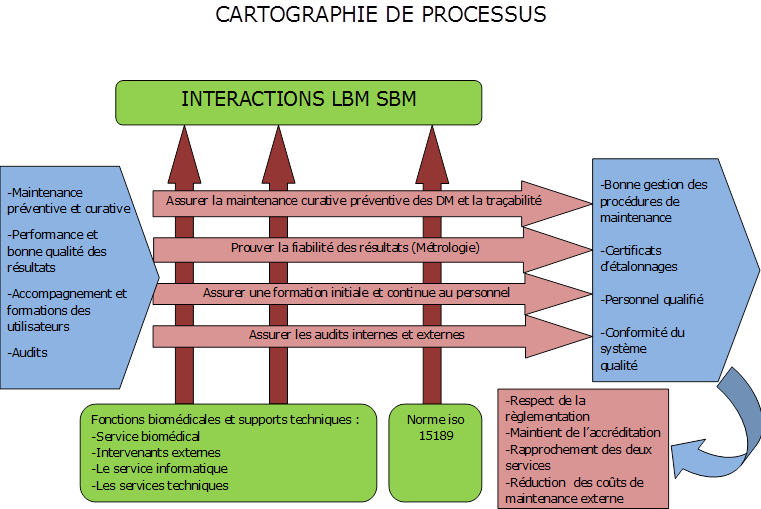
e.Synthèse des interactions
Les quatre items développés auparavant (maintenance, métrologie,
formation et audits) représentent les principales interactions
entre un SBM et un LBM. Afin de les visualiser, ils sont
représentés dans la cartographie matricielle des processus des
interactions LBM - SBM ci-après.
Les besoins du LBM sont pris en compte en entrée de
processus. Le laboratoire, les fonctions biomédicales et la
norme ISO 15189 participent à la réalisation des quatre
sous-processus. Les livrables apparaissent en sortie, à droite.
Les acteurs intervenant dans le processus sont le service
biomédical, les fournisseurs, le service informatique et les
services techniques.
f. Prestations complémentaires :
Des prestations non évoquées jusqu’à présent pourront être
considérées comme complémentaires.
On peut citer par exemple :
- L’obligation de vérifier la performance
d’un équipement après une réparation avant qu’il ne soit
réutilisé au laboratoire, ou à réception lorsqu’il intègre
le laboratoire (caractérisation à t0).
- Le conseil à l’uniformisation des DM,
en termes de marque d’équipement, de modèle, pour des
facilités de dépannage, d’approvisionnement des pièces
détachées etc.
- La détermination de la criticité des DM
au sens de la norme NF EN ISO 14971[15]. Celle-ci permet
d’identifier les phénomènes dangereux associés à un
dispositif médical y compris les dispositifs médicaux
de diagnostic in vitro. Le SBM pourra être partie
prenante de l’évaluation des risques, de la maîtrise des
risques et de son l’efficacité.
- Sa contribution au choix de
fournisseurs pour la maintenance ou la métrologie :
o Pour proposer des solutions au LBM pour que
celui-ci ne soit pas trop dépendant des fournisseurs
(maintenance, métrologie principalement)
o Pour la recherche de fournisseur
certifié COFRAC
- Renseigner des procédures dégradées de
fonctionnement en accord avec la certification, de façon à
parer à d’éventuelles situations de blocage plausibles (par
exemple, pouvoir continuer le processus analytique si un
graveur de CD en sortie d’automate est arrêté)
retour
sommaire
g) Rôle dans la plannification
- Les interventions de maintenance, de
métrologie nécessitent de ne pas utiliser les équipements ou
de les mettre à l’arrêt.
- Afin de coordonner les disponibilités
des deux services, l’élaboration d’un planning commun semble
une évidence. Au cours de son élaboration, les ressources
humaines et en matériel seront évoquées.
- Un rappel périodique du planning des
maintenances préventives, des contrôles qualité, des
contrôles de sécurité électrique permettrait l’utilisation
optimale des équipements pour en optimiser les temps d’arrêt
des équipements.
- L’idéal serait que le laboratoire dispose d’un
tableau de bord concernant ses équipements, issu des
informations de la Gestion de Maintenance Assistée par
Ordinateur du Service biomédical.
h. Des prestations de conseil
Le SBM pourra aider au choix des fournisseurs.
Si le LBM est amené à travailler avec un prestataire de
service, il faut dans un premier temps vérifier ses
références, savoir s’il est certifié ISO 9001, accrédité ISO
17025, ou s’il respecte le référentiel NFS 99-170. Le site
COFRAC liste les fournisseurs accrédités.
Il pourra aussi donner son avis sur un
prestataire ou un fournisseur, à partir de son expérience vécue
avec eux.
Les prestataires proposés par le SBM doivent être approuvés par
le LBM, afin de vérifier leur performance.
Lors d’une consultation pour une prestation
externe, une comparaison des devis de plusieurs fournisseurs est
souhaitable, ce qui peut éviter d’en favoriser un.
i.Des prestations de suivi :
On peut citer par exemple
- La vérification de l’identification des
équipements du laboratoire
- La vérification de la tenue à jour des
fiches de vie des appareils
- Vérifier la présence de notices
techniques en français à jour, selon les documents
réglementaires du Code de la Santé Publique CSP R5211-22
alinéa 7
- Le suivi du matériel mis à disposition
au LBM ou prêté.
retour
sommaire
La spécificité des interactions étudiées découle de l’obligation
du SBM de se conformer aux exigences de la norme ISO 15189, en
termes de traçabilité notamment.
Nous avons dégagé les prestations qu’un SBM pourrait délivrer au
laboratoire.
Un établissement de santé, public ou privé, peut les faire
réaliser en interne ou en externe. Il peut faire appel
- aux personnes assurant les fonctions
biomédicales.
- à la sous-traitance, en s’adressant
- à
des sociétés de tierce maintenance
- à ces deux ressources (cas le plus
fréquent en établissement public)
On connait maintenant les prestations qu’un SBM peut proposer à
un LBM, afin de participer à garantir la qualité, la traçabilité
des analyses médicales, ceci dans l’intérêt du patient et des
équipes médicales.
On constate immédiatement un déséquilibre possible entre les
exigences et les pratiques du laboratoire strictement encadrées,
et les prestations délivrées par un personnel qui n’est, en 2014
tout au moins, pas soumis à une quelconque certification ou
habilitation. Il faut savoir que des prestations peuvent êtres
certifiées par des sous-traitants, en métrologie par exemple.
Les compétences du personnel LBM sont obligatoirement prouvées
par l’accréditation. Qu’en est-il du personnel du SBM ?
3. La garantie du savoir-faire
Afin d’assurer une qualité de soins pour le patient, toujours
plus élevée, l’évolution du secteur biomédical amènera
probablement la nécessité d’une certification ou d’une
accréditation pour assurer la fonction biomédicale. La
radiologie, les laboratoires de biologie médicale, les
dispositifs médicaux sont maintenant encadrés par des
décrets, des ordonnances et des lois.
A ce jour, il n’existe pas de contrainte de certification
pour la fonction biomédicale, même si les techniciens évoluant
dans le secteur se conforment à la réglementation concernant les
équipements.
Dans les établissements publics de santé, les SBM proposant des
prestations aux laboratoires se trouvent en situation de
concurrence avec les prestataires du privé qui peuvent être
certifiés ISO 17025 ou accrédités COFRAC.
L’intérêt des SBM à entrer dans une démarche qualité reconnue va
grandissant, et leur certification pourrait constituer à terme
un enjeu pour l’emploi. En 2013, d’après un sondage, seulement
dix-sept
[16] services
biomédicaux étaient certifiés ISO 9001.
La stratégie à adopter est propre à chaque établissement.
Il sera intéressant d’avoir des retours du COFRAC à ce sujet,
suite à l’accréditation des laboratoires.
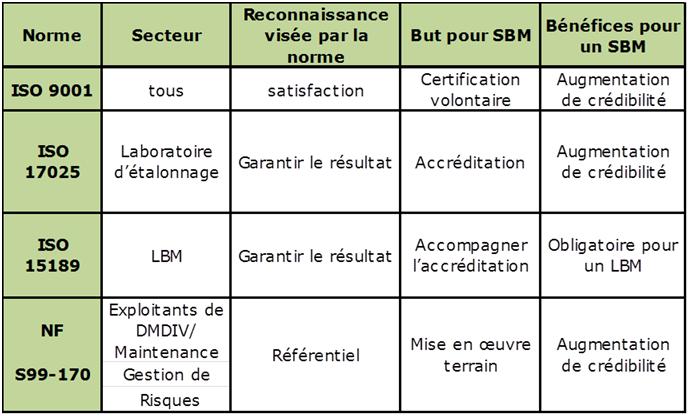
Enumérons seulement quelques possibilités qui s’offrent à un SBM
proposant ses prestations à un LBM.
- Certification selon ISO 9001 : elle
propose un système qualité basé sur l’approche processus
;la norme concerne tous les secteurs, elle est donc
destinée aussi aux pôles médicaux ; bien diffusée, d’accès
désormais classique, elle n'est pas spécifique au
laboratoire.
- Certification selon ISO 17025 : la
norme est applicable au laboratoire d’essais ou
d’étalonnage. Elle est plus générale que la norme ISO 15189,
mais non spécifique des laboratoires de biologie médicale.
- Respect du référentiel NFS 99-170 :
c’est une norme française non associée à une certification ;
elle définit un système de management de la qualité pour la
maintenance et la gestion des risques associés à
l'exploitation des dispositifs médicaux. Elle s’adresse aux
exploitants de dispositifs médicaux, directement concernés
par le plan de gestion des DM et le plan de gestion des
risques. C’est un référentiel simplifié (un manuel et
trente-deux preuves écrites.
IV.
ADAPTATION DES SERVICES AUX BESOINS
1. Généralités
Maintenant que nous avons cerné les besoins d’un laboratoire
d’analyses médicales et dégagé les compétences d’un service
biomédical, nous devrons les utiliser, affiner, réorienter,
développer pour les adapter à la demande du laboratoire.
Nos propositions doivent s’inscrire dans un processus plus
global où le LBM et le SBM sont parties prenantes au même titre
que les autres services d’un établissement de santé.
Dans cette étude, pour ne pas s’autolimiter et favoriser la
création, nous avons considéré d’abord les ressources non
limitées, avant d’envisager les fortes contraintes. Les
considérations économiques ne sont pas négligées, la recherche
du meilleur rapport coût sur qualité étant essentielles dans un
environnement économique à budget constant.
Quelques idées vont orienter les choix d’adaptation.
Service biomédical ou sous-traitance ?
L’obligation de traçabilité, de faire appel, pour la métrologie,
à des sous-traitants certifiés ou accrédités, va obliger à
considérer ce que le SBM peut prendre en charge lui-même, pour
des considérations d’efficience, de sa compétence actuelle et
future et de limitations de coûts.
Les compétences des quatre acteurs cités plus
haut (le service biomédical, les fournisseurs, le service
informatique et les services techniques) sont généralement
complémentaires si on considère un grand parc d’équipements du
laboratoire.
- Par exemple, au Centre Chirurgical Marie Lannelongue (Le
Plessis Robinson-Ile de France), le service biomédical
intervient sur des petites pannes des DM du LBM, comme pour le
remplacement d'une ampoule sur un microscope, et en maintenance
préventive sur les centrifugeuses pour le remplacement des
vérins de portes et le test de fonctionnement, ou bien en
maintenance curative pour le remplacement de tous types de
pièces.
- Les maintenances effectuées sur les automates sont
généralement confiées aux fournisseurs ou à des sociétés de
tierce maintenance, puisqu’ils ont les compétences et les outils
pour les opérations de maintenance qui ne peuvent être
effectuées en interne sur ces équipements spécialisés. Des
pièces détachées sont parfois difficiles à obtenir en
raison de contraintes budgétaires et de difficultés
d'approvisionnement, notamment en cas d'achat à l'étranger.
L’avantage de faire appel au SBM, c'est qu’il peut intervenir en
très peu de temps, étant sur place dans l’établissement de
santé, avec parfois une astreinte assurée par les techniciens.
Il a aussi l’historique de l’équipement, ce qui est parfois
déterminant pour comprendre son comportement au fil du temps.
La contrainte induite est d’assurer un bon management du
personnel. Les prétextes avancés au recours à la sous-traitance
peuvent concerner la difficulté de faire exécuter certaines
tâches à du personnel, pour des raisons de manque de formation
ou de motivation.
Aspects économiques
Pour une même prestation, est-ce moins cher de faire appel à la
sous-traitance ?
Il est difficile de prévoir les ressources à affecter à la
maintenance.
Il faut considérer les ressources financières, matérielles et
humaines nécessaires pour exécuter convenablement les activités.
Cela requiert également de la part du personnel de maintenance
des compétences, une formation, et une expérience adéquates.
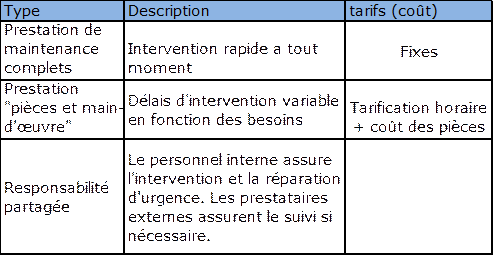
Le tableau ci-après décrit trois niveaux de prestation décrits
dans une proposition de contrat : la maintenance est totalement
sous-traitée dans les deux premières lignes, et partagée
dans la troisième ligne.
Pour une prestation équivalente, il faudra considérer les
aspects coûts et délais d’intervention, pour des prestations à
la demande ou par contrats annuels. Ils seront à comparer au
salaire annuel moyen d’un technicien biomédical. En 2012, il
était d’environ 35 k€.
Les conséquences de faire appel à la sous-traitance sont à
considérer :
- Un service SBM, qui se trouverait peu
impliqué, voire écarté du laboratoire, pourrait, à la
longue, perdre sa crédibilité, et la confiance que les
autres services peuvent lui accorder. S’il n’intervient que
sur des appareils qui demandent peu de connaissances, il
n’augmentera pas son niveau technique. Il serait dommage de
ne pas faire profiter au laboratoire de toutes les
compétences que le SBM a capitalisé au fil des années dans
l’exercice de ses fonctions.
- Un prestataire externe coûte du temps à
l’établissement, puisqu’il sera pris en charge par un
technicien du SBM, qui aura mis son activité entre
parenthèses afin que le prestataire intervienne sur
l’équipement au LBM. C'est donc du temps biomédical
consommé.
- Dans les établissements publics, la
mise en situation de compétition des SBM avec les
sous-traitants peut être durement vécue par le
personnel.
- Les avantages d’une grande implication
du SBM au laboratoire découlent du sens qu’on lui accordera,
notamment celui de participer à la mutation des LBM pendant
de très nombreuses années.
Le support technique de la fonction biomédicale peut être
apportée au laboratoire par
Pour le biologiste, la possibilité de confier tout ou partie des
équipements peut lui permettre de libérer du temps
biologie.
Il sera nécessaire de prendre connaissance des accords,
contrats existants dans l’hôpital, entre la Direction et
le LBM, entre la Direction et le SBM, et également de consulter
le manuel qualité de l’établissement.
L’état des lieux étant réalisé, la démarche consistera à se
focaliser sur l’essentiel et l’obligatoire, puis de quantifier
les écarts, enfin de décider conjointement des actions à
entreprendre pour réduire les écarts.
C’est tout l’intérêt d’un outil d’autodiagnostic.
2. Outil d’autodiagnostic créé
Nous avons imaginé un outil d’autodiagnostic dédié à nos
interactions.
L’objectif de notre outil est de permettre aux laboratoires de
biologie médicale de s’auto-évaluer, dans le but d’améliorer
leurs interactions avec les acteurs biomédicaux, selon les
exigences de la norme ISO 15189.
Utilisation :
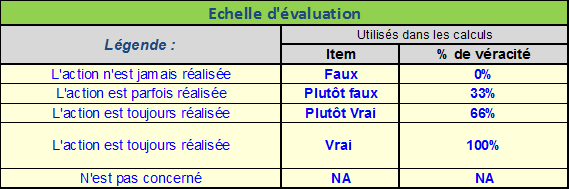
C’est un fichier de type Excel qui commence par une première
page expliquant son fonctionnement ainsi qu’une échelle
d’évaluation qui correspond à un pourcentage de véracité.
Grille d’autodiagnostic
En deuxième page, une grille d’autodiagnostic regroupe nos
quatre interactions choisies et décline 21 affirmations
basées sur les exigences de la norme ISO 15189.
Les chapitres 4.14 pour les audits, 5.1 pour la formation et 5.3
pour la maintenance et la métrologie.
Pour augmenter la rapidité de l’autodiagnostic nous avons décidé
d’offrir une seule option de réponse par affirmation ce qui
permet une analyse rapide de 10
minutes.
La synthèse des résultats est représentée par un radar qui
contient les quatre interactions et le résultat de
l’évaluation entre 0% et 100%.
Le laboratoire de biologie médicale pourra de ce fait évaluer
leur position par rapport à la norme pour ces
interactions, dans le but de s’améliorer.
Amélioration de l’outil d’autodiagnostic :
Afin de rendre notre outil opérationnel, il faudra le soumettre
à des tests auprès de laboratoires de biologie médicale pour
mieux adapter à leur besoins.
3. Outil d’autodiagnostic de NF S99-170
La norme NFS 99170 sur la maintenance des dispositifs médicaux
et le système management de la qualité concerne directement les
services biomédicaux et toutes les autres structures utilisant
les dispositifs médicaux et les dispositifs de diagnostic
in-vitro.
Le tableau ci-dessous est une synthèse comparative des exigences
des normes NFS 99-170, tirées de son outil d’autodiagnostic
existant, et celle de notre outil d’auto-diagnostic basé sur
l’ISO 15189 destiné aux LBM. On remarque une similitude entre
elles.
Un service biomédical peut donc utiliser l’outil
d’autodiagnostic de la norme NFS 99-170 existant, pour évaluer
ses pratiques au laboratoire de biologie médicale.
Synthèse sur les outils d’autodiagnostic:
Au final, nous proposons au LBM et au SBM deux outils
d’autodiagnostic.
Celui du référentiel NF S99-170 est disponible, et celui que
nous proposons sera à développer et à valider.
4. Elaborer une coopération
Nous avons constaté que les relations entre un SBM et un
laboratoire de biologie médicale étaient bidirectionnelles, que
les plannings étaient en partie élaborés conjointement, que les
services avaient intérêt à se synchroniser pour la formation
dispensée par des fournisseurs, que certaines informations
devaient circuler dans les deux sens etc.
Il va sans dire qu’une coopération, au sens d’action de
participer à une œuvre commune, serait tout indiquée, ceci dans
l’intérêt des deux services.
Elle aurait un « prix à payer », sous la forme de temps à
consacrer pour mettre les parties d’accord, mais beaucoup
d’avantages dont :
- Faire correspondre les services
rendus aux attentes du LBM
- Permettre d’exprimer les besoins
implicites et explicites de chacun des services concernés
- Permettre de définir le rôle de chacune
des parties pour les différentes activités prévues,
principalement quand les fournisseurs et les services
techniques s’y ajoutent.
- Permettre d’avoir des écrits et de
pouvoir les adapter à des situations nouvelles
- Permettre d’envisager des alternatives
dans la plupart des cas plausibles, afin d’éviter de
rencontrer des situations inattendues.
- Gagner en crédibilité vis-à-vis des
auditeurs COFRAC, d’autant plus si cette coopération
était actée dans un document.
Une coopération réussie passera inévitablement par un
accompagnement au changement. L’information à la démarche, le
développement de la motivation des équipes, la psychologie (pour
ne pas imposer une solution), seront essentielles à sa réussite.
La coopération envisagée peut prendre de multiples formes, selon
le mode de fonctionnement du SBM et du LBM, selon leur
constitution, leur organisation, leur équipement, leurs
intentions, leur motivation etc.
Essayons d’en imaginer quelques-unes.
5. Exemples de coopération
Exemple 1 : Coopération légère
Le LBM détient beaucoup d’automates de tri et d’analyses, et il
conclut des contrats de maintenance avec ses fournisseurs.
Il sollicite le SBM au coup par coup.
C’est l'exemple du CCML (Centre Chirurgical Marie Lannelongue)
évoqué plus haut.
Inconvénient pour le SBM : il n’intervient qu’en maintenance
curative, pour des petits dépannages.
Exemple 2 : Coopération rapprochée
Le SBM fait des propositions d’interactions en fonction de ses
propres ressources humaines et matérielles.
A périmètre constant de ressources, le SBM et le LBM vont se
mettre d’accord sur certaines opérations planifiées comme les
maintenances préventives, les contrôles qualité, les tests
de sécurité électriques.
Si l’organisation confie plus d’interventions au SBM, le LBM
peut gagner du temps biologie.
Exemple 3 : Contrat de coopération
La fonction support du SBM est contractualisée, comme peut
l’être la sous-traitance externe. Celle-ci a du sens pour
COFRAC, parce que la formalisation des prestations SBM sous
forme de contrat permet de cadrer le champ d’actions et de
rassurer le LBM par rapport à ses besoins.
Avantages:
- la responsabilisation du LBM par
rapport au SBM, vis-à-vis de la répartition des rôles dans
l’entretien des équipements, de la criticité d’analyses des
équipements.
-
Une évaluation de ce qui est décidé est possible, par le
choix de quelques indicateurs par exemple.
-
Si l’organisation confie plus d’interventions au SBM, le LBM
peut gagner du temps biologie.
Inconvénient : du temps nécessaire pour la mise en place d’une
phase d’identification des besoins, des services attendus, et
des moyens envisagés.
Synthèse sur l’adaptation des services aux
besoins
Nous constatons rapidement qu’il est difficile d’être exhaustif
pour décrire l’adaptation des services aux besoins du LBM.
Nous avons compris que la coopération envisagée peut être
multiforme entre les deux services, qu’elle doit prendre en
compte la politique qualité de l’établissement, sa politique de
ressources humaines, un contrat de pôle éventuel pour
remplir des missions définies par le projet médical
d’établissement.
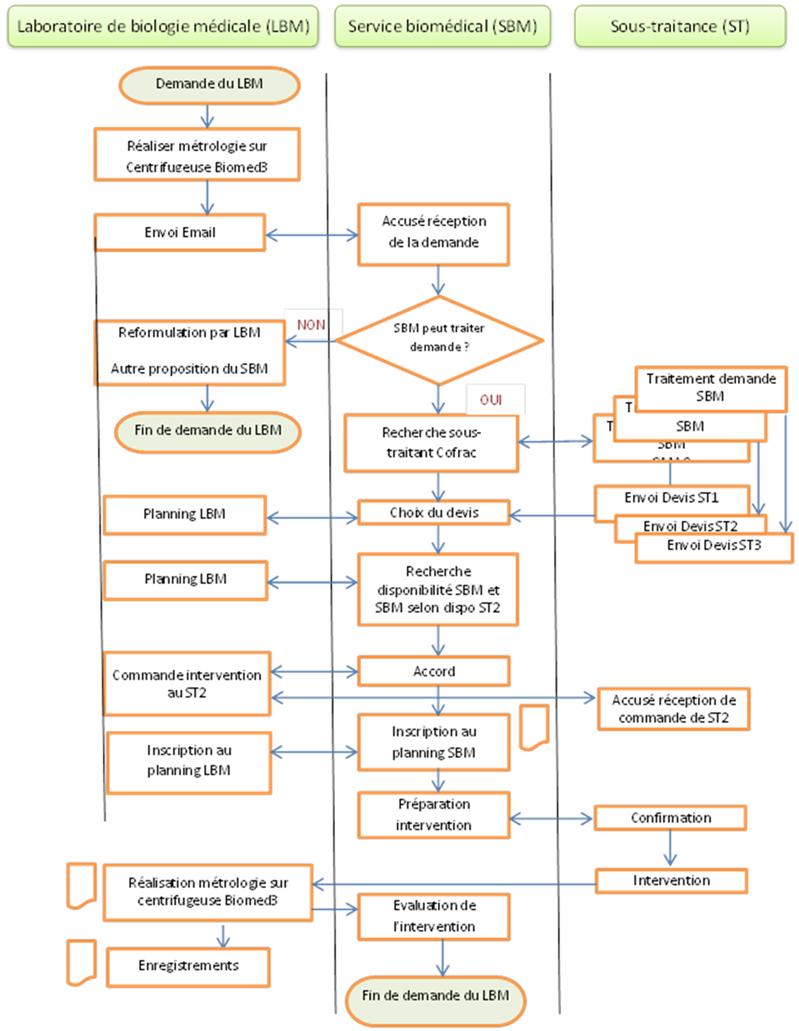
Pour exemple, les échanges entre les parties prenantes d’une
demande de métrologie sur une centrifugeuse pourraient se
représenter dans l’oganigramme ci-après.
6. Analyse du projet
Nous pourrions envisager l’utilisation d’un tableau à double
entrées, les besoins en ligne, les services en colonnes, et
développer à leur intersection les cas envisageables selon les
coopérations souhaitées ou possibles. On s’acheminerait
rapidement vers un tableau à triple entrées d’une réalisation
beaucoup plus difficile.
Une autre approche possible est l’utilisation d’un outil
pour guider dans la démarche entreprise.
Son contenu devrait être spécifique au besoin, généré à
l’initiative des LBM et SBM. Ce sont les caractéristiques d’un
guide de bonne pratique d’activité connexe du domaine
biomédical, comme l’Université de Technologie de Compiègne les
envisage dans ses différentes publications.
7. Propositions d’une bonne pratique pour la
gestion des interactions entre le service biomédical et le
laboratoire de biologie médicale
Le laboratoire a besoin de support technique pour l’entretien,
le suivi de ses équipements pour obtenir ou conserver son
accréditation COFRAC relative à la norme ISO 15189.
La personne, ou le service qui assure la fonction biomédicale,
trouvera quelques idées directrices dans cette ébauche de guide
de bonne pratique.
A. Sens
-
Cette bonne pratique s’adresse aux établissements publics et
privés qui désirent organiser les interactions entre un
service biomédical et un laboratoire dans une démarche
d’accréditation ou déjà accrédité selon la norme ISO 15189.
-
La démarche d’accréditation engagée par les laboratoires est
vitale puisqu’elle conditionne leur autorisation
administrative d’exister.
Ils ont besoin de support technique pour l’entretien, le suivi
de tous les équipements, afin de satisfaire les conditions
imposées par la norme et contrôlées périodiquement lors des
audits internes et par ceux effectués par le COFRAC.
Organiser les interactions, relations bidirectionnelles, entre
LBM et SBM, pour assurer un support technique au LBM, dans le
respect de la norme ISO 15189.
Faire des propositions applicables au secteur public ou
privé, adaptable aux besoins du LBM.
Garantir la qualité, la sécurité, la disponibilité, les
performances des équipements
Améliorer la compétence et l’efficience d’un SBM.
-
L’innovation dans cette bonne pratique vise à
contractualiser les interactions entre un SBM et un LBM sous
forme d’un contrat de coopération élaboré conjointement.
-
Le progrès repose sur l’amélioration continue afin
d’optimiser les interactions entre le service biomédical et
le laboratoire, par une adaptation des interactions à
l’évolution des besoins et des ressources du laboratoire et
du service biomédical.
B. Soutien
- Laboratoire de biologie médicale
- Personne assurant la fonction
biomédicale ou service biomédical
- Services demandeurs d’analyses,
prescripteurs
- Internes à l’établissement
Responsable qualité
Service de métrologie
Services techniques
Service informatique
Service achats
- Externes à l’établissement
Fournisseurs, sous-traitants
COFRAC
- Monde –Europe : normes ISO 15189, ISO
17025, ISO 10012
- France : Référentiel NFS 99-170
C. Suivi
-
Processus et critères de réalisation
Quatre items découlent de la cartographie des processus
proposée.
La maintenance, la métrologie, la formation et l’audit.
-
Evaluation de la performance
Des indicateurs basés sur l’activité du SBM relative à
l’entretien du parc d’équipements du laboratoire (temps
d’immobilisation machine, nombre d’anomalies constatées…)
Elle peut s’apprécier par la facilité de résolution des
problèmes
Elle peut se mesurer à l’aide d’indicateurs biens choisis
permettant de mesurer la satisfaction du laboratoire, concernant
les interventions du SBM en maintenance, en métrologie, en
formation et relatives au résultat d’audits internes ou
réalisées par le COFRAC.
CONCLUSION
Les analyses médicales ont une importance grandissante dans le
parcours de santé des patients. Nous avons cherché à comprendre
la situation des laboratoires de biologie médicale, qui
sont soumis à la pression de l’accréditation selon la norme ISO
15189, sur toutes les analyses, au plus tard en 2020.
Nous avons entrevu l’apport possible, en termes de prestations,
prenant la forme d’une coopération entre le SBM et le LBM, qu’un
service biomédical peut apporter à un laboratoire accrédité, ou
en cours d’accréditation.
N’étant pas lui-même soumis à une quelconque certification
obligatoire, et mis en concurrence avec le domaine privé, le
service biomédical aurait tout intérêt à s’engager dans une
démarche qualité ISO 9001, ou de respecter le référentiel NFS
99-170.
Notre étude pourrait enfin apporter des éléments pour
l’élaboration d’un futur guide de bonne pratique, et participer
à une problématique qui va bientôt concerner des centaines de
laboratoires et de services biomédicaux.