|
Apport de l'IRM dans le diagnostic antenatal, Projet DESS "TBH", UTC, 2001, URL : https://www.utc.fr/~farges/DESS_TBH/00-01/Projets/IRMvsUS/IRMvsUS.htm |
|
 |
 |
|
|
|
|
|
| Si vous arrivez directement sur cette page, sachez que ce travail est un rapport d'étudiants et doit être pris comme tel. Il peut donc comporter des imperfections ou des imprécisions que le lecteur doit admettre et donc supporter. Il a été réalisé pendant la période de formation et constitue avant-tout un travail de compilation bibliographique, d'initiation et d'analyse sur des thématiques associées aux technologies biomédicales. Nous ne faisons aucun usage commercial et la duplication est libre. Si vous avez des raisons de contester ce droit d'usage, merci de nous en faire part . L'objectif de la présentation sur le Web est de permettre l'accès à l'information et d'augmenter ainsi les échanges professionnels. En cas d'usage du document, n'oubliez pas de le citer comme source bibliographique. Bonne lecture... |
|
|
|
Apport de l'IRM dans le diagnostic antenatal, Projet DESS "TBH", UTC, 2001, URL : https://www.utc.fr/~farges/DESS_TBH/00-01/Projets/IRMvsUS/IRMvsUS.htm |
|
 |
 |
|
|
|
|
Voici environ une douzaine d’années que s’est développée l’imagerie par résonance fśtale. Cette nouvelle technique d’imagerie du fśtus ne saurait remplacer l’échographie qui reste l’examen clé en matière de diagnostic anténatal. Cependant, certains points faibles de l’échographie ont conduit à la recherche d’une autre technique permettant notamment d’étudier plus finement le cerveau fśtal. C’est donc surtout dans ce domaine que se sont axés les principaux travaux d’IRM fśtale, le but étant essentiellement de mieux analyser les malformations cérébrales et extra-cérébrale par exemple : l’IRM a permis le diagnostic étiologique des dilatations ventriculaires dans 79% des cas contre 46% pour l’échographie. Mots clé: échographie, IRM, apports, fśtus, grossesse. |
|
Magnetic Resonance Imaging (MRI) of the foetus has been developed over the last 10 to 15 years. This technique cannot take over ultrasonography, which remains the key examination for antenatal diagnosis but can't add further improvements over ultrasonography findings, particularly in evaluating the foetal brain. MRI of the fśtus has thus been focused in this area, the main studies aiming at analysing brain malformations and searching for ischemic or hemorrhagic lesions and possible gyration abnormalities. It is obviously in this field that principal study of magnetic resonance of the foetus was carried out, the goal being primarily a better malformations cerebral and extra-cerebral analysing for instance: the MRI allowed the diagnosis etiologic of ventricular dilations in 79% of the cases against 46% for sonography. Keywords: sonography, MRI, adds, foetus, pregnancy. |
REMERCIEMENTS
Nous tenons tout d’abord à remercier Mr LANGEVIN, enseignant-chercheur à l’UTC (Université de Technologie de Compiègne), pour nous avoir permis de réaliser ce projet, et pour nous avoir aidé et suivi tout au long de notre étude.
Nous souhaitons remercier le Dr GARRIOT, gynécologue obstétricien à la Clinique Saint-Côme à COMPIEGNE pour son aide et pour nous avoir permis d’assister à un examen échographique fśtal.
Nous remercions également le Dr GAREL, gynécologue obstétricien à l’Hôpital Robert Debré à PARIS pour son aide et son soutien.
Enfin, nous tenons à remercier
tous ceux qui nous ont aidé dans la progression de notre étude,
et en particulier les praticiens d’IRM fśtale des différents Centres
Hospitaliers de France qui ont bien voulu répondre à nos
questions.
L’échographie fśtale s’est développée depuis maintenant une vingtaine d’années. Son essor considérable qui en a fait l’examen clé en matière de diagnostic anténatal est lié à son faible coût, son innocuité et donc sa reproductibilité, la possibilité d’étudier le fśtus en temps réel dans les trois plans de l’espace et d’accéder ainsi au dépistage d’un grand nombre de malformations congénitales.
Cependant, cet examen n’est pas réalisable dans toute condition et notamment l’obésité de la mère, l’interposition d’anses digestives maternelles, ou la présence d’un oligoamnios altèrent considérablement la qualité de l’image obtenue. De plus, l’étude de la tête fśtale peut être très difficile à réaliser si celle-ci est profondément engagée et la voie endo-vaginale ne permet pas toujours une bonne visibilité de toutes les structures intra-crâniennes. Toute interposition de squelette fśtal masque les structures sous-jacentes. C’est le cas notamment de la voûte du crâne dont l’ossification progressive altère l’étude des structures intra-crâniennes.
De plus, l’appréciation du contraste et de la caractérisation tissulaire se heurte à des limites inhérentes à la nature même de la technique ultra-sonographique. Cet inconvénient est particulièrement patent en matière de pathologie intra-crânienne (mauvaise sensibilité dans la détection de troubles de la giration, de lésions clastiques ou hémorragiques).
Du fait des différents points faibles de l’échographie, on a cherché d’autres techniques d’imagerie susceptibles d’aller au delà de ces limites.
L’imagerie par résonance magnétique (IRM), non irradiante, non-invasive, permettant une étude dans de multiples plans, s’est tout naturellement développée dans le vaste champ du diagnostic anténatal.
Les premières publications remontent à 1983. De nombreux travaux leur ont rapidement succédé qui soulignent tous la principale faiblesse de la technique, c’est à dire l’altération de l’image en rapport avec les artéfacts cinétiques liés aux mouvements fśtaux. Ceci explique la recherche ultérieure de facteurs tendant à supprimer les mouvements fśtaux et le développement de techniques d’IRM visant à réduire le temps d’acquisition.
Nous ferons tout d’abord un résumé
des différentes techniques et examens de surveillance de la grossesse
existants, puis nous nous intéresserons plus particulièrement
à l’examen échographie et aux apports et limites de l’IRM
par rapport à l’échographique traditionnelle.
I. Les différentes techniques de diagnostic et examens anténatal
1.2.2) Prélèvements de villosités choriales et de sang fśtal
1.2.5) Rythme cardiaque fśtal et score de bien-être fśtal
2.2) Echographie du 1er trimestre
2.3) Echographie du 2ème trimestre
2.4) Echographie du 3ème trimestre
3.2) Séquences rapides en écho de spin (Turbo Spin Echo ou Fast Spin Echo)
3.3) La famille écho de gradient
3.4) Séquences rapides en écho de gradient (Turbo Gradient Echo : TGE)
3.5)
Combinaison écho de spin et écho de gradient : les séquences
hybrides
4.3) Comparaison des résultats de l'IRM et de l'échographie
5.1) Indications extra-cérébrales
5.3) IRM du tube digestif fśtal
5.4) IRM de l’appareil urinaire fśtale
VI.
Limites et contre-indications de l’IRM
I. LES DIFFERENTES TECHNIQUES DE DIAGNOSTIC ET EXAMENS ANTENATAL
Face à un taux de mortalité et de morbidité fśtal important et qui reste encore élevé au jour d’aujourd’hui , les examens biologiques et autres techniques de diagnostic se sont vus de plus en plus nombreux.
En 1992, le Ministère de la Santé a fait passer un décret listant tous les examens biologiques anténataux rendus obligatoires afin de mieux prévenir et de pouvoir diagnostiquer le plus tôt possible les pathologies chez le fśtus.
1.1.1)
Les examens obligatoires (décret du 14 février 1992)
| 1er examen | En cas de
1ère grossesse
Dans tous les cas |
- détermination
des groupes sanguins (ABO, phénotype Rhésus complet et Kell)
si la patiente ne possède pas de carte de groupe sanguin complète
(2 déterminations)
- dépistage de la syphilis - sérologie de la rubéole et de la toxoplasmose en l’absence de résultats écrits permettant de considérer l’immunité comme acquise - la recherche d’anticorps irréguliers, à l’exclusion des anticorps dirigés contre les antigènes A et B ; si la recherche est positive, l’identification et le tirage des anticorps sont obligatoires |
| A partir du 2ème examen prénatal | Si l’immunité n’est pas acquise | - la sérologie toxoplasmique est répétée chaque mois |
| 4ème
examen
6ème mois |
- dépistage
de l’antigène HbS
- numération globulaire, recherche d’ anticorps irréguliers - chez les femmes à rhésus négatif ou précédemment transfusées |
|
| 6ème ou 7ème examen | - 2ème détermination du groupe sanguin ABO, Rhésus standard si nécessaire | |
| 6ème
et 7ème examens
8ème et 9ème mois |
- chez les femmes à rhésus négatif ou précédemment transfusées, la recherche d’anticorps irréguliers | |
| Examen postnatal dans les 8 semaines qui suivent l’accouchement |
A chaque examen prénatal, une recherche du sucre et de l’albumine dans les urines (bandelettes urinaires) est réalisée.
D’autres examens biologiques non obligatoires sont pratiqués tels que l’évaluation biologique du risque de la trisomie 21.
Les dosages sériques maternels au nombre d’au moins deux (hCG + alpha-foetoprotéines et/ou l’oestriol), en combinaison avec l’âge maternel, permettent une évaluation du risque de trisomie 21, exprimée en pourcentage.
Au dessus d’un certain seuil, une amniocentèse pour caryotype fśtal est proposée.
Le prélévement doit être réalisé entre 15 et 18 SA.
Ces tests permettent de dépister les deux tiers des trisomies 21, en effectuant des amniocentèses pour 5% des grossesses.
1.2) Les autres techniques de diagnostic
Technique : ponction de la cavité amniotique écho-guidée en zone extra-placentaire.
Amniocentèse précoce
Date : 16-17 SA (risque de perte fśtale de 0,5 à 1%).
Indications :
Détermination du caryotype (délai minimal 15 jours)
Amniocentèse tardive
On retrouve les mêmes indications que ci-dessus.
Sont plus spécifiques les amniocentèses répétées pour l’évaluation de l’allo-immunisation Rhésus (dosage de la bilirubinamnie). Elles peuvent être aussi demandées pour évaluer la maturité pulmonaire, le risque d’infection amniotique ou le diagnostic de rupture des membranes. Elles relèvent du spécialiste.
1.2.2) Prélèvements de villosités choriales et de sang fśtal
Prélèvements de villosités choriales
Technique : aspiration écho-guidée du trophoblaste par voie abdominale de préférence.
Date : de 11 à 12 SA voire jusqu’au 3ème trimestre. Risque fśtal (de 1 à 2 %).
Indications :
Technique : ponction écho-guidée d’un vaisseau ombilical (en général la veine).
Date : de la 20ème SA jusqu’à terme. Risque fśtal (de 1 à 2 %).
La vélocimétrie Doppler est principalement réalisée lors de grossesses à hauts risques.
Doppler de l’artère utérine
Date de réalisation : 20-24 SA
Le Doppler utérin peut être proposé pour la surveillance des grossesses à risque vasculaire maternel et à risque de RCIU (environ de 10 à 20 % des grossesses).
Doppler de l’artère ombilicale
Date de réalisation : 28-34 SA
Doppler des artères cérébrales
Date de l’examen : à partir de 26 SA jusqu’après terme
La mesure du Doppler cérébral est toujours associée à celle du Doppler ombilical.
Les dosages hormonaux faisaient autrefois partie des examens complémentaires sur lesquels le médecin s’appuyait pour évaluer l’évolution de la grossesse. Ils ont été remplacés par d’autres explorations, au premier rang desquelles on retrouve l’échographie, le Doppler et le rythme cardiaque fśtal. En pratique courante, seules l’hormone gonadotrophine chorionique (hCG) et l’oestriol ont un intérêt.
1.2.5) Rythme cardiaque fśtal et score de bien-être fśtal
Le rythme cardiaque fśtal (RCF) a été depuis 1969 et reste actuellement l’un des examens complémentaires qui ont entraîné une diminution de la mortalité périnatale. C’est un des marqueurs les plus facilement accessibles de l’hypoxie fśtale. C’est pourquoi, après avoir été utilisée pendant le travail, la méthode fut étendue à la surveillance de la grossesse.
1.2.6) Les examens radiologiques
La radiopelvimétrie est indiquée surtout :
- en cas de présentation du siège
- devant une suspicion de rétrécissement du bassin.
La radiographie de l’abdomen sans préparation ou radio fśtale garde un intérêt pour le diagnostic des malformations osseuses fśtales.
1.2.7) Compte des mouvements actifs
La surveillance des mouvements fśtaux, par la mère elle-même, au troisième trimestre, fait partie de la surveillance de la grossesse : ils diminuent ou disparaissent le plus souvent quelques heures ou jours avant la mort fśtale.
S’il y a diminution voire disparition
des mouvements actifs : un examen clinique, une échographie, mais
surtout immédiatement un ERCF permettront de porter un diagnostic
de souffrance fśtale.
II. LES EXAMENS ECHOGRAPHIQUES
(voir rappels sur l’échographie en annexe 1)
Acte médical complexe, pris en charge financièrement par la collectivité, l'échographie n'a pas pour principal objectif de montrer l'enfant ou son sexe mais sert à :
Atteindre ces objectifs nécessite des conditions strictes :
Des échos sans anomalie ne sauraient être une assurance certaine de normalité.
Moyennant cette réserve, l'écho a révolutionné le suivi de la grossesse.
Le fśtus devient de ce fait de plus en plus un patient à part entière qu'il convient de respecter et de soigner bien avant sa naissance légale.
3 échographies remboursées
par la Sécurité Sociale sont obligatoires au cours de la
grossesse.
2.2) Echographie du 1er trimestre
C'est une échographie de "morphologie embryonnaire".
En plus de la détermination du nombre d'embryons, de leur vitalité, de la mesure de la longueur du col utérin, ses objectifs sont triples :
Déterminer l'âge de la grossesse (datation)
Dépister les anomalies chromosomiques (clarté nucale)
9-11 semaines de grossesse (11-13 semaines d'aménorrhée)
C'est pourquoi une échographie plus précoce sera parfois demandée au préalable pour déterminer avec certitude la date de début de grossesse.
Elle permettra de programmer secondairement,
à la bonne date, sans erreur, l'échographie de morphologie
embryonnaire.
Datation:
Longueur cranio-caudale ou LCC
(1)tête (2)pôle caudal (3)cavité amniotique (4)utérus
On détermine l'âge de la grossesse (ou âge échographique) en mesurant :
Les Médecins et les Sages-femmes rajoutent systématiquement 2 semaines pour obtenir l'âge gestationnel en semaines d'aménorrhée ou SA :
Exemple : BIP de 20 mm correspondant à un âge de 10 semaines soit 12 SA.
Cet âge gestationnel permettra de calculer la date de début de grossesse.
Cette date est la seule information obtenue par échographie dont il est prouvé qu'elle améliore le pronostic de la grossesse.
Cela fait donc de l'échographie
du 1er trimestre la plus importante de toutes.
Clarté nucale :
Clarté nucale
La recherche des anomalies chromosomiques se fait par la mesure de l'épaisseur de la clarté nucale.
La valeur de cette mesure permet d'estimer le risque réel pour la patiente d'avoir un embryon porteur d'une anomalie chromosomique.
La plus fréquente est la trisomie 21 mais on peut citer le syndrome de TURNER, la trisomie 13 ou 18 par exemple.
Malformations :
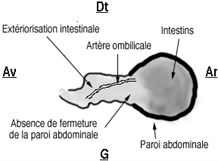
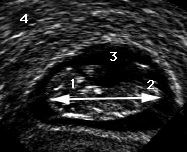
Anomalie de fermeture
de la paroi abdominale (omphalocèle)
Permet le dépistage précoce des malformations embryonnaires les plus sévères :
2.3) Echographie du 2ème trimestre
C'est une échographie de morphologie fśtale qui est réalisée entre la 19ème et la 21ème semaines de grossesse (21 à 23 semaines d'aménorrhée) et qui sert à détecter :
les anomalies de la croissance fśtale:
Tête:
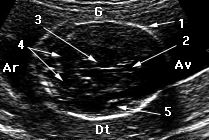
Coupe du biparietal
(BIP)
(1) boite crânienne (2)
septum lucidum
(3) faux du cerveau (4) cervelet
(5) vallée sylvienne
Coupe de la tête, grossièrement horizontale, passant juste au-dessus des oreilles.
Outre la mesure du diamètre bipariétal, elle permet d'analyser le cerveau fśtal :
![]()
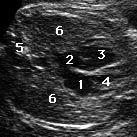
Coupe des 4 cavités cardiaques;
et (4)droit (5)rachis et (6)poumons
Permet, en association avec la coupe dite des vaisseaux de la base, de repérer une partie des malformations cardiaques.
Cordon:
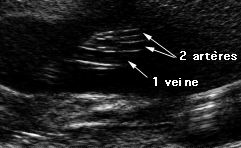
Cette coupe analyse le cordon qui contient :
2.4) Echographie du 3ème trimestre
C'est l'échographie biométrique et morphologique du 3ème trimestre.
Elle se passe entre 29 et 31 semaines de grossesse (31 à 33 semaines d'aménorrhée).
Abdomen:
![]()
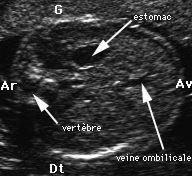
C'est la mesure la plus précise pour détecter les anomalies de croissance fśtale :
Ce qui ne sera vrai que dans environ 50 à 75% des cas.
Reins:
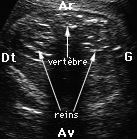
Comprend l'étude :
La régulation du volume de liquide est obtenue par :
A l'inverse, toute augmentation des mictions ou diminution de la déglutition donnera une augmentation du volume de liquide ou hydramnios.
Annexes:
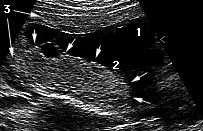
Les annexes fśtales comprennent :
Cette nouvelle technique n'est qu'une amélioration du traitement informatique de l'image échographique standard.
L'écho 3 D présente deux intérêts :
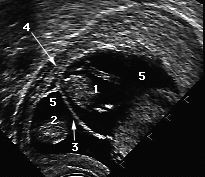
(1-2) embryons (3) cloison (4)
utérus (5) cavités amniotiques
(voir rappels sur les techniques en IRM en annexe 2)
Les applications cliniques de l'IRM présentent un essor extrême avec l'avènement de l'imagerie ultra-rapide sur les imageurs cliniques. Celle-ci rend désormais possible des explorations à la fois morphologiques et fonctionnelles. Le gain en vitesse est obtenu grâce aux progrès des bobines de gradient, de l'électronique, des méthodes de lecture du plan de Fourier, ainsi que de l'informatique permettant le traitement de volumes de données toujours plus importants.
L'application des hypergradients (gradients d'intensité élevés de 20 - 30mT/m à temps de commutation courts (0,2 - 0,4 msec) est le point de départ des nouvelles séquences et de l'imagerie ultra-rapide.
En effet, l'intensité maximale des gradients et leur temps de montée déterminent non seulement la résolution spatiale en terme d'épaisseur de coupe et de dimension de champ de vue d'une part, mais également la résolution temporelle et la résolution en contraste par l'intermédiaire du temps d'écho et du temps de répétition d'autre part .
Plusieurs approches permettent de raccourcir le temps d'acquisition. Elles reposent sur un balayage rapide et plus ou moins complet du plan de Fourier. La méthode actuellement la plus rapide est celle de l'écho-planar (EPI) avec balayage en dents de scie de la totalité du plan de Fourier en un seul signal. Elle fournit une pondération T2*.
Les acquisitions "single shot" ne comportent qu'une seule impulsion à 90° suivie d'un train d'échos de refocalisation beaucoup plus long (110 à 250 ou plus) ce qui permet de lire tout (single shot FSE ou single shot TSE) ou partie (HASTE) du plan de Fourier dans des temps très courts de l'ordre de 1 à 7,5 secondes.
De telles techniques nécessitent une installation moins coûteuse que l'écho-planar et fournissent une pondération T2.
Les impulsions à 180° et les échos de gradient peuvent être conjugués pour former des séquences hybrides (GRASE, TGSE) ayant pour avantage la diminution des effets de susceptibilité magnétique et la diminution du taux d'absorption d'ondes RF.
L'imagerie ultra-rapide permet ainsi d'observer ou de supprimer des mouvements physiologiques (cardio-vasculaires, respiratoires, intestinaux).
L'avantage essentiel des séquences
spin écho est de pouvoir obtenir des images en vrai T2. En effet,
dans les séquences qui n'utilisent pas l'écho de spin, T2
est perdu dans T2*. L'angle de bascule de 90° n'est pas obligatoire
mais c'est celui qui représente le meilleur compromis. La vraie
caractéristique de la famille Spin Echo est l'existence d'une impulsion
de 180° de rephasage des spins. C'est elle qui permet d'avoir un vrai
T2. Le schéma ci-dessous représente la séquence spin
écho classique.
Séquence en spin écho classique avec 2 échos
3.2) Séquences rapides en écho de spin (Turbo Spin Echo ou Fast Spin Echo)
La séquence spin écho rapide est un perfectionnement particulièrement intéressant. En spin écho conventionnel, le gradient de codage de phase est appliqué une seule fois, même si l'on recueille plusieurs échos. En spin écho rapide, l'impulsion initiale est suivie d'un train d'impulsions à 180°, donc d'un train d'échos (de 2 à 128), et un gradient de codage de phase différent est utilisé pour chaque écho, ce qui raccourcit le temps d'acquisition d'un facteur de 2 à 128 suivant le nombre d'échos recueillis (le plus souvent 8 ou 16). Ce nombre est appelé TURBO facteur. Lorsque le turbo facteur est très élevé, le signal diminue, et seuls les liquides qui ont un T2 très long vont encore donner un signal.
Une autre séquence particulière en Turbo Spin Echo est la séquence HASTE où seulement un demi-plan de Fourier est acquis ce qui permet d'obtenir une coupe en une seconde.
3.3) La famille écho de gradient
Ce qui caractérise la famille
écho de gradient, c'est l'absence d'impulsion de 180° de rephasage
des spins.
Le rephasage des spins est obtenu
en inversant les gradients, ce qui est réalisable beaucoup plus
rapidement qu'une impulsion RF. C'est pourquoi l'avantage essentiel des
premières séquences en écho de gradient a été
le gain de temps (de deux à quatre fois) par rapport au spin écho
classique.
Cette séquence de base en écho de gradient a reçu des noms différents suivant les constructeurs. Par exemple la même séquence s'appelle GRASS (Gradient écho in the Steady State) chez General Electric, FAST (Fourier Acquired Steady State) chez Picker, FFE (Fast Field Echo) chez Philips et FISP chez Siemens.
Il existe des variantes de la séquence
de base en écho de gradient. Lorsque le TR est très court
par rapport à T2, (en pratique en dessous de 25 msec), il reste
une magnétisation transversale résiduelle au moment de la
nouvelle impulsion RF. Cette magnétisation transversale résiduelle
entraîne un hypersignal parasite des liquides. Elle est détruite
au moyen d'un gradient puissant appelé SPOILER.
Ce sont les séquences appelées FLASH (Fast Low Angle SHot), SPGR (SPoiled Gradient Recalled), etc. …
Il existe d'autres variantes d'intérêt plus restreint.
3.4) Séquences rapides en écho de gradient (Turbo Gradient Echo : TGE)
Le principe est le même que
pour les séquences rapides en écho de spin. On utilise un
gradient oscillant rapidement pour former un train d'échos à
la suite d'une seule impulsion RF. Chaque écho est codé différemment
par le gradient de codage de phase qui est administré en même
temps.
3.5) Combinaison écho de spin et écho de gradient : les séquences hybrides
Si les méthodes "turbo" dont il vient d'être question donnent des images de bonne qualité, en des temps parfois aussi brefs qu'une ou quelques dizaines de secondes, leur combinaison permet d'obtenir des images en un temps inférieur à la seconde. Ce sont les perfectionnements techniques incessants apportés aux antennes, aux gradients et à l'informatique qui permettent de réaliser l'acquisition du signal de la totalité d'un plan avec une seule impulsion.
On peut combiner écho de spin et écho de gradient de plusieurs manières. La première est de partir d'une séquence turbo spin écho. Dans "l'enveloppe" de chaque écho on applique un gradient oscillant. On combine donc les effets positifs des deux séquences turbo, d'où le nom de TGSE (Turbo Gradient Spin Echo) ou encore de GRASE (GRadient And Spin Echo).
Dans cette séquence on n'utilise pas des "turbo" facteurs très élevés, car on est encore limité par des facteurs techniques.
La deuxième est connue sous le nom de séquence écho-planar (EPI). Sur le plan théorique, c'est presque une simplification de la précédente. La première partie de cette séquence est une séquence spin écho classique, c'est-à-dire qu'on y voit se succéder deux impulsions, l'une de 90°, l'autre de 180°.
Sur cette base classique, on rajoute
un gradient de lecture Gx qui oscille rapidement d'une amplitude positive
à une amplitude négative pour former un train d'échos
de gradients. Chaque écho est codé différemment par
le codage de phase Gy qui est administré en même temps. Les
lignes du plan de Fourier au lieu d'être acquises l'une après
l'autre, sont acquises en une seule fois (EPI-single shot). Chaque oscillation
du gradient de lecture correspond à une ligne du plan de Fourier
et chaque incrémentation du gradient de phase correspond à
un changement de ligne. Si on désire une matrice de 256 et si on
décide de lire 32 lignes à la fois, il faudra en technique
multi-shot 266/32 = 8 passages. Par rapport à un seul passage, la
qualité de l'image sera nettement améliorée car il
y aura moins de distorsions géométr! iques. Cette technique
ultra-rapide donne des coupes en quelques millisecondes et ouvre la porte
à l'exploration des mouvements articulaires, des flux comme celui
du liquide céphalo-rachidien, du cśur et des vaisseaux, et à
l'examen des malades non-coopérants et des enfants. Il permet l'imagerie
de l'abdomen pendant une simple pause respiratoire. Néanmoins, pour
les temps très court, la qualité de l'image n'est encore
pas compétitive avec les séquences classiques et l'écho-planar
doit être considéré avant tout comme un additif à
une exploration standard, pour obtenir des informations fonctionnelles.
IV IRM CEREBRALE FŚTALE
Cette imagerie, exceptionnellement de première intention, est pratiquement toujours décidée et orientée par une exploration ultrasonore anténatale douteuse, difficile ou anormale.
L’IRM permet dans la plupart des cas d’affirmer ou de confirmer un diagnostic, ou de rechercher des anomalies associées aux signes d’appels décelés lors d’un examen échographique. L’IRM de l’encéphale est la plus pratiquée. Mais il existe une exploration croissante de la face, du thorax et de l’abdomen.
Les IRM cérébrales représentent environs 70% des indications. La technique est développée depuis 1983 et les indications sont surtout justifiées pour des dilatations ou des infections, l’IRM permet de surmonter les limites de l’échographie (facteurs maternels, ossification de la voûte crânienne).
Les principales pathologies sont :
- Les dilatations ventriculaires, d’origine malformative (par exemple sténose de l’aqueduc de Sylvius), hémorragique, infectieux (par exemple CMV, l’IRM est plus performante que l’échographie pour démontrer les calcifications). L’IRM est utile dans ce bilan, avec un bilan infectieux et une analyse du caryotype.
Exemple : Sténose
de l'aqueduc de Sylvius avec hydrocéphalie importante.
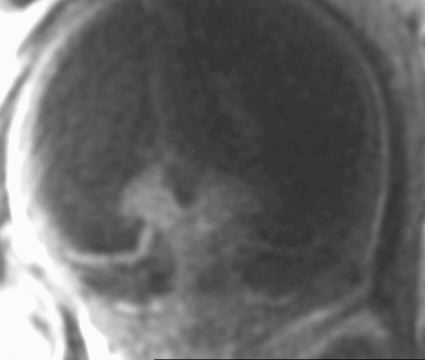
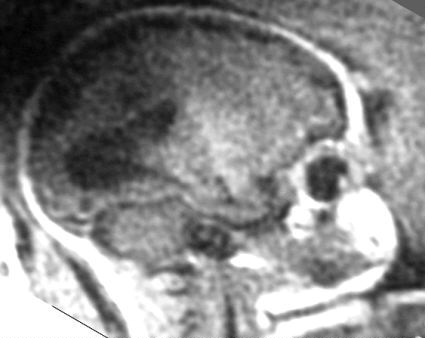
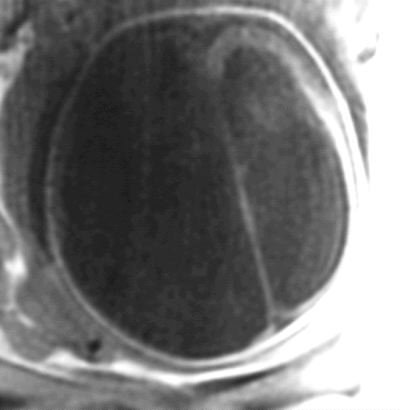
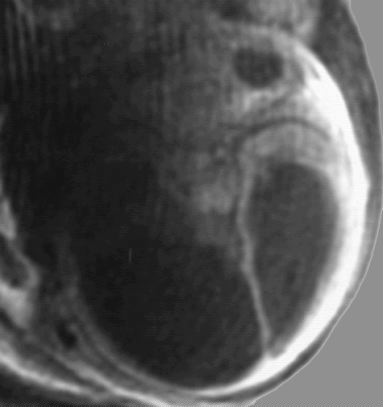
Absence de parenchyme cérébral remplacé par une
structure liquidienne. Présence d'une septation médiane.
Les structures diencéphaliques sont visibles.
Exemple : Dilatation isolée des carrefours ventriculaires, modérée, stable.
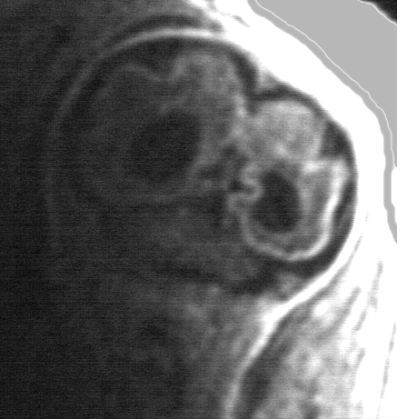
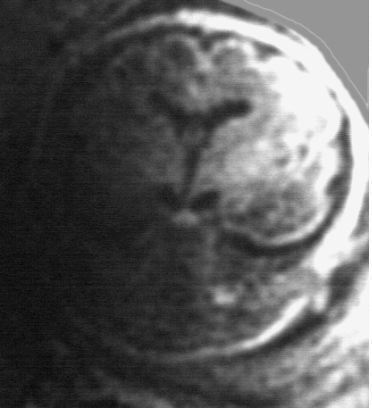
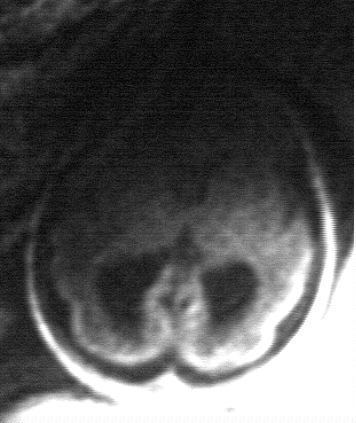
1)
Coupe frontale postérieure. Dilatation des carrefours
ventriculaires. Fosse postérieure normale sur cette incidence.
2)
Coupe frontale médiane. Normalité de la gyration.
Corps calleux présent. Pas d'anomalie parenchymateuse cérébrale.
3)
Coupe axiale. Dilatation des carrefours ventriculaires
- Les anomalies de la ligne médiane
(agénésie du corps calleux, associée ou nom à
d’autres malformations, syndrome de Dandy-Walker, holoprosencéphalie).
Exemple : Agénésie du corps calleux.
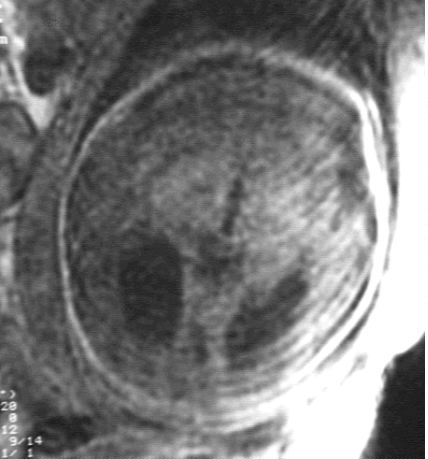 Coupe
axiale. Dilatation des carrefours ventriculaires.
Coupe
axiale. Dilatation des carrefours ventriculaires.
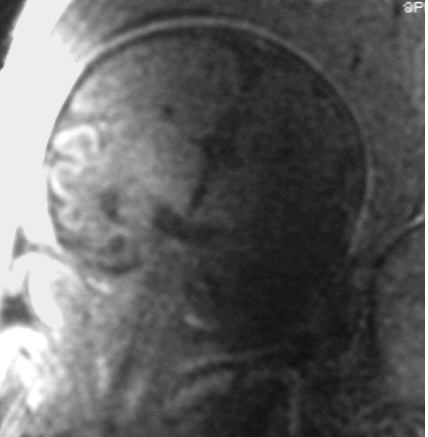
Coupe frontale. Agrandissement : aspect typique en "corne de taureau"
avec ascension du troisième ventricule.
Absence de corps calleux.
Exemple : Holoprosencéphalie lobaire.
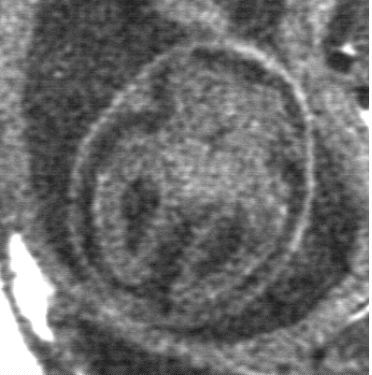 Coupe axiale. Dilatation des deux carrefours ventriculaires
Coupe axiale. Dilatation des deux carrefours ventriculaires
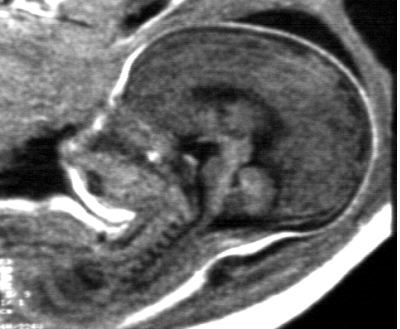 Coupe sagittale. Pas d'anomalie de fosse postérieure, ni de
la ligne médiane.
Coupe sagittale. Pas d'anomalie de fosse postérieure, ni de
la ligne médiane.
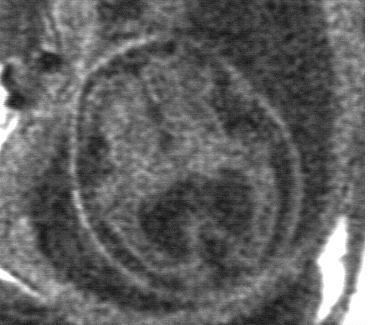 Coupe axiale. Aspect de fusion des ventricules latéraux (postérieure).
Coupe axiale. Aspect de fusion des ventricules latéraux (postérieure).
- Infection à CMV. Lors de séroconversion ou de réinfections, d’explosion (toxique, médicamenteuse), confirmée par amniocentèse, l’IRM est utile pour rechercher des atteintes parenchymateuses, plus efficacement que l’échographie.
- Recherche de lésions ischémiques intraparenchymateuses (substance grise, substance blanche, noyau gris).
- Etude des sillons et des circonvolutions à la recherche d’un trouble de la migration neuronale.
- Autres anomalies : kystes, anomalies de la fosse postérieur, microcéphalies, troubles circulatoires (doppler pathologique), facteurs de risques héréditaires (sclérose tubéreuse de Bourneville).
Exemple : Kyste du septum lucidum.
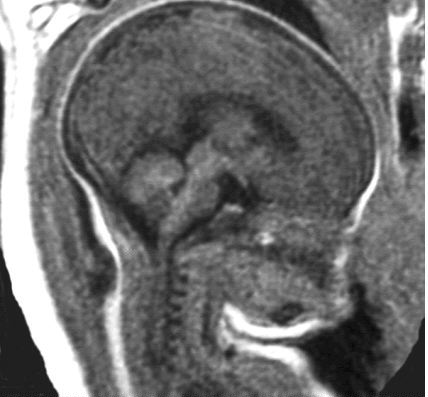 Coupe sagittale médiane. Normalité des structures
cérébrales et de la fosse postérieure.
Coupe sagittale médiane. Normalité des structures
cérébrales et de la fosse postérieure.
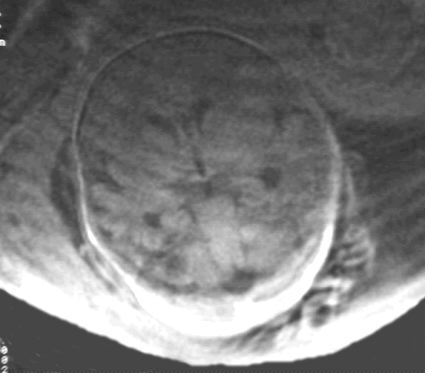 Coupe frontale montrant l'aspect normal du système ventriculaire,
des structures cérébrales, fosse postérieure.
Coupe frontale montrant l'aspect normal du système ventriculaire,
des structures cérébrales, fosse postérieure.
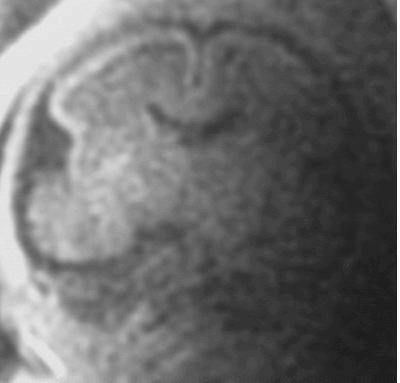 Coupe frontale. Aspect lisse, physiologique, du cerveau. Indentation
sylvienne déjà visible. Les espaces péricérébraux
sont larges jusqu'à 26 SA environ.
Coupe frontale. Aspect lisse, physiologique, du cerveau. Indentation
sylvienne déjà visible. Les espaces péricérébraux
sont larges jusqu'à 26 SA environ.
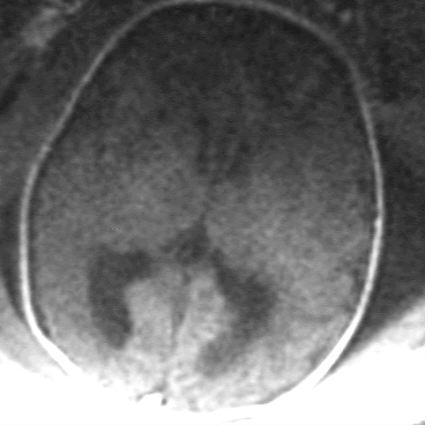 Coupe axiale normale.
Coupe axiale normale.
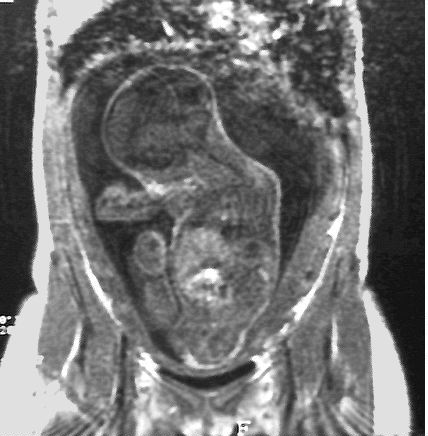
Coupe frontale. La présentation
en siège s'avère comme une limite de la méthode, les
artefacts de mouvements étant trop nombreux (respiration ?).
Les séquences sont prises en T1 (liquide noir, utile pour recherche de sang ou de calcification) ou en T2 (liquide blanc, utile pour l’analyse morphologique du cerveau).
Le protocole IRM de base comprend toujours une étude des trois plans de l’espace et toujours des séquences T2, et la plupart du temps l’obtention de séquences T1. Les séquences T2 rapides en une vingtaine à une trentaine de secondes sont soit en FSE, soit en Single Shot.
L’examen est pratiqué en antenne de surface dans la majorité des cas. L’échographie concomitante à l’IRM est quelques foi réalisée en particulier pour repérer la position de la tête.
Une étude biométrique est réalisée dans la plupart des cas. Les mesures les plus souvent pratiquées sont le diamètre bi-pariétal et fronto-occipital. L’analyse de la giration est effectuée vers 30 à 32 semaines.
Le cerveau du fśtus est exploré dans les trois plans de l’espace (sagittale, coronale et axiale). L’étude permet :
- de faire la biométrie de chaque partie du cerveau,
- d’observer la gyration des sillons,
- d’observer la myelisation du cerveau.
4.3) Comparaison des résultats de l'IRM et de l'échographie
Pour pouvoir bien comparer les apports
de l’IRM par rapport à l’échographie, nous avons fait un
résumé des résultats de différentes études
qui ont été réalisées sur le sujet (notamment
l’étude réalisée par le Dr F Lain-Milan et al). Il
s’agit d’études rétrospectives sur 34 IRM réalisées
entre 1992 et 1996 chez 29 patientes âgées de 21 à
41 ans. Pendant cette période, une IRM a été réalisée
de façon systématique devant toute anomalie encéphalique
détectée en échographie obstétricale.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Tableau 4.3.1 Tableau récapitulatif des examens d’échographie & d’IRM réalisés dans certains hôpitaux.
Les 24 cas de dilatation ventriculaire échographique ont été confirmés en IRM. L’IRM a retrouvé l’étiologie à la dilatation ventriculaire dans 19 cas (n=24), alors que l’échographie n’en a retrouvé que dans 11 cas (n=24).
Parmi les 13 cas avec dilatation isolée en échographie (cf. tableau 4.3.1), l’IRM a retrouvé dans 9 cas, une étiologie méconnue par l’échographie :
- 5 ACC (Agénésie du Corps Calleux),
- 2 anomalies corticales : une hémimégalencéphalie et une atrophie unilatérale d’origine ischémique,
- 1 kyste interhémisphérique,
- 1 hémorragie intraventriculaire de grade III.
Dans 4 cas, L’IRM n’a pas pu retrouver de cause à cette dilatation ventriculaire.
Dans 11 cas, l’échographie retrouvait des anomalies associées à la dilatation ventriculaire ; ces 11 cas représentaient 13 malformations sus et sous tentorielles :
- dans 3 cas, l’IRM a confirmé le diagnostic échographique, il s’agissait d’une ACC, d’une holoprosencéphalie et d’un anévrisme de la veine Galien (cas n° 16, 22 et 23).
- dans 2 cas, l’IRM a précisé le diagnostic échographique de microcéphalie (cas n°24) en montrant une hydranencéphalie et le diagnostic échographique d’anomalie corticale (cas n°21) en montrant une lissencéphalie.
- dans 3 cas, l’IRM a modifié le diagnostic en infirmant (cas n° 14 & 15) ou affirmant (cas n°17) le diagnostic d’agénésie du corps calleux.
- enfin les 5 suspicions de malformation de la fosse postérieure ont été confirmées par l’IRM. Dans 3 cas, les précisions anatomiques ont été apportées (cas n° 14, 17 & 18) ; dans 2 cas de malformation non kystique, aucune des deux techniques n’a pu préciser s’il s’agissait d’une agénésie cérébelleuse ou d’une malformation de Chiari II (cas n° 19 & 20).
Dans les cinq derniers cas, l’IRM n’était pas justifiée par la découverte échographique d’une dilatation ventriculaire :
- dans 3 cas, l’IRM n’a pas apporté d’argument supplémentaire aux diagnostics de microcéphalie (cas n° 24 & 17) et de lipome du corps calleux (cas n° 28).
- dans 1 cas, une suspicion d’anomalie temporale n’a pas été confirmée par l’IRM (cas n° 29).
- enfin dans le cas n° 26, alors que l’échographie suspectait la présence d’une ménigocèle occipitale, l’IRM a été considérée comme normale sur deux examens réalisés durant le deuxième trimestre de vie fśtale.
Dans l’ensemble, l’IRM anténatale est un examen fiable puisqu’il n’y a eu que deux faux négatifs (cas n° 25 & 26). Dans l’étude, la dilatation ventriculaire représente l’indication la plus fréquente de l’IRM (24 cas sur 29). Cette technique est plus performante que l’échographie pour le diagnostic étiologique de la dilatation ventriculaire (79% contre 46%). Les anomalies méconnues par l’échographie sont malformatives (ACC, anomalies corticales, kyste interhémisphérique) ou hémorragiques. Dans 37% des cas de cette série (n=29), l’IRM a clairement modifié la prise en charge des patientes. Les hémorragies intracérébrales ont un hypersignal caractéristique sur les séquences pondérées en T1 qui rend l’IRM plus performante que l’échographie pour ce diagnostic comme pour le cas n° 3. Devant une dilatation ve! ntriculaire anténatale, l’ACC est l’étiologie la plus fréquemment découverte (33% n=24). Ce diagnostic a été fait dans tous les cas par l’IRM, alors qu’il a été méconnu dans 5 cas et posé par excès en échographie dans 2 cas. Dans 7 cas, l’IRM a donc modifié les résultats de l’échographie, qui avait pourtant été exploitée au maximum : voie endovaginale, Doppler sur l’artère pericalleuse.
L’IRM est également plus performante que l’échographie pour le diagnostic de malformation corticale puisque 2 sur 3 avaient été méconnues par l’échographie (cas n° 5 & 9). Sur les séquences pondérées en T1, le meilleur signe indirecte est l’orientation anormale des vallées sylviennes qui se ferment normalement vers la 28ème SA.
Il y a eu deux faux négatifs dans cette étude (cas n° 25 & 26). Dans le cas n° 26, le résultat négatif de l’IRM a modifié la conduite thérapeutique, laissant naître un enfant qui présentait un syndrome d’Apert. Dans le cas 25, la petite taille des structures a rendu difficile l’interprétation des clichés difficile.
La découverte échographique d’une dilatation ventriculaire du cerveau fśtal est une bonne indication d’IRM anténatale si les critères échographiques de dilatation pathologique sont respectés.
Le terme optimal pour effectuer cet examen est supérieure à 28 SA (les structures cérébrales ont un volume suffisant). L’IRM est souvent décisionnelle, confirmant un diagnostic posé en échographie, le modifiant ou le changeant ainsi la conduite thérapeutique. Par son intérêt anatomique (bonne visualisation de la ligne médiane, du cortex, de la fosse postérieure,…), l’IRM constitue un acte objectif, utile en particulier en cas de décision d’ITG.
Le meilleur intervalle pendant lequel il est intéressant de réaliser une IRM fśtale pour étudier la gyration se situe entre la 28ème et la 34ème SA. Cette étude a été réalisée sur la majorité des coupes permettant l'étude des sillons du cerveau. En principe, un sillon est défini comme "absent" s'il est visualisé dans moins de 25% des cas, il est "détectable" entre 25 et 75% des cas et "présent" s'il est visualisé dans plus de 75% des cas.
Les sillons de la face interne des hémisphères sont mieux étudiés en coupe sagittale et ceux des faces inférieures et externes en coupe coronale.
Les études en IRM ont montré que les principaux sillons apparaissent entre le 5ème et le 8ème mois de la grossesse et que le dernier mois de grossesse présente une complexité croissante des sillons et des circonvolutions.
En fait, en IRM, la meilleure corrélation entre un sillon et l'âge gestationnel est obtenue pour des sillons après la 28ème SA. Après la 34ème SA, la finesse des espaces gêne la visibilité des sillons.
L'étude de la gyration n'est pas bien analysée en échographie fśtale car la visibilité des sillons cérébraux dépend de la qualité de l'échographe (résolution spatiale, etc.…). Alors qu'en IRM, elle permet une image plus détaillée et plus vraie.
La myelisation est étudiée en pondération T1 sur une coupe transversale passant par le IVème ventricule. Une myelisation se caractérise par un hypersignal en T1. La myelisation est considérée comme étant la dernière phase de maturation cérébrale. Cette phase débute au 2ème trimestre de la vie fśtale intra-utérine et se poursuit au-delà de la naissance. Au cours cette phase, on observe une augmentation de lipides et de protéines. La myelisation du cerveau fśtal a été étudiée en foeto-pathologie et elle est considérée à l'instar de la gyration comme un index de maturation cérébrale fśtale.
L'IRM
est une méthode d'imagerie bien adaptée au phénomène
de myelisation dont les modifications se traduisent par des variations
du signal du parenchyme cérébral. L'hypersignal en T1 reflète
l'augmentation de la densité cellulaire (concentration élevée
de glycérol et des glycolipides). On commence à observer
un hypersignal en T1 à partir de la 35ème SA en
IRM extra-cérébrale fśtale.
V. IRM EXTRA-CEREBRALE FOETALE
L'échographie est l'examen de dépistage des malformations extra cérébrales. L'imagerie par résonance magnétique fśtale peut s'avérer un examen complémentaire utile lorsqu'il existe des obstacles à la transmission du faisceau ultrasonore (obésité, oligoaminos, malformation utérine, etc.…), lorsque la malformation en cause est complexe (masse cervico-thoracique) ou lorsque l'US est incapable de préciser le diagnostic et le pronostic fśtaux.
5.1) Indications extra-cérébrales
Quelques indications extra-cérébrales sont en cours d’évaluation. Actuellement, la principale indication extra-céphalique est pulmonaire (hernie, hypoplasie).
- Analyse du parenchyme pulmonaire : les anomalies adénomateuses sont bien mises en évidence, permettant de monter la partie du poumon non malade ; d’autres opacités liquidiennes comme les kystes bronchogéniques sont bien mises en évidence, ou en cas de malformation des voies respiratoires par exemple : agénésie trachéale. Lors d’hernie diaphragmatique, la persistance ou non de parenchyme pulmonaire pourrait avoir un facteur pronostic, un protocole est en cours. L’IRM est meilleure que l’échographie dans la recherche de malformation associée.
- Analyse abdomino-pelvienne : kyste du petit bassin : méningocèle, tératome kystique ou anomalie intestinale (duplication atrésie) peuvent être défini. L’IRM permet un bon bilan d’extension et permet d’éviter d’autres examens inutiles à la naissance. Ce type d’IRM est à faire entre 30 et 35 semaines, avec une approche pluridisciplinaire.
- Des explorations de la face sont également de plus en plus réalisées.
L'examen est réalisé avec une prémédication maternelle afin de réduire les mouvements fśtaux ou bien, de plus en plus souvent sans prémédication à l'aide des séquences rapides (FSE en T2, HASTE). Les séquences HASTE, plus rapides, sont moins sensibles aux artéfacts de mouvement mais offrent une résolution spatiale inférieure à celle obtenue grâce aux séquences FSE T2. Les séquences en écho de gradient T1, sensibles ou non au flux, permettent l'individualisation des structures vasculaires et des structures graisseuses. Les séquences sont réalisées dans les plans axial, frontal et sagittal.
En pondération T2, la trachée,
les bronches souches, les bronches lobaires et l'śsophage sont plus aisément
individualisable au sein du médiastin qu'en échographie.
Le signal du thymus, homogène, est discrètement plus intense
que le myocarde adjacent. Les gros vaisseaux médiastinaux, les cavités
cardiaques présentent un signal plus faible que celui du myocarde
adjacent. Il est actuellement possible d'obtenir des coupes des quatre
cavités à l'IRM. Les cavités cardiaques, l'aorte,
les vaisseaux de la gerbe aortique, les veines caves, les veines pulmonaires
et la veine azygos sont parfaitement visibles en pondération T1.
Dans cette même pondération, la thyroïde présente
un signal intense. Les organes sous-diaphragmatiques (foie, rate, estomac,
colon, intestin grêle, surrénales, reins) sont aisément
identifiés.
Les avantages de l’IRM par rapport à l’US dans la pathologie thoracique fśtale sont :
5.3) IRM du tube digestif fśtal
Ce type d’imagerie a été développé parce qu’il existe de réelles insuffisances dans le diagnostic échographique anténatal d’une pathologie du tube digestif. Actuellement, l’image ultrasonore se borne à dépister une dilatation des anses digestives ou à mettre en évidence des intestin hyperéchogène. Par rapport à l’échographie, l’IRM propose un signal spécifique (d’aspect différent selon les séquences) du contenu de l’intestin grêle et du colon apportant ainsi des potentialités diagnostiques en particulier dans la pathologie digestive grave du fśtus.
A partir de la 28ème SA, l’intestin grêle se rempli progressivement du liquide amniotique dégluti et le côlon se comporte comme un réservoir à méconium, ceci est essentiel car ces constatations vont conditionner le signal IRM du tube digestif.
Un des gros avantages de l’IRM du tube digestif fśtale (par l’intermédiaire des signaux spécifiques de l’estomac, du grêle et du côlon) est la possibilité de situer très précisément le siège de l’obstruction du côlon et du grêle alors que ce n’est pas toujours le cas pour l’échographie. L’IRM fśtale paraît également bien supérieure à l’exploration ultrasonore sur la nature de l’obstruction : atrésie ou iléus méconial.
Dans une étude réalisée [A. Couture et al, 1997], l’IRM du tube digestif semble ouvrir de grande potentialités dans la mise en évidence de pathologie digestives graves. C’est ainsi que contrairement aux données échographiques, l’IRM permet de mettre en évidence le microcôlon d’un syndrome obstructif. Le diagnostic étiologique est probablement possible par l’intermédiaire de l’IRM : très importante dilatation liquidienne en hypersignal T2 modéré sur les séquences T1 dans le cadre d’une atrésie jéjunale ou iléale ; dilatation plus modérée des anses d’amont en hypersignal modéré sur les séquence T1 du fait de la présence de méconium ; microcôlon majeur.
Le diagnostic échographique anténatal des malformations anorectales reste très difficiles en échographie. Dans une autre étude faite par la même équipe, l’IRM permet de montrer des signes évocateurs : dilatation du côlon et modification du contenu colique. Tous ces éléments sont en faveur d’une communication anormale entre le système urinaire et le côlon. Les signes IRM sont facile à déduire : côlon dilaté en hypersignal T2, hyposignal T1 du fait de la présence d’urine dans le système digestif.
5.4) IRM de l’appareil urinaire fśtale
Les anomalies de l’appareil urinaires représentent 14 à 50% [Metens et al, 1999] des malformations congénitales. Dans des rares circonstances, les renseignements fournis par l’échographie sont insuffisantes pour poser un diagnostic ; l’imagerie par résonance magnétique peut alors s’avérer un examen complémentaire utile.
La technique d’examen ne se différencie pas fondamentalement des autres examens d’IRM fśtale. La sédation maternelle n’est dans la plupart des cas plus indispensable grâce aux séquences rapides disponibles (SE rapide, HASTE, EPI, …). Les séquences fortement pondérées T2 sont les plus utiles pour étudier la morphologie de l’appareil urinaire dans son ensemble. Les séquences T1 permettent de rechercher des composantes graisseuses (tératome), d’apprécier les effets de masse sur les gros vaisseaux ou encore d’identifier des structures digestives riches en méconium.
Les avantages de l’IRM reposent sur
son large champ de vision et sa résolution tissulaire. Par rapport
à l’échographie, l’IRM identifie ou précise l’insertion
ectopique des uretères, l’anatomie des malformations pelvienne de
type cloaque, l’extension intrapelvienne des tératomes, la localisation
des masses rétropéritonéales, la localisation médullaire
de certains kystes rénaux, l’existence ou non des reins en cas d’anamnios.
Elle détecte également l’extension des lésions ischémiques
rénales en cas de thrombose veineuse. Ces renseignements permettent
parfois de modifier le diagnostic échographique présomptif,
de préciser l’anatomie des anomalies fśtales, de conforter une décision
de poursuite ou d’interruption de grossesse au vu de l’extension des anomalies
observées. Enfin, l’intérêt compléme! ntaire
de l’IRM est la compréhension plus aisée des clichés
par les cliniciens.
VI. LIMITES ET CONTRE-INDICATIONS DE L’IRM
L’IRM fśtale n’est pas capable actuellement d’apporter les renseignements anatomiques et hémodynamiques obtenus par l’échographie et le Doppler en particulier pour l’étude du cśur fśtal. La résolution spatial de l’IRM est inférieure à celle de l’US mais est compensée par sa résolution en contraste. En fonction de l’âge gestationnel et de la taille des lésions, certaines structures échappent au diagnostic (en particulier certains petits vaisseaux ou kystes observés dans les malformations parenchymateuses pulmonaires ou cérébrales).
Les contre-indications générales à l'IRM doivent être respectées. D'exceptionnels cas de claustrophobie maternelle empêchent parfois la réalisation de l'examen. Aucun effet délétère de l’IRM fśtale n’a été démontré jusqu’à présent chez l’être humain alors que les premiers articles décrivant son utilisations en clinique datent des années 80. Il convient cependant de rester prudent et de restreindre ses indications aux problèmes non résolus par l’échographie.
L’IRM est à éviter au cours du premier trimestre de la grossesse (organogenèse) en raison de sa moins bonne résolution spatiale par rapport à l’US et du fait de la petite taille des structures fśtales qui sont un obstacle à une IRM réellement fiable.
L'IRM n'est donc pas un examen de
dépistage. Elle ne se justifie qu'après examen échographique
détaillé, enquête familiale, examen caryotypique et
bactériologique et est idéalement réalisée
par des équipes multidisciplinaires connaissant la pathologie anté
et périnatale. L'IRM ne se justifie que si les renseignements fournis
sont susceptibles de modifier le diagnostic, le pronostic et / ou l'attitude
obstétricale et néonatale. US et IRM sont complémentaires;
l'idéal est de combiner les deux approches dans un même temps
et pour la surveillance des grossesses compliquées.
Pour conclure, d’un point de vue éthique, à l’heure actuelle des travaux expérimentaux et cliniques ne permettent pas d’établir de preuves d’effets délétères sur le développement du fśtus induits par une exposition à un champs électromagnétique. Cependant en France il est recommandé de ne pas réaliser d’IRM pendant le premier trimestre, période d’organogenèse, sauf si la grossesse est interrompue. De même, l’usage du gadolinium (produit de contraste utilisé en IRM) est proscrit pendant la grossesse en l’absence de preuves de son innocuité chez le fśtus.
En dehors de ces problèmes d’innocuité, l’IRM présente incontestablement plusieurs handicaps vis-à-vis de l’échographie. Il s’agit d’un examen coûteux (environ 10 fois plus cher qu’une échographie) qui ne peut être utilisé dans un dépistage de masse. C’est un examen long, l’étude d’une région durant environ 40 minutes (20 minutes pour une échographie morphologique complète du fśtus). La région à explorer , le plus souvent la tête, est repérée en échographie juste avant l’IRM Les coupes réalisées ne sont pas toujours reproductibles et des mouvements, mêmes faibles, gênent leur repérage.
L’IRM fśtale est cependant une technique
en plein essor et ses débuts paraissent déjà lointains,
alors que les premières images ne permettaient que de réaliser
quelques mesures ou de confirmer des diagnostics évidents. Son principal
champ d’investigation reste le cerveau fśtal, pour mettre en évidence
les anomalies de la gyration, les lésions ischémo-hémorragiques
et les anomalies de la fosse postérieure. Les progrès de
logiciels de post-traitement de l’image, les acquisitions volumiques, le
développement de la technique d’écho-planar et de séquences
de forte pondération T2 offrent des perspectives d’avenir.
Nous voudrions terminer en insistant
sur le fait que, en l’état actuel des choses, la contribution réelle
de cet examen est encore dans une phase d’évaluation. A ce titre,
il devrait faire l’objet de protocoles stricts réservés à
certains centres pluridisciplinaires de diagnostic prénatal, l’IRM
se plaçant en sus de l’échographie pour tenter d’apprécier
au mieux le pronostic fśtal notamment cérébral.
Age de la grossesse
Déterminée en semaines à partir du jour de la fécondation auquel on rajoute, arbitrairement, 2 semaines pour obtenir un terme en semaine d'aménorrhée ou SA.
Agenesie du corps calleux
L'agénésie est l'absence totale ou partielle d’un tissu, d’un organe ou d’une structure, depuis la vie embryonnaire, et secondaire à une cause héréditaire.
Le corps calleux est la partie réunissant les deux hémisphères cérébraux constituant le cerveau.
Aménorrhée
Ce mot signifie arrêt des règles, l'âge d'une grossesse se compte en semaines d'aménorrhée.
Amniocentèse
Prélèvement de liquide amniotique que l'on fait à l'aiguille au travers du ventre de la mère, l'analyse du liquide peut donner des renseignements utiles sur le bébé (Caryotype notamment) on peut la réaliser à partir de la 16 à la 17 semaine.
Anencéphalie
Anomalie globale, définie par l'absence de fermeture de tube neural à son extrêmité céphalique.
Aplasie
Absence d'un organe provoquée par l'absence de développement de son ébauche embryonnaire. Exemple : aplasie surrénalienne.
Atrasie
Variété d'aplasie consistant en l'absence de développement de la lumière d'un organe creux avec, éventuellement, absence de certains segments de cet organe.
Bilirubinamnie
Le dosage de la bilirubinamnie est l’évaluation de l'allo-immunisation Rhésus. Elles peuvent être aussi demandées pour évaluer la maturité pulmonaire.
BIP : diamètre biparietal
C'est la mesure d'un os pariétal à l'autre c'est à dire de la largeur de la tête du bébé.
Clarté nucale
Epaississement transitoire de la région postérieure du cou de tous les embryons en fin de 1er trimestre.
CMV : Cytomegalovirus
Virus responsable d’infections.
DAT : Diametre Abdominal Transverse
Dysraphie médullaire
Ce sont des malformations de la moelle, de ses enveloppes ou du canal rachidien, consécutives à une anomalie de fermeture du tube neural.
Encéphalocèle
Extériorisation du tissu cérébral à travers une brèche crânienne.
ERCF
Il s'agit de l'enregistrement du rythme cardiaque fśtal, en fait le monitoring trace deux courbe l'une pour l'activité utérine et l'autre pour les variations des battements par mn. Le papier enregistreur défile à 1 cm par mn, une feuille de tracé représente 10 mn.
Héminégalencéphalie
C’est une malformation rare caractérisée par une asymétrie, une dysplasie corticale avec neurone géants et une perte de la cytoarichitectonie normale.
Hémorragie intraparenchymateuse
Hyperéchogénicité du parenchyme.
Holoproencephalie
L’holoproencéphalie correspond à l’absence de séparation des deux hémisphères dans les trois sens : sagittal, transversal et longitudinal.
Hormone de grossesse
Encore appelée HCG, elle est sécrétée par la grossesse très précocement ; on peut la mettre en évidence par des tests spécifiques sur les urines ou le sang.
HT21
Il s'agit d'un test de dépistage de la trisomie 21, il s'adresse à toutes les femmes qui le désirent et qui n'ont pas encore l'âge requis pour une amniocentèse systématique. La positivité de ce test signifie que vous présentez un risque plus élevé d'avoir un enfant atteint par cette maladie et qu'une amniocentèse vous sera proposée.
Hydramnios
Excès anormal du volume de liquide amniotique défini en échographie par une citerne de liquide amniotique supérieure à 8 cm ou un index amniotique supérieur à 25 cm.
Hypotrophie
Anomalie de la trophicité.
Hydranencephalie
C'est une structure liquidienne anormale.
Le manteau cérébral est réduit à une fine membrane.
La faux du cerveau est réduite voire absente.
Kyste arachnoïdiens
Correspondant à une anomalie du développement de l'arachnoïde avec dédoublement de sa membrane.
LLC : Longueur Cranio-Caudale
lipome
Tumeur bénigne formée par des adipocytes.
Liquide amniotique
C'est le liquide qui entoure votre bébé, il est contenu dans le sac amniotique, le bébé le déglutit et l'inhale, il le rejette par ses urines un peu en " circuit fermé ". La perte du liquide amniotique traduit une rupture de la poche des eaux (ou sac amniotique).
Macrosomie
Il s'agit d'un bébé trop gros pour son âge de naissance, la macrosomie se définit par un percentile de naissance supérieur à 95, c'est à dire que 95% des bébés du même âge sont plus petits. Cette pathologie s'observe plus fréquemment en cas de diabète maternel mal équilibré, contrairement à ce que l'on pourrait penser elle est associée à une fragilité plus grande du bébé qui en est atteint.
Malformations d'Arnold-Chiari type II
Correspond à une ectopie de la partie inférieure du vermis, de la protubérance et du 4ème ventricule dans le trou occipital. La fosse postérieure est étroite; les hémisphères cérébelleux sont hypoplasiques; une dilatation ventriculaire est fréquemment associée.
Oligoamnios
Il s'agit d'une diminution pathologique de la quantité de liquide amniotique dont le diagnostic est échographique : plus large citerne de liquide amniotique inférieure à 2 cm ou index amniotique des 4 quadrants inférieur ou égal à 5 cm. Fréquence : de 0,5 à 1%.
Stéroïde cristallin fabriqué par les ovaires et possédant des propriétés oestrogènes.
Omphalocèle
Anomalies de l'intestin moyen : malformations liées à une fermeture incomplète de la paroi abdominale antérieure.
Purpura thrombopenique
Destruction plaquettaire périphérique de nature auto-immune par des anticorps antiplaquettes.
Présentation
Ce terme désigne la position
de votre bébé dans votre utérus, il s'agit de la partie
qu'il " présente " au médecin lors du toucher vaginal. Le
bébé peut être en présentation céphalique
c'est à dire tête en bas, dos à droite ou à
gauche, ou en présentation du siège
ou podalique. Dans d'autre cas la présentation est transverse
c'est à dire que le bébé est en travers dans votre
utérus.
RCIU
Le retard de croissance intra utérin (RCIU) concerne tous les bébés trop petits à la naissance, il est définit par un percentile de naissance inférieur à 10 ce qui veut dire que seulement 10% des bébés du même âge ont une taille inférieure.
SA : Semaine d'Aménorrhée
Par convention les médecins indiquent l'âge d'une grossesse en fonction du nombre de semaines écoulées depuis le premier jour des dernières règles ; mais il s'agit d'une convention ce qui veut dire que vous n'avez pas forcément saigné ce jour là.
Siège
Encore appelé présentation podalique, cela veut dire que votre bébé a la tête en haut et les fesses vers le bas ; il peut s'agir d'un siège complet si le bébé a les pieds en premier ou un siège décomplété s'il a les fesses en premier.
Spina Bifida
Défaut de fermeture osseuse.
Syndrome de Turner
Maladie génétique caractérisée par l'absence d'1 des 2 chromosomes dits sexuels. Il y a donc 45 chromosomes au lieu de 46.
Syndrome de Dandy Walker
Associe une dilatation kystique du 4ème ventricule à une agénésie ou une hypoplasie du vermis ; il peut coexister une agénésie du corps calleux et une hydrocéphalie d'importance variable.
Schizencephalie
Résulte d'un défaut de perfusion cérébrale à une période critique de la migration neuronale vers les 7 - 8e semaines.
Terme
Le terme de la grossesse représente la date prévue de l'accouchement pour une grossesse qui dure 9 mois (c'est à dire 280 jours ou encore 10 mois lunaires).
Trisomie 21
Il s'agit d'une anomalie des chromosomes se traduisant par un chromosome 21 supplémentaire. On l'appelle encore mongolisme ou syndrome de Down.
Trophoblaste
C'est la région de l'śuf où
se font les échanges entre la grossesse et l'utérus maternel,
au deuxième trimestre les échanges seront plus intimes avec
une pénétration plus forte dans l'utérus maternel,
il prendra le nom de placenta.
OUVRAGES
Guide de Surveillance de la Grossesse
Agence Nationale pour le Développement de l’Evaluation Médicale (ANDEM)
1996
Le développement du cerveau fśtal
ATLAS IRM et biométrie
C. Garel avec la collaboration de : G. Sebag, H. Brisse, M. Elmaleh, M. Hassan
Sauramps médical 2000
ARTICLES
Imagerie par résonance magnétique chez le fśtus
Apport au diagnostic anténatal
C. Garel, G. Sebag, H. Brisse, M. Elmaleh, J.F. Oury, M. Hassan
La Presse Médicale, 16 mars 1996 ; 25, n° 9
IRM encéphalique anténatale
Etude rétrospective à propos de 34 examens
F. Lair-Milan, A. Gelot, JM. Baron, F. Lewin, Ch. André et C. Adamsbaum
J Radiol 1997 ; 78 : 499-505
New Applications of MRI : Chest, Lung, and Bowel
MRI of the Fetus
(adapted from : Deborah Levine, Patrick D. Barnes, Robert R. Edelman, State of the Art : Obstetric MR Imaging, Radiology, in press, 1999)
http://bungie.bidmc.harvard.edu/redelman/fetal_mri.html
Malformations cérébrales et médullaires
Diagnostic anténatal
P. DROULLÉ (Nancy)
http://www.pediaweb.com/AFPA/dij1.htm
Quantitative analysis of the neonatal brain by ultrasound
B. Simaeys, W. Philips, I. Lemahieu, P. Govaert
Computerized Medical Imaging and Graphics 24 (2000) 11-18
Pratique de l'Imagerie fśtale
Enquête SFIP 1997 - Protocole d'examen IRM du fśtus (Thorax pour étude du volume pulmonaire) - Centres pratiquant l'IRM fśtale : contacts.
http://www.sfr-radiologie.asso.fr/soc_org/SFIP/IRMFOET.HTM
Aspect IRM anténatal et post-natal des malformations cérébrales
F. Brunelle
http://www.gyneweb.fr/sources/congres/jta/94/21.htm
Pathologie crânio-encéphalique
B. Maugey-Laulom, M. Brun, C. Soussotte, C.Garel, G. Sebag, P. Sonigo, F. Brunelle
IRM cérébrale fśtale : quand, comment, pourquoi ?
Actualités et potentialités
A. Couture, C. Veyrac, C. Baud, J.L. Ferran, P. Boulot, F. Deschamps
http://www.gyneweb.fr/sources/echographie/jpecho/97/irm.htm
IRM fśtale
Dr C. Durand
Colloque du mardi 15 juin 1999 ? Hôpital cantonal de Genève
Apport de l'IRM dans le diagnostic et le pronostic des malformations de la fosse postérieure
J. de La Veaucoupet
http://www.gyneweb.fr/sources/echographie/jpecho/97/fpirm.htm
Les anomalies de croissance précoces
Monique Kohler, Romain Favre
http://pro.gyneweb.fr/sources/echographie/collegeb/96/anomcr.html
Les anomalies de croissance fśtale
E.Cynober;R.Jeny
http://pro.gyneweb.fr/sources/echographie/collegeb/94/anomcro.html
Les retards de croissance intra-utérins
P. Andrini
http://www-sante.ujf-grenoble.fr/SANTE/TDMCorpus/Q222.html
L'analyse morphologique de l'embryon
Marianne Fontanges-Darriet
http://pro.gyneweb.fr/sources/echographie/collegeb/94/emb.html
Evolution des structures cérébrales au deuxième et troisième trimestre de la gestation
Catherine Lalondrelle
http://pro.gyneweb.fr/sources/echographie/collegeb/94/hoce~1.html
La croissance fśtale et le placenta les aspects normaux
Jean-Pierre Laulom
http://pro.gyneweb.fr/sources/echographie/collegeb/96/croissan.html
I.R.M. et tube digestif fśtal
A. Couture, C. Veyrac, C. Baud, M. Saguintaah
http://www.sfr-radiologie.asso.fr/soc_org/SFIP/EPUBRU00/coubru00.HTM
Imagerie par résonance magnétique de l'appareil urinaire fśtale
F Rypens, Th Metens, A Massez, S Ouertani, M Cassart, D Thomas, C Donner, F Avni
ULB, Bruxelles
http://www.sfr-radiologie.asso.fr/soc_org/SFIP/EPUBRU00/ry1bru00.HTM
IRM des dysraphismes lombaires fśtaux (à l'exclusion des myélo-méningocèles)
P. Sonigo
Hôpital Necker-Enfants Malades
http://www.sfr-radiologie.asso.fr/soc_org/SFIP/EPUBRU00/sonbru00.HTM
IRM thoracique fśtale
F Rypens, T Metens, M S Ouertani, C Donner, A Pardou, M Cassart, D Eurin, Y Robert,
Groupe pédiatrique de recherche en imagerie fśtale
http://www.sfr-radiologie.asso.fr/soc_org/SFIP/EPUBRU00/ry2bru00.HTM
SITES INTERNET
Site de gynécologie obstétrique.
http://www.sfr-radiologie.asso.fr/soc_org/SFIP/EPUBRU00/PRGBRU00.HTM
Site de la SFR (Société Française de radiologie).
http://www.med.univ-rennes1.fr/cerf/iconocerf/PE/index.html
Site de la Faculté de Médecine
de l’Université de Rennes 1.
ANNEXES
ANNEXE 1
1.1) Principes physiques
a) Les ultrasons (US)
Les ultrasons sont des vibrations mécaniques dont la fréquence est supérieure à celle des sons audibles par l’oreille humaine. Les fréquences utiles à l’imagerie ultrasonore médicale vont de 1 Mhz à 12 Mhz. La fréquence est le nombre d’oscillations par seconde exprimé en Hertz (Hz).
Les ultrasons sont des ondes de pression
qui se propagent de proche en proche dans un milieu matériel en
provoquant localement des variations de pression et des déplacements
infimes de matière autour de la position d’équilibre.
La vitesse de propagation de l’onde (ou célérité) est caractéristique du milieu de propagation. Dans les tissus mous les ultrasons se propagent sensiblement à la même vitesse (1 500 m/s). (ceau = 1 540 m/s, cgraisse = 1 450 m/s, cmuscle = 1 600 m/s). En revanche les vitesses de propagation de l’air ou de l’os sont très différentes (cair = 330 m/s, cos = 3 000 à 4 000 m/s).
La longueur d’onde qui représente l’étendue spatiale d’une oscillation est reliée à la fréquence par la relation ? = c/f.
L’interaction des ultrasons avec la matière induit deux principaux phénomènes physiques :
b) La réflexion
Lorsqu’une onde ultrasonore passe
d’un milieu à un autre, une partie de l’énergie incidente
est réfléchie.
Les conditions de la réflexion
à l’interface de deux milieux dépend de la différence
des impédances acoustiques de ces deux milieux. L’impédance
acoustique Z d’un tissu est définie par le produit de la densité
par la vitesse de propagation (Z = ?c). La proportion d’énergie
réfléchie à l’interface de deux milieux d’impédance
acoustiques Z1 et Z2 est donné par :
Par exemple, pour une interface graisse/muscle, 1,5 % seulement de l’énergie inscidente est réfléchie. Les échos sont cependant d’amplitude suffisante pour être détectés.
La plus grande partie de l’énergie est transmise à travers l’interface et peut explorer des structures plus profondes. En revanche l’air ou l’os, dont les impédances sont très différentes de celles des tissus mous, sont très fortement réfléchissants et représentent un obstacle à la propagation des ultrasons.
c) L’atténuation
L’énergie de l’onde est atténuée au cours de sa propagation dans les tissus. Les échos lointains sont donc beaucoup plus faibles. Par ailleurs, l’absorption croît avec la fréquence, c’est ce qui limite l’utilisation des appareils à haute résolution aux explorations superficielles.
Les mécanismes d’atténuation sont multiples. Ce sont les interactions au cours desquelles l’énergie est prélevée au faisceau incident pour être réemise dans les directions différentes (réflexion ou diffusion) ou absorbée par le tissu et transformée en chaleur (absorption).
L’intensité du faisceau ultrasonore s’exprime en W/cm2. Elle ne doit pas dépasser 100W/cm2. Elle se situe habituellement entre 10W/cm2 et 10mW/cm2, très en dessous du risque biologique. L’intensité ultrasonore décroît exponentiellement avec la profondeur z de pénétration dans les tissus et s’écrit :
Dans les tissus mous l’atténuation
augmente à la fois avec la fréquence et la profondeur de
pénétration. L’atténuation dépend de la nature
des tissus, mais en moyenne elle vaut environs 1 dB/cm/MHz dans les tissus
mous (de l’ordre de 0,3 à 1,5 dB/cm/MHz dans les conditions habituelles
du diagnostic médical). Par contre, l’atténuation est très
forte dans l’os : 10 dB/cm/MHz et dans le poumon : 20dB/cm/MHz.
1.2) Les différents modes d’échographie
L’utilisation des ultrasons en médecine est fondée sur la réception des échos ultrasonores renvoyés par les surfaces de discontinuité d’impédance situées dans les tissus. Il importe que l’impédance du matériau exploré ne soit ni trop faible (cas de l’air, donc des tissus pulmonaires ou de l’appareil digestif) ni trop élevée (cas des matières minérales dures, donc de l’os), et c’est pourquoi la technique d’échographie trouve sont principal champs d’application dans l’étude des tissus mous.
En effet si l’on émet une impulsion ultrasonore sur la peau, elle va se propager et donner des échos à chaque structure rencontrée. Mais ces échos ne retournent qu’une faible partie de l’énergie, le reste de l’onde poursuit l’exploration vers la profondeur des tissus. Le temps séparant l’émission de la réception d’un écho nous renseigne sur la profondeur de la structure qui lui a donné naissance.
a) Mode B temps réel
Lorsque l’on émet une impulsion ultrasonore, on reçoit en retour une succession d’échos décalés dans le temps, provenant des différentes structures anatomiques rencontrées.
Dans l’exploration dite en mode B, on représente ces échos sous forme de points brillants sur un écran de télévision, le long d’une ligne correspondant à la trajectoire explorée. Si l’on déplace suffisamment rapidement cette dernière, on crée sur l’écran une image de la coupe de tissu exploré dans le plan du balayage.
L’amplitude des échos reçus décroît avec la profondeur à cause des phénomènes d’atténuation. Ce phénomène est compensé par une amplification croissante avec le temps.
b) L’effet Doppler
Imaginons une source émettant une onde sonore tout en se déplaçant à la vitesse v. Un observateur O1 dont la source se rapproche voit une onde à fréquence plus élevée que l’observateur O2 qui s’en éloigne. Ce phénomène de décalage de la fréquence lié au mouvement s’appelle l’effet Doppler.
Si l’on éclaire des globules
rouges circulant dans un vaisseau avec un faisceau ultrasonore de fréquence
f0, le phénomène se produit deux fois : d’abord
lorsque l’hématie reçoit l’onde provenant de l’émetteur
puis à nouveau lorsqu’elle la retourne vers le récepteur.
La vitesse des hématies projetée
sur l’axe du vaisseau vaut VR = V.cos?. Le décalage de
fréquence Doppler fD vaut alors :
Il s’agit d’un signal dans la gamme des sons audibles que l’électronique de l’appareil Doppler nous permettra d’écouter. De plus, connaissant l’angle ?, on pourra calculer la vitesse moyenne du sang à partir de la fréquence moyenne du signal Doppler.
1.3) Emission-réception
a) La sonde ou transducteur
La sonde est un convertisseur d’énergie transformant l’énergie électrique en énergie mécanique et inversement. Son fonctionnement fait appel à la piézo-électricité.
Si l’on applique une différence de potentiel sur les bords du cristal : une distorsion mécanique est observée (augmentation ou diminution de l’épaisseur du cristal).
Si la différence de potentiel
est alternative, le cristal oscille produisant des trains d’ondes ultrasonores.
Il existe deux types de fonctionnement de la sonde :
Le mode continu : une différence de potentiel est appliquée à un cristal de façon continue. Un second cristal est utilisé en réception.
Le mode pulsé : une différence de potentiel est appliquée en de brèves séquences (pulses). On peut alors utiliser un élément en émetteur et récepteur.
b) Les différents modes de balayage
Le balayage mécanique sectoriel. Le ou les transducteurs focalisés sont montés sur une partie mobile, tournante ou oscillante à l’intérieur de la sonde. Le champ exploré est de type sectoriel. D’autres constructeurs préfèrent utiliser un transducteur fixe dont le faisceau est dévié par un miroir mobile.
Le balayage linéaire électronique. La sonde est constituée d’une barrette de transducteurs. La zone active est déplacée ligne après ligne le long de cette barrette grâce à des commutations électroniques. La zone explorée est de forme rectangulaire. D’autre part la focalisation du faisceau n’est plus assurée par une lentille, mais au niveau de l’électronique. Si on retarde convenablement les impulsions des bords de l’ouverture, on peut générer un front d’onde de type cylindrique et donc convergent.
Le balayage sectoriel électronique. On utilise dans ce cas tous les éléments d’une petite barrette de transducteurs. Ceux-ci sont excités avec un décalage temporel linéaire qui crée un front d’onde défléchi à volonté. La propagation se fait dans une direction perpendiculaire au front d’onde et le champ exploré est un secteur.
La résolution axiale, dans l’axe du faisceau, est liée à la durée des échos obtenus. Elle vaut environ une à deux longueur d’onde : moins de 0,4 mm à 5 MHz par exemple.
La résolution latérale
dépend du degré de focalisation du faisceau, mais n’est bonne
qu’au voisinage du point focal. C’est pourquoi, on fait varier électroniquement
la position du point focal en cours de réception pour faire en quelque
sorte un zoom sur les échos. C’est ce qu’on appelle la focalisation
dynamique ou en poursuite d’échos. Deux à quatre longueurs
d’onde sont des qualités de résolution couramment rencontrées.
ANNEXE 2
2) Rappels d’IRM
2.2) Vecteur champ magnétique
2.3) Temps de relaxation
b) Relaxation T2
2.5).La concentration en hydrogène : la densité de protons
2.6) Rapport signal
sur bruit
2.1) Spin de particules élémentaires
Les particules élémentaires sont caractérisées par des grandeurs scalaires telles que la masse, la charges et des grandeurs vectorielles telles que le moment cinétiques intrinsèques ou spin et moment magnétique (MM). Le moment magnétique d’une particule est proportionnel à son moment cinétique :
MM = g (moment cinétique intrinsèque)
Où g est appelé rapport gyromagnétique.
L rapport g , caractéristique de la particule peut être positif ou négatif. Lorsque le spin d’une particule élémentaire est nul, son moment magnétique l’est aussi. La valeur du spin, comme celle de toutes les grandeurs qui caractérisent les particules élémentaires est une donnée expérimentale : elle est déterminée par le comportement des particules dans un champs magnétique.
2.2) Vecteur champ magnétique
Les propriétés d’un champ magnétique sont quantifiées en introduisant, en chaque point de l’espace. Si le champ est uniforme et constant dans le temps, le vecteur champ magnétique est un vecteur constant noté B0 (s’exprime en teslas ou en gauss [1T=10-4G]).
Description quantique
Si une particule est placée
dans un champ B0, la projection de son moment magnétique
sur un axe z, parallèle à B0, ne peut obtenir
que certaines valeurs discrètes.
Pour les particules comme le proton, le neutron ou l’électron, l’expérience montre que ces valeurs se réduisent à deux, un état « up » (+g h/2) et un état « down » (-g h/2, h = constant de Planck).
Fréquence de Larmor
Le moment magnétique d’une particule est soumis à un couple de forces, dont le moment mécaniques est proportionnel à la valeur du vecteur champ magnétique et à celle du moment magnétique concerné. Sous l’action de ce couple, le moment magnétique intrinsèque du proton, placé dans B0, présente un mouvement de rotation appelé précession.
Fig. 3.2.1 Précession d’un moment protonique m placé dans un champ magnétique uniforme B0.
Dans ce mouvement, le moment magnétique de la particule balaye un cône dont l’axe est parallèle au vecteur de champ magnétique B0, et son extrémité uniformément un cercle avec une fréquence caractéristique, appelé fréquence de Larmor (fig. x). L’angle que fait le moment m avec l’axe du cône reste constant au cours du mouvement mais peut avoir une valeur quelconque (comprise entre 0 et p ).
La fréquence de précession, f0, vérifie la relation fondamentale dite de Larmor :
f0 = (g /2p )B0
où g est le rapport gyromagnétique de la particule et B0 la valeur du vecteur champ magnétique.
Fréquence de Larmor du proton
La fréquence de Larmor f0
du moment protonique se déduit de la relation de Larmor. Pour une
valeur de B0 égale à 1 T, elle vaut 42.577 MHz.
Cette valeur de 42.6 MHz est importante à mémoriser, puisqu’elle
permet de connaître la valeur de la fréquence de Larmor du
proton pour toute valeur de B0. Il suffit de multiplier la valeur
de B0 par le facteur « 42.6 » (tableau 1.1)
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Tableau 3.1 Fréquence de précession et vitesse angulaire du moment protonique en fonction de B0.
2.3) Temps de relaxation
a) Relaxation T1
La transition de l’état «
down » à « up » s’accompagne d’un transfert d’énergie
à l’environnement du proton. De façon macroscopique, la relaxation
T1 est caractérisée par le retour de la magnétisation
longitudinale vers son état fondamental avec un vecteur de champ
magnétique maximum. La relaxation T1 qui implique un
transfert d’énergie des protons à leurs environnement est
aussi appelé relaxation spin-réseau (ou spin-lattice). Son
retour à l’état fondamental suit une fonction exponentielle
suivante :
Le temps T1 est le temps pour que la magnétisation retourne à 63% de sa valeur originale. Après 2*T1, la magnétisation est à 86% de sa valeur originale. Les spins sont complètement relaxés après 3-5 T1. La relaxation T1 est la plus rapide quand le mouvement du noyau (rotation & translation) correspond à la fréquence de Larmor. Par conséquent, La relaxation T1 est dépendante de la dureté du champ magnétique donc de la fréquence de Larmor. Des champs magnétiques intenses sont associés avec des périodes T1 longues.
b) Relaxation T2
La période T2 ou relaxation spin-spin arrive quand les spins dans les états d’énergie haut et bas échangent leurs énergies mais ne perdent pas d’énergie vers l’environnement. Cela résulte de façon macroscopique, à une perte de la magnétisation transverse. Dans l’eau pure, T1 et T2
Sont identique, 2-3 secondes. Dans
les matières biologiques, T2 est considérablement
plus petit que T1. Pour la matière blanche du cerveau
T1 = 0.5s & T2
= 0.07s. La relaxation à
la même représentation exponentielle que T1 avec
63% de la magnétisation transverse à 1* T2 .
2.4) Gradient de champ magnétique
Pour produire un champ magnétique,
on superpose au champ magnétique B0 un vecteur
champ magnétique b, parallèle à B0. La
valeur de ce champ b est de l’ordre de quelque millitesla, donc bien inférieur
à B0. Les variations de b sont produites selon les trois
axes x, y et z.
Fig.3.4.1 Exemple de gradient pouvant être généré en IRM. Gradient cranio-caudal selon l’axe z. Le valeur champ magnétique est égale à la variation de b par unité de longueur selon l’axe Z
Les gradients sont crées par des enroulements de fils conducteurs (bobines de gradients) parcourus par des courants électriques. Les bobines de gradients (trois assemblages d’architecture particulière de bobines destinées à créer des gradients selon les axes x, y, z de l’aimant). Le gradient selon l’axe z est crée à l’aide de deux bobines circulaires identiques dont l’axe z est confondue avec l’axe de symétrie de l’aimant.
La technologie pour créer
des gradients sur l’axe x et y est différent. Les gradients sont
crée par quatre bobines en formes de selles, orientées selon
l’axe z et disposées dans les parties droite et gauche de l’aimant.
Le gradient x permet d’effectuer des coupes sagittales, le gradient y des
coupes frontales et le gradient z des coupes axiales.
Coupes en IRM
Les coupes sont réaliser grâce
à l’application d’une impulsion de champ magnétique tournant
B0, de fréquence f0 et de largeur d f. Le
phénomène de résonance n’agit efficacement que sur
Fig. 1.1 Sélection d’une tranche d’épaisseur d z et de cote z
les moments protoniques dont les fréquences de précession sont situés dans une bande de fréquence de largeur d f, centrée sur f0.
2.5) La concentration en hydrogène : la densité des protons
Il est clair que s’il n’y a pas de d’hydrogène, c’est-à-dire pas de protons, il n’y a pas de signal (du moins lorsqu’on fait de l’imagerie du proton). C’est ce que l’on constate dans l’air et dans l’os où la concentration est très faible. Donc tous les organes contenant de l’air (poumons, sinus, trachée, pharyngo-larynx, tube digestif) ne donnent pas de signal de même que la corticale osseuse et les calcifications.
Dans les tissus du corps humain, la concentration en hydrogène ne varie que de 20% environ, alors que les différences de T1 et T2 peuvent varier de 500%.
EN pratique, la concentration en hydrogène est donc un élément peu important dans le contraste de l’image par rapport à T1 et T2. Cependant certaines valeurs de TR et TE qui diminuent l’influence de T1 et T2 peuvent faire apparaître davantage la concentration en hydrogène.
C’est le cas pour un TR long (1,5 sec) et un temps d’écho court (30 msec). Ces images sont en général peu contrastées et sont appelées images en densité de proton.
2.6) Rapport signal sur bruit
Sur une image de résonance magnétique, le bruit est constitué par des signaux parasites réceptionnés et qui non seulement ne contribuent pas à l’image, mais la dégradent.
Le rapport signal sur bruit exprime
l’importance relative des deux paramètres. Il est évident
que l’on doit essayer d’avoir le rapport le plus élevé possible.
On peut le faire, soit en augmentant le signal, soit en diminuant le bruit.