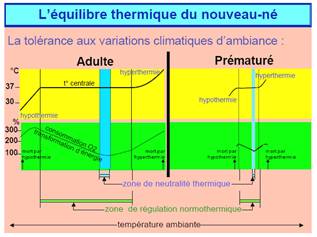
Fig.1 : Un équilibre
thermique
fragile. La
neutralité thermique (zone de températures pour laquelle
l’individu n’a
pas à
fournir d’effort pour maintenir sa température) à
équilibre est bien
plus
délicate chez le nourrisson. De même, la zone de
normothermie (zone de
températures dans laquelle l’individu arrive à maintenir
sa
température) est
bien plus étroite chez le bébé.
-source : Cours Master MTS, Draeger-
Il faut 3 jours pour
qu’un bébé atteigne un équilibre thermique.
Au-delà
de ce délai, il est pratiquement inutile de surveiller la
température.
La naissance
représente
un choc thermique important. Le premier geste
est alors de le mettre sous une lampe chauffante pour éviter un
trop
rapide
refroidissement. Par contre, on oublie trop souvent le geste le plus
urgent, à
savoir de le sécher.
I-1-b-
Comment le nouveau-né se
refroidit-il ?
A la naissance, il arrive
dans un univers radicalement différent :
non seulement il fait brutalement froid de 10 à 15°C, mais,
de plus, l’eau a disparu et la peau est en
contact
avec de l’air, ce qui augmente considérablement tous les
échanges :
thermiques et hydriques.
La
perte de chaleur va se situer
à ces deux niveaux : échanges thermiques
aériens directs et
pertes
d’eau réchauffée à 37°.
Deux organes
entraînent
principalement ces pertes:
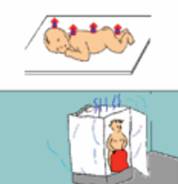
Fig.2 : Pertes hydriques
et
calorifiques par évaporation et par respiration
-source : Master
MTS, Draeger-
La peau est une large surface
exposée brutalement au froid et au
sec. Chez le nouveau-né, elle est très fine et
perméable. C’est pourquoi la
température descend vite. Le temps nécessaire aux
premiers soins et à
l’habillage suffit pour mettre le bébé en
déséquilibre grave, même si ces
gestes sont effectués sous rampes chauffantes. En effet, en
chauffant, les
rampes déshydratent le nourrisson.
La respiration participe
aussi à la perte de chaleur et d’eau. L’air qui entre froid et
plus ou moins sec
dans les narines ressort chaud et humide. Le nouveau-né perd
ainsi beaucoup
d’eau et de chaleur : d’autant plus que l’air inspiré est
plus sec et plus
froid.
I-2-
Une assistance technique : les incubateurs
Deux
solutions techniques sont proposées :
- la rampe chauffante.
Elle ne chauffe que par-dessus le nouveau-né,
par rayonnement. Les pertes hydriques et calorifiques sont maximales.
En
revanche, ils permettent au personnel soignant des manipulations
délicates
qu’un incubateur fermé ne permettrait pas de réaliser.

- l’incubateur
fermé est
un espace clos. La température est plus
facilement contrôlable, tout comme le contrôle de
l’humidité de l’air.
L’inconvénient majeur est le manque d’accessibilité du
personnel pour
effectuer
des gestes techniques.
En revanche, si ces deux
techniques ne sont pas aussi performantes que
le bain utérin ou le contact direct avec la maman, elles n’en
sont pas
moins un
bon ersatz. Elles permettent au nourrisson de faire la transition entre
son
ancien milieu aquatique et le monde des hommes terrestres.
II-
Principes de fonctionnement des incubateurs
II-1-
les
échanges thermiques possibles
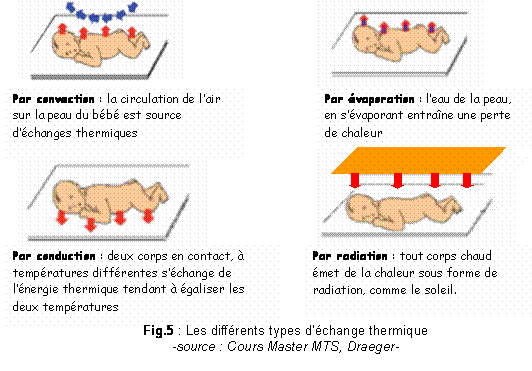
Avant de commencer
à
décrire le fonctionnement des incubateurs, il est
intéressant de
schématiser les différents types d’échanges
thermiques que les incubateurs auront à maîtriser afin de
maintenir le
nouveau-né à bonne température.
Comme cela a
été introduit dans la partie précédente, il
existe sur le
marché deux types d’incubateurs :
ü
Les incubateurs
fermés ou couveuses
ü
Les incubateurs ouverts
ou radiants
En ce qui concerne les
incubateurs fermés, les incubateurs de transport se
distinguent des incubateurs fixes. Bien que leur principe de
fonctionnement
soit identique, leur fonctionnalité différente implique
quelques particularités
(autonomie électrique, seuils d’acceptabilité des
paramètres sonores,
température ou humidité).
II-2-
Principe de fonctionnement des incubateurs ouverts
Le principe de
fonctionnement est très simple, il utilise le chauffage
par radiation et par conduction.
- Pour le chauffage par
radiation, une lampe chauffante est placée au-dessus du
nourrisson, sur une rampe à hauteur variable. Plus la lampe est
haute, moins elle chauffe le nouveau-né. Il est également
possible de régler l’intensité de radiation de la lampe.
- Pour le chauffage par
conduction, le matelas sur lequel repose bébé est en
gel à forte capacité thermique. Il est chauffé par
une résistance interne. Tous les fabricants ne complètent
pas le chauffage par radiation par le chauffage par conduction.

Les avantages que propose
ce type d’incubateur sont les suivants :
- Accessibilité
optimale pour les soins techniques,
- Possibilité de
fixer des planches radiologiques ainsi que des systèmes de
photothérapie,
- Facilité
d’entretien.
Mais ce type de
dispositif présente également deux inconvénients
majeurs :
- il n’y a pas
d’humidificateur,
- le chauffage est
peu homogène.
II-3-
Principe de fonctionnement des incubateurs fermés
Le nourrisson est
placé sous une cloche en plastique transparent. Le
chauffage utilisé est un chauffage par convection :
un ventilateur
chauffant brasse de l’air qui circule dans la cloche.
L’air
est humidifié par un humidificateur qui
diffuse soit des particules d’eau prises par le flux d’air chaud, soit
de la
vapeur d’eau. L’humidificateur pose souvent des problèmes de
développement
bactériologique. En effet, l’eau et la chaleur peuvent
être d’excellents nids
bactériologiques.
Les incubateurs
fermés présentent les avantages suivants :
- le
chauffage est homogène dans l’ensemble de l’habitacle,
-
le taux d’humidification est contrôlé car l’espace de
l’habitacle est clos.
Mais ils regroupent
quelques
inconvénients :
- la difficulté
d’accès au nouveau-né pour les soins techniques,
- l’entretien
difficile de l’incubateur pour les opérations de nettoyage
quotidien.
III-
Dispositifs existants sur le marché
III-1-
Les incubateurs ouverts
Bien que le
réchauffement proprement dit soit moins efficace que pour
les incubateurs fermés, l’avantage principal de ce type de
dispositif est
l’accessibilité au bébé. Il est ainsi envisageable
d’opérer le nourrisson avec
beaucoup d’aisance tout en le maintenant à bonne
température. Outre l’aspect chirurgical,
on ne peut pas oublier que ce système peut être facilement
adapté au dessus
d’un fauteuil permettant à la mère de prendre son enfant
dans les bras, de le
caresser et de lui donner toute l’affection dont il a besoin, en
limitant les
risques de perte de chaleur.
Les trois principales
marques que l’ont trouve sur le marché sont
Draeger, Air-Shields et Médipréma. Seront
présentés les
modèles les plus récents de chaque compagnie.
III-1-a-
Draeger et son Babytherm 8010
Grâce à un
système de pivotement autofocus, la rampe chauffante est
toujours dirigée vers le patient quelque soit sa position.
Le refroidissement du
nourrisson pendant les procédures de radiologie est
terminé. Par ailleurs, ce
dispositif propose une répartition de chaleur homogène
sur la surface du lit.
Par la combinaison des
apports de chaleur par conduction du matelas gel
chauffant et par radiation de la lampe, ce dispositif crée un
climat favorable
minimisant les pertes d’eau dues au chauffage radiant. Ainsi, pour un
même réchauffement,
la puissance de la lampe est réduite de 30%. Le
réchauffement est donc moins
agressif.
III-1-b-
L’incubateur ouvert REF. 4045 de Medipréma
Lorsqu’un
bébé rentre en phase d’hypothermie, une de ses
premières réactions physiologiques
au « stress thermique » est la vasoconstriction,
dans le but de
réduire les pertes de chaleur périphériques
La combinaison d’une
température cutanée et centrale classique et d’une
température cutanée périphérique (sur les
pieds par exemple), donne les signes
précoces d’un état de stress thermique, ce qui permet de
détecter plus tôt un
début de stress thermique. C’est ce qui s’appelle le
thermomonitoring.
III-1-c-
Comparaison des spécifications techniques
Elle concerne les aspects
techniques des marques Draeger et Air-Shields
(rachetée en juillet 2004 par Draeger)
|
Modèle
|
Babytherm 8010
|
Air-shields RW 82
|
|
Hauteur du plan de travail
|
910-1200 mm
|
950-1140 mm
|
|
Proclive/déclive
|
+20°-(-15°)
|
+10°-(-10°)
|
|
Puissance absorbée
|
630-1260 W
|
750 W
|
|
Précision de la
chaîne complète de mesure
|
+/- 0.2°C
|
+/- 0.2°C
|
|
Caractéristiques
de chauffe
|
·
Intensité de
réchauffement entre le lit et la lampe :
Niveau 3 : 10 mW/cm²
Niveau 10 : 32 mW/cm²
·
Plage de réglage
du matelas chauffant :
30°C-38.5°C (précision +/- 0.5°C)
|
·
Pas de matelas chauffant
·
Mesure de la
température cutanée entre 18°C et 43°C
·
Indicateur de puissance
de 0% à 100%
|
III-2-
Les incubateurs fermés

L’observation de la vie
quotidienne des services a permis de pouvoir
définir des innovations qui répondent mieux aux besoins
du personnel. Quelque
soit le fabriquant, les points cruciaux du développement des
innovations sont
les suivants :
Accessibilité
Facilité
d’utilisation
Soin de
développement
Modularité
III-2-a-
Le Caléo de Draeger

Les grandes portes avant
et arrière,
les trappes tête et pieds ou le couvercle escamotable
offrent un accès
encore plus important. Le passage des multiples tuyaux, sondes, fils ou
autres
câbles est grandement facilité grâce aux dix larges
passants amovibles.
III-2-b-
Le Satis de Medipréma
Autrement appelés
« dévelopmental
care », les soins de développement sont une pratique
en pleine expansion
destinée à optimiser l’environnement du nouveau-né
ainsi que les relations avec
son entourage.
Les mouvements de hauteur
et de proclive/déclive se font
sans bruit ni vibration.
L’utilisation du tiroir
à cassette radio, des portes et
hublots, balance intégrée ou du tiroir de rangement ne
génère aucun stimulus négatif.

Une différence
majeure avec le Caléo de Draeger est la
technique utilisée pour humidifier l’habitacle. Draeger envoie
de la vapeur
d’eau dans l’habitacle, tandis que Medipréma envoie des
particules d’eau liquide
en suspension. Un piézoélectrique, en vibrant fournit ces
gouttelettes d’eau.
En outre, une lampe fournit un rayonnement UV qui détruit les
bactéries,
évitant les risques infectieux.
Pour la prise en charge
des grands prématurés, le réglage
électrique de
la proclive/déclive et de la hauteur est très
appréciable car il est très doux
et silencieux. Le Caléo propose également un tiroir
à cassette radio intégré,
utilisable sans l’ouverture de l’habitacle pour préserver la
tranquillité du nouveau-né.
Dans le même esprit, la balance intégrée permet une
pesée sans la sortie de
l’habitacle.
III-3-
Les incubateurs de transport
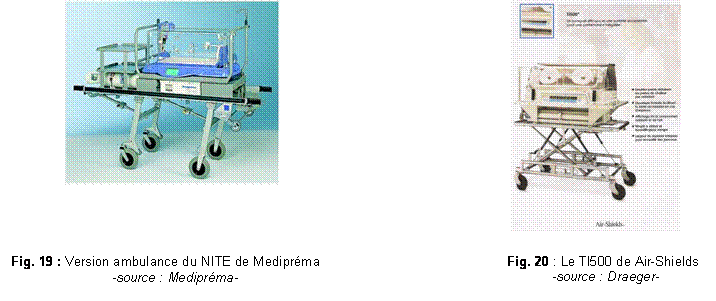
Globalement, les
objectifs
recherchés sont les mêmes que pour les incubateurs
fermés, ainsi que les
principes de fonctionnement. La différence est uniquement sur le
mode
d’utilisation de ce dispositif : le transport du nourrisson. Les
paramètres vont être plus souples, l’ergonomie sera plus
commode et l’autonomie
plus grande.
IV) Le Koala et
l’assurance qualité des
incubateurs
IV-1- Présentation
Le Koala est un testeur
d’incubateur original, conçu par la société
Gamida en réponse au besoin des équipes
biomédicales. Son originalité
consiste
dans l’intégration, dans un seul équipement, de tous les
capteurs
nécessaires à
l’acquisition des paramètres fonctionnels de l’incubateur,
à
savoir :
Température de
l’incubateur
Niveau de pression
acoustique
Humidité relative
Vitesse de l’air dans
l’enceinte
IV-2- Les
paramètres à
contrôler
La
température de l’incubateur
La température
doit
être proche de celle fixée
par
l’utilisateur, avec une tolérance maximale de dérivation.
La température de l’air trop élevée
entraîne
un gonflement dans la gorge, donc une gêne respiratoire. Il est
également
possible de contrôler la température du matelas chauffant.
L’hygrométrie
L’humidité
relative
participe aux soins du système respiratoire du nouveau-né
et influe sur
les
échanges calorifiques, les pertes étant majorées
quand l’humidité
relative
diminue.
Le
niveau sonore
L’exposition continue
à des niveaux de bruit élevé peut provoquer une
perte auditive et
provoquer un
stress prolongeant le séjour en couveuse.
Une valeur seuil
reposant sur l’opinion de l’expert a été retenue.
La
vitesse de l’air
Une vitesse maximale
doit être imposée face au stress et au risque de
déshydratation du
nouveau-né par
évaporation. De plus,
les régimes de circulation
d’air influence l’équilibre calorifique du patient et les seuils
de
régulation
thermique de l’incubateur.
IV-3- Quelles normes pour
quels incubateurs ?
L’assurance
qualité des
incubateurs repose aujourd’hui sur leur
conformité par rapport à 3 normes principales :
la norme EN
60 601-2-19 est applicable aux incubateurs
fermés
la norme EN
60 601-2-20 précise les règles de
sécurité des
incubateurs de transport,
la norme
EN 60 601-2-21
concerne les incubateurs ouverts qui utilisent des radiateurs par
rayonnement.
|
|
Incubateur fixe
|
Incubateur de transport
|
|
|
normes 601-2-19 et
601-2-21
|
normes 601-2-20
|
|
T° convection (°C)
|
+/- 1.5 (1)
|
+/- 2.0 (1)
|
|
T° radiation (°C)
|
+/- 0.5 (1)
|
(-)
|
|
Hygrométrie (% HR)
|
+/- 10 (2)
|
+/-5 (2)
|
|
Vélocité de
l'air (m/s)
|
0.35 (2)
|
0.35 (2)
|
|
Niveau sonore (dBA)
|
60 (3)
|
60 (3)
|
|
|
|
|
|
(1) : tolérance par
rapport à la température de consigne
|
|
(2) : seuil maximum
admissible
|
|
|
(3) : seuil maximum
admissible hors alarme
|
|
|
|
|
|
|
Fig.22 : Principales
prescriptions des normes applicables en matière d'incubateurs
|
IV-4- Un instrument de
l’assurance qualité
Le Koala a
été pensé et
réalisé comme un véritable outil
d’assurance qualité en matière d’incubateur :
la visualisation des
résultats en
mode graphique ou numérique, facilite l’interprétation
des mesures et
leur
rapprochement des seuils de la norme et des données «
constructeur
» ;
l’enregistrement
numérique améliore
la traçabilité, l’archivage, et donc la démarche
médicolégale ;
il offre une autonomie
électrique de
24 h.
PARTIE II : Assistance respiratoire
I- Aspects pathologiques
La détresse
respiratoire du nouveau-né est la pathologie la plus
fréquente de la période néonatale, facteur de
mortalité et de
morbidité. Elle est due à
des difficultés
d'adaptation à la vie
aérienne en rapport avec une immaturité (maladie des
membranes
hyalines,
détresse respiratoire transitoire) ou une malformation (hernie
diaphragmatique
congénitale...).
La
détresse
respiratoire du nouveau-né survient avant l'âge
de 28 jours et constitue une urgence vitale. Le risque majeur des
détresses
respiratoires néonatales est l'hypoxémie [Cf
glossaire] pouvant
entraîner
des séquelles neurologiques définitives. Cela souligne
l'importance
considérable du dépistage et du traitement précoce
de ces détresses
respiratoires.
Les trois
affections respiratoires qui dominent les causes de
détresse
respiratoire
chez le nouveau-né sont brièvement décrites
ci-après.
I-1- La maladie des
membranes hyalines
Cette maladie arrive au
premier rang des problèmes
respiratoires du prématuré. Elle est provoquée par
l'absence ou
l’insuffisance
de surfactant. Le surfactant [Cf glossaire] est une
substance
fabriquée par les poumons du fœtus pendant le dernier trimestre
de la
grossesse
et qui aide les poumons à rester gonflés à chaque
nouvelle inspiration.
Autrement dit, le rôle du surfactant est d’empêcher les
alvéoles de
s’aplatir
lors de l'expiration. L'insuffisance de ce produit peut être due
à
l'immaturité
enzymatique des cellules alvéolaires chez un
prématuré. En effet, cette
maladie
atteint presque exclusivement les nouveaux-nés arrivés
avant terme.
C’est très vite
après la
naissance, quelques minutes le plus souvent,
quelques heures parfois, que des symptômes inquiétants
vont alarmer les
médecins : l'enfant geint et présente une
polypnée [Cf
glossaire], un battement des ailes du nez et une cyanose [Cf
glossaire] en cas d'oxygénation insuffisante.
I-2-
Détresse
respiratoire transitoire (DRT)
Elle est due à un
trouble
de la résorption du liquide
pulmonaire foetal qui doit normalement se faire très vite
à la
naissance dans
le cadre de l'adaptation
respiratoire à la vie aérienne. Ce retard de
résorption est
très
fréquent dans le contexte de la césarienne, mais est le
plus souvent
pas ou peu
symptomatique. Sauf exception, l'évolution est typiquement
rapidement
bénigne
sous oxygénothérapie simple.
I-3- Inhalation méconiale
Elle est moins
fréquente aujourd'hui du fait de
l'amélioration du diagnostic et de la prévention de
l'asphyxie
périnatale.
La détresse
respiratoire
est une maladie des poumons
empêchant le sang de s’oxygéner. Il faut alors aider le
nouveau-né par
un
traitement d’oxygène et une assistance respiratoire.
Ainsi, le but
du traitement de cette maladie est de
maintenir un taux d’oxygène dans le sang (PaO2)
normal. L’oxygénation
se fait soit :
sous enceinte
céphalique
(hood)
avec un apport d’oxygène
réchauffé,humidifié
en surveillant en permanence la FiO2 [Cf
glossaire],
soit avec une ventilation
pharyngée
et une pression de distension alvéolaire (C.P.A.P. =
Continuous
Positive
Airway Pressure),
soit en ventilation
assistée
conventionnelle ou par oscillations à haute
fréquence selon
les
indications.
II- Principes de
fonctionnement des dispositifs médicaux
II-1- Traitement des
détresses
respiratoires du nouveau-né
Il y a dans l'air ambiant
qu'on inspire une concentration en
oxygène (FiO2) de 21% qui suffit à
l'oxygénation correcte
des
individus normaux. En cas de pathologie pulmonaire, la FiO2
doit
être supérieure pour assurer un taux d'oxygène
suffisant dans le sang
(PaO2
[Cf glossaire]).
Afin de faire respirer
une atmosphère plus riche en oxygène au
nouveau-né placé en incubateur, les pédiatres
utilisent une petite
enceinte en
matière plastique qui recouvre uniquement la tête de
l'enfant, appelée enceinte
de Hood.
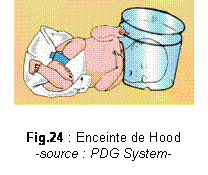
Ils calculent un
mélange d'air et d'oxygène qui parvient dans le Hood
grâce à un tuyau.
Un
oxymètre (analyseur d’oxygène) contrôle la FiO2,
obtenue
dans
l'enceinte et qui doit osciller entre 25 et 45%. Ils surveillent
également les
gaz du sang afin de s'assurer que cette FiO2 permet de
créer
une PaO2
et une PaCO2 correctes.
Remarque : Si la PaO2
est insuffisante, il faut
augmenter la FiO2 au-delà de 50%. Dans ce cas, le
Hood ne
suffit
pas, et il est alors nécessaire d'intuber l'enfant
(placer un
tube dans
la trachée) et d'assurer une ventilation artificielle
à l'aide
d'un
respirateur mécanique. Cette réanimation permet la survie
de nombreux
nouveau-nés qui seraient morts de détresse respiratoire
si elle n'avait
pas été
entreprise. Toutefois, cette survie se fait parfois au prix d'une
maladie
respiratoire nouvelle : la dysplasie broncho-pulmonaire ou "maladie des
ventilés", dans laquelle la ventilation artificielle et
l'oxygénation
longtemps maintenue (plus d'une semaine) jouent un rôle
fondamental.
II-2-
Oxygénothérapie
sous Hood
L’oxygénothérapie consiste à
administrer
de l’oxygène au nouveau-né
pour oxygéner son sang. On peut faire respirer à l’enfant
un air riche
en
oxygène en plaçant sa tête sous une cloche en
plastique appelée appareil
de
Hood. Ce moyen est utilisé dans le traitement des
hypoxémies pour
les
nouveau-nés et les nourrissons (souvent < 6 mois).
Le but de l‘oxygénothérapie
sous Hood est
d’obtenir une PaO2 entre 8 et 10 KPa chez le
nouveau-né ou
une SPO2
[Cf glossaire] comprise entre 92 et 95 %.
En néonatalogie,
c’est
le hood dit classique qui est utilisé : la ventilation est
assurée
par le
seul débit fourni par les fluides muraux. L’autre type
d’enceintes, le
hood dit
à ailettes, comprend un ventilateur effectuant un mélange
avec l’air
ambiant ; c’est un dispositif plus simple mais utilisable chez de
plus
grands enfants, l’enceinte étant plus grande.
Quelle que soit
l’installation et la technique, l’utilisation d’un oxymètre est obligatoire
et son alarme est réglée à plus ou moins 5% de la
FiO2 prescrite
(l’oxygène est toxique à forte
dose).
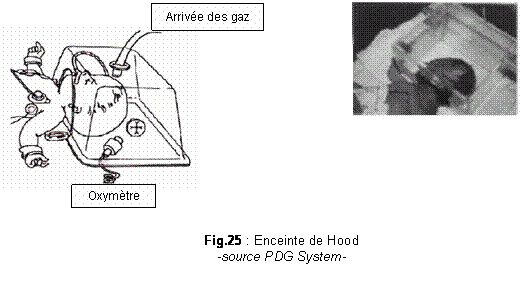
L’enfant est
installé
sur le dos (sur le ventre sur prescription médicale), avec un
petit
billot sous
les épaules pour lui mettre la tête en
légère extension. Pour libérer
les voies
aériennes, un dispositif d’aspiration est mis en place par le
nez et la
bouche.
II-3-
Ventilateurs
II-3-a- Généralités
La ventilation
" naturelle " ou
" spontanée " assure au niveau des poumons, le
renouvellement des gaz contenus dans les alvéoles pulmonaires.
Dans ce
cas, la
" force motrice " est naturellement produite par les
muscles respiratoires.
Avec la ventilation
" artificielle ",
c’est le respirateur qui crée la pression nécessaire et
qui permet de
régler le
taux d’oxygène dans les poumons et d’éliminer le gaz
carbonique (CO2).
Dans ce cas, la " force motrice " est artificiellement
produite par une machine : le respirateur ou ventilateur. En imposant
lors de
la phase inspiratoire une pression positive au sein des voies
respiratoires le
respirateur prend le relais des muscles respiratoires et du diaphragme,
ce qui
permet une diminution de la consommation de l’O2 par ces
muscles mis
au repos.
Il existe 2 types de
respirateurs.
Les respirateurs dits
" volumétriques "
C’est
en réglant le volume courant [Cf glossaire]
et
la fréquence que l’on obtient la ventilation par minute
prescrite par
le
médecin. La pression dépend de ces réglages et
s'adapte aux résistances
bronchiques du patient. En revanche, en cas de fuites, la pression
nécessaire
pour délivrer le volume déterminé peut ne pas
être atteinte, et le
volume
risque de baisser (des alarmes basses pressions sont prévues
à cet
effet).
Les respirateurs non
volumétriques : " barométriques " ou Aide
Inspiratoire
Ces
machines sont d’un type nouveau. On règle seulement la pression
dans les voies respiratoires pendant l’inspiration. C’est le patient
qui
déclenche le début et la fin de l’inspiration et qui
détermine la
fréquence.
Ces
respirateurs semblent donc à priori plus confortables pour les
patients mais la fiabilité de la ventilation est peut être
moins
garantie
qu’avec les machines volumétriques. De plus, ce type d’appareil
ne
permet pas
automatiquement l’adaptation de la pression, si les résistances
du
malade
augmentent ; on ne peut donc pas toujours être assuré
de la
délivrance du
volume courant.
En
néonatalogie :
Le ventilateur
de néonatalogie fonctionne sur le même
principe que les respirateurs de réanimation pour adultes. La
principale
différence est l'utilisation d'un circuit patient avec des
tuyaux de
diamètre
moindre associés à des plages de réglages
adaptées à la ventilation du
nourrisson : petits volumes courants (5mL contre 500 mL chez un
adulte), plage
de fréquences plus élevées.
En effet, la compliance [Cf
glossaire] de la cage thoracique d’un
nouveau-né ou d’un nourrisson est très
élevée, donc très souple, et
ceci
n'autorise qu'un volume courant très petit et un espace
mort [Cf
glossaire]
faible. En conséquence, le nouveau-né ou le nourrisson
jusqu'à l'âge
d'un an
doit maintenir dynamiquement une suppléance fonctionnelle. De
plus, les
diamètres bronchiques du nouveau-né et du nourrisson sont
très étroits.
Ainsi, les capteurs
de débit et de pression pour le nouveau-né et
le nourrisson présentent certaines particularités. En
effet, les
capteurs de
débit et de pression doivent être adaptés à
cette population. La mesure
tant du
débit que de la pression doit être réalisée
juste avant la sonde
d’intubation
(pièce en Y). Le capteur de débit doit avoir un espace
mort minimal.
Les capteurs doivent avoir une gamme de mesure adaptée à
cette
population pour
obtenir une précision correcte ; ainsi, les débits
générés par un
prématuré (30
à 80 mL/sec) nécessitent des capteurs de débit
très sensibles.
Remarques : - il
est important de tenir compte de la réponse en fréquence
des capteurs
au regard
des fréquences respiratoires spontanées
élevées, et tout
particulièrement pour
l’exploration en Ventilation à Haute Fréquence ;
- de plus, deux éléments sont à prendre en
compte dans les mesures réalisées : les fuites avec les
sondes sans
ballonnet
qui rendent très imprécises ou fausses les mesures de la
mécanique
respiratoire, et la résistance du tube, très
élevée en néonatalogie
(2,5 à 3,5
mm de diamètre).
La ventilation
assistée
est l’un des éléments essentiels de la prise en charge de
la détresse
respiratoire des nouveau-nés prématurés.
Différentes techniques sont à
disposition des néonatalogues afin de permettre des
échanges gazeux
adéquats.
II-3-b- CPAP
nasale
La CPAP nasale
(Continuous Positive Airway Pressure = Pression Positive
Continue
Nasale de voie aérienne) offre une alternative à des
modes de
ventilation
plus invasifs comme la ventilation conventionnelle ou la ventilation
sous
oscillation à haute fréquence. Depuis le début des
années 90, quelques
études
concluent que la CPAP nasale précoce, introduite dans la
première heure
de vie,
est un traitement efficace du syndrome de détresse respiratoire
des
prématurés.
Son
principe repose sur l’association du mode de Ventilation
Spontané (VS) et la Pression Positive continue de fin
d’Expiration ou
PEP [Cf
glossaire].
Les
appareils de Pression Positive Continue (PPC) sont des générateurs
de
pression. Ils propulsent l’air ambiant au patient avec une
«pression
positive» (prescrite par le médecin) par
l’intermédiaire d’un circuit
qui
écarte les parois du pharynx à la façon d’une
attelle pneumatique.
Cette
pression est prescrite et mesurée soit en cm d’eau, soit en
millibar.
Ces
appareils sont le plus souvent prévus pour délivrer une
pression
réglable de 3
à 20 cm H2O.
Cette technique est
administrée aux nourrissons d'âge
gestationnel inférieur ou égal à 31-32 semaines
pendant 15, 30, ou 60
minutes.
Le matériel est simple et bon marché. On peut utiliser
cette technique,
si dès
les premières minutes de vie, on constate l'apparition
précoce de
signes
d'insuffisance respiratoire.
Pour l'enfant
prématuré, elle peut être
une solution
d'attente avant le transfert vers une unité
hospitalier
adaptée. Pour
l'enfant
proche du terme, elle peut
permettre d'éviter un transfert inutile et une intubation,
à condition
de
rester vigilant. Ainsi, le nouveau-né ne sera
transféré que si son état
respiratoire se dégrade.
La technique de CPAP
nasale est facile à mettre en œuvre,
toutefois elle présente certaines contraintes. En effet, elle
demande
une surveillance
rapprochée,
donc du personnel,
pour vérifier que la canule nasale soit en place et
n'abîme pas le nez,
pour
faire des soins de nez (aspiration douce), et pour vérifier que
l'état
de
l'enfant ne se dégrade pas. Une certaine expérience est
donc nécessaire.
II-3-c-
Ventilation à Haute Fréquence (VHF)
La
nécessité de
développer de nouveaux modes de
ventilation peut se justifier par deux raisons majeures :
le besoin d’obtenir une
meilleure élimination du CO2 et/ou une meilleure
oxygénation
dans
certaines situations où la ventilation mécanique
conventionnelle
échoue ;
l’espoir de diminuer les
lésions trachéo-broncho-pulmonaires provoquées par
la ventilation
mécanique,
suite à une intubation.
Ainsi, les recherches
se sont orientées dans 2
grandes directions :
l’amélioration de la
ventilation mécanique conventionnelle, avec l’introduction de la
synchronisation sur les respirateurs néonatals et la
réduction de
l’espace mort
par lavage trachéal ;
la Ventilation à
Haute Fréquence utilisant de faibles volumes courants et des
fréquences
élevées, qui après des résultats
expérimentaux très prometteurs est de
plus en
plus utilisée en clinique depuis quelques années.
Le principe
clé de la
VHF repose sur l’utilisation de
volumes courants égaux ou inférieurs au volume mort,
à des fréquences
très
élevées. Mais, il est indispensable de préciser le
principe de
fonctionnement
des appareils de Ventilation à Haute Fréquence. Dans
le circuit
du
respirateur, une oscillation est imprimée sur un débit
continu,
permettant la
mobilisation de petits volumes courants, souvent inférieurs
à l'espace
mort physiologique
des voies aériennes. L'oscillation sera
générée, en fonction de
l'appareil
utilisé, soit par un piston, soit par le déplacement d'un
haut-parleur
au sein
d'un champ électro-magnétique.
Ce type de ventilateur se
compose d’un piston oscillant ou d’un système
dérivé du haut-parleur commandé par un
oscillateur électronique.
Cette
technique utilise des tubes trachéaux standards ; l’inspiration
et
l’expiration
sont actives, le rapport inspiration/expiration [Cf glossaire]
étant en
général proche de 1/1. L’élimination du CO2
est assurée par
un débit
de gaz auxiliaire continu qui permet d’apporter des gaz frais au
système.
La VHFO peut
être définie comme une ventilation
mécanique délivrant :
un volume courant inférieur ou égal à
l’espace mort (Vt < 2mL/kg)
une
fréquence
respiratoire > 3 Hz ou > à 4 fois la fréquence
naturelle du
patient. Il
est bon de noter que la ventilation à haute fréquence par
oscillations
utilise
le plus souvent une fréquence entre 10 et 15 Hz (600 à
900 cycles/min).
La Ventilation à Haute Fréquence a
démontré sa capacité à améliorer
l’élimination du CO2 et à
fournir
une oxygénation adéquate, en évitant l’utilisation
de pressions
d’insufflation
élevées. Elle offre une alternative efficace, là
où la ventilation
conventionnelle est incapable de maintenir les pressions partielles de
gaz du
sang acceptables dans les limites de pression d’insufflation
raisonnables. Il a
été suggéré que l’utilisation de pressions
moyennes [Cf glossaire] inférieures
à 12 mbar dans les voies aériennes évite les
complications.
Ce type de ventilation
est utilisé en deuxième intention,
après résistance à une ventilation classique.
Cependant, les
ventilateurs de
néonatologie possédant la fonction Ventilation
à Haute Fréquence
(VHF)
ne sont pas nombreux sur le marché.
Les indications
de la ventilation à l’aide de la VHF sont :
les
pathologies alvéolaires néo-natales
modérément sévères ou graves :
maladie des
membranes hyalines du prématuré, syndrome de
détresse respiratoire du
nouveau-né à terme, …
dans les situations
d’hypoxémie réfractaire,
dans d’autres situations
où la ventilation mécanique conventionnelle comporte un
risque
d’aggravation
important.
L’appellation
« Ventilation à Haute Fréquence »
recouvre de très nombreux modes ventilatoires, dont la
Ventilation
à Haute
Fréquence par Oscillations (VHFO).
La VHFO est une
méthode d’avenir, qui se développe depuis la mise
à disposition d’un
équipement
adéquat, ayant permis de résoudre les problèmes
d’humidification des
gaz
inhalés. De plus, elle permet de réduire les
barotraumatismes
pulmonaires chez
les prématurés.
Les avantages
théoriques de la VHFO comprennent :
- un maintien de
l’ouverture
des voies aériennes,
- un faible volume
courant
et faible variation de pression,
- une diminution de la
pression des voies aériennes,
- moins de modifications
hémodynamiques.
II-3-d- Aide inspiratoire
(AI) :
Perspective d’avenir
Bien que
les
modes ventilatoires avec trigger du type VACI (Ventilation
Assistée
Contrôlée Intermittente) ou VAC (Ventilation
Assistée Contrôlée) soient
d’un
usage fréquent en néonatalogie, l’Aide Inspiratoire (AI),
disponible
sur
certains ventilateurs destinés aux soins néonatals, est
rarement
utilisée dans
cette spécialité du fait de ses limites techniques.
En
ventilation conventionnelle, les nouveaux-nés sont
ventilés par des
ventilateurs à débit continu, pression limitée et
logique
chronométrique. La
ventilation déclenchée par trigger constitue une
amélioration majeure
dans le
domaine de la ventilation néonatale. Différents modes de
ventilation
avec
trigger ont été mis au point pour les
nouveaux-nés : VACI, VAC, et
plus
récemment l’Aide inspiratoire.
L’Aide
Inspiratoire est le mode qui laisse le plus de liberté au
patient : en
effet, c’est lui-même qui décide du début de
l’inspiration et de
l’expiration,
et par conséquent, qui contrôle le temps d’inspiration, la
fréquence
respiratoire et le volume minute. En effet, l’Aide Inspiratoire est un mode
ventilatoire en pression, où l’inspiration est
déclenchée par le
patient
puis assistée. A chaque inspiration, l’assistance ventilatoire
est
assurée par
une courbe de pression positive synchronisée avec les appels
inspiratoires du
patient, dont celui-ci détermine le début et la fin.
La
désynchronisation entre ventilation spontanée et
ventilation mécanique
présente
un risque potentiel. Selon le réglage du ventilateur, il peut
provoquer
un
conflit ponctuel ou systématique entre expiration active et
insufflation du
ventilateur. L’expiration active est susceptible d’entraîner une
baisse
du
volume courant et du volume minute, une augmentation de la consommation
d’oxygène, une augmentation de la pression intrathoracique, une
baisse
du débit
cardiaque et une augmentation de la pression veineuse.
Un des
moyens pour parvenir à la synchronisation consiste à
diminuer le temps
inspiratoire et/ou à augmenter la fréquence ventilatoire
de manière à
adapter
les réglages du ventilateur à la fréquence
respiratoire spontanée du
nouveau-né. Mais ces modifications ne donnent pas toujours de
bons
résultats et
les fréquences élevées nécessaires à
la mise en œuvre de cette solution
font
qu’elle est généralement rejetée dans la pratique
clinique. Toutefois,
une
autre approche consiste à détecter l’appel inspiratoire
de l’enfant et
à s’en
servir pour déclencher le cycle machine.
De plus,
les
fuites au niveau de la sonde endotrachéale limitait
l’utilisation de
l’AI en néonatalogie auparavant. En fin d’inspiration, avec les
sondes
trachéales sans ballonnet, un débit permanent
s’échappait entre la
trachée et
la sonde d’intubation (débit de fuite). Si cette fuite
excédait le
critère
d’arrêt de l’inspiration (trigger expiratoire), le système
était
incapable de
déterminer la fin de l’inspiration. Aujourd’hui, de nouvelles
technologies
permettent d’utiliser ce mode en
néonatalogie.
III- Dispositifs
existants sur le marché
III-1- VS-PEP
nasale
L’Infant
Flow – Société EME
Le système de
VS-PEP
nasale Infant Flow permet
l'administration d'une pression positive continue très stable
tout en minimisant
le travail respiratoire.
Ce système est
essentiellement constitué d’un générateur et
de la pièce nasale, alimentés par le Driver
Infant Flow.
L'originalité du
principe
de
fonctionnement du générateur Infant Flow réside
dans la bascule de flux.
Celle-ci se produit à l'intérieur du
générateur. Elle est synchronisée
par la
ventilation du patient. Le circuit interne du générateur,
breveté,
conditionne le débit gazeux, de manière à assurer
une VS-PEP stable au
niveau
des voies aériennes du patient.
Le générateur repose donc sur une bascule fluidique.
L'absence de
valves ou de
tout autre dispositif mécanique rend la réponse de
l'appareil à
l'effort du
patient presque instantanée.
La pièce nasale de
forme
anatomique
est constituée exclusivement de silicone. Elle existe en trois
tailles
permettant l'utilisation du très grand prématuré
au nouveau-né à terme.
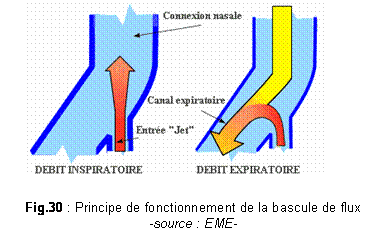
Le flux gazeux est
projeté par des buses vers le nez de l'enfant à
l'inspiration, juste quand il en a besoin. Pendant l'expiration, au
contraire,
la bascule de flux aide l'expiration. La bascule de flux
élimine les
problèmes liés à la VS-PEP conventionnelle.
Le flux
généré par le Driver
est accéléré dans
les buses du générateur. Quand le patient fait un effort
inspiratoire
spontané, le générateur lui donne une aide en
transformant l'énergie
cinétique
du flux gazeux en pression, ce qui réduit le travail
respiratoire du
patient.
Lorsque le patient fait
un effort expiratoire
spontané, la pression qu'il applique sur le
générateur renverse le flux
provenant des buses. Ce flux quitte alors le système via le bras
expiratoire.
Ainsi, la VS-PEP est maintenue constante dans les voies
aériennes. Dès
que
l'effort expiratoire est interrompu, le flux se renverse de nouveau en
position
d'inspiration.
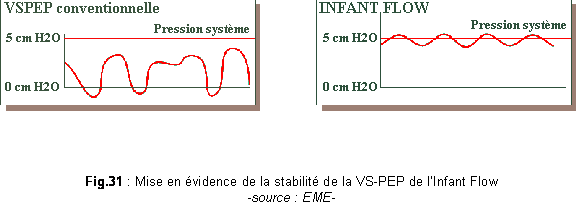
Le résultat final
de
l'application de cette logique fluidique, démontré en
laboratoire et en
pratique clinique, est de réduire le travail respiratoire
additionnel
et de
générer une pression positive constante et stable.
Une utilisation attentive
et précoce de la VSPEP nasale
pourrait diminuer la morbidité et le coût des soins
néonatals.
Le
générateur et son
système fluidique sont activés par le Driver
de l'Infant Flow. Le fonctionnement correct du renversement du flux
dans le
générateur nécessite une pression d'alimentation
minimum de 110 cm H2O.
Le Driver comporte un mélangeur d'oxygène et tous les
dispositifs
propres à
sécuriser la VS-PEP nasale y compris la surveillance des
paramètres avec
alarmes
intégrées.
Le Driver fait partie
intégrante du système Infant Flow. En effet, le
générateur ne
fonctionne
correctement et en toute sécurité que s'il est
alimenté par le Driver
Infant
Flow.
III-2- Ventilateur
à
Haute Fréquence (VHF)
Le Bear Cub
750psv – Société Bear Medical Systems
La mise sur le
marché du
ventilateur BEAR CUB 750pvs marque
l'évolution de l'assistance ventilatoire néonatale.
L'appareil peut
prendre en
charge tous les patients, du petit nouveau né à l'enfant
de trente
kilos. Il
intègre toutes les fonctionnalités essentielles, alliant
l'universalité
clinique
à un design moderne. De plus, il présente une fonction de
Ventilation à
Haute
Fréquence.
Il permet le monitoring
du volume courant (grâce au moniteur
Graphics connecté au ventilateur) et un déclenchement
rapide et
précis de
l'insufflation en fonction du débit proximal (ventilation
synchronisée
intégrée). Le capteur de débit, type
anémomètre à fil chauffant, assure
la
mesure cycle par cycle des volumes courants inspiratoire et expiratoire
au
cours des cycles mécaniques et spontanés. Il mesure
également la fuite
gazeuse.
Le déclenchement
sur le
débit proximal offre la sensibilité
et le temps de réponse nécessaires aux petits
prématurés dont la
fréquence respiratoire
est élevée. La synchronisation entre le ventilateur et le
patient est
constante, le travail respiratoire diminue.
Ce ventilateur
possède un
limiteur de volume breveté. Le limiteur
de volume est une innovation fondamentale pour les soins intensifs du
nouveau
né ; voici ci-après pourquoi c’est un outil
essentiel du
traitement.
La ventilation
conventionnelle en limitation de pression et temps
contrôlé (TCPL) se complique fréquemment d'une
distension excessive des
tissus
pulmonaires, provoquant un volutraumatisme. Pour y parer, le 75Ovs
dispose de
la limitation de volume.
Le volutraumatisme est
habituellement associé à une
augmentation de la compliance pulmonaire. En ventilation
spontanée, le
patient
contrôle tous les aspects de son effort inspiratoire, le risque
de
volutraumatisme lors d'une augmentation brutale de la compliance est
donc très
faible.
Lors
d'un cycle
mécanique, le risque est beaucoup plus important. En effet, pour
un
niveau de
pression inspiratoire donné, l'augmentation de la compliance
entraîne
une
augmentation du volume courant.
Les ventilateurs
conventionnels fonctionnant en TCPL ne
limitent que la pression, l'insufflation continue tant que le temps qui
lui est
imparti n'est pas écoulé et le volume continue
d'augmenter, parfois
jusqu'à des
niveaux dangereux. Un trop grand volume insufflé risque de
distendre le
poumon
jusqu'à la lésion. Ainsi, la limitation de volume
interdit de dépasser
une
valeur inoffensive lors des cycles mécaniques.
III-3-
Ventilateurs à Haute Fréquence par Oscillations (VHFO)
III-3-a- Le
Stephanie – Société
STEPHAN
Stéphanie,
ventilateur
pour grands prématurés et nouveaux-nés, applique
les méthodes de traitement connues pour compléter de
manière optimale
le type
de respiration des patients avec insuffisance respiratoire. Il permet
d’élargir
les formes thérapeutiques respiratoires actuelles par une
respiration
assistée
guidée par le flux de volume, et une ventilation oscillatoire
à haute
fréquence
(VHFO), complétant ainsi les thérapies
conventionnelles.
III-3-b- Le 3100A
Sensormedics –
Société SEBAC
Le 3100A Sensormedics est
un ventilateur de type oscillant à
commande et contrôle électronique. Son oscillateur
constitué d'une
membrane
(diaphragme) dont le déplacement pic à pic et la
fréquence sont
ajustables,
produit des ondes de pression de 3 à 15 Hz se superposant
à une
pression
moyenne positive ajustable des voies respiratoires.
Le 3100A est
capable de prendre en charge les très
grands prématurés ainsi que les nouveaux-nés
à terme. Il possède une
expiration
active et est le seul oscillateur à permettre
l'ajustement du
rapport
I/E.
III-3-c- Le SLE 5000 –
Société SLE
Le SLE 5000 est
particulièrement bien adapté aux nouveaux-nés.
Il permet de délivrer l’ensemble des modes de ventilation, y
compris la
Ventilation
à Haute Fréquence par Oscillations. Il peut aussi
être aussi
utilisé pour
la CPAP nasale.
Le principe sans valve,
breveté, assure une
ventilation efficace pour tous les modes, et offre une expiration
active lors
de la VHFO. Cette caractéristique présente divers
avantages, parmi
lesquels : une amélioration de la ventilation à de
très faibles
pressions,
une réduction des fuites et une meilleure oxygénation
chez les
nouveaux-nés
atteints sévèrement de détresse respiratoire.
III-4- Ventilateurs
combinant les
différents modes
III-4-a- VS-PEP et
VHF : Le Christina – Société STEPHAN
Ce ventilateur de
néonatologie applique toutes les formes de
respiration. Il possède le mode VS-CPAP avec
surveillance
fiable de
l’apnée et offre la possibilité d’utiliser une Ventilation
à Haute
Fréquence.
III-4-b- VS-PEP
nasale et Aide Inspiratoire (AI) : L’Infant Flow advance™ -
Société EME
Le module Infant Flow
advance™ apporte un supplément d'air
enrichi en oxygène à un débit réglable par
le réanimateur entre 0 et
5
L/min. Il peut ainsi générer une aide inspiratoire pour
un patient
ventilant
spontanément et fonctionne selon quatre modes :
- VS-PEP nasale : thérapeutique
déjà testée
et
évaluée dans le monde entier à
l'aide
du système Infant Flow™ original ;
- VS-PEP nasale avec
monitoring des apnées : ce système
présente tous
les
avantages de la VS-PEP nasale, combinés à ceux du
monitoring des
apnées. A
l'aide d'un simple capteur abdominal, détectant les
apnées, il devient
possible
d'administrer une pression supplémentaire pour stimuler la
ventilation
pendant
un épisode d'apnée. Cela permet de laisser le patient
sous VS-PEP
nasale
évitant ainsi intubation et ventilation conventionnelle et leurs
complications
et coûts supplémentaires ;
- Aide inspiratoire avec
monitoring des apnées :
l'aide
inspiratoire
asynchrone à deux niveaux pendant l'inspiration pourrait
améliorer la
tolérance
de la VSPEP nasale. En réglant le débit, le
réanimateur, choisit
l'amplitude de
l'aide inspiratoire. En réglant le temps inspiratoire, il
modifie la
durée
d'application du débit supplémentaire. Cela pourrait
réduire le nombre
des épisodes
d'apnée ainsi que le recours à une ventilation
mécanique ;
- Aide inspiratoire
synchronisée : dans ce
cas, l'aide
inspiratoire est déclenchée par la détection d'un
effort inspiratoire.
Elle
s'accompagne d'une ventilation de secours en cas d'apnée. Le
réanimateur peut
également faire varier la fréquence et la durée de
la délivrance du
débit
additionnel par le générateur. L'aide inspiratoire est
réalisée par
l'augmentation du débit. Par rapport à une VS-PEP nasale
conventionnelle, elle
peut améliorer le volume courant.
III-4-c- VS-PEP nasale,
VHF et Aide
Inspiratoire (AI) :
Le Babylog 8000 Plus –
Société DRAEGER
Dans
le mode VHF, le Babylog 8000 fait vibrer la membrane expiratoire sous
contrôle
du microprocesseur, à des fréquences comprises entre 5 et
20 Hz.
Le mode VHF du Babylog 8000 est une
option permettant de ventiler à des fréquences
supérieures à 5 Hz avec
un
respirateur néonatal conventionnel de type découpeur de
flux.
Selon son principe de
fonctionnement, le Babylog 8000 VHF ne peut pas être
classé dans la
catégorie
des oscillateurs bien connus « à piston »
mais plutôt du type
oscillateur à membrane.
En ventilation conventionnelle,
la valve électromagnétique de PEP vient activer la
membrane en silicone
située
dans le bloc expiratoire et applique une pression de commande dans le
circuit
au rythme des temps réglés. Le débit continu
réglé est
« découpé »
par la valve expiratoire.
En mode VHF, la
valve expiratoire commande de la même
façon les pressions dans le circuit, mais à une
fréquence plus élevée.
Pour
assurer une Pmoy constante, le Babylog 8000 détermine
automatiquement le débit continu nécessaire et le rapport
I/E.
Le
Babylog 8000 permet la
combinaison des modes de ventilation : VHF + VCI (Ventilation
Contrôlée
Intermittente). Un cycle contrôlé périodique
pendant la VHF assurera
les
pressions d’ouverture nécessaires pour recruter les
alvéoles
atélectasiées,
réduisant ainsi le besoin de pressions moyennes
élevées dans les voies
aériennes pour obtenir une oxygénation appropriée.
L’introduction
progressive
des cycles contrôlés pendant la VHF peut, de plus,
réentraîner le
système
respiratoire à la respiration spontanée, et par suite,
améliorer le
sevrage en
stimulant le processus normal de ventilation.
Pour comprendre l’effet résultant de
la thérapie ventilatoire sur le patient, il est important de
surveiller
les
modes de ventilation ou la modification des réglages du
ventilateur. Le
Babylog
8000 permet une surveillance complète des voies aériennes
pour chaque
cycle
contrôlé, cycle haute fréquence et cycle de
respiration spontanée.
Enfin, l’humidificateur
dédié, l’Aquamod, et le circuit
patient utilisé présentent une compliance
extrêmement faible :
0,25
mL/mbar. Cette spécificité se révèle
particulièrement avantageuse
pendant la
VHF, puisque les cycles sont transmis directement au patient sans perte
de
puissance.
Le système de CPAP nasale
BabyFlow, conçu pour les ventilateurs Babylog série
8000, procure
une bonne
stabilité de la PEP et permet de diminuer très
sensiblement les coûts
d’utilisation,
grâce à son adaptation directe sur le circuit patient
standard du
Babylog 8000.
Ce système présente les
caractéristiques suivantes :
les canules nasales
sont à usage unique,
elles restent en
place de manière plus efficace grâce à un
système de fixation qui
ajuste le
BabyFlow avec un confort maximal pour le nouveau-né,
le Babylog 8000
présente une transition souple entre la ventilation
conventionnelle et
la CPAP
nasale,
le très faible
niveau
sonore est conforme à la philosophie des soins de
développement,
la gestion de
matériel est simplifiée et les coûts sont
réduits,
la formation et la
manipulation sont très faciles.
Le
Babylog 8000 Plus permet de disposer désormais d’une Aide
Inspiratoire
spécifiquement conçue pour les nouveau-nés. En
effet, il est muni d’un
système
de correction avec modélisation des fuites qui adapte
automatiquement
la
sensibilité du trigger inspiratoire et le critère
d’arrêt inspiratoire
(trigger
expiratoire) au débit de fuite réel. Cette correction
automatique des
fuites
permet d’éviter les auto-déclenchements du trigger et la
non-reconnaissance de
la fin de l’inspiration du patient et garantit une parfaite
synchronisation
avec la respiration spontanée. Par conséquent, avec le
Babylog 8000
Plus, l’AI
fonctionne avec des fuites de plus de 60 % et plus et il devient
possible de
l’utiliser chez les nouveau-nés.
Ainsi, l’Aide Inspiratoire du
Babylog 8000 Plus s’harmonise de manière remarquable avec la
respiration
spontanée du patient, c’est pourquoi elle constitue le mode
ventilatoire idéal
pour le sevrage.
PARTIE III : Ictère du nouveau-né
I) Aspects pathologiques
Les
premiers jours, l’épiderme du bébé pèle
finement, puis
devient plus claire. Mais il arrive aussi très souvent, dans 80
% des
cas que
la peau jaunisse le deuxième ou le troisième jour, c’est
l’ictère
physiologique
du nouveau-né qui est dû à l’excès d’un
pigment jaune, la bilirubine.

Les symptômes : Deux
jours environ après sa naissance, le nouveau-né peut
« virer » au
jaune. Sa
peau se teinte plus ou moins légèrement, son blanc de
l’œil devient lui
aussi
jaunâtre et ses urines foncent. Il se montre vraiment très
somnolent et
n’ouvre
guère les yeux.
Les causes : A la
naissance, un nourrisson détruit une partie de ses globules
rouges
fœtaux, trop
nombreux. Cette opération libère un pigment : la
bilirubine.
Pour ne pas être envahi par
cette substance pouvant être dangereuse pour certaines structures
du
cerveau,
l’organisme la détruit en partie, notamment grâce au foie.
Dans le cas d’un ictère
physiologique, la quantité de bilirubine est normale (elle ne
dépasse
pas 170 à
220 mmol/L), mais il
manque au nourrisson une enzyme hépatique qui permet de
transformer le
bilirubine en un produit éliminable (bilirubine
conjuguée). Cet ictère
n’est
absolument pas dangereux, à condition que la bilirubine ne
dépasse pas
un
certain taux (la bilirubinémie non conjuguée peut
être toxique lorsque
le taux
est supérieur à 340 mmol/L) : c’est pour
cela que l’on surveille les ictères.
Certains nouveau-nés ne parviennent
pas à détruire ce pigment :
les prématurés au foie
encore trop
immature ;
les nourrissons nés avec des
hématomes (en se
résorbant, ils libèrent beaucoup de bilirubine) ;
- les nouveau-nés
présentant une
incompatibilité
de groupe sanguin avec leur maman (ictère hémolytique) et
qui, de ce
fait, ont
des globules rouges en très grande quantité à
détruire.
Le traitement :
Grâce
au bilirubinomètre
transcutané – petit appareil que l’on applique sur la peau
du
nourrisson –,
il est possible de surveiller le taux de ce pigment. Quand il devient
trop
élevé (entre 220 et 250 mmol/L pour un
nouveau-né
et à partir de 170 mmol/L pour un
prématuré),
donc
dangereux, on effectue une photothérapie.
En cas d’un ictère sévère
([bilirubine] = 400 mmol/L à 430 mmol/L), les
médecins ont
recours à l’exsanguino-transfusion. Cependant cette
technique reste peu utilisée car le risque de mortalité
est élevé (3
pour 1000
procédures).
II – Principe de
fonctionnement des techniques
II-1-
Le Bilirubinomètre
La mesure
de la bilirubine peut se réaliser sous deux
formes :
invasive par une prise
de sang et dosage par spectrophotométrie directe,
non invasive en
utilisant un bilirubinomètre transcutané, Btc (analyse de
la lumière
réfléchie par la peau
et les tissus
sous cutanés).
Il n’existe pas de protocole précis de la mesure de la
bilirubine transcutanée. Elle est recommandée en cas
d’ictère
visualisable
cliniquement. Toutefois, un service de réanimation
pédiatrique ou une
maternité
peut mettre au point son propre protocole et mettre en place une mesure
systématique de la Btc, 12 h après la naissance.
II-2- La Photothérapie
Le
nourrisson est placé dans une couveuse au chaud, les yeux
protégés et
est
exposé plusieurs heures durant sous des lumières bleues,
dont la
longueur
d’ondes (410 à 460 nm) détruit la bilirubine à
travers l’épiderme
jusqu’à une
profondeur de 2mm. L’efficacité du traitement dépend de
plusieurs
facteurs :
de
l’éclairement
énergétique / dose d’énergie radiante,
de la distance tubes-enfant,
de la
durée
de l’exposition,
de la position du nouveau-né
qui
doit se faire
alternativement en position dorsale
et ventrale,
de
l’appareil, de sa technologie et de sa maintenance.
II-2-a-
Risques induits :
Les risques
ophtalmologiques (lésion
rétinienne)
Du fait
des longueurs d’onde utilisées en photothérapie, les
cellules cônes
(cellules
constitutives de la rétine sensibles aux radiations violettes
(380 nm))
sont
les plus sensibles et donc vulnérables. Cependant, la
lumière utilisée
en
photothérapie ne contenant pas de composante UV, elle ne
présente a
priori pas
de dangers potentiellement nocifs. Par précaution, les yeux du
nourrisson sont
couverts.
L’élévation
de température
Les risques d’hyperthermie ne peuvent être
écartés. C’est
pourquoi les constructeurs et les fournisseurs de dispositifs de
photothérapie
recommandent de réduire la température des incubateurs
fermés et de
surveiller
la température de la pièce où sont placés
l’incubateur et le dispositif
de
photothérapie. Généralement, les dispositifs de
photothérapie sont
ventilés permettant
ainsi une évacuation des calories dégagées par les
tubes lumineux.
La
déshydratation
Si le
risque théorique existe, il n’a jamais été
véritablement décrit dans la
littérature.
Le risque
mutagène [Cf
glossaire] ?
Une
exposition à des longueurs d’ondes comprises entre 350
et 450 nm est inductrice de risques mutagènes voire
cancérigènes. Or,
la
lumière bleue utilisée en hyperbilirubinémie est
comprise entre 460 et
510 nm.
Les
précautions à prendre :
Pour surveiller le nouveau-né lors
d’une séance de photothérapie, un moniteur simple du
rythme
cardio-respiratoire
permettant de surveiller les trois paramètres classiques (ECG,
PNI, SpO2)
est suffisant.
II-2-b-
Dispositifs d’éclairage
.
|
|
TUBE
FLUORESCENT
|
LAMPE
HALOGENE
|
LAMPE AUX
HALOGENES METALLIQUES
|
|
PRINCIPE
|
Tube de
verre dont la paroi interne est recouverte d’une mince couche de
substance photolumineuse et dont les extrémités
comportent une
électrode renfermant de la vapeur de mercure basse pression.
La
décharge
électrique dans la vapeur de mercure provoque l’émission
de rayonnement
ultraviolet qui par interaction avec la couche mince photolumineuse
donne de la lumière visible.
|
Lampes
à
incandescence classique remplies d’un gaz diatomique de la famille des
halogènes (fluor, chlore, brome, iode…). Elles utilisent le plus
souvent de l’iode ou des dérivés bromés (bromure
ou dibromure de
méthyle).
Le cycle
halogène a pour but de limiter la sublimation du
tungstène constituant
le filament. L’enveloppe portée à haute
température permet la stabilité
du cycle. L’enveloppe est constituée soit en quartz, soit en
verres
spéciaux.
|
Formation
d’un arc électrique dans une ampoule contenant des
halogénures
métalliques ainsi que des vapeurs de mercure à haute
pression. Les
éléments halogénés concentrent les
métaux vaporisés
dans la zone chaude de l’arc.
|
|
CARACTERISTIQUES
|
80 % de
l’énergie est dégagée sous forme de chaleur :
Déperdition
qui a des conséquences non négligeables sur les
conditions de
traitement du bébé, en particulier sur la surveillance de
la
température et de la déperdition hydrique.
C’est
pourquoi de nombreux constructeurs de dispositifs de
photothérapie
ventilent les rampes de tubes fluorescents afin d’augmenter leur
efficacité en fonction du temps et d’éviter de trop grand
transfert de
chaleur du dispositif vers le patient.
|
Emission d’une
lumière
blanche, très vive, très brillante, de
température
de couleur proche de 3000° K.
Très faible
rendement.
90 % environ de
l’énergie
est dissipée sous forme de chaleur.
Inconvénient
principal :
production de
rayonnements ultraviolets, non absorbés par le quartz.
Solution : Utilisation d’un
filtre en verre ou en matière plastique, positionné
devant la lampe.
|
Emission
d’une lumière blanche vive avec un très bon rendu de
couleurs.
Inconvénient :
Ampoule en quartz donc laisse passer les rayonnements ultraviolets. Le
filtrage est alors nécessaire.
|
III – Dispositifs
existants sur le marché
III-1-Les
bilirubinomètres
Actuellement,
trois bilirubinomètres transcutanés, de
technologies différentes sont présents sur le
marché :
III-1-a-
Le JM 103, Minolta-AirShields (companie
rachetée depuis juillet
2004 par Draeger)
Il est
basé
sur une mesure
spectrophotométrique. Pour réaliser la mesure, il suffit
de placer
l’embout
contre le front ou le sternum de l’enfant et de presser doucement.
Le principe repose alors sur une
analyse de la lumière émise par une lampe xénon
délivrant des flashs.
La
lumière est transmise par fibre optique, et
réfléchie par la peau et
les tissus
sous cutanés. Cette lumière réfléchie est
transmise par fibre optique
sur un
miroir dichroïque [Cf glossaire] et parvient à deux
détecteurs
spectrophotométriques, munis chacun d’un filtre (550 nm et
460
nm). La
durée de vie de la batterie est d’au moins 400 mesures à
pleine charge.
Cet appareil donne une valeur
estimée du taux sanguin de bilirubine exprimé en mmol/L ou mg/dL
quelque soit la couleur de peau du nouveau-né.
De plus, il permet d’aide à la décision concernant la
nécessité de
faire un
dosage sanguin de bilirubine ou de mettre en route un traitement. Son
coût
d’acquisition est d’environ 5500 Euros
III-1-b- Le
Bilicheck, commercialisé
par Airox
Il
est basé sur le même principe que le JM 103
à savoir l’analyse de la lumière blanche
réfléchie par les tissus sous
cutanés
chargés en bilirubine.
L’originalité
réside
dans une analyse très large bande de la réponse, 221
bandes de
longueurs
d’onde, confrontées à une source étalon.
En revanche, ce
dispositif utilise un consommable : un embout jetable qui est
appliqué sur
le site de mesure (front, poitrine, sternum). La durée de vie de
l’ampoule est
de minimum 30000 mesures. Cet appareil fonctionne sur piles dont
l’autonomie
est de 100 mesures minimum.
III-1-c-Le Bilimed,
conçu par Medick:
une nouveauté
C’est un
boîtier
portable autonome qui effectue des
mesures par voie non invasive et sans contact avec la peau du
nourrisson.
Il permet de réaliser un contrôle du taux de bilirubine
sans
traumatisme et
sans risque d’infection pour l’enfant.
Le cycle de
fonctionnement chronologique de l’appareil est le suivant : le
personnel
médical met en marche le Bilimed qui réalise
automatiquement un
autodiagnostic
de son fonctionnement ainsi qu’un étalonnage des diodes
électroluminescentes
(DEL) avant chaque mesure.
Un
ensemble de DEL, disposées en couronne, à 35°
d’inclinaison afin
d’avoir un
point de rencontre précis, s’allument.
L’opérateur
pointe les faisceaux des DEL en
direction de la zone de peau de l’enfant à analyser, soit sur le
front
soit sur
le sternum.

Lors
de la convergence des faisceaux, l’appareil, à l’aide de
photodiodes,
détecte
le maximum d’intensité réfléchie par la peau et
lance automatiquement
un cycle
de mesures en allumant successivement les autres DEL et en quantifiant
l’intensité de lumière réfléchie pour
chacune d’entre elles.
Ensuite, un
signal sonore avertit l’opérateur que la mesure est
terminée. Après
calculs,
analyses et moyennes des valeurs mesurées, le résultat
est affiché sur
l’écran.
Si le résultat est supérieur à un seuil d’alarme,
qui peut être
préréglé par le
médecin, un signal sonore est émis, le résultat
clignote sur l’écran.
Une fois
la mesure affichée, l’opérateur peut imprimer un ticket
de traçabilité
à l’aide
de l’imprimante thermique interne à l’appareil.
Le Bilimed
possède au moins 10 diodes (DEL)
:
3 DEL
jaunes de référence à 520 nm,
2 DEL
rouges entre 620 et 720 nm pour la
pigmentation,
2 DEL
bleues vers 460 nm pour la
bilirubine,
et 3 DEL
vertes vers 545 nm et 575 nm
pour l’hémoglobine.
La
prise de l’échantillonnage de la peau est réalisée
sur une surface d’un
centimètre, sur un vaisseau ou une artère, ce qui donnera
un meilleur
diagnostic. L’appareil reconnaît toutes les ethnies. Il est
doté d’une
alimentation par batteries rechargeables sur un socle raccordé
au
secteur.
III-2-Les dispositifs de photothérapie
Les
différents dispositifs de photothérapie doivent
répondre
aux exigences du marquage CE, au sens de la directive 93/42/CE et sont
de classe
IIa. Le marché présente des systèmes
halogénés, à décharges
d’halogénures
métalliques, des systèmes de rayonnement bleu, blanc,
bleu-blanc.
Pour les systèmes courants, la longueur d’onde
conseillée
est comprise entre 400 et 500 nm, sachant que l’absorption maximale se
situe à
460 nm.
Deux
systèmes
existent :
la photothérapie
traditionnelle dont l’éclairement énergétique
se situe entre 1 et 2
mW /cm² ;
la photothérapie
intensive (l’enfant est irradié sur le dos et l’abdomen
à la fois)
dont
l’éclairement énergétique se situe entre 2 et 5
mW /cm².
III-2-a-La
photothérapie traditionnelle
Dispositifs
à halogène
et à halogénures métalliques :
La
technologie quartz halogène présente un
inconvénient majeur :
l’enveloppe
de quartz laisse passer les rayonnements ultraviolets, qu’il est indispensable de filtrer.
Le
positionnement de la lumière (spot) sur le nourrisson est
très
important pour
que le traitement soit efficace. La distance optimale
source/nouveau-né
est de l’ordre de 50 cm : à cette distance le
dégagement de
chaleur est
moindre et non nocif pour le patient.
Les
incubateurs et/ou les tables de réanimation néonatale,
quelque soient
leurs
origines, intègrent un dispositif de photothérapie, de
base ou en
option, comme
le précise le tableau ci-après.
|
Nom
|
Babylog 8010,
équipée
en option d’une photothérapie
|
Giraffe
Spot PT Lite
|
|
Marque
|
Draeger
|
Ohmeda
|
|
Caractéristiques
|
Ampoule
|
6 spots
quartz halogène basse tension (12V)
Puissance
nominale (50W)
|
Ampoule aux
Halide
|
|
Durée
de
vie ampoule
|
1000 h
|
2500 h
|
|
Intensité
lumineuse
|
Distance
source/patient : 80 cm, distance raisonnable pour obtenir un
traitement par photothérapie et un réchauffement du
nouveau-né sans
risque de brûlures cutanées.
|
A 38 cm du
bébé :
30 à 40 mW/cm²/nm
|
|
Autres
|
Filtre UV : Plaque
de verre
Angle d’ouverture de
rayonnement : 24°
Prix Babylog sans
photothérapie : 14000 € HT
Prix avec
photothérapie : 16000 € HT
|
Niveau
sonore < 60 dBA, mesuré à 90 cm de l’appareil
Prix
incubateur radiant avec le système Giraffe : 30000 € HT
|
Dispositifs de rayonnement
de lumière bleu blanc
Les
principaux dispositifs et leurs
caractéristiques sont regroupés dans le tableau suivant.
|
Nom
|
Photo-Therapy 4000
|
Ampliflux
|
Ampliflux à 2 capots
|
Lampe photothérapie
|
|
Marque
|
Draeger
|
Medipréma
|
Medipréma
|
Médéla
|
|
Caractéristiques
|
Se place
directement au-dessus de l’habitacle d’un incubateur ou d’un berceau
chauffé
4 tubes
fluorescents à lumière bleue
2 tubes
fluorescents à lumière blanche
A 40 cm du
bébé, l’intensité de rayonnement est de :
avec 4
tubes fluorescents bleus, 1,4 mW/cm2 ;
avec 6 tubes
fluorescents bleus, 2,0 mW/cm²
Durée
de
vie recommandée des tubes de lumière
« bleue » : 1000 h
Compteur
horaire d’utilisation intégré
|
Se positionne facilement
sur les incubateurs fermés et les berceaux
Capot diffuseur pivotant
6 tubes de traitements
bleus
A 36 cm du nourrisson, le
flux lumineux est de : 1 mW/cm²
Minuterie permettant
programmation du temps d’exposition de 0 à 12 h
Compteurs horaire du
temps total d’utilisation des tubes (2000h max)
|
Se place sur incubateurs
ouverts ou fermés
2 Capots diffuseurs
pivotants
12 tubes de traitements
bleus
A 36 cm du nourrisson, le
flux lumineux est de : 2 mW/cm²
Programmation du temps
d’exposition
Compteurs horaire du
temps total d’utilisation des tubes (2000h max)
|
Source :
4 tubes
fluorescents,
lumière bleue ou blanche
Classe de
protection : I, Type B
Surveillance
opto-électronique du spectre thérapeutique efficace
Réglable
et
pivotable en continu
|
|
Remarques
|
Les tubes
bleus en forme de U d’une puissance nominale de 18 W sont
spécifiques à
la société Draeger.
Les tubes
blancs sont des tubes fluorescents classiques.
Prix :
3200 € HT
|
Tubes de Type : TL
20 W/52
|
Tubes de Type : TL
20 W/52
|
Consomme
peu d'énergie
|
III-2-b-
La photothérapie intensive
Elle met en
œuvre un éclairement énergétique et est
appliquée pratiquement sur toute la surface corporelle. La
distance
source
lumière/nouveau-né est de l’ordre de 20 à 30 cm.
On obtient par ce
traitement
d’une durée de 4 h une chute spectaculaire du taux de la
bilirubine.
Ampliflux
360, Medipréma
Il est
équipé de 16 tubes bleus de
marque Philips
de type TL
20W/52, dont l’éclairement énergétique est de 3
mW/cm².
Il est muni d’un compteur horaire
qui émet un signal lumineux avertissant que les tubes ont servi
au
moins 2000 h
et qu’il convient de les changer.
Afin d’augmenter l’efficacité des
tubes néon, ceux-ci sont ventilés (un capteur de
température d’ambiance
est
présent).
Un deuxième compteur horaire est
destiné à la programmation de la durée de la
séance. Il est constitué
de 3
fenêtres pour permettre une surveillance du nouveau-né.
Son
coût
d’acquisition est d’environ 8700 €.
Bilicrystal
Bulle 2, Medestrime SA
C’est un
« bac à lumière »
équipé de 6 tubes fluorescents classiques qui
délivrent un éclairement
énergétique de 3,6 mW/cm². Ce bac est doté
d’un matelas gel. Il peut
être placé
dans un incubateur fermé ou radiant.
Associé au système à double coupole
orientable Bilicrystal Duo 2 (chacune des coupoles est
équipée de
4 tubes fluorescents bleus classiques - 2,5 mW/cm² -), il devient
avec
un
éclairement énergétique de 5,5 mW/cm² un
dispositif de photothérapie
intensive.
Il présente :
l’avantage de visibilité du
patient
lors de la
séance de traitement,
l’inconvénient
de surveiller la
température centrale ainsi que les paramètres
physiologiques.
Futura/Innova,
Airox
Il délivre un éclairement
énergétique supérieur à 3,11 mW / cm²
à 35 cm. Le berceau Innova
potentialise l’efficacité de la
photothérapie en répartissant l’éclairement
énergétique sur un maximum
de la
surface corporelle du bébé. Il peut aussi s’utiliser dans
un incubateur.
Le Futura
est pivotant sur 360° et possède 6 tubes de traitement et 2
d’éclairage. Un
compteur horaire permet de programmer la durée des
séances entre 0 et
12 h.
III-1-c-
La photothérapie par fibres optiques : une perspective d’avenir
L’intérêt
majeur de cette technique de photothérapie réside
dans le fait que le nouveau-né n’est pas séparé de
sa mère et qu’il
peut être
tenu dans ses bras lors de la séance.
Biliblanket
Plus à haut flux, Ohmeda
L’originalité réside dans le fait
que le système utilise un câble composé de fibres
optiques permettant
de faire
parvenir de la lumière à partir d’une lampe à
haute intensité jusqu’à
une natte
tissée de fibres optiques. Celle-ci est placée dans une
housse jetable
en
contact avec le patient.
Ce dernier est exposé à une lumière d’une longueur
d’onde comprise
entre 400 et
500 nm.
Le système de
photothérapie BiliBlanket Plus High Output se
compose
d’un
illuminateur et d’une natte lumineuse associée à un
câble en fibres
optique de
1,2 m de long.
L’illuminateur
contient une lampe, des filtres de lumière, une source
d’alimentation,
un
système de refroidissement et une protection contre la
surchauffe près
de la
lampe.
La lampe de l’illuminateur est une
ampoule halogène à filament au tungstène à
haute intensité, avec
réflecteur
incorporé. Le réflecteur est recouvert d’une fine couche
de dichroïque [Cf
glossaire] qui diminue les émissions infrarouges.
Cette lampe est spécialement conçue
pour répondre aux exigences du système. Sa durée
de vie est de 800 h
pour une
tension nominale à une température ambiante de 25°C.
L’éclairement
énergétique
délivré est de 45 mW/cm²/nm.
Bilibed
System, Médéla
Ce concept de photothérapie où l’enfant est en
contact ou
proche de la mère et sans avoir les yeux protégés
par un masque semble
très
intéressant. La société Médéla
propose un dispositif utilisant lui des
tubes
fluorescents classiques, le Bilibed System.
Le nourrisson est placé dans une
couverture qui le maintient en position (ventrale ou dorsale) et
couché
sur une
feuille laissant passer la lumière bleue. Celle-ci est
générée par le
bloc
d’irradiation qui remplace le matelas du berceau dans lequel est
placé
le
patient.
Le bloc
d’irradiation comporte un tube fluorescent
de forme adaptée
dont la durée de vie est de 1500 h. Il est doté de deux
compteurs
horaires,
l’un pour la durée de traitement, l’autre destiné au
temps de
fonctionnement. L’éclairement
énergétique varie entre 2 et 3 mW/cm²
Conclusion
Ce projet d’étude
bibliographique traite des principes de fonctionnement
de quatre dispositifs médicaux dédiés à la
néonatalogie : les
incubateurs, certains
systèmes d’assistance respiratoire, les bilirubinomètres
et les
appareils de
photothérapie.
Il présente
également une
liste non exhaustive des matériels existants
sur le marché et évoque quelques innovations dans ce
domaine : le
contrôle
qualité des incubateurs par le Koala, l’utilisation de l’Aide
Inspiratoire, la mesure de la bilirubine
sans contact avec la peau du
nourrisson et la photothérapie par fibres optiques.
Ainsi, ces innovations
montrent l’intérêt des industriels à
développer
puis commercialiser des équipements destinés aux
nourrissons.
En 2001, environ 10 %
des nouveau-nés ont effectué un séjour dans un
service de médecine
néonatale,
dont 3 à 5 % en réanimation proprement dit avec 50
à 80 % de succès.
Ces
chiffres plus ou moins inquiétants justifient que la prise en
charge du
nouveau-né mobilise néonatalogistes, ingénieurs
biomédicaux et
industriels.
Ainsi, une collaboration systématique de ces acteurs permettrait
d’assurer des
soins de qualité adaptés à chaque
nouveau-né, et de se doter
d’équipements
adéquats.
Actuellement, on note une
augmentation du nombre de grands prématurés.
Ceci est dû notamment au décalage des naissances vers un
âge maternel
plus
élevé. Ce phénomène est inquiétant
dans la mesure où les risques, à la
fois
pour le nouveau-né et la mère, augmentent de
manière sensible avec
l’âge de la
mère. Ainsi, des progrès sont attendus dans le suivi des
grands
prématurés et
dans le diagnostic anténatal.
Parallèlement,
diverses
études mettent en évidence le rôle majeur d’une
prise en charge adaptée aux grands prématurés,
dans leur développement
physiologique. Ainsi, on peut supposer que la recherche du pôle
Génie
Biologique et Médical, Périnatalité – Enfance, de
Picardie contribue,
de plus
en plus, au développement futur de nouveaux dispositifs
médicaux liés à
la
néonatalogie ainsi qu’au diagnostic prénatal.
Glossaire
Compliance :
élasticité.
Cyanose : coloration
bleuâtre de la
peau due à une diminution du taux d’O2 liée à
l’hémoglobine.
Dichroïque :
objet présentant la propriété que possède
certaines substances d’offrir
des
colorations diverses suivant la direction de l’observation.
Espace mort ou volume
résiduel :
volume d’air qui ne
participe pas aux échanges alvéo-capillaires.
FiO2 : fraction
d’oxygène dans
les gaz
inspirés. Autrement dit, c’est la proportion d’oxygène
dans le mélange
apporté
à l’enfant. Elle est exprimée en pourcentage, ou en
fraction de 1
(norme
internationale). La FiO2 de l’air ambiant est 0,21 (21 %).
Hypoxémie : état du
poumon
appauvri en
oxygène.
Mode de ventilation
spontanée :
dans ce mode, le patient
possède suffisamment de réflexes respiratoires pour
déclencher la
machine, qui
est alors chargée de combler les forces défaillantes du
patient.
Mutagène : gène
susceptible
de
provoquer des mutations chez les êtres vivants.
Normothermie : zone de
température dans
laquelle l’individu arrive à maintenir sa température.
PaO2 : pression
partielle
d’oxygène dans le sang artériel. L’unité est le
kiloPascal (KPa) (norme
internationale), ou le mm de mercure (TORR). 1 KPa = 7,5 TORR.
PEP : Pression
Positive continue de fin d’Expiration. La PEP est une technique de
ventilation
au cours de laquelle la pression des voies aériennes est
maintenue au
cours de
l'expiration à niveau supérieur à la pression
atmosphérique, qui peut
s'appliquer à tous les modes de ventilation.
Polypnée :
accélération du
rythme
respiratoire.
Pmoy : intégrale
des
pressions
inspirées et expirées, pression très significative
de l’état du patient.
Rapport
inspiration/expiration : correspond au
cycle
ventilatoire en fonction du temps.
Exemple : I/E =
½ signifie : 1 phase
d’inspiration pour 2
phases d’expiration.
SPO2 : mesure
percutanée de la
saturation de l’hémoglobine en oxygène (SaO2).
On parle
aussi de
saturométrie.
Surfactant :
substance fabriquée par les poumons du fœtus pendant le dernier
trimestre de la
grossesse et qui aide les poumons à rester gonflés
à chaque nouvelle
inspiration. Autrement dit, le rôle du surfactant est
d’empêcher les
alvéoles
de s’aplatir lors de l'expiration.
Volume courant : volume d’air
insufflé à
chaque inspiration.
Bibliographie
Ouvrages
Dr Marie THIRION. Les
compétences du
nouveau né. Nouvelle édition, Coll. Bibliothèque
de la famille, Ed.
Albin
Michel, 2002, Paris
Dr Claude
BEYSSAC-FARGUES, Sabine
SYFUSS-ARNAUD. Le bébé prématuré :
l’accueillir, le découvrir, le
soutenir.
Coll. Bibliothèque de la famille, Ed. Albin Michel, 2000, Paris
Pr Jean Christophe ROZE,
Thomas
KRUGER. L’Aide Inspiratoire – un nouveau mode ventilatoire
synchronisé
pour les nouveaux-nés, Dräger
Dr Philippe JOUVET.
Babylog 8000 –
la HFV en pratique. Département Réanimation Dräger,
1996
Réglementation
Arrêté du
25 avril 2000 relatif aux locaux de prétravail, aux dispositifs
médicaux et aux
examens pratiques en néonatalogie et en réanimation
néonatale
Articles
Le Banc d’Essai :
Anesthésie-Néonatologie. ITBM RBM, 21
: n°2, p15, Avril 2000
Le Cahier
Technique : l’assurance qualité des
incubateurs néonataux. ITBM RBM, 22 : n°6, pp 16
à 18, Décembre
2001
Le Banc d’Essai :
Néonatologie. ITBM RBM, 22 : n°2,
Avril 2001
Processus de mise en
conformité de
l’arrêté de périnatalité du 25 avril 2000.
ITBM RBM, 23 : n°1, pp
60 à 67,
Février 2002
Le Cahier
Technique : la photothérapie. ITBM RBM,
23 : n°2, 2002
Sites
web
Equilibre
thermique
http://www.ohmeda.com
http://www.draeger.com
http://www.mediprema.com
http://www.flukebiomedical.com
Assistance
respiratoire
http://www.hc-sc.gc.ca/pphb-dgspsp/publicat/cphr-rspc00/pdf/rspc00f.pdf
http://frankpaillard.chez.tiscali.fr/anesthesie_physiologie_neonatale_premature.htm
http://bienetre.nouvelobs.com/site/search.asp
http://www.enfant-magazine.com/article/index.jsp?docId=462279&rubId=9229
http://www.airox.fr
http://www.asincoprob.free.fr/compterendus/pathoneonat2.htm
http://www.france5.fr/f5_ref/magazine_sante.htm
http://fn.bmjjournals.com/cgi/content/full/fetalneonatal%3b88/3/F168
http://www.respironics.com/power_programs/infant_neonatal_care.cfm
http://www.pdgsystem.com
http://www.hosmat.com
http://www.draeger.com
http://www.sebac.fr
http://www.ventworld.com
http://www.sle.co.uk
Bilirubimétrie
– Photothérapie
http://www.med.univ-rennes1.fr/etud/pediatrie/ictere.htm
http://www.cs.nsw.gov.av/rpa/neonatal/html/nursing
http://www.airox.fr
http://www.mediprema.com
http://www.medela.fr
http://www.ohmedamedical.com
http://www-sante.ujf-grenoble.fr
http://persowanadoo.fr/ipa.sante.htm
http://www.babyfrance.com/soins.ictere.htm
Autres
Cours du Master
MTS : Les incubateurs