|
Avertissement |
Si vous arrivez
directement sur cette page, sachez que ce travail est un rapport
d'étudiants et doit être pris comme tel. Il peut donc
comporter des imperfections ou des imprécisions que le lecteur
doit admettre et donc supporter. Il a été
réalisé pendant la période de formation et
constitue avant-tout un travail de compilation bibliographique,
d'initiation et d'analyse sur des thématiques associées
aux concepts, méthodes, outils et expériences sur les
démarches qualité dans les organisations. Nous ne faisons aucun usage commercial et la
duplication est libre. Si vous avez des raisons de contester ce droit
d'usage, merci de nous en faire part .
L'objectif de la présentation sur le Web est de
permettre l'accès à l'information et d'augmenter ainsi
les échanges professionnels. En cas d'usage du document,
n'oubliez pas de le citer comme source bibliographique. Bonne
lecture... |
|
Développement de la
structure d’Assurance-Qualité
du Laboratoire de Physiologie et d’Evaluation Neuromusculaire
dans la perspective de
l’accréditation COFRAC suivant le référentiel NF
EN ISO/CEI 17025 : 2005
|

Abla TOUITA KABBAJ
|
Référence
bibliographique à rappeler pour tout usage :
Développement de la structure d'Assurance Qualité du
laboratoire de Physiologie et d'Evaluation Neuromusculaire dans la
perspective de l'accréditation COFRAC selon le
référentiel NF EN ISO/CEI 17025, Abla TOUITA KABBAJ,
stage professionnel de fin d'études, MASTER Management de la
Qualité (MQ), UTC, 2006-2007
URL : https://www.utc.fr/mastermq
; Université de
Technologie de Compiègne |
|
Résumé
Gage de
compétences des
laboratoires d’essais et
d’étalonnages, l’accréditation est le sésame de
tous les laboratoires qui
souhaitent offrir une assurance aux clients sur le niveau de
performance et
d’efficacité de leurs services. Pour obtenir cette garantie, les
laboratoires
doivent mettre en place un système de management qualité
conforme à la norme NF
EN ISO/CEI 17025. En effet le Laboratoire de Physiologie et
d’Evaluation
Neuromusculaire réalise des mesures de force depuis presque 10
ans, et lui
semble primordial de mettre en place une structure qualité
permettant d’assurer
la justesse, la reproductibilité et la fidélité de
ces mesures. Ceci dans le
but de prouver que les conclusions des études cliniques
s’appuient sur des
données fiables et robustes. En développant cette
démarche, le Laboratoire
cherche également à renforcer sa
crédibilité vis-à-vis des partenaires industriels
pharmaceutiques et à constituer un centre moteur pour d’autres
centres de
mesure afin d’harmoniser les modes opératoires
d’évaluation des fonctions
motrices dans le cadre des protocoles multicentriques.
Mots clés : Laboratoire
d’essai, mesure de
force, structure qualité, performance, efficacité,
services, norme NF EN
ISO/CEI 17025, accréditation
|
|
Abstract
Guarantee
competences of the test laboratories and calibrations, the
accreditation is the
sesame of all the laboratories which wish to offer an insurance to the
customers on the level of performance and effectiveness of their
services. To
obtain this guarantee, the laboratories must set up a system of
management
quality in conformity with standard NF IN ISO/CEI 17025. Indeed the
Laboratory
of Physiology and Neuromusculaire Evaluation has carried out
measurements of
force for almost 10 years, and seems to him paramount to set up a
structure
quality allowing to ensure the accuracy, the reproducibility and the
fidelity
of these measurements. This with an aim of proving that the conclusions
of the
clinical studies are based on reliable and robust data. By developing
this
step, the Laboratory also seeks to reinforce its credibility with
respect to
the pharmaceutical industrial partners and to constitute a driving
center for
other centers of measurement in order to harmonize the procedures of
evaluation
of the driving functions within the framework of the protocols
multicentric.
Key word : Test
laboratory, measure of force,
structure quality, performance, effectiveness, services, NF IN ISO/CEI
17025
normalizes, accreditation
|
Remerciements
Tout d’abord je tiens à
remercier Jean-Yves Hogrel, responsable du Laboratoire de Physiologie
et d’Evaluation Neuromusculaire, pour m’avoir accueillie au sein de son
service. Je lui suis reconnaissante pour le temps, l’aide et la
confiance qu’il m’a accordés durant tout le stage.
Je tiens à témoigner ma reconnaissance à Gwenn
Ollivier, kinésithérapeute, pour le temps qu’elle m’a
consacré, les informations
qu’elle m’a communiquées, et la gentillesse
témoignée à mon égard.
Mes remerciements chaleureux vont à Isabelle Ledoux,
Ingénieur biomédical, pour son aide et sa sympathie.
Je tiens à souligner que ces personnes se sont investies dans la
démarche qualité et ont pris le temps pour
répondre à mes questions et m’aider ainsi à
réaliser ce travail.
Je souhaite remercier Stéphane Roques, secrétaire
général de l’Institut de Myologie, pour ses remarques
pertinentes et le temps qu’il m’a accordé.
Je remercie également Aurélie Canal,
kinésithérapeute et Gilles Ngamanye, stagiaire UTC, pour
leur dévouement et leur bonne humeur permanente.
Finalement je n’oublie pas de remercier mes professeurs de
l’Université de Technologie de Compiègne, mon encadrant
Gilbert Farges et Jean-Pierre Caliste pour les conseils judicieux et
l’enseignement qu’ils m’ont prodigué.
INTRODUCTION
A. CONTEXTE PROFESSIONNEL
I . L’ASSOCIATION
FRANÇAISE CONTRE LES MYOPATHIES (AFM)
II . L’INSTITUT DE MYOLOGIE
III . LE LABORATOIRE
DE PHYSIOLOGIE ET D’EVALUATION NEUROMUSCULAIRE
B. STAGE
I. DEPLOIEMENT DU PROJET
1. Planning prévisionnel
2. Déroulement du
projet
3. Risques Management du
projet
II. PROBLEMATIQUE
1. Clarification de
la problématique
2. Cadrage de la
problématique
III. OBJECTIFS
QUALITE DU LABORATOIRE
IV. PROCESSUS DES
ACTIONS A ENTREPRENDRE
1. Définition
du processus d’actions
2. Définition des
sous processus
CONCLUSION
GLOSSAIRE
BIBLIOGRAPHIE
ANNEXES
ANNEXE 1 : CHECK-LISTE
ENVOYEE AUX INVESTIGATEURS
ANNEXE 2 : RISQUE
MANAGEMENT DE MA MISSION
Introduction
Au sein de l’Institut de Myologie, les
objectifs fondateurs du Laboratoire de Physiologie et d’Evaluation
Neuromusculaire (LPEN) sont d’une part le développement d’outils
et de méthodes pour le diagnostic, l’évaluation et le
suivi de patients atteints de maladies neuromusculaires, et d’autre
part, la mise en œuvre de protocoles permettant d’accroître les
connaissances des cliniciens et de mettre en évidence les effets
d’une thérapie. Le LPEN est ainsi impliqué dans de
nombreux protocoles de recherche clinique monocentriques et
multicentriques, visant à évaluer l’effet d’une
thérapie ou à établir l’histoire naturelle d’une
maladie. Pour cette dernière, l’évaluation de la fonction
motrice permet aux cliniciens de prévoir, d’anticiper et de
prévenir les conséquences délétères
de la pathologie. Il est donc indispensable de disposer d’outils de
mesure des capacités fonctionnelles des patients, conformes aux
exigences de la science : précis, sensibles et fiables. Le
laboratoire étudie à cet effet, la pertinence, la
fidélité et la validité des modes
opératoires disponibles pour l’évaluation et le suivi des
performances motrices, afin de déterminer les outils les mieux
adaptés. En résumé, le LPEN s’évertue
à développer et à améliorer en permanence
des outils de mesure de la fonction motrice, de façon à
obtenir des résultats justes et reproductibles, et appuyer ainsi
les conclusions des études cliniques. Dans ce contexte, le
laboratoire s’engage à développer une démarche
d’assurance-qualité selon le référentiel NF EN
ISO/CEI 17025.
De part répondre aux besoins
de ses clients, en mettant en place cette démarche, le
laboratoire cherche également à renforcer sa
crédibilité vis-à-vis des partenaires industriels,
et à sensibiliser les autres centres de myologie à
l’importance de l’harmonisation des pratiques de mesure de force, dans
le cadre des protocoles multicentriques.
L’objectif de mon stage est donc de
mettre en place le système qualité dans la perspective de
l’accréditation COFRAC selon le référentiel NF EN
ISO/CEI 17025, et par conséquent d’appliquer toutes les
exigences requises par cette norme. Dans ce cadre j’ai
délimité le périmètre de
l’accréditation avec le personnel du laboratoire, puis j’ai
clarifié la problématique et élucidé les
attentes des acteurs concernés par cette démarche. J’ai
élaboré ensuite des plans d’actions ciblés et
maîtrisés, afin d’améliorer les faiblesses
organisationnelles et le fonctionnement interne du laboratoire.
Dans ce rapport, nous aborderons en
premier lieu le contexte dans lequel s’inscrit ma mission. Ensuite nous
verrons la problématique du sujet puis la démarche
employée pour mener à bien l’action.
A. Contexte professionnel
Cette partie a pour vocation de
présenter l’Association Française contre les Myopathies,
l’Institut de Myologie et le Laboratoire de Physiologie et d’Evaluation
Neuromusculaire.
I . L’Association
Française contre les Myopathies (AFM)
De la première description
clinique de la myopathie à la mise en place d’une classification
des maladies neuromusculaires et l'avènement des prémices
de la thérapie génique, il s’est écoulé
près d’un siècle. Les maladies et les malades ont
été oubliés à la fois par le corps
médical, le milieu de la recherche et les pouvoirs publics.
C’est essentiellement sous l’impulsion de l’association de malades et
de parents que peu à peu les myopathies sont sorties de l’oubli.
Ainsi, en 1958 un mouvement associatif est né : l’AFM.
L’AFM est une association de malades et de familles de malades, dont le
fondement réside sur un principe simple : ne pas subir la
maladie mais au contraire réagir.
Elle s’est donc donné comme missions d’obtenir la
guérison des maladies neuromusculaires, et de réduire les
handicaps qu’elles entrainent afin de donner à chaque malade une
plus grande autonomie.
Dans ce but, l’AFM propose de :
· Promouvoir toutes les recherches permettant,
directement ou indirectement, la compréhension des maladies
neuromusculaires, pour la plupart d’origine génétique.
· Mettre au point des traitements pour la
prévention des handicaps.
· Favoriser la diffusion et l’exploitation des
connaissances.
· Sensibiliser l’opinion publique, les
pouvoirs publics et tous les organismes ou institutions sur le plan
national ou international, aux problèmes de recherche, de soins,
de prévention et de guérison pour en susciter la prise en
compte.
· Apporter une aide matérielle, morale
et technique aux malades.
· Favoriser leur intégration sociale et
défendre leurs intérêts.
Pour remplir ces missions, l’AFM organise, depuis 1987, chaque premier
week-end de décembre, le Téléthon,
opération de collecte de fonds et de sensibilisation du grand
public combinant une émission télévisée de
30 heures et des dizaines
de milliers de manifestations dans toute la
France. Le Téléthon est le moyen de collecte
quasi-exclusif de l’Association. C’est également un vecteur
d’information et de communication essentiel pour l’AFM.
D’ailleurs depuis le premier Téléthon, des
évolutions et révolutions déterminantes ont
marqué le combat de l’AFM, porté par la
détermination des malades, des familles et des scientifiques.
II . L’Institut de Myologie
Depuis longtemps, l’AFM souhaitait
donner au muscle la place qu’il mérite dans les études
médicales et faire émerger progressivement une
spécialité clinique : la myologie. Pour réaliser
ce projet, l’AFM a développé un partenariat fructueux
avec l’Assistance Publique des Hôpitaux de Paris : l’Institut de
Myologie.
En effet, l’Institut de Myologie est créé en 1996, au
cœur du plus grand centre hospitalier d’Europe, la
Pitié-Salpêtrière, où le Dr Duchenne
décrit au milieu du XIXe siècle, la première
myopathie. Bientôt suivi, dans les mêmes lieux, par
d’autres médecins : Charcot, Landouzy,
Déjerine….Situé dans le bâtiment Babinski,
accueillant des services de pointe consacrés aux pathologies de
la tête et du cou (neurochirurgie, neuroradiologie,
ophtalmologie, oto-rhino-laryngologie), l’Institut de Myologie occupe
une surface de 3500 m².
Il a pour vocation d’être un centre d’expertise
dédié au muscle qu’il soit sain, malade, accidenté
ou vieillissant. Point de rencontre du muscle pathologique et du muscle
sain, il rassemble dans un même lieu recherche fondamentale et
clinique, soins et enseignement.
Il s’est fixé l’objectif de favoriser l’existence et la
reconnaissance de la myologie.
Depuis Octobre 2005, l’Institut de Myologie est géré par
l’association loi 1901 du même nom Association Institut de
Myologie (AIM) qui a pour missions d’impulser et de coordonner avec
tous les partenaires, le développement et la réalisation
du site, et de préparer à moyen terme, la création
d’une fondation de Myologie. Cette association représente le
combat des malades. Elle dispose des locaux et elle soutient
financièrement l’ensemble des pôles.
L’Institut de Myologie est également le fruit d’un partenariat
étroit entre l’AFM, et des partenaires majeurs dans les domaines
de la santé, de la recherche et de l’enseignement : l’Inserm
(Institut National Scientifique pour la Recherche Médicale),
l’Université Pierre Marie Curie (Paris VI) et le CEA
(Commissariat à l’Energie Atomique). Il est également en
collaboration étroite avec Génethon (Centre de recherche
et d’application sur les thérapies géniques).
Il s’agit également d’une structure multidisciplinaire,
puisqu’il s’articule autour de sept pôles en interaction
permanente :
· La consultation pluridisciplinaire de
pathologie neuromusculaire
· Le laboratoire d’histopathologie
· Le pôle de physiologie et
d’évaluation neuromusculaire où j’effectue mon stage
· Le pôle de résonance
magnétique nucléaire (RMN)
· L’Unité Inserm U582 «
Physiologie et thérapie du muscle strié »
· L’UMR787 « Biologie musculaire et
cellules souches » (Unité mixte de recherche Inserm/Paris
VI)
· La banque de tissus pour la recherche (BTR)
Ces pôles concourent au développement de deux
activités transversales : l’enseignement indispensable à
la diffusion des connaissances et à la reconnaissance de la
myologie, et les essais cliniques pour comprendre et soigner le muscle.
III . Le
Laboratoire de Physiologie et d’Evaluation Neuromusculaire
Le pôle de Physiologie et
d’Evaluation Neuromusculaire développe et améliore en
permanence des outils et des méthodes pour :
· Le diagnostic et le suivi des performances
musculaires des patients atteints de pathologies neuromusculaires
notamment dans la perspective de l’évaluation quantifiée
des effets des thérapies (pharmacologiques, géniques ou
cellulaires).
· Une meilleure compréhension des
mécanismes physiopathologiques à l’origine des
modifications fonctionnelles observées, dans le cadre des essais
thérapeutiques.
Ces outils sont utilisés directement par le LPEN ou mis à
la disposition d’autres équipes dans le cadre des consultations
ou des essais cliniques. Des outils spécifiques tels que des
électrodes de surface non invasives ou une poignée de
handgrip ont pu ainsi être développées afin de
mesurer l’activité motrice et la force musculaire de
manière fiable et reproductible. Grâce à ses
activités de veille, d’innovation et de transfert technologique,
le laboratoire examine les possibilités de valorisation et de
transfert clinique des nouvelles techniques et méthodes de
diagnostic et de suivi des pathologies neuromusculaires.
L’appréciation de la force musculaire occupe une place centrale
dans l’évaluation des patients : Pour chaque protocole, le choix
des outils, des modes opératoires et des fonctions musculaires
à évaluer diffère selon la pathologie en question.
La démarche du LPEN consiste ainsi à opérer une
veille scientifique et technologique des outils les plus pertinents et
les mieux adaptés, aux modes opératoires utilisées
et aux fonctions motrices évaluées.
Si l’outil n’est pas commercialisé, le laboratoire le
développe suite aux spécifications du cahier des charges
identifiées à partir des attentes des investigateurs. La
validation se fait ensuite grâce à une expertise technique
et à plusieurs campagnes d’essais. Un mode opératoire est
enfin rédigé pour les fonctions motrices
évaluées dans le cadre du protocole (figure 1).
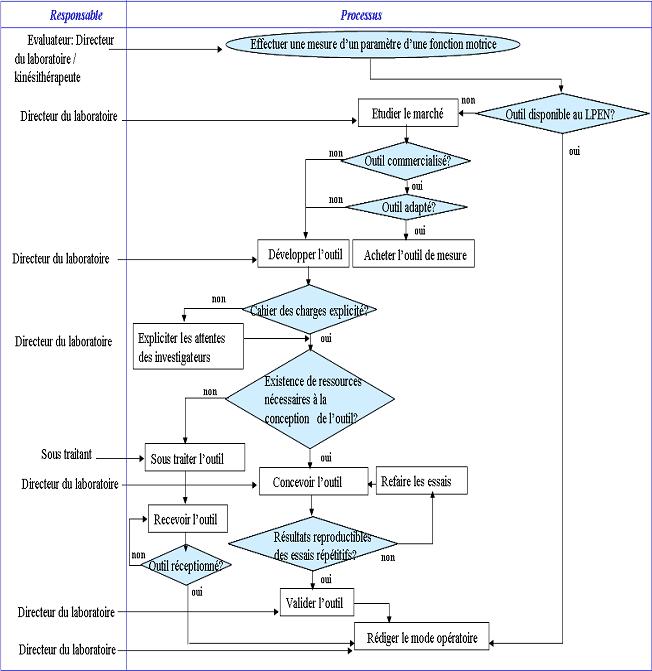 Figure 1 :
Figure 1 : Logigramme
de la démarche adoptée par le LPEN pour
concevoir un outil d'
évaluation d’une
fonction motrice
I. Déploiement du projet
1. Planning prévisionnel
Pour mener à bien ma mission
tout au long des six mois avec organisation et rigueur, j’ai
établi un planning prévisionnel pour pouvoir :
· Déterminer les étapes de mise
en place du projet
· Maitriser les actions à mettre en
œuvre
· Faire un bilan à la fin du stage
Ce retro-planning m’a permis de formaliser les objectifs attendus par
rapport au stage, de recentrer les missions pendant l’avancement des
différentes tâches et de noter tous les
événements qui ont pu se produire pendant les 6
mois. C’est également un outil de pilotage et un planning de
travail pour pouvoir s’organiser (figure 2).
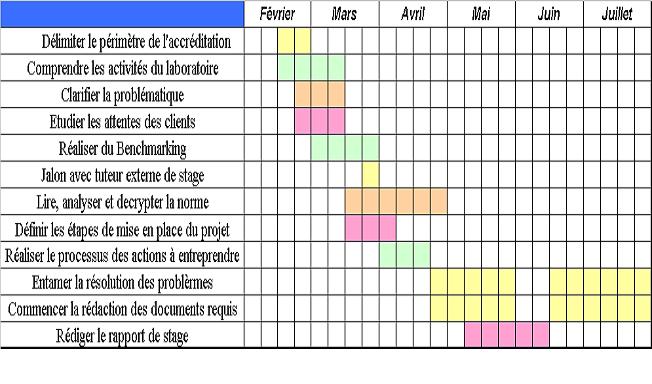 Figure 2 :
Figure 2 : Planning
prévisionnel de travail durant les 6 mois de stage
Le projet de stage s’est
déroulé en 2 grandes phases :
Ø La 1ère phase a consisté
à délimiter le périmètre de
l’accréditation du laboratoire et à déterminer les
activités rentrant dans ce
périmètre. Celui-ci a été
décidé avec l’accord du personnel du laboratoire et du
secrétaire général de l’Institut de Myologie.
C’était également une phase d’approche et de
découverte, durant laquelle j’ai réalisé plusieurs
entretiens avec le personnel, assisté aux différentes
évaluations de la fonction motrice sur des patients afin de voir
leurs déroulements. Cette phase a été primordiale
pour clarifier la problématique, dégager les faiblesses
et les forces du fonctionnement du laboratoire et déterminer les
acteurs concernés par cette démarche.
Ø La 2ème phase s’est organisée
en trois étapes :
o D’abord une étape de Benchmarking que j’ai
réalisé auprès de laboratoires
accrédités selon le référentiel NF EN
ISO/CEI 17025, notamment le
Laboratoire de Biomécanique à l’ENSAM (Ecole Nationale
Supérieure d’Arts et Métiers). Cela dans le but
d’analyser la démarche adoptée afin de mettre en place la
structure qualité.
o Suivie d’une étape de lecture de la norme et
de son analyse.
Pour cela j’ai souligné tous les verbes d’exigence et ensuite
déterminé le type de document où il faut consigner
l’exigence : manuel qualité, procédure, instruction
ou enregistrement.
Je me suis également
procuré des livres
en management de
la qualité qui m’ont permis de déterminer les
critères permettant de distinguer les quatre types d’exigences
ainsi que les principales étapes de mise en place d’une
démarche qualité. Celles-ci sont :
· L’analyse de l’existant : Elle est
indispensable pour justifier auprès de l’ensemble du personnel
des raisons de la démarche de mise en place du système
qualité.
· La détermination de la
politique qualité : Elle doit être claire et
précise pour guider le responsable qualité. Elle doit
fournir les principes et les intentions de la direction en
matière de management de la qualité.
· La désignation d’un responsable
qualité : Il s’agit d’une tâche difficile, conditionnant
dans la plupart des cas la réussite du projet. Cette fonction
nécessite de la part de la personne qui doit l’assumer une
certaine expérience dans la conduite de projet, un sens de
l’organisation et de la rigueur, une compétence dans le domaine
du management de la qualité et une grande connaissance des
référentiels.
· L’identification des objectifs
qualité : Ces objectifs qu’ils soient à court, moyen et
long terme doivent être mesurables et limités dans le
temps. Ils se traduisent par une série d’actions afin
d’atteindre la cible fixée.
· La sensibilisation et la motivation de
personnel : La mise en place du projet requiert la participation active
de tous dans les initiatives de progrès. Des affiches sur la
qualité, des petites réunions avec la direction
rapportant l’état d’avancement du projet, des formations
à la qualité, des déjeuners destinés
à faire le point dans une atmosphère plus conviviale sont
autant d’idées qui peuvent impliquer le personnel dans cette
démarche.
· Le choix d’une méthodologie de
rédaction des différents documents : La forme des
documents n’a que peu d’importance, seule compte l’accessibilité
à l’information qui doit être la plus simple possible.
· L’identification des documents correspondant
à chacune des exigences : Il est nécessaire de
spécifier la nature des documents qui permettront au laboratoire
d’obtenir une image positive de son organisation et de son savoir
faire. Ce n’est pas parce que la norme impose de rédiger une
procédure, que le laboratoire doit obligatoirement produire un
document indépendant portant ce titre.
· La répartition des tâches de
rédaction : Cette étape a deux caractéristiques
particulières, elle est d’abord une affaire de personne «
qui fait quoi ? » et puis une question de délai «
quand ? ».
· L’élaboration de toute la
documentation : Il existe deux méthodologies
générales pour l’élaboration de la documentation.
Méthodologie
aval : Elle s’appuie en priorité sur le
référentiel choisi. Après l’identification du
thème à traiter, il faut détecter les exigences
normatives, les prendre comme base de travail et en déduire les
éléments organisationnels, techniques et administratifs
puis identifier les moyens permettant de les satisfaire.
Cette méthodologie permet de définir un véritable
projet en fixant toutes les étapes à respecter. Elle
offre au responsable qualité un véritable outil de
pilotage pour sa mise en place. Mais elle présente
l’inconvénient de ne pas s’appuyer sur l’existant dans le
laboratoire. Le responsable ne doit pas omettre cet aspect car il
peut avoir un effet négatif sur la suite et créer des
freins.
Méthodologie
amont : A l’inverse de la méthodologie aval,
la méthodologie amont part de l’existant du laboratoire. Elle
consiste à identifier chaque document dans un premier temps et
à rédiger dans un second temps le processus support
conduisant à son établissement. S’il s’agit d’un
processus technique, le document sera un mode opératoire ou une
instruction mais, lorsqu’il s’agit d’un processus organisationnel il
sera question d’une procédure. La première étape
consiste à lister l’ensemble des documents et informations
existants et la description des processus supports correspondants.
L’inconvénient de cette méthodologie c’est qu’elle ne
permet pas de répondre à toutes les exigences. Il
convient donc après la première phase, de procéder
à des audits internes permettant de mesurer la distance entre la
situation au moment de l’audit et les objectifs à atteindre.
· Réaliser un audit blanc : Il peut
être réalisé, sans enjeux, ni conséquences
sur le laboratoire, dans le but de vérifier la conformité
des actions mises en œuvre.
· Décider des actions correctives :
C’est une étape très importante, puisque l’objectif
d’accréditation ne doit être mis en place qu’après
avoir vérifié qu’aucune action corrective n’impose de
longs délais, que tous les écarts ont été
détectés et ont fait l’objet d’une prise en compte
planifiée.
o Enfin j’ai défini un plan d’actions pour que
le laboratoire puisse répondre aux besoins des clients, tout en
tenant compte des exigences de la norme.
Tout au long du projet nous avons réalisé des
réunions pour s’assurer de l’évolution de la
démarche, grâce à la tenue d’indicateurs
pertinents. Ces indicateurs sont dans notre cas les documents
rédigés. Le logigramme suivant présente les
différentes étapes de déploiement du projet de
mise en place de la démarche qualité (figure 3).
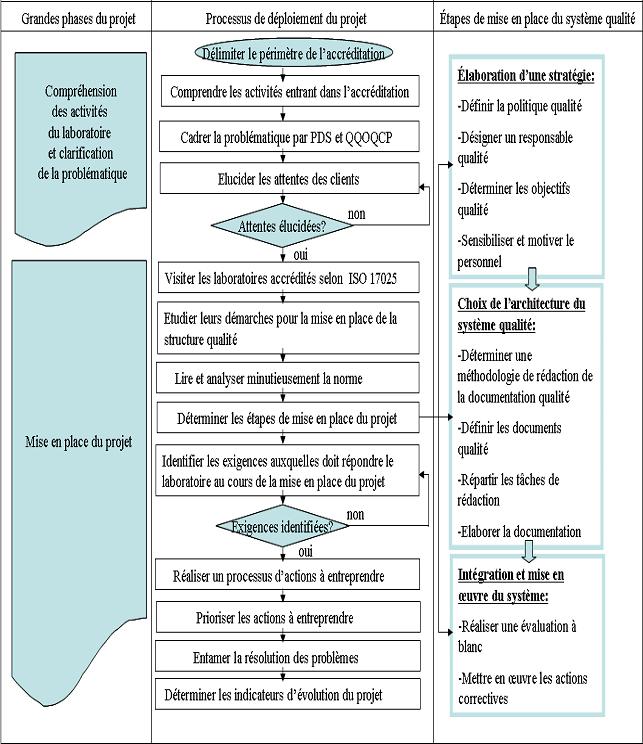 Figure 3 :
Figure 3 : Processus
de déroulement du projet
3. Risques Management du
projet
Dès le commencement de ma
mission, j’ai compris que mon stage s’inscrivait dans un contexte
difficile. D’une part, il n’y avait aucune structure qualité en
place,
d’autre part, il m’a fallu du temps pour comprendre tous les protocoles
de recherche existants.
J’ai eu également des difficultés à rencontrer les
investigateurs, qui sont les premiers « clients » du
laboratoire, du fait de leur surcharge de travail, et de leur
éloignement géographique dans le cadre des protocoles
multicentriques.
C’est ainsi que j’ai décidé d’élaborer une
check-liste et de la leur envoyer par courrier électronique. Les
investigateurs pouvaient répondre de manière binaire et
également émettre leurs avis quant aux idées
suggérées. Le diagramme de décision suivant
présente les différentes activités entreprises
dans le cadre de la mise en place de la démarche, les
éventuels risques pouvant survenir ainsi que les alternatives
respectives (figure 4).
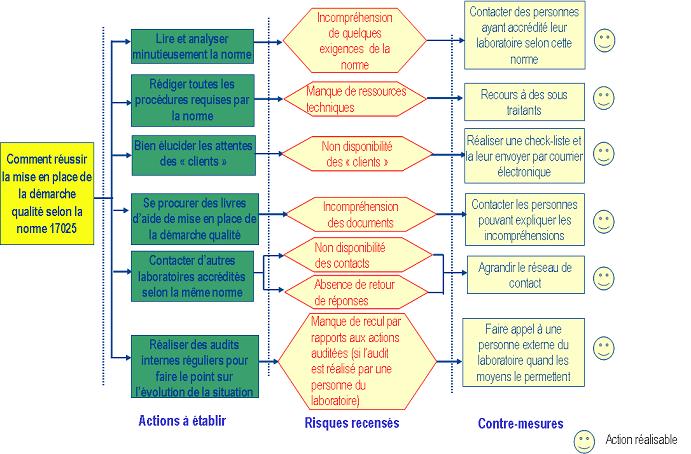 Figure 4 :
Figure 4 : Diagramme de
décision présentant les risques management du projet
II. Problématique
J’ai réalisé une
immersion complète au sein du laboratoire lors de mon
arrivée afin de comprendre son fonctionnement et
d’établir par la suite un bilan en terme de forces et de
faiblesses.
De part la nouveauté, la complexité et la densité
de l’activité du laboratoire, mon immersion au sein de celui ci
s’est un peu prolongée, afin d’identifier tous les modes
opératoires, et les outils d’évaluation des fonctions
motrices employés. J’ai pu également identifier les
acteurs concernés par cette démarche, notamment
«les clients» du laboratoire qui sont les investigateurs et
le personnel du laboratoire.
L’état des lieux a fait l’objet d’une réunion
détaillée avec le personnel du LPEN et le
secrétaire général de l’Institut de Myologie. A la
suite de cette réunion, j’ai établi un planning
prévisionnel de travail durant ces 6 mois.
En résumé, cette étape d’approche a
été primordiale et m’a permis d’avoir une vision
d’ensemble du service.
1. Clarification de
la problématique
Pour avoir une approche
structurée de la problématique, j’ai établi une
planification dynamique stratégique.
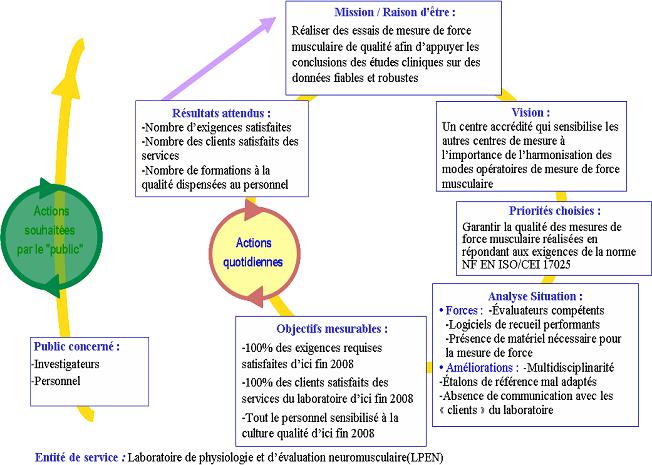
Figure 5 : Planification
dynamique stratégique du projet
2. Cadrage de la
problématique
Afin de bien cerner la
problématique, il a fallu interroger le personnel du laboratoire
et les investigateurs pour identifier au mieux leur motivation, mesurer
leur intérêt vis-à-vis de
l’accréditation et connaître le bénéfice
qu’ils pouvaient en tirer.
a.
Personnel
J’ai pu élucider les attentes
du personnel grâce aux entretiens réguliers faits avec
lui. Celui ci a fait preuve d’une grande disponibilité
témoignant d’une forte sensibilité vis à vis de la
qualité (figure 6).
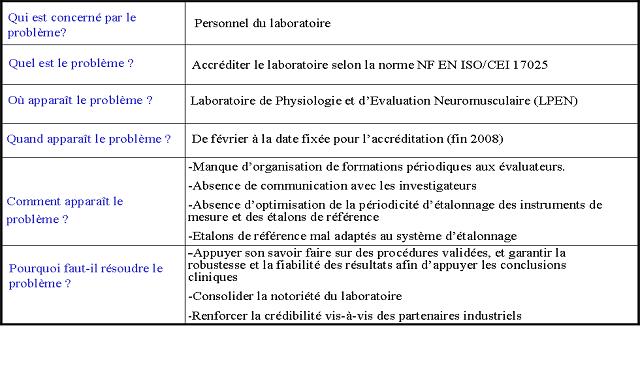 Figure 6 :
Figure 6 : QQOQCP
permettant de cadrer la problématique et d’identifier les
attentes du personnel du laboratoire
b.
Investigateurs
N’ayant pas pu rencontrer les investigateurs, j’ai essayé
dans un premier temps de discerner leurs attentes.
 Figure 7 :
Figure 7 : QQOQCP
permettant de cadrer la problématique et d’identifier les
attentes des investigateurs
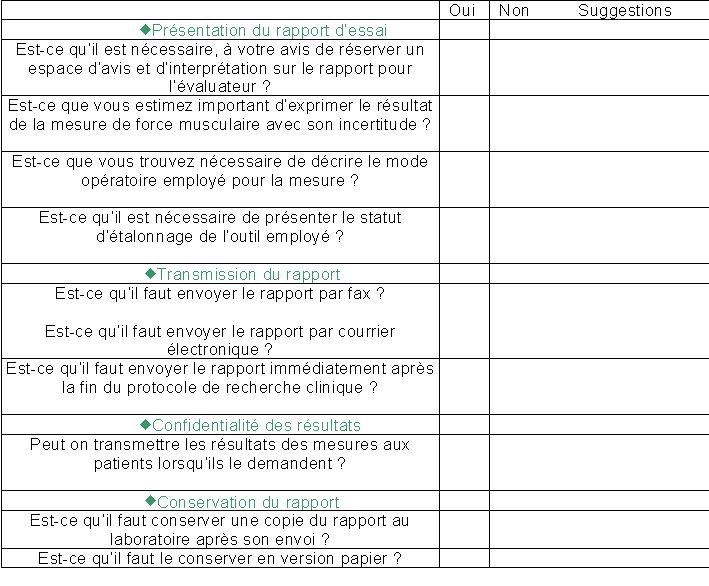
Souhaitant connaître davantage
sur les attentes des investigateurs, j’ai créé, mis en
œuvre et analysé les résultats d’un sondage sous forme
d’une check-liste dont les objectifs étaient d’établir un
premier contact avec eux et de vérifier que la
réalisation des protocoles d’essais cliniques correspondait
à leurs attentes en terme:
· De performance du mode opératoire
employé
· Du choix de l’outil utilisé pour
mesurer la force musculaire
· De présentation du rapport d’essai
· De présentation du résultat de
mesure de force (avec ou sans incertitude)
· Du mode de transmission des rapports d’essai
et de leur durée de conservation
· De confidentialité des
résultats de mesure de force
Le but final étant d’évaluer le niveau de qualité
perçu par les clients
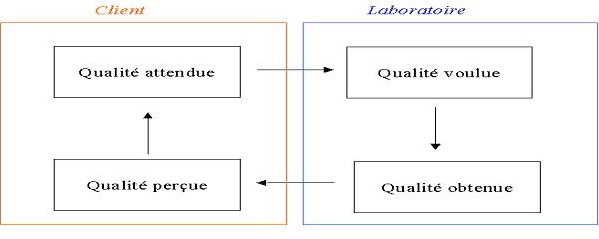
Figure 8 : Figure
montrant la relation qualité laboratoire-client
Les objectifs, la cible
et le mode de l’enquête étant
clairement définis, j’ai établi la méthodologie
d’action suivante pour mener cette mission:
Identifier
les items:
Il m’a semblé judicieux
d’adapter un outil de base de la qualité afin d’être
le plus exhaustif possible dans la recherche des items de la
check-liste. J’ai ainsi réalisé un mini-brainstorming
avec la kinésithérapeute qui effectue les essais. Puis
nous avons utilisé le diagramme des affinités (figure 9)
afin de regrouper nos idées et ébaucher ainsi la
structure de la future check-liste. Le classement des idées a
débouché sur 4 grandes catégories:
· Présentation du rapport d’essai
· Transmission du rapport d’essai
· Conservation du rapport d’essai
· Confidentialité des Résultats
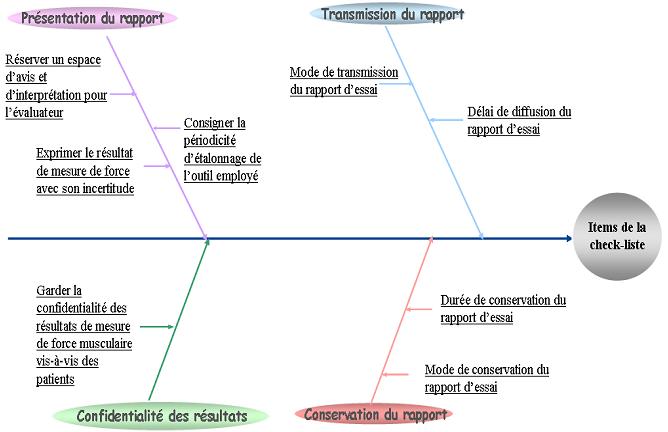
Figure 9 : Diagramme
des affinités rassemblant les différents items
de la check-liste
Construction
de la check-liste:
Un encadré en tête de la
check-liste recueille les
coordonnées de l’interviewé. Les idées ont
été rédigées sous forme de questions
fermées. Un espace était prévu à l’issue de
chaque item, pour que les investigateurs émettent leurs
suggestions. Nous avons également défini un modèle
de rapport que nous avons envoyé afin qu’ils donnent leurs avis.
III. Objectifs
qualité du Laboratoire
Afin de satisfaire les exigences de
la norme NF EN ISO/CEI 17025, et d’obtenir par conséquent
l’accréditation, le laboratoire s’est fixé les objectifs
suivants :
- Répondre aux exigences de la qualité
dans un domaine qui nécessite beaucoup de précision et de
rigueur, qui est le domaine de myologie. Ceci permettra d’obtenir des
résultats justes et fiables et consolidera les conclusions des
cliniciens quant aux différents protocoles.
- Consolider sa notoriété par :
· Le développement et le maintien des
meilleurs services techniques
· La présentation d’un questionnaire de
satisfaction clients pour toutes les activités rentrant dans le
cadre de l’accréditation
· La communication de la démarche
qualité sous forme de présentation, de site web
- Maintenir le bon fonctionnement interne du
laboratoire par :
· La formation régulière
à tout le personnel pour se familiariser avec la documentation
qualité
· Des méthodes formalisées pour
les essais
· La gestion des documents
· L’assurance que le personnel applique les
procédures et les instructions du système qualité
· Une formation plus personnalisée aux
nouveaux arrivants
· La détection et le traitement des
anomalies
· La capitalisation de toutes les
connaissances et les expertises
- L’amélioration du système
qualité et du fonctionnement du laboratoire par :
· L’amélioration au quotidien du
système (la mise à jour des différents documents)
· La mise en place d’indicateurs pertinents
permettant le suivi de la qualité en temps réel.
IV. Processus des
actions à entreprendre
Après avoir clarifié la
problématique et élucidé les attentes de mes
interlocuteurs, il a fallu mettre en place un processus qui soit
efficace avec des actions ciblées, maitrisées et
répondant au mieux aux exigences de la norme.
J’ai commencé dans un premier temps par lire la norme pour
prendre connaissance de son contenu, sans trop me préoccuper de
comment répondre aux exigences.
Suivi d’une phase de décryptage de la norme qui s’est
déroulée en trois étapes :
· Surligner les verbes d’exigence
· Identifier la nature de l’exigence
· Lister les actions dans les documents
adéquats : manuel qualité, procédures,
instructions ou enregistrement.
L’état des lieux effectué au départ s’est
appuyé sur une analyse au travers d’un diagramme d’Ishikawa ce
qui a permis d’identifier les facteurs qui devraient être remplis
pour atteindre l’accréditation.
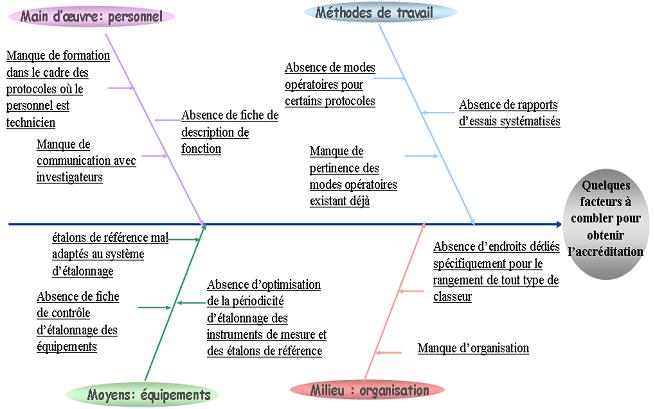 Figure 10 :
Figure 10 : Diagramme
des affinités rassemblant quelques facteurs à
combler afin d’obtenir l’accréditation
1. Définition du
processus d’actions
a. Plan
d’action
général
J’ai d’abord établi un
processus général retraçant les différentes
actions devant être menées, en intégrant la
notion d’amélioration continue (PDCA), afin d’atteindre
l’accréditation. Ceci dans le but de donner au personnel du
laboratoire une vision générale de la marche à
suivre dans le déploiement du projet qualité (figure 11).
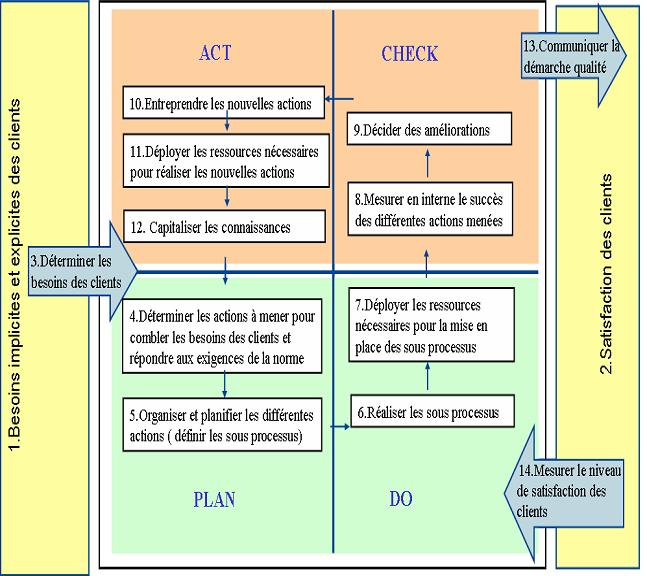 Figure 11 :
Figure 11 : Processus
d’actions élucidant les différentes
étapes de mise en place de la démarche qualité
b.
Plan d’action
spécifique au laboratoire
Dans un deuxième temps j’ai
élaboré un processus spécifique au laboratoire
où j’ai défini les actions à entreprendre pour
atteindre l’objectif d’accréditation et par conséquent la
consolidation de la notoriété du laboratoire (figure 12).
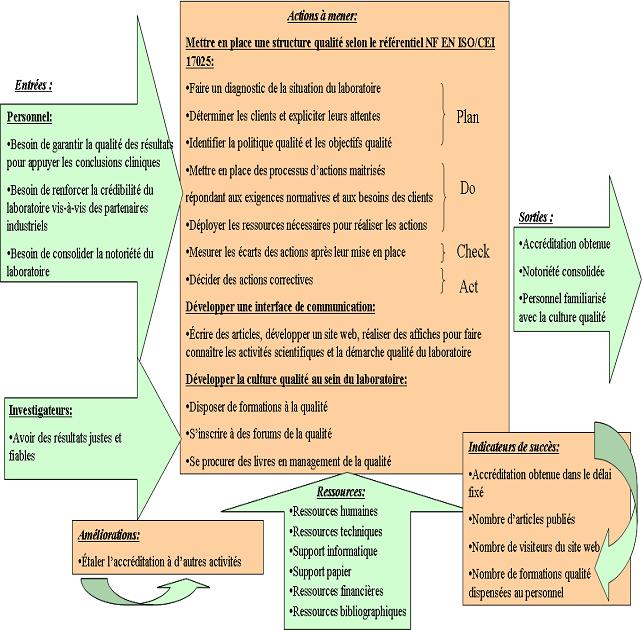 Figure 12 :
Figure 12 : Processus
général du laboratoire montrant les
différentes actions à mener pour atteindre l’objectif
d’accréditation
2. Définition des
sous processus
Nous avons décidé
d’aborder la partie technique en premier lieu, et plus
précisément les chapitres : méthodes d’essais et
validation, équipement et traçabilité de mesurage.
Pour élaborer la documentation, j’ai adopté la
méthodologie aval qui m’a semblé
plus efficace que la
méthodologie amont quant à la structuration du travail,
sans oublier de faire une analyse de l’existant. Ainsi, la
démarche menée pour étudier les 3 chapitres a
été la même, c'est-à-dire :
· La définition des exigences
normatives requises
· La détermination de leur type (manuel
qualité, procédure, instruction ou enregistrement)
· L’analyse de l’existant
· La définition des sous processus
d’actions
· La décision des actions prioritaires
· Le choix des moyens permettant de
réaliser les actions définies
· La répartition des tâches de
rédaction
a. Processus
d’actions pour les
méthodes de travail et leur validation
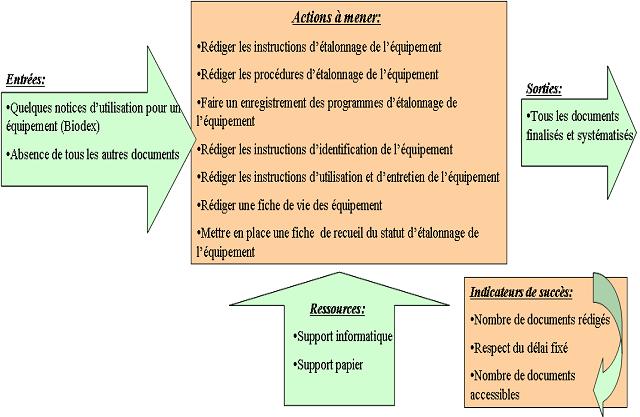 Figure 13 :
Figure 13 : Processus
d’actions à mener afin de répondre aux
exigences du chapitre méthodes de travail
Après avoir établi le
processus des méthodes de travail, nous avons
décidé de résoudre les actions suivantes :
· Rédaction des modes
opératoires de tous les essais
· Rédaction des procédures de
réalisation des essais
· Rédaction des procédures
d’estimation de l’incertitude de mesure
A cet effet, j’ai mis en place un tableau pour assurer le suivi de
l’élaboration de la documentation. Il présente le
document en question, le responsable de sa rédaction, le
délai spécifié, une date de vérification et
une dernière colonne indiquant l’état du document.
Tableau
du
suivi de l’élaboration de la documentation:
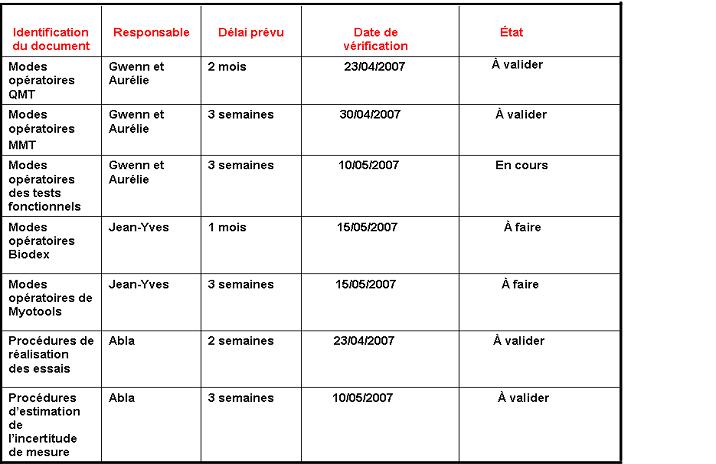 Figure 14 :
Figure 14 : Tableau
du suivi de la rédaction des documents requis par le
chapitre des méthodes de travail
Facteurs
influençant la mesure de force musculaire:
Afin de rédiger les procédures d’estimation
d’incertitude, il a fallu identifier tous les facteurs pouvant
influencer la mesure de force musculaire.
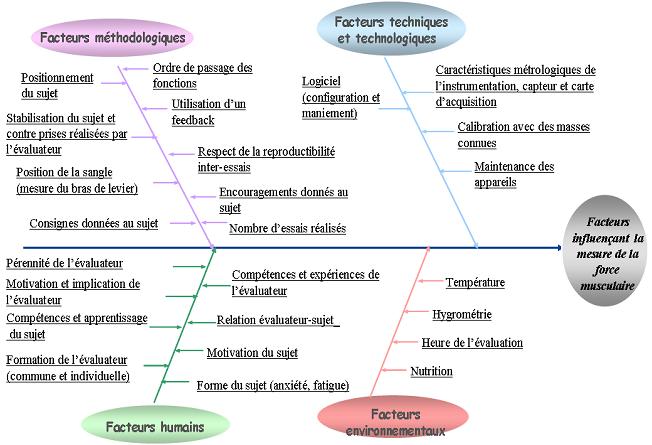 Figure 15 :
Figure 15 : Facteurs
pouvant influencer la mesure de force musculaire
b.
Processus d’actions pour
l’équipement
 Figure 16 :
Figure 16 : Processus
des actions à réaliser afin de satisfaire les
exigences du chapitre équipement
Nous avons également
déterminé les actions prioritaires pour ce chapitre, qui
sont :
· Rédaction des instructions
d’étalonnage des instruments de mesure
· Rédaction des procédures
d’étalonnage des instruments de mesure
· Mise en place d’une fiche de recueil des
données d’étalonnage des instruments de mesure
Tableau
de suivi de
l’élaboration de la documentation:
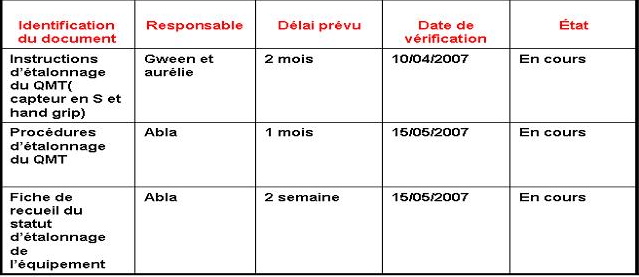
Figure 17 : Tableau
du suivi de rédaction de documents concernant les
exigences de l’équipement
c.
Processus d’actions pour la
traçabilité de mesurage
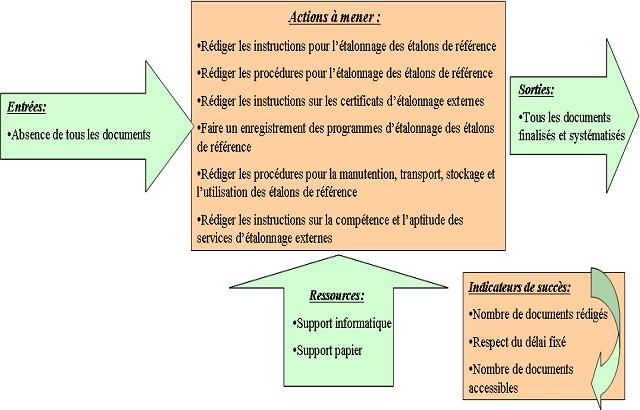
Figure 18 : Processus
des actions à mener afin d’assurer la conformité aux
exigences du chapitre de traçabilité de mesurage
Pour ce chapitre nous avons
commencé par la résolution des actions suivantes :
· Rédiger les instructions
d’étalonnage des étalons de référence
· Rédiger les procédures
d’étalonnage des étalons de référence
· Mettre en place les fiches de recueil
d’étalonnage des étalons de référence
· Réaliser un enregistrement des
programmes d’étalonnage des étalons de
référence
Tableau
de
l’élaboration de la documentation:
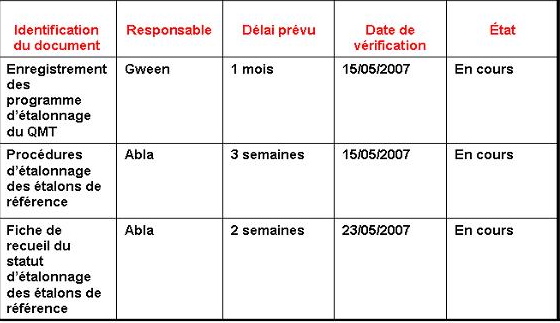 Figure 19 :
Figure 19 : Tableau
de suivi de la rédaction des documents concernant la
traçabilité de mesurage
Les 3 tableaux ont servi d’outil de pilotage pour l’élaboration
des différents documents et ont été
diffusés au personnel pour l’informer de l’avancée
du projet.
Ce stage m’a permis de mettre en
application les connaissances assimilées au cours de ma
formation et de percevoir plus concrètement les notions
restées floues en théorie. J’ai pu réaliser qu’une
démarche qualité requiert un grand sens d’organisation et
de rigueur. J’ai également compris que certains facteurs avaient
une grande importance sur l’évolution de la démarche,
notamment :
· L’implication de la direction
· La motivation du personnel
· Les objectifs qualité fixés au
départ
De plus, afin de répondre aux besoins des clients, j’ai
développé des capacités d’écoute, de
synthèse et d’autonomie.
D’autre part, le travail réalisé a été d’un
grand intérêt pour le laboratoire. Ceci de part
l’engouement suscité au sein du personnel. En effet, ce dernier
était convaincu de l’importance de cette démarche et y
était profondément impliqué, se souciant en
permanence de garantir la qualité des mesures de force
réalisées. Il a fait preuve de beaucoup de patience et
d’attention lors des entretiens effectués, m’a accordé
toute sa confiance et a mis en valeur mes connaissances.
Enfin, j’ai décidé de réaliser un bilan à
la fin du stage, des documents rédigés afin de mesurer
concrètement l’avancée de la démarche. Si ce bilan
se révèle positif, et que les objectifs fixés
à courts terme sont atteints, les objectifs à moyen terme
deviendront des objectifs à court terme. Ce bilan pourra ensuite
être affiché ou diffusé à l’ensemble des
acteurs concernés par la démarche, et permettra de
déclencher ainsi une motivation propice à
l’évolution du projet.
Norme
NF EN ISO/CEI 17025 : Cette
norme concerne aussi bien les laboratoires d’étalonnage que les
laboratoires d’essai utilisant des méthodes normalisées,
des méthodes non normalisées ou développées
en interne.
Elle se présente sous la forme de deux groupes de prescriptions :
· Celles relatives au management et qui sont
les prescriptions organisationnelles.
· Celles à caractère plus
technique qui font chaque fois que cela a été jugé
utile, la différence entre ce qui est spécifique aux
laboratoires d’étalonnage ou aux laboratoires d’essais
Protocole : Recherche
organisée et pratiquée sur l’être humain en vue des
développements des connaissances biologiques ou médicales.
Cette recherche ne peut être effectuée sur l’être
humain :
· Si elle ne se fonde pas sur le dernier
état des connaissances scientifiques et sur une
expérimentation préclinique suffisante
· Si le risque prévisible encouru par
les personnes qui se prêtent à la recherche est hors de
proportion avec le bénéfice escompté pour ces
personnes ou l’intérêt de cette recherche.
· Si elle ne vise pas à étendre
la connaissance scientifique de l’être humain et les moyens
susceptibles d’améliorer sa condition.
Le protocole peut également être un essai
thérapeutique mis en place pour mesurer l'efficacité
d'une molécule ou d'une combinaison de molécules,
déterminer la toxicité éventuelle du produit, ses
effets secondaires et définir la posologie adaptée.
L’essai thérapeutique obéit à des règles
définies par la loi Huriet, qui garantit la protection des
personnes se prêtant à des recherches biomédicales.
La loi ne relève pas le médecin de ses obligations
déontologiques et juridiques. Elle impose d'obtenir l'avis d'un
comité consultatif de protection des personnes. Elle impose
surtout de fournir au patient une information particulièrement
détaillée sur le traitement qu'il va recevoir.
Investigateur : Personne qui
dirige et surveille la réalisation et le déroulement du
protocole.
QMT (le Testing Manuel
Quantifié) : Cette méthode consiste à
mesurer les niveaux de force maximale volontaire isométrique
développés par des groupes musculaires
déterminés du patient lors des contractions
réalisées à position angulaire constante contre
résistance.
Le testing musculaire quantifié nécessite un appareillage
de mesure qui peut être un dynamomètre ou un capteur de
force.
Le patient étant positionné de façon
spécifique, contenu par l’évaluateur (QMT) ou par des
dispositifs à base de sangles pour éviter les mouvements
parasites des autres parties du corps, l’articulation est
immobilisée dans la position angulaire choisie, le dispositif de
mesure est appliqué sur le segment corporel (soit directement,
soit au moyen d’un lien) dont la mobilisation dépend du groupe
musculaire étudié.
MMT (le Testing Musculaire Manuel) :
Il s’agit de la méthode la plus simple et la plus
utilisée en milieu clinique pour évaluer la force d’un
muscle ou d’un groupe musculaire. Elle ne nécessite aucun
appareillage et peut être effectuée par des
opérateurs généralement
kinésithérapeutes ou des médecins. Elle
nécessite un contact direct entre le clinicien et le patient et
est très facile à appréhender par le patient.
Cette méthode consiste en l’évaluation de la force que
développe le sujet lors de l’exécution d’un mouvement
contre une résistance produite par l’examinateur. Celui-ci
évalue le niveau de résistance qu’il doit produire pour
s’opposer au mouvement du sujet, et cote le résultat
évalué sur une échelle. Les échelles
utilisées différent selon les équipes, les
écoles et les pays.
Le testing manuel peut être fonctionnel (fonction) ou analytique
(muscle).
Documents
du COFRAC :
-Modalités de candidature à l’accréditation
par la
section Laboratoires du COFRAC, document LAB INF 20-révision
00-Février 2006, Section Laboratoires, Edition COFRAC.
-Exigences pour l’accréditation des laboratoires selon la norme
NF EN ISO /CEI 17025, document LAB REF 02-révision 03-Novembre
2006, Section Laboratoires, Edition COFRAC.
-Règlement d’accréditation, document LAB REF
05-révision 02-Novembre 2005, Section Laboratoires, Edition
COFRAC.
-Expression et évaluation des portées
d’accréditation, document LAB REF 08-révision 01-
Novembre 2006, Section Laboratoires, Edition COFRAC.
-Questionnaire de renseignements généraux, document LAB
FORM 05-révision 01-Novembre 2005, Section Laboratoires, Edition
COFRAC.
-Questionnaire d’auto-évaluation préparation des visites
d’évaluation, document LAB FORM 03-révision
01-Décembre 2005, Section Laboratoires, Edition COFRAC.
-Questionnaire de renseignements techniques, document LAB FORM
06-révision 00-Novembre 2005, Section Laboratoires, Edition
COFRAC.
Normes :
-Norme NF EN ISO/CEI 17025, exigences générales
concernant la compétence des laboratoires d’étalonnage et
d’essais, Septembre 2005, Edition AFNOR.
Ouvrages :
-Qualité dans les laboratoires d’étalonnages et d’essais.
Une amélioration des processus, Gilles Revoil, 2001,
édition AFNOR.
-Estimer l’incertitude. Mesures-essais, Christophe Perruchet, M. Priel,
2000, édition AFNOR.
-Métrologie dans l’entreprise. Outil de la qualité,
2ème édition AFNOR.
-Manuel qualité, essais-mesures, Laboratoire de
Biomécanique, ENSAM.
Articles et revues:
-Journées neuromusculaires, testing musculaire manuel et
quantifié dans les maladies neuromusculaires. Comment assurer la
qualité des mesures de dans les protocoles cliniques ?,
J.Y.Hogrel, G.Ollivier, C. Desnuelle, Rev Neurol (paris) 2006, p
427-436.
-De la validation des méthodes d’analyse à
l’évaluation de l’incertitude des résultats de mesure,
Michèle Désenfant, Marc Priel, Cédric Rivier,
Laboratoire National d’Essais BNM-LNE.
-Principales maladies neuromusculaires, fiche technique, Novembre 2006,
Association Française contre les Myopathies.
Thèses professionnelles :
-Participation à la mise en œuvre du système de
management de la qualité du laboratoire de radioanalyse et de
chimie de l’environnement du CEA de Saclay dans la perspective de
l’accréditation COFRAC suivant le référentiel NF
EN ISO/CEI 17025 : 2000, Sylvie Lemoine, session mars 2003,
thèse professionnelle du mastère NQCE, UTC.
Sites internet :
-Loi Huriet :
http://www.arcat-sante.org/essais/annexes/huriet.html
-Site de l’AFNOR :
http://www.afnor.org/portail.asp
-Site du COFRAC :
http://www.cofrac.fr/
-Site du Master Management de la Qualité (UTC) :
https://www.utc.fr/mastermq
Annexe
1 :
Check-list envoyée aux investigateurs
Annexe 2 : Risques
management de ma mission




















