Le présent rapport
s’inscrit dans le cadre de la préparation du master
« Technologie en Territoire de Santé (TTS) ». En
effet, outre les objectifs pédagogiques de gestion de projet, de
maitrise des outils qualité et de génération de documents
(Mémoire d’Intelligence Méthodologique MIM) basés sur un travail
bibliographique consistant, d’autres objectifs à caractère
opérationnel s’ajoutent à la panoplie de compétences visée par
les responsables de filière et notamment, l’étude de situation
de la vie professionnelle réelle, l’organisation et le
leadership en travail de groupe et l’habilité à la communication
via différent support (oral-poster, web, publication…).
De ce fait, plusieurs
projets tirés de thématiques professionnelles, joignant qualité
et santé (le cœur de métier visé) sont proposés. Chaque groupe
d’étudiant est amené à présenter l’état d’avancement de son
projet de façon périodique (Jalon). Le résultat final sera
délivré sous format poster.
Le groupe 03, a
choisi pour thématique de travail : « Bilan des
Bonnes Pratiques de l'Ingénierie Biomédicale en Etablissement
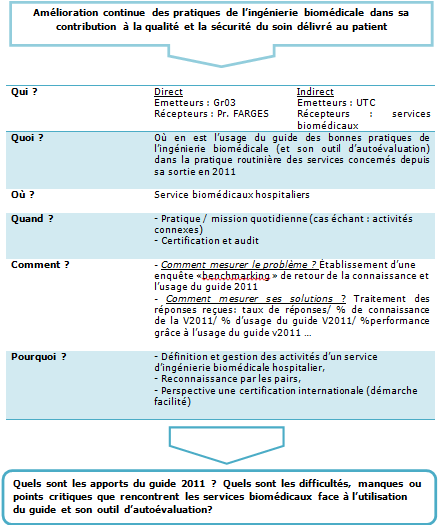
de Santé (2011) ». L’objectif est de dresser un bilan
d'usage du guide biomédical (version2011) et de son outil
d'autodiagnostic, de définir les apports réels, soulever les
difficultés, manques ou points critiques que rencontrent les
services biomédicaux face à l’utilisation de ces documents.
Pour ce faire, une
étude dite « benshmarking » sera menée auprès des
associations biomédicales co-auteures du guide 2011.
retour sommaire
1 INGENIERIE BIOMEDICALE, UN CONTEXTE
REGLEMENTAIRE ET NORMATIF IMPORTANT
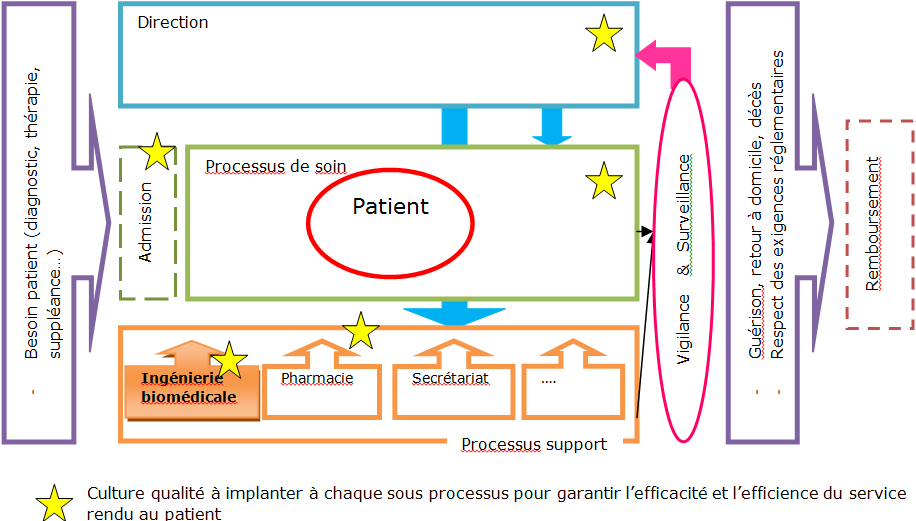
Figure 1 : Cartographie simplifiée
du système de soin. [24]
Le début des années
1990 a été marqué par une législation française des plus
exigeantes. Les établissements de santé français doivent
justifier de moyens adéquats et de procédures permettant
d’évaluer leur activité de soin[1]. Processus support à
l’activité de soin, bien que le service biomédical n’ait pas de
lien direct avec le patient, son expertise biomédicale lui
accorde le rôle légitime dans l’assurance de la sécurité dans
l’exploitation des DM. C’est pourquoi, très vite après la
réforme hospitalière, un arrêté [2]particulièrement destiné aux services
biomédicaux a été publié, définissant les modalités
d’utilisation et de contrôle des matériels et dispositifs
médicaux. Plus tard, d’autre
décrets se rapportant à l’obligation de maintenance[3], ou au contrôle des
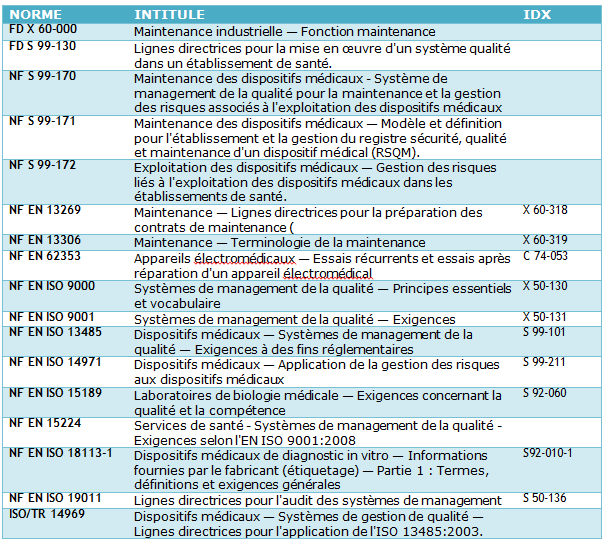
instrument de mesure[4], … en été édité. Dès
lors, plusieurs démarches au niveau international (cf. Tableau 1 annexe p. 2) qu’au niveau national [5] ont été entretenues afin
de garantir une qualité du service rendu et surtout une maitrise
du risque lié aux activités de soin et notamment celui relatif à
l’utilisation des DM.
D’autre
part, dans un contexte de plus en plus marqué par la
judiciarisation (plusieurs directives internationales sont
transcrites en lois nationales afin de protéger les usagers)
d’une société de plus en plus calquée sur le modèle américain,
les organismes sont aujourd’hui conscients de leur
responsabilité [6] sociétale et sont donc
fortement encouragés à obtenir des certifications[7].
Dans ce sens
plusieurs référentiels qualité internationaux (normes ISO 9001,
9004[8], modèle EFQM) ou
nationaux (Le critère 8K du manuel d’accréditation HAS v2010)[9] peuvent être suivi dans
la mise en place de l’organisation d’un service
biomédical.Cependant, pour les premiers, la démarche peut
s'avérer trop ambitieuse avec les caractères "stricte" que
véhiculent les normes : établir des exigences à connaitre par
cœur et à respecter, chose qui peut être un frein à leur mise en
place. Pour le second, il est jugé incomplet puisqu'il ne
s'intéresse qu'à la gestion des dispositifs médicaux, ceux-ci
sont en effet le lien entre le service biomédicale et le patient[10],
mais n'englobe pas la fonction biomédicale dans toute la réalité
du métier.
Mais depuis 2002, un
guide des Bonnes Pratiques Biomédicales [11][12] existe et les
professionnels concernés l’ont mis en place pour organiser et
valoriser leur métier. Cet outil rassemble les comportements et
objectifs visés dans la définition et la gestion des missions du
service biomédical et propose les clefs pour bien appréhender
les principaux concepts et savoir les appliquer à bon escient [13].
Dans une démarche
d’amélioration continue, suite aux enquêtes réalisées (les
retours d’expérience[14], [15], [16], [17]), l’équipe projet
responsable de la première version du guide a sorti en 2011, une
deuxième version plus élaborée ainsi qu’un outil
d’autoévaluation permettant de mesurer l’atteinte de chaque
objectif définit dans le document. Ceci dans le but de
l’associer aux principaux référentiels qualité à l’échelle
internationale.
Parce que
l’environnement dans lequel nous progressons est en perpétuel
changement (une nouvelle politique sanitaire mondiale, de
nouvelles restrictions budgétaires, environnement concurrentiel
rude, etc.), il est nécessaire, dans une démarche d’amélioration
continue, de revoir nos pratiques pour pouvoir accompagner ces
changements et tendre vers un système de soin encore plus
performant où la sécurité du patient est au cœur des
préoccupations.
Depuis
des années maintenant, le monde médical connait une importante
intégration des technologies dans son activité. Aujourd’hui, se
sont des plateaux d’équipements complexes à la pointe de la
technologie qui font la fierté des structures où ils sont
installés. La France, est un marché estimé à plus de 19Mds d’Euro[18].
Cependant, pour
assurer la continuité du service rendu par ces dispositifs et
installations, répondre aux exigences réglementaires et légales,
satisfaire les attentes politiques et économiques mondiales et
nationales, une importante organisation et une gestion des
ressources matérielles et humaines, notamment les métiers de
l’ingénierie biomédicale, s’avère un facteur clef de succès.

Figure 2 : schéma
PESTEL d'une macroanalyse lié à l'environnement de
l'ingénierie biomédical. [24]
La conception du
Guide des Bonnes Pratiques en Ingénierie Biomédicale dans sa
version 2011, a veillé à inclure les principes des référentiels
internationaux ISO (cf.Figure 3). En effet, les
résultats de retours d’expérience[11][19] sur la première version
du guide ainsi que la réglementation dans ce domaine, qui s’est
vu encore plus élaborée et plus exigente, ont permis d’étoffer
la seconde version. Fait par et pour les professionnels
biomédicaux, ce guide et son outil d’autoévaluation[20] démontrent leur force en
représentant une vision réaliste des métiers biomédicaux dans
leur pratique routinière.
De ce fait, l’enjeu
majeur qui peut être décliné à travers l’utilisation de ce guide
réside dans la capacité à accompagner des utilisateurs dans une
démarche d’organisation de leurs activités vers une
reconnaissance établie par consensus des nombreux acteurs
internationaux qui avaient participé à l’élaboration du guide.
La qualité et la sécurité des soins présentent des
enjeux majeurs dans le monde technologique médical, où souvent
la performance des systèmes et installations biomédicales est
liées à un haut niveau de complexité. D’où l’importance de
définir une stratégie d’où découlera par la suite des plans
d’action pour atteindre les objectifs définit par le service
afin d’assurer ces enjeux.
Les services biomédicaux dans leur pratiques
quotidiennes, ont vu petit à petit leur métier se diversifier,
et notamment à cause d’une évolution de la réglementation et des
recommandations liées à leur activité. Il n’en reste que
d’envisager un processus d’amélioration continue dans le but de
suivre les évolutions et prétendre à une performance du service
rendu. Dans ce cadre, le projet de réaliser un bilan de l’usage
du Guide des Bonnes Pratiques en Ingénierie Biomédicale répond à
cet enjeu de performance et d’amélioration de l’avenir des
métiers biomédicaux.
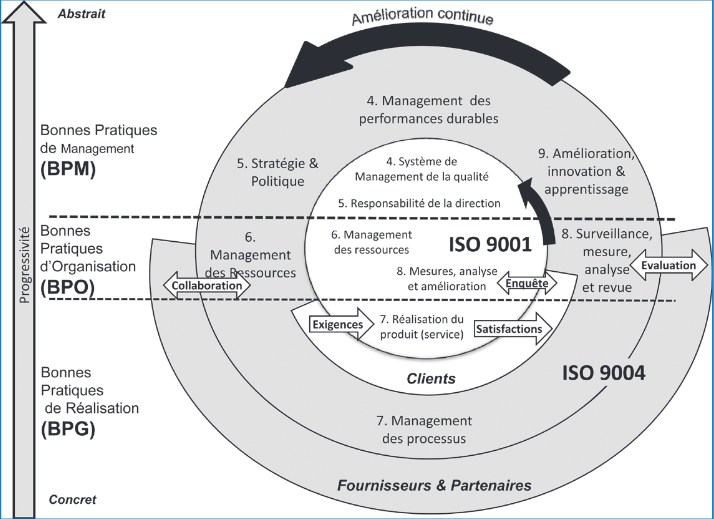
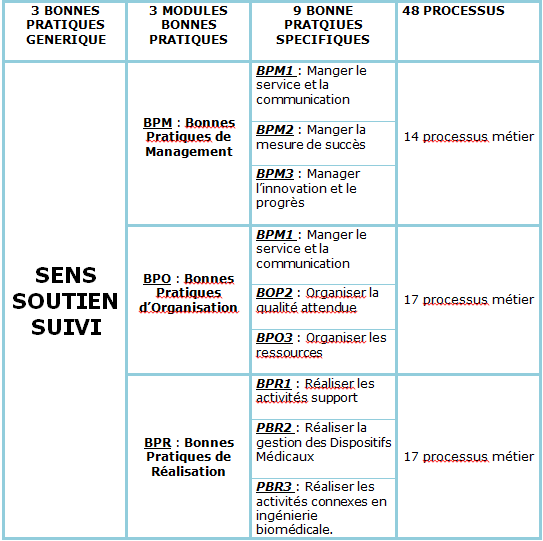
Figure 3 : intégration des référentiels
internationaux dans la logique de conception du guide version
2011
[17]
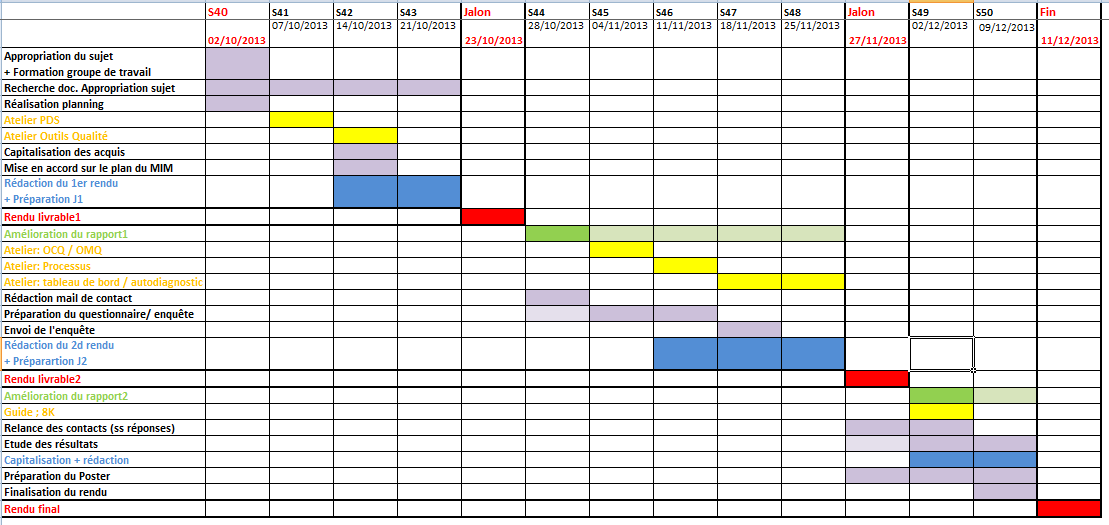
Pour
des contraintes de temps (voir Rétro planning : annexe p.4) et d’accessibilité à la
cible (une large diffusion du questionnaire sur tout le
territoire national et international), le questionnaire sera
réalisé et envoyé par le moyen de « Google docs ». Cet
outil permet l’élaboration simple et complète d’un questionnaire
avec retour des résultats sous forme pré-analysée.
L’enquête à mener
décrit plusieurs étapes en fonction du profil de la
personne qui répondra au questionnaire. Il faut prévoir
les éventuelles réponses émises par la personne concernée
en fonction des résultats voulus : connaissance,
perception, usage du guide des BPIB v2011 et/ou
recommandations d’amélioration. En effet, différentes
possibilités peuvent être envisagées.
- Les services
biomédicaux connaissant et utilisant le guide v2002
- Les services
biomédicaux connaissant et utilisant le guide v2011
- Les services
biomédicaux ne connaissant aucune version
- Les services
biomédicaux connaissant le guide v2011 mais utilisant
toujours la version 2002
- Les services
biomédicaux connaissant le guide v2002 mais utilisant la
version 2011
- Les services
biomédicaux connaissant et utilisant les deux versions du
guide 2002 et 2011
- Les services
biomédicaux connaissant les guides mais n’utilisant aucune
version
Suite à
cette première approche la personne est dirigée vers
le profil de questionnement qui lui correspond. Par
exemple, les personnes utilisant le guide version
2011, sont dirigées directement vers la partie du
questionnaire du guide version 2011. Pour les
utilisateurs du guide version 2002 un premier
questionnement sur son utilisation de ce guide
ensuite la logique du questionnaire lui propose si
l’utilisation future du guide 2011 est envisageable.
C’est alors que le répondant est renvoyé vers la
page du questionnaire sur l’utilisation future du
guide 2011. Enfin, pour les non utilisateurs de
guides le déroulement du questionnaire propose de
passer directement sur le guide 2011.
La construction
du questionnaire prend en compte aussi la promotion du
questionnaire et la communication de lien utile vers
la documentation des Guides de Bonnes Pratiques en
Ingénierie Biomédicale. Le répondant au questionnaire,
s’il ne connait pas les guides et leurs outils
d’autodiagnostic, peut en effet, accéder à un
téléchargement libre du guide 2002 [12] et son outil
d’autodiagnostic. L’outil d’autodiagnostic, de la
version 2011, est libre aussi, seul le Guide des
Bonnes Pratiques en Ingénierie Biomédicale est payant.
Le présent projet
s’articule autour de trois phases globales:
· 1ère phase : Faire un état de l’art par rapport à
l’ancienne version du Guide de Bonnes pratiques (version
2002) et de son outil d’auto diagnostique ;
· 2ème phase : Réaliser l’enquête auprès des services
biomédicaux dans les établissements de santé ;
· 3ème phase : Exposer les résultats.
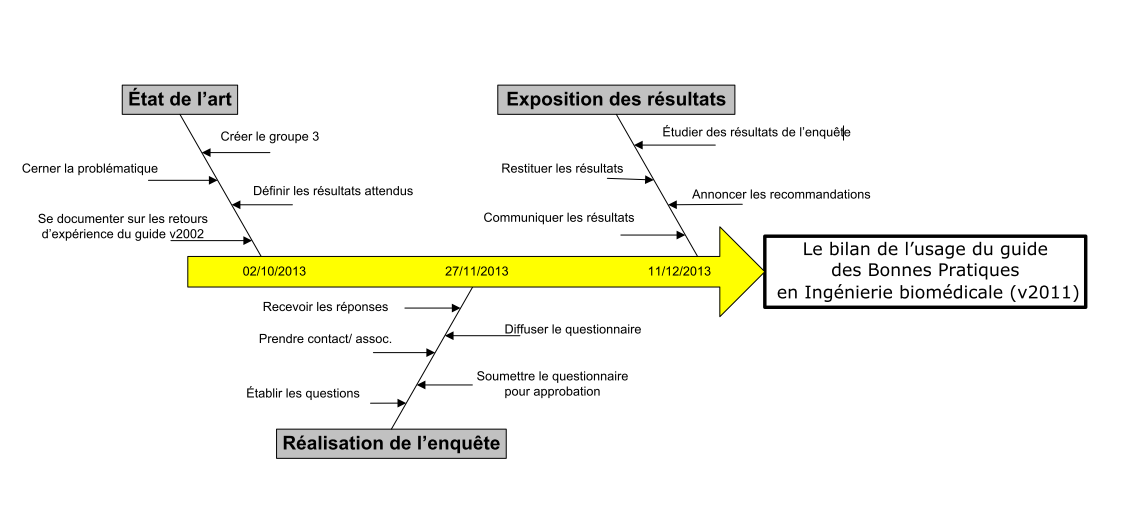
Figure 4 : diagramme d'Ishikawa
présentant la logique de progression du projet par l'équipe
.
[24]
Au cours de la
première étape de ce projet, il fallait tout d’abord
cerner la problématique liée au sujet, et qui est :
« où on est de l’usage du guide de bonnes pratiques
en ingénierie biomédicale et de son outil d’auto
évaluation, au sein des services biomédicaux, depuis sa
sortie en 2011 ?
Ensuite, il
fallait faire un état de l’art sur la situation des bonnes
pratiques au seines services
biomédicaux dans les établissements de santé, à l’échelle
nationale et internationale, en s’imprégnant des résultats
du Guide de Bonne Pratiques Version 2002.
Après la
détermination de la problématique du projet, et la
réalisation de l’état de l’art, il était nécessaire de
bien définir les résultats attendus de ce travail, et qui
sont :
« Définir
l’état réel de la connaissance et de l’usage du guide de
bonnes pratiques en ingénierie biomédicale depuis sa
parution en 2011 ».
La menace réelle
liée à cette première phase du projet, était de diverger
de la mission principale du travail, et de partir sur une
fausse piste. Mais l’exploitation des différents outils de
qualité (la PDS, le brainstorming, les outils de base en
qualité, de contrôle qualité ainsi que les outils de
management qualité) a permis de bien cadrer les objectifs
de ce travail, et définir un plan d’action bien précis
tout au long des différentes phases du projet.
La deuxième étape
du projet repose sur la réalisation de l’enquête auprès
des services biomédicaux à l‘échelle nationale et
internationale, essentiellement les services biomédicaux
adhérant aux associations biomédicales co-auteures des
guides de BPB. En commençant par établir un questionnaire
synthétique et direct (cf. Figure 5).
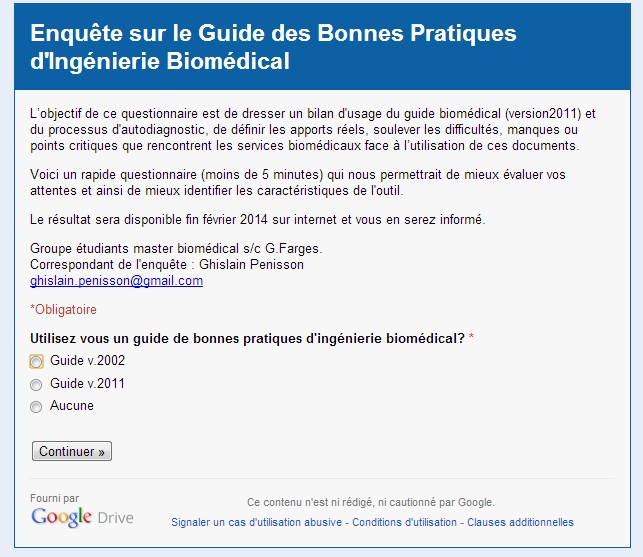
Figure 5 : capture d'écran de la première page du
questionnaire en ligne : lien
ici
Les risques liés à
cette phase :
· Questionnaire mal
conçu ;
· Manque de retour ou
retour insuffisant pour faire un bilan sur la situation
réelle de l’usage du Guide des Bonnes Pratiques en
Ingénierie Biomédicale et de son outil d’Autodiagnostic
v2011
Et pour éviter que les questions soient mal
conçues, la soumission du questionnaire à l’initiateur du
projet parait une étape nécessaire (cf : Figure 7 ci-dessus). C’est pour
cette raison qu’elle a été intégrée aux phase de suivi du
projet. Après son approbation, il sera diffusé aux acteurs
biomédicaux, qui par leur participation à cette enquête,
en envoyant leurs réponses et leur retour d’expérience
(autoévaluation), constituent une matière première pour
faire un bilan d’usage du guide de bonnes pratiques et de
son outil d’autodiagnostic. Le passage par l’initiateur du
projet, M. FARGES, en sa qualité d’auteur de ces
documents, et l’un des pionniers de la qualité dans le
milieu médical, pour l’approbation et la diffusion du
questionnaire donnera un caractère plus professionnel à
cette enquête et appuiera notre requête auprès des
services biomédicaux.
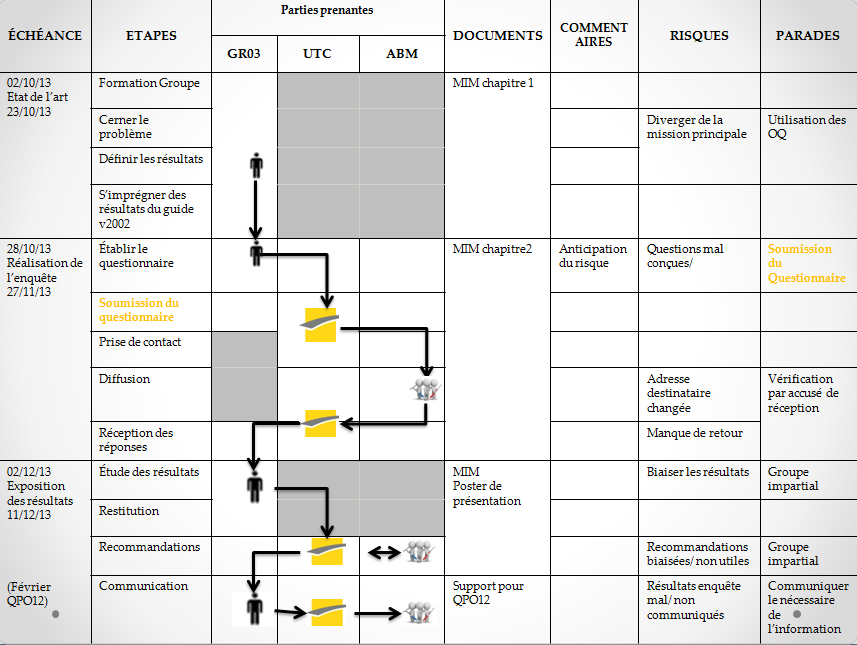
Figure 6: Diagramme de décision incluant les
risques-projet et les solutions proposées.
[24]
Analyser le taux de connaissance et
d’exploitation du guide, relever les points forts et les
points faibles de cette version (2011), et proposer
éventuellement des améliorations, constituent les
résultats espérés derrière ce projet.
Le présent projet
ne demande pas une attente particulière ou précise des
résultats. En effet, l’enquête n’est pas réalisée pour
déterminer un résultat concret mais pour évaluer l’intérêt
des services biomédicaux envers le Guide des Bonnes
Pratiques en Ingénierie Biomédicale.
L’attente espérée
est donc une réception massive de réponses à l’enquête qui
nous permettra de mettre en relief l’évolution ou non de
l’utilisation de ce guide.
L’analyse des
réponses reçues, des différents acteurs biomédicaux,
constitue la troisième et dernière phase de ce projet. En
fonction des retours et des taux de participation à cette
enquête, une étude des résultats sera indispensable pour
présenter un état des lieux sur l’usage du guide et
de son outil d’autodiagnostic aux seins de services
biomédicaux, et aussi pour démontrer le rôle du Guide de
Bonnes Pratiques en Ingénierie Biomédicale version 2011,
dans la pratique quotidienne des acteurs biomédicaux au
sein des établissements de santé, à l’échelle nationale et
internationale.
Le bilan, du Guide
de Bonnes Pratiques en Ingénierie Biomédicale (version
2011), se basera sur l’étude et l’analyse des résultats de
l’enquête, et sera communiqué lors des événements
intéressant la qualité et l’ingénierie biomédicales.
Les risques liés à
cette étape du projet sont :
· Fournir des
résultats biaisés ;
· Résultats non ou
mal communiqués ;
L’essence même de
ce projet est de projeter une vision, la plus objective
possible, de l’usage du guide des bonnes pratiques en
ingénierie biomédicale. Ce projet est réalisé et est mené
par des étudiants impartiaux et aucun conflit d’intérêt
n’est à relever, pouvant biaiser les résultats de
l’investigation menée.
Une fois le questionnaire réalisé, il a été
envoyé lundi 02 décembre 2013 à 214 contacts biomédicaux
ayant contribué au guide biomédical. Sur une période d’une
semaine, les réponses reçues ont permis de faire une
première analyse.
Utilisateurs du
guide 2002 :
Pour cette partie,
seulement trois réponses ont été émises. Il faut donc être
très relatif quant à leur pertinence.
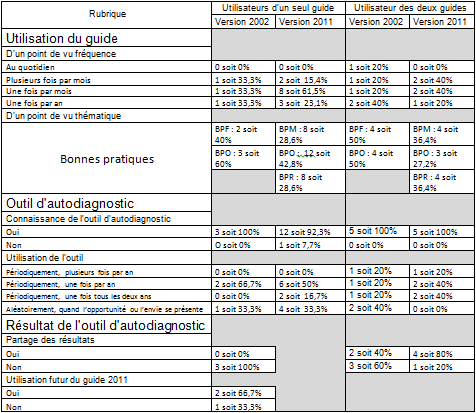
Parmi les
utilisateurs du guide version 2002, on remarque que
l’utilisation en terme de fréquence est répartie de façon
égale entre plusieurs fois par mois, une fois par mois et
une fois par an. De même au niveau thématique, malgré une
légère tendance pour le thème BPO : aspect
opérationnel (60%).
En ce qui concerne
l’outil d’autodiagnostic, la totalité des personnes
connaissent l’existence de l’outil d’autodiagnostic. En
revanche l’utilisation est partagée entre une fois par an
(66%) et aléatoirement. Le partage des résultats n’est pas encore
encré dans les mœurs car aucun des utilisateurs n’a
partagé ses résultats. Enfin, seulement deux personnes sur
trois pensent utiliser prochainement le guide 2011.
Utilisateurs du
guide 2011 :
Ce côté de
l’enquête est plus révélateur avec 13 réponses. Mais reste
tout de même faible par rapport au nombre de service
biomédicaux ayant reçu l’enquête.
L’utilisation du
guide est majoritairement d’une fois par mois avec plus de
60% des réponses. Le reste se partage entre plusieurs fois
par mois et une fois par an. Pour ce qui concerne les
thèmes, les BPO occupent 42% des réponses et les deux
autres possèdent le même pourcentage d’utilisation.
L’outil
d’autodiagnostic est utilisé par la totalité des
utilisateurs excepté une personne. Il est également
utilisé à 50% des personnes une fois par an, 16,7% une
fois tous les deux ans et 33,3% aléatoirement.
Utilisateurs des
deux guides :
5 des répondants
utilisent les deux guides de manière simultanée. Les
informations sont excrètes selon les deux guides.
Pour l’utilisation
de la version 2002, La répartition se fait, d’un
point de vu fréquence, de manière uniforme : au
quotidien 20%, plusieurs fois par mois 20%, une fois par
mois 20% et une fois par an 40%. Pour les thèmes
d’utilisations, c’est réparti de manière parfaitement
égale entre les BPO et BPF.
Pour l’utilisation
de l’outil d’autodiagnostic, tous les utilisateurs
utilisent l’outil, mais de manières différentes en termes
de périodicité. Nous avons 20% qui l’utilisent
périodiquement, plusieurs fois par an, 20% périodiquement,
une fois par an, 20% périodiquement, une fois tous les
deux ans et 40% qui l’utilisent aléatoirement.
Pour les résultats
de l’outil, seulement 40% partagent les résultats contre
60% qui ne le font pas.
Pour l’utilisation
de la version 2011, La répartition se fait, d’un
point de vu fréquence, de manière uniforme : au
quotidien 0%, plusieurs fois par mois 40%, une fois par
mois 40% et une fois par an 20%. Pour les thèmes
d’utilisations, c’est réparti de manière égale entre les
BPO (27,2%), BPM (36,4%) et BPR (36,4%).
Pour l’utilisation
de l’outil d’autodiagnostic, tous les répondants utilisent
l’outil, mais de manières différentes en terme de
périodicité. Nous avons 20% qui l’utilisent
périodiquement, plusieurs fois par an, 40% périodiquement,
une fois par an, 40% périodiquement, une fois tous les
deux ans et 0% qui l’utilisent aléatoirement.
Pour les résultats
de l’outil, nous avons 80% des réponses qui pensent
partager les résultats et 20% ne le feront surement pas.
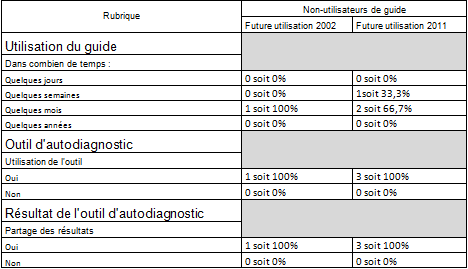
Les non utilisateurs des guides
Nous avons 10
réponses qui n’utilisent pas de guides. Parmi ces 10
réponse seulement 4 pensent utiliser un des deux guides
prochainement, soit 40%, 3 pour le guide 2011 et seulement
1 réponses pour utiliser le guide 2002.
Les futurs
utilisateurs du guide version 2002 possédant une seul
réponse, les informations extraites ne sont d’aucune
pertinence.
Pour les futurs
utilisateurs du guide version 2011, une réponse pense
l’utiliser dans quelques semaines et les deux autres dans
quelques mois. Les trois réponses pensent utiliser l’outil
d’autodiagnostic et partager les réponses.
Utilisation des
guides :
La présente
enquête a permis d’apprécier l’utilisation des différents
guides ainsi que leur outil d’autodiagnostic à l’heure
actuelle.
On remarque que se
soit des utilisateurs d’un seul guide ou des deux guides
simultanément, l’utilisation reste uniforme tant en terme
de fréquence que de thématique, excepté les usagers
uniques du guide 2011, qui voient une forte préférence
d’une utilisation moins régulière. Ceci nous indique que
l’utilisation plus régulière du guide est plutôt difficile
par les acteurs biomédicaux.
Utilisation de
l’outil d’autodiagnostic :
L’outil
d’autodiagnostic possède une utilisation quasi-totale pour
tous les différents types d’utilisateurs. Cet outil se
révèle plutôt convainquant auprès des utilisateurs avec
des retours plutôt favorables. La grande suggestion qui
revient sur les différents outils d’autodiagnostic est
qu’il gagnerait à être moins complet, pour éviter le
découragement et certaines redondances repérées. De plus,
une autre suggestion qui est très pertinente est de mettre
l’outil d’autodiagnostic sous forme de logiciel pour une
convivialité plus importante.
Les résultats de l’outil
d’autodiagnostic :
Le premier point
critique, que révèle cette enquête, est le partage des
résultats de l’outil d’autodiagnostic. Pour la version
2002 seulement 25% ont partagés les résultats pour raison
de manque de temps. En effet, les utilisateurs par manque
de temps (majoritairement 67%) ne pensent pas à partager
les résultats.
Il est donc
pensable, comme dit précédemment, dans la partie pour
l’outil d’autodiagnostic, qu’il serait bénéfique de rendre
cet outil plus concis et plus simple d’envoi (format
logiciel plutôt qu’Excel). Cela permettrait un benchmark
plus exhaustif et plus représentatif des différents
services biomédicaux.
Les futurs
utilisateurs des guides :
Le faible
pourcentage, de la future utilisation des guides, tend à
montrer qu’il existe des freins à leurs utilisations.
Les différents
freins révélés sont :
· Manque d’effectif
(dans la plus part des cas) ;
· Donner une priorité
à la certification ISO 9001, n’exigeant pas l’utilisation
du guide des bonnes pratiques ;
· Non
connaissance ou le non présence du guide dans les services
Biomédicaux.
Très peu de temps est passé entre le moment
d’envoi et le traitement des résultats. En une semaine les
réponses reçues ne représentent que 14% (30 retours pour
214 envois). La fin d’année est cette période, qui est
généralement réservée au bilan de l’exercice de l’année en
cours. Ce qui laisse à penser que les personnes
interrogées étaient assez occupées.
L’équipe projet continuera à relancer les
services biomédicaux dans le cas de non réponse jusqu’à
atteindre un échantillon représentatif (au moins 84
réponses).
Deux des membres de l’équipe continuent en
QPO12. Ça sera l’occasion pour, d’une part continuer la
collecte et le traitement des réponses au questionnaire,
et d’autre part communiquer les résultats obtenus.
L’écriture d’un article fait partie de la compagne de
communication prévue qui aura pour objectif l’information
des acteurs biomédicaux, à grande échelle, des résultats
de l’enquête à laquelle ils ont participée et promouvoir
l’utilisation des documents de bonnes pratiques en
ingénierie biomédicale (guides et outils
d’autodiagnostic).
En parallèle à ce projet, un groupe de
collègue (groupe 1) ont travaillé sur un autre thème
toujours dans le périmètre d’activité biomédicale ;
« management de la maintenance des DM selon la norme
NF S99-170 » durant lequel ils étaient amenés à
envoyer, à leur tour, un questionnaire afin d’apprécier
l’intérêt de l’usage d’une norme spécifique à la
maintenance biomédicale. Parmi les retours qu’ils ont
reçus, les répondants affirment exploiter le guide des
BPIB pour son caractère introductif des normes
internationales dans sa conception. Il est envisagé
d’intégrer ces résultats à la conclusion de connaissance
des documents de BPIB.
Les documents de bonnes pratiques en ingénierie
biomédicales V2011 (guide et outils d’autodiagnostic) sont
des documents de travail directement applicables à la
pratique quotidienne d’un service biomédical. Elaborés
suivant une logique de référentiels internationaux
rassemblant les principes de management, d’organisation et
de réalisation, ils y joignent autant la pratique métier
qu’un ensemble d’activités connexes (accueil stagiaire,
radioprotection,…). L’outil d’autodiagnostic reprend les
critères de réalisation de chaque bonne pratique du guide
et lui confère un niveau de maturité définissable en
fonction des réponses associées. Lors d’un exercice, un
questionnement est surgit : « pourquoi ne pas
intégrer les indicateurs d’efficacité, d’efficience et
qualité perçue directement dans la conception du
guide ? ». Au lieu de répondre en tenant en
compte des niveaux de maturité, s’auto évaluer directement
par les indicateurs de performance proposés dans le guide. Cela pourrait
faire l’objet d’une étude prochaine, toujours dans une
perspective d’amélioration continue de BPIB.
Ce premier projet de bilan des BPIB v2011, est
réalisé après 2 ans de présence des documents dans les
services biomédicaux. Des actions similaires pourraient
être envisagées périodiquement à l’occasion d’autres
retours d’expérience.
Pour conclure sur les résultats de cette
enquête, les quelques retours reçus ne permettent pas de
tirer un enseignement quant à l’utilisation réelle des
guides et de leur outil d’autodiagnostic. En effet, un si
faible pourcentage de réponse n’est pas assez
caractéristique de la population ciblée.
De plus, lors de l’exploitation des résultats
deux points critiques ont été remarqués. Le premier est le
manque d’une question sur l’envoi des résultats de l’outil
d’autodiagnostic du guide version 2011. Cette question
aurait permis de voir la tendance de la diffusion ou non
de leur résultats, prochainement.
Le deuxième point est une information à extraire pour les
personnes utilisant à la fois le guide version 2011 et le
2002. La redondance est à la fin du questionnaire sur le
guide version 2002 où ils sont renvoyés vers l’utilisation
future du guide 2011.
Malgré cela les bonnes informations ont pu être
exploitées, en triant les données dans le tableur Excel.
D’autre part, la nouveauté apportée par le guide
2011 est essentiellement la notion de management et
d’organisation de la pratique. Dans un environnement
technique à la base, œuvrant pour des résultats
opérationnels sur les DM, cela pourrait demander un
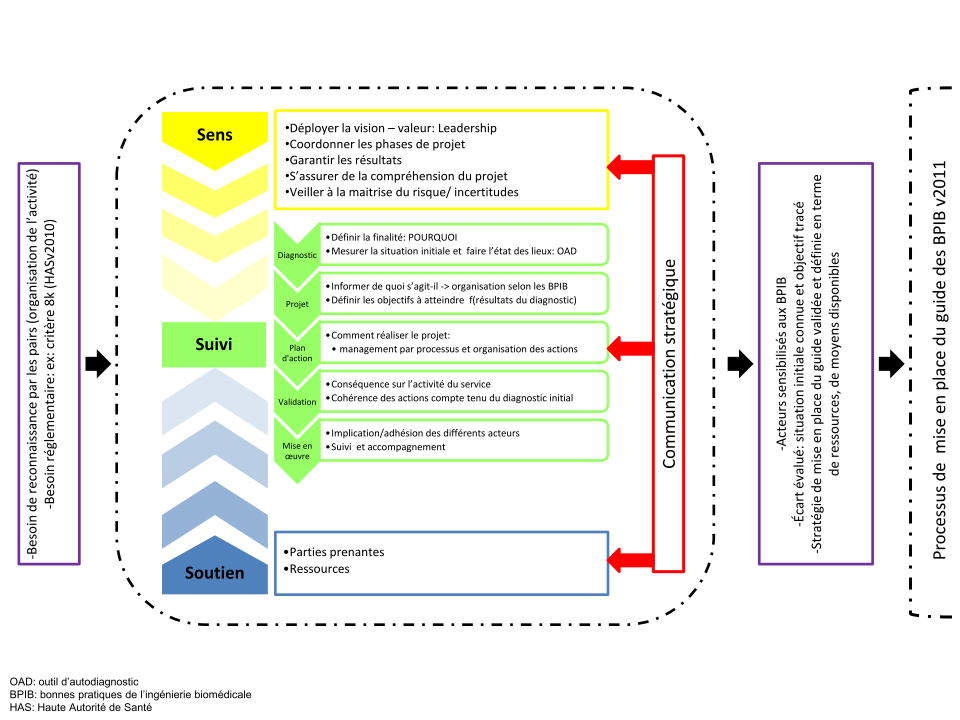
certain temps pour s’imprégner dans la pratique. Une phase
d’avant projet de mise en place des bonnes pratiques
pourrait être essentielle dans une démarche
d’accompagnement en conduite de changement
(en annexe Figure 8: proposition de mise
en place des BPIB). [23]
[1] Légifrance, « Loi n° 91-748 du 31 juillet 1991
portant réforme hospitalière ». 02-août-1996.
[2] Légifrance, Arrêté du 3 octobre 1995 relatif aux
modalités d’utilisation et de contrôle des matériels et
dispositifs médicaux. .
[3] Texte réglementaire, « Décret n°2001-1154
relatif à l’obligation de maintenance et au contrôle de
qualité des dispositifs médicaux prévus à l’article L.
5212-1 du code de la santé publique (troisième partie :
Décrets) ». Legifrance, www.legifrance.gouv.fr,
05-déc-2001.
[4] Texte réglementaire, « Décret n°2001-387 relatif
au contrôle des instruments de mesure ». Legifrance,
www.legifrance.gouv.fr, 03-mai-2001.
[5] Texte réglementaire, « Manuel de certification
des établissements de santé V2010 ». Ed Haute Autorité
de Santé, www.has-sante.fr, avr-2011.
[6] « Saga Web - NF ISO 26000 ». [En ligne].
Disponible sur: http://sagaweb.afnor.org/fr-FR/sw/Consultation/Xml/1280377?lng=fr.
[Consulté le: 26-nov-2013].
[7] Légifrance, « Ordonnance n° 96-346 du 24 avril
1996 portant réforme de l’hospitalisation publique et privée
| Legifrance ». [En ligne]. Disponible sur: http://www.legifrance.gouv.fr/affichTexte.do?cidTexte=LEGITEXT000005620817&dateTexte=20100517.
[Consulté le: 26-nov-2013].
[8] « ISO 9004 – Gestion des performances durables
d’un organisme – Approche de management par la qualité -
Techniques de l’Ingénieur ». [En ligne]. Disponible
sur: http://www.techniques-ingenieur.fr/fiche-pratique/genie-industriel-th6/piloter-et-animer-la-qualite-dt34/iso-9004-gestion-des-performances-durables-d-un-organisme-approche-de-management-par-la-qualite-0382/.
[Consulté le: 26-nov-2013].
[9] G. Farges, S. Aguida, L. Ricaud, E. Germanicus, A.
Kwizera, E. Lemarchand, et T. Roblès, « Gestion des
équipements biomédicaux, selon le référentiel
HAS v2010 : impacts et outil
d’autodiagnostic », IRBM News, vol. 30, no 6, p. 3‑7, déc. 2009.
[10] A. Achmirowicz, P.-Y. Delobel, C. Kichenassamy-Appou,
et G. Farges, « Convergence des référentiels de qualité
et implications pour la fonction technique
biomédicale », ITBM-RBM News, vol. 26, no 5, p. 15‑17,
oct. 2005.
[11] G. Farges, « Premiers retours d’expérience du
« Guide des bonnes pratiques biomédicales en établissement
de santé », ITBM-RBM News, vol. 25, no 1, p. 5‑9, févr. 2004.
[12] G. Farges et al., Guide des bonnes pratiques
biomédicales en établissement de , édition 2002, ITBM
RBM News., vol. 23, supll. 2 vol. Elsevier, 2002.
[13] H. Jacquemoud, L. Garet, et D. Gouillon,
« Retour d’expérience sur la mise en place du Guide des
bonnes pratiques en ingénierie biomédicale pour les
établissements de santé “version 2011” », IRBM News,
vol. 34, no 5‑6, p. 144‑149, oct. 2013.
[14] G. Farges, « Enseignements 2003-2008 et projet
v2010 du Guide des bonnes pratiques biomédicales en
établissement de santé », IRBM News, vol. 29, no 6, p. 3‑9, nov. 2008.
[15] G. Farges, « Guide des bonnes pratiques
biomédicales : évolutions 2004-2007 et perspectives d’une
version 2 », IRBM News, vol. 28, no 4, p. 7‑12,
nov. 2007.
[16] A. Richard, A. Viollet, B. Hernandez, et G. Farges,
« Guide des bonnes pratiques biomédicales en
établissement de santé: Un outil qui atteint son
objectif? », ITBM-RBM News, vol. 26, no 3‑4, p. 28‑30, juin 2005.
[17] A. Bahi, V. Bonneton, M.-E. Cauffy-Akissi, H.
Gautier, et G. Farges, « Guide des bonnes pratiques
biomédicales version 2 : compatibilité, progressivité
et simplicité », IRBM News, vol. 31, no 4, p. 5‑10,
sept. 2010.
[18] PIPAM, « Dispositifs médicaux : diagnostic et
potentialités de
développement de la filière française dans la
concurrence internationale ». juin-2011. lien : ici
[19] G. Farges, « Guide des bonnes pratiques
biomédicales en établissement de santé : retours
d’expérience 2004 », ITBM-RBM News, vol. 26, no 3‑4,
p. 31‑34, juin 2005.
[20] G. Farges et al., Addenda 2013 au Guide 2011 des
bonnes pratiques de l’ingénierie biomédicale en
établissement de santé, Les Pratiques de la
Performance. Editions Lexitis,
www.lespratiquesdelaperformance.fr, 2013. lien
téléchargement : http://www.lespratiquesdelaperformance.fr/fr/addenda-2013-guide-2011-des-bonnes-pratiques-de-lingenierie-biomedicale-en-etablissement-de-sante.html
[21] mouvement Wallon pour la qualité, « Le
benchmarking, se comparer pour s’améliorer ». .
[22] « Le monde des études : construire un
questionnaire », 23-oct-2013. [En ligne]. Disponible
sur: http://lemondedesetudes.fr/tag/construire-un-questionnaire/.
[Consulté le: 23-oct-2013].
[23] Lucie GARET, « Mise en place du guide des bonnes
pratiques de l’ingénierie biomédicale & Procédures
d’achats en établissement de santé », Hospices Civils
de Lyon, Stage de fin d’études, Master Technologies et
Territoires de Santé (TTS), UTC, 2012-2013 TTS_01, 2013
2012.
[23] G.
Farges et al., Guide des bonnes pratiques de l’ingénierie
biomédicale en établissement de Santé , édition 2011.
[24] G. Penisson et FZ. Meskini,
Memoire d'intelligence methodologique : "Bilan des bonnes
pratiques en ingénierie biomédical. Téléchargeable en haut de page.