|
Avertissement |
Si vous arrivez
directement sur cette page, sachez que ce travail est un rapport
d'étudiants et doit être pris comme tel. Il peut donc
comporter des imperfections ou des imprécisions que le lecteur
doit admettre et donc supporter. Il a été
réalisé pendant la période de formation et
constitue avant-tout un travail de compilation bibliographique,
d'initiation et d'analyse sur des thématiques associées
aux technologies biomédicales. Nous
ne faisons aucun usage commercial et la duplication est libre. Si vous
avez des raisons de contester ce droit d'usage, merci de nous en faire part .
L'objectif de la présentation sur le Web est de
permettre l'accès à l'information et d'augmenter ainsi
les échanges professionnels. En cas d'usage du document,
n'oubliez pas de le citer comme source bibliographique. Bonne
lecture... |
Elaboration des nouveaux contenus du Guide des
Bonnes Pratiques Biomédicales pour sa Version 2010
|

Olivier
BELAVAL |

Yao
Claudin BOHOUSSOU |
|

Hervé
FALAISE
|
Référence
bibliographique à rappeler pour tout usage :
Elaboration des nouveaux
contenus du
Guide des Bonnes Pratiques Biomédicales pour sa Version 2010,
Belaval Olivier - Bohoussou Yao Claudin- Burat Patrick - Falaise
Hervé,
Projet d'intégration, Certification Professionnelle
TSIBH, UTC, 2009, URL : http://www.utc.fr/tsibh
; Université de
Technologie de Compiègne |
|
RESUME
Les
bonnes pratiques biomédicales jouent un rôle important
au sein du service biomédical car la qualité du savoir
faire des acteurs
biomédicaux contribue à améliorer le niveau des
soins apportés aux patients.
L’évolution du guide des bonnes pratiques vers sa version 2
passe par la
compatibilité avec le critère 8k de l’HAS v2010 et de
l’ISO 9001, mais aussi
par l’identification des ressources matérielles et
immatérielles.
Cela,
pour permettre une mise en place plus efficiente du
Guide des Bonnes Pratiques orienté vers l’internationalisation
et une mise en
commun des ressources.
Mots
clés : Guide
des bonnes pratiques biomédicales (GBPB),
HAS v2010 critère 8k, ISO 9001, ressources.
|
|
ABSTRACT
Good biomedical
practices in healthcare institutions play an important role in the biomedical
service, since the quality of work done by biomedical actors to equipment,
contribute to
improve clinical actions to patients. The development of good practice
guide to
version 2 will be compatible with the criterion 8k HAS v2010 and ISO
9001, but
also by the identification of the material and immaterial resources.
This, to enable a more efficient in the Guide of Good
Practices oriented
towards internationalization and a pooling of resources.
Key words: Guide of the good biomedical practices (GBPB), HAS
v2010 8k criterion, ISO 9001, resources.
|
Remerciements
Nous
tenons à remercier les
personnes suivantes, pour leurs aides apportées à la
réalisation de ce
projet :
- Notre
tuteur de projet d’intégration M. Gilbert
FARGES, enseignant chercheur, responsable de la formation TSIBH
(Technicien
Supérieur en Ingénierie Biomédicale
Hospitalière) à l’UTC (Université
Technologique de Compiègne).
- M.
Pol Manoël FELAN, responsable pédagogique de
la formation TSBIH à l’UTC
- Mme
Isabelle NATTIER
pour sa sympathie, son accueil et son professionnalisme en ce
qui
concerne les points logistiques et administratifs.
- A
l’ensemble de l’équipe, des intervenants et
tous les centres hospitaliers qui ont bien voulu répondre
à notre enquête, ce
qui nous a permis de mener à bien notre projet.
Sommaire
1
Description de la
situation
1.1
Bilan de la situation
actuelle
1.1.1 Actions
entreprises pour l’amélioration
du
GBPB
1.1.2 Retour
des grilles
d’autoévaluations
1.1.3
Autodiagnostics
comparés
1.1.4
Conclusion
2
Contexte
2.1 La
HAS
2.1.1
Statut de la
HAS
2.1.2
Rôle de
l’HAS
2.2
L’ISO
2.2.1
Découvrez
l'ISO
2.2.2 Le rôle des
normes
2.2.3 Certification ISO
9001 :
2008
2.3
Conclusion
3
Enjeu
4
Démarche
5 Analyse des
résultats de
l’enquête
6
Propositions de
Ressources
7 Conclusion et
perspective
d’avenir
BIBLIOGRAPHIE
GLOSSAIRE
Annexes
1.
DESCRIPTION DE LA SITUATION
La
première version du Guide des Bonnes Pratiques
Biomédicales [1], publiée en novembre 2002, a
été réalisée dans un esprit
d’accompagnement progressif à l’amélioration quotidienne
des pratiques biomédicales dans les établissements de
santé.
Celui-ci regroupait les bonnes
pratiques et l’état de l’art dans le domaine du
biomédical.
Nombreux service biomédicaux se sont alors lancés
dans l’application de ce guide.
La démarche qualité
des services biomédicaux s’impose à l’ensemble des
hôpitaux comme un passage obligé vers une certification
ISO 9001[2], mais est aussi une bonne préparation à la
certification de l’HAS v2010.
En effet, dans ce nouveau manuel
de certification, la gestion des équipements
biomédicaux fait son apparition (critère 8k).
Fig.1 Critère issue du manuel de certification de l’HAS [3]
Le Guide des Bonnes Pratiques
Biomédicales a fait des
émules et traversé nos frontières et même
l’atlantique. En effet l’adaptation du guide au Québec [4] et en
Suisse [5] ouvre une voie pour l’uniformisation de la pratique
biomédicale.
Cette nouvelle mouture doit « s’ouvrir
à l’international
» afin de permettre aux différents acteurs du
biomédical de pouvoir échanger par l’intermédiaire
du réseau ouvert de cette nouvelle ère qu’est l’Internet,
et qui permet au monde actuel une diffusion instantanée du
savoir et de l’information.
Ne plus être seul, voilà un nouveau
challenge à
relever, que l’on soit en CHU en France, dans un dispensaire en Afrique
ou une clinique du Canada. Grâce à un site interactif
compatible WEB 2.0, les biomédicaux pourront échanger,
comparer, communiquer…
Dans ce
contexte une évolution du Guide des Bonnes Pratiques
Biomédicales semble naturelle.
Ce guide sera
à usage progressif en 3 parties
(Réalisation, organisation et Management).
Ce qui
permettra aux
services biomédicaux une mise en place simplifiée
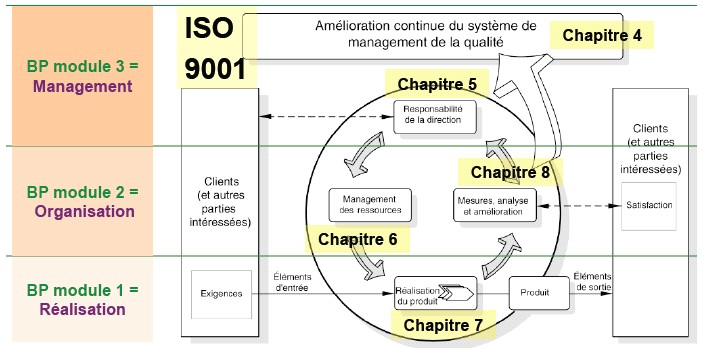
Fig.2 Proposition de nouvelle organisation du Guide des Bonnes Pratiques
(Source
: Présentation 2008 Aamb_Pau Bilans 2003-2008 et Enseignements pour
une Version 2 du Guide des Bonnes Pratiques Biomédicales (par G. Farges)
Cette nouvelle version sera interactive, flexible, évolutive et
doit générer une dynamique de progrès.
Tout cela dans
le but d’être acteur dans la vaste chaîne
que représentent les soins, tout en gardant à l’esprit
qu’à l’extrémité se trouve le patient.
1.1 Bilan de la
version
actuelle (Source : « Mr Gilbert
Farges - Journées Aamb - Pau :
Présentation » )
1.1.1-Actions entreprises pour l’amélioration
du GBPB
La 1ère
édition du guide des bonnes pratiques est parue
en novembre 2002 et fut
envoyée aux adhérents de l’Afib,
l’Aamb et de l’Atd permettant ainsi de faire connaître aux
acteurs biomédicaux le guide des bonnes pratiques.
Ouverture d’un site web
dédié aux bonnes pratiques en
avril 2003 (http://www.utc.fr/~farges/bonnes_pratiques/bpb.htm),
regroupant différentes informations utiles au guide et se
rapportant à la démarche qualité.
Une enquête
par mail fut réalisée en juillet 2003
et envoyée à 315
acteurs biomédicaux. L’analyse de
cette enquête fit apparaître que le guide des bonnes
pratiques biomédicales était bien perçu comme un
outil et qu’il était exploitable.
L’enquête a mis en évidence un besoin
pour des
autoévaluations et des audits interservices biomédicaux.
Suite à cette enquête une
grille d’autodiagnostic a
été réalisée et communiquée aux
acteurs biomédicaux en
février 2004. Cet outil est
important, il permet d’auto évaluer le service biomédical
par rapport aux bonnes pratiques mis en place. Cette grille met en
évidence les axes
d’amélioration possible du service
biomédical.
Suite à des accords avec l’éditeur en mai 2004, diffusion
gratuite sur le site web, du
guide des bonnes pratiques permettant une
information plus large des acteurs biomédicaux.
1.1.2-Retour
des grilles d’autoévaluations
En 2004,
donc 2 ans après la parution du GBPB, 22 hôpitaux (dont 3 sont ISO
9001) ont répondu partiellement ou en totalités aux
bonnes pratiques par le biais de la grille d’autodiagnostics.
En 2005 aucune grille
d’autoévaluations n’a été
retournée. Pas de retour
spontané des services biomédicaux ayant
répondus en 2004.
En 2006, une
initiative de 23 services biomédicaux de l’Assistance Publique
des Hôpitaux de Paris (APHP) ont permis de recenser des
informations. Comme en 2005 aucune relance des acteurs
biomédicaux n’a été effectuée.
En juillet
2007 sur 570
biomédicaux contactés, seul 41 grilles d’autoévaluations furent
retournées pour analyses. Sur ces 41 retours, 11 venaient de
l’international (9 du Québec, 1 Belgique et 1 en Cote d’ivoire).
En 2008, 607 acteurs biomédicaux ont
été sollicités et seulement
40 retours de grilles d’autodiagnostics. Dont 2 venant de
l’international (Luxembourg et Allemagne).
Sans stimulations de la part de
Mr Gilbert Farges, les services biomédicaux ne renvoient pas
spontanément les grilles d’autoévaluations.
Le guide des bonnes pratiques s’adaptent à des structures de
taille différente (CHU, CH, clinique et institut).
Le guide des bonnes pratiques s’internationalise, en effet il s’exporte
dans les pays francophones et Européen (Québec, Suisse,
Belgique, Luxembourg, Allemagne, …).
1.1.3-Autodiagnostics
comparés
a-
Autodiagnostic
des hôpitaux et cliniques
françaises sur 3 années.
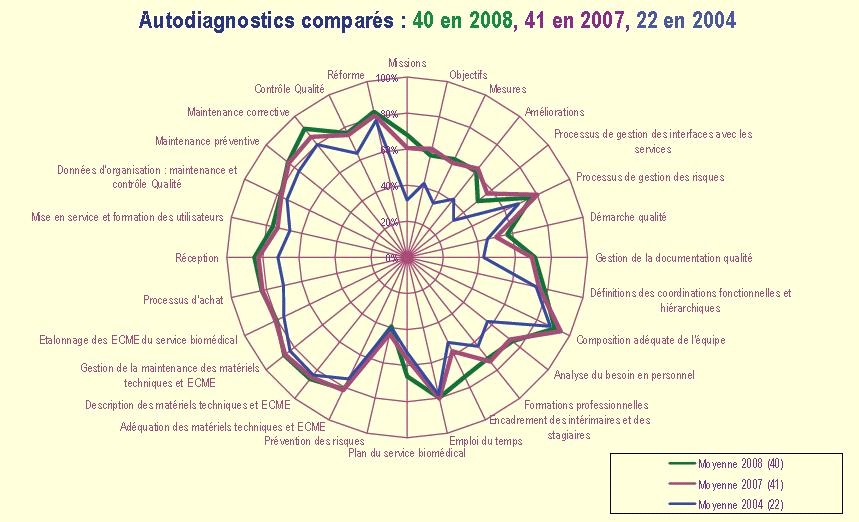
Source : « Mr Gilbert
Farges -
Journées Aamb - Pau :
Présentation »
b- Autodiagnostic comparé
service biomédical ISO 9001 et
non ISO
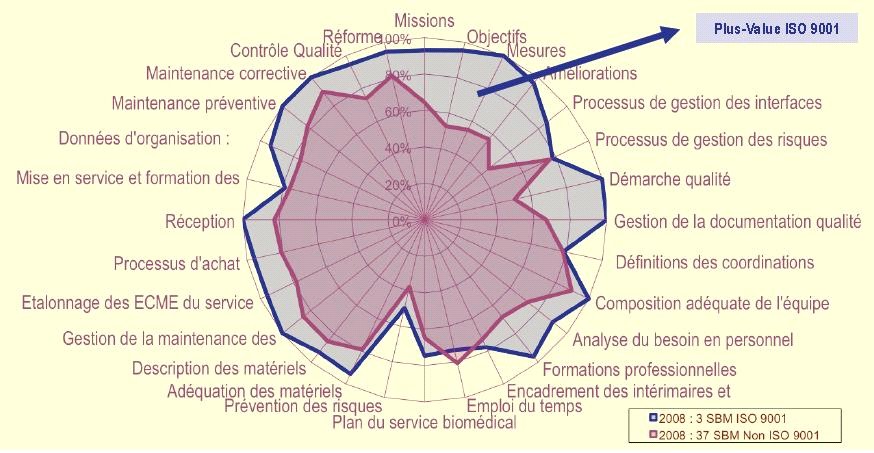
Source
: « Mr Gilbert Farges - Journées Aamb - Pau :
Présentation »
Il y a peu d’écart entre 2007 et 2008 sur le
premier autodiagnostic. Sur le second, une nette différence
entre les services biomédicaux ISO 9001 et les non ISO et l’on
peut voir une plus value sur toutes les bonnes pratiques.
1.1.4
Conclusion
Le bilan est plutôt positif, de nombreux services
biomédicaux se sont intéressé au guide des bonnes
pratiques et ceci dès sa parution. Ces services
biomédicaux ont participés à l’amélioration
du guide des bonnes pratiques ; ils ont mis en évidence ces
points forts et ses points faibles, permettant sont évolutions
permanentes.
L’intéressement des pays étrangers aux bonnes pratiques
et la plus value de la certification ISO 9001 peuvent être
bénéfiques pour l’évolution du guide des bonnes
pratiques biomédicales.
2. CONTEXTE
Les deux
certifications que sont l’HAS v2010 et l’ISO 9001, sont
aujourd’hui incontournables pour les services biomédicaux.
La première est un passage obligé que
doit franchir tout
établissement de santé, seul le critère 8k
concerne les dispositifs médicaux, la seconde est
facultative,
mais devient de plus en plus incontournable surtout en matière
de reconnaissance tant pour sa hiérarchie que pour ses pairs
extérieurs. Un grand nombre de services biomédicaux,
après avoir mis en place le Guide des Bonne Pratiques,
s’intéressent à la démarche ISO 9001.
C’est une
suite logique, mais qui soulève un bon nombre de question :
- Quand peut-on être certifié ?
- Existe-t-il une aide ?
- Combien de temps cela prendra t il ?
- De quel moyen je dispose ?
- Quels plus en rapport au GBPB
- A quel moment ?
Aussi convenait- il que la nouvelle version du GBPB intègre
ces
certifications. Du moins permettre un passage plus facile, plus fluide
grâce à des outils plus pertinents.
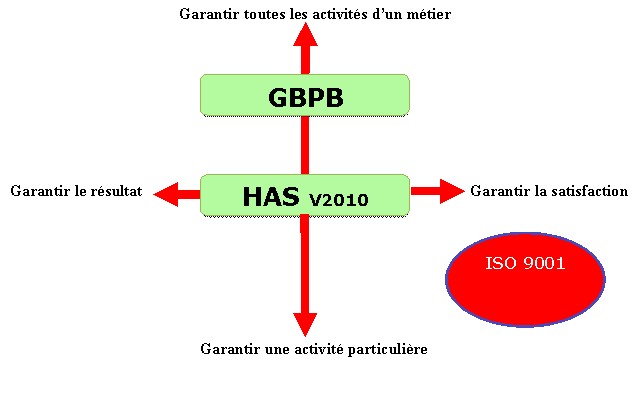
2.1
Présentation de
L’HAS et de L’ISO 9001
Voici une présentation très rapide et
succincte de l’HAS
v2010 et de l’ISO 9001, en vue d’une intégration future dans la
deuxième version du
guide.
2.1.1 Statut de la HAS
:
Autorité publique indépendante
à caractère
scientifique, dotée de la personnalité morale et
disposant de l’autonomie financière.
La certification des établissements de santé est un
dispositif évolutif. La certification, crée par
l’ordonnance d’avril 1996 sous le terme accréditation, a permis
de structurer les démarches Qualités dans les
établissements de santé.
Avec la 2ème version et l’apparition de l’évaluation des
pratiques professionnelles cela a permis notamment une plus grande
implication des médecins.
Enfin une dernière version « 2010 » est
apparue, elle a pour but de renforcer l’effet de la Qualité et
de la sécurité des soins, tout en réduisant
les contraintes formelles de la procédure elle-même.
Source : http://www.has-sante.fr
2.1.2
Rôle de l’HAS
La Haute Autorité de Santé (HAS) est
chargée :
- d’évaluer scientifiquement
l’intérêt médical des médicaments, des
dispositifs médicaux et des actes professionnels et de proposer
ou non leur remboursement par l’assurance maladie;
- de promouvoir les bonnes
pratiques et le bon
usage des soins auprès des professionnels de santé et des
usagers de santé;
- d’améliorer la
qualité des soins
dans les établissements de santé et en médecine de
ville;
- de veiller à la
qualité de
l’information médicale diffusée;
- d'informer les professionnels de
santé
et le grand public et d'améliorer la qualité de
l'information médicale;
- de développer la
concertation et la
collaboration avec les acteurs du système de santé en
France et à l'étranger.
2.2 L'ISO
2.2.1
Découvrez l'ISO
Les normes permettent de garantir certaines
caractéristiques des
produits et services, notamment la qualité, le respect de
l’environnement, la sécurité, la fiabilité,
l’efficacité et l'interchangeabilité - à un
coût économique.
Lorsque les produits, les systèmes, les machines et les
dispositifs fonctionnent bien, en toute sécurité - c'est
souvent parce qu’ils sont conformes à des normes. L'Organisation
responsable de milliers de normes dont bénéficie le monde
entier est l'ISO.
Lorsque les normes font défaut, nous ne tardons pas à le
constater.
2.2.2
Le rôle des normes
Les normes ISO:
- permettent de développer, fabriquer et
fournir des produits et services plus efficaces, plus sûrs et
plus propres
- facilitent le commerce entre les pays et le rendent
plus équitable
- fournissent aux gouvernements une base technique
pour la santé, la sécurité et la
législation relative à l’environnement, ainsi que
l’évaluation de la conformité
- assurent le partage des avancées
technologiques et des bonnes pratiques de gestion
- contribuent à diffuser l’innovation
- servent à protéger les consommateurs,
et les utilisateurs en général, de produits et services
- simplifient la vie en apportant des solutions aux
problèmes communs.
L’ISO n’est pas un organe de réglementation ou de
législation. Les normes ISO sont utiles partout dans le monde.
Source : http://www.iso.org/iso/fr/
2.2.3 Certification ISO 9001 :
2008
L’ISO 9001:2008 est une référence internationale en
matière de management de la qualité dans les relations
interentreprises.
Le système de management de la qualité (SMQ) est un outil
de management permettant à tout organisme le mettant en oeuvre
de :
- Répondre aux
exigences qualité de ses clients
- Répondre aux
exigences réglementaires applicables
- Améliorer la
satisfaction du client
- Réaliser une
amélioration continue de ses performances
La norme ISO 9001:2008 est une norme générique ; ceci
signifie qu’elle peut-être appliquée :
- A tout organisme, quel que soit sa taille, son
produit, ses services
- A tout secteur d'activité
- A tout type d’organisme qu'il soit une entreprise
industrielle ou
commerciale, une administration publique ou une association.
Source:
http://www.moody-certification.fr/
2.3 Conclusion
La mise en place d’une démarche
qualité est un projet global d’entreprise mobilisant l’ensemble
du personnel. Elle implique la définition d’une
«organisation qualité» s’intégrant et
s’articulant avec l’organisation existante.
3. LES
ENJEUX DU GUIDE v2010
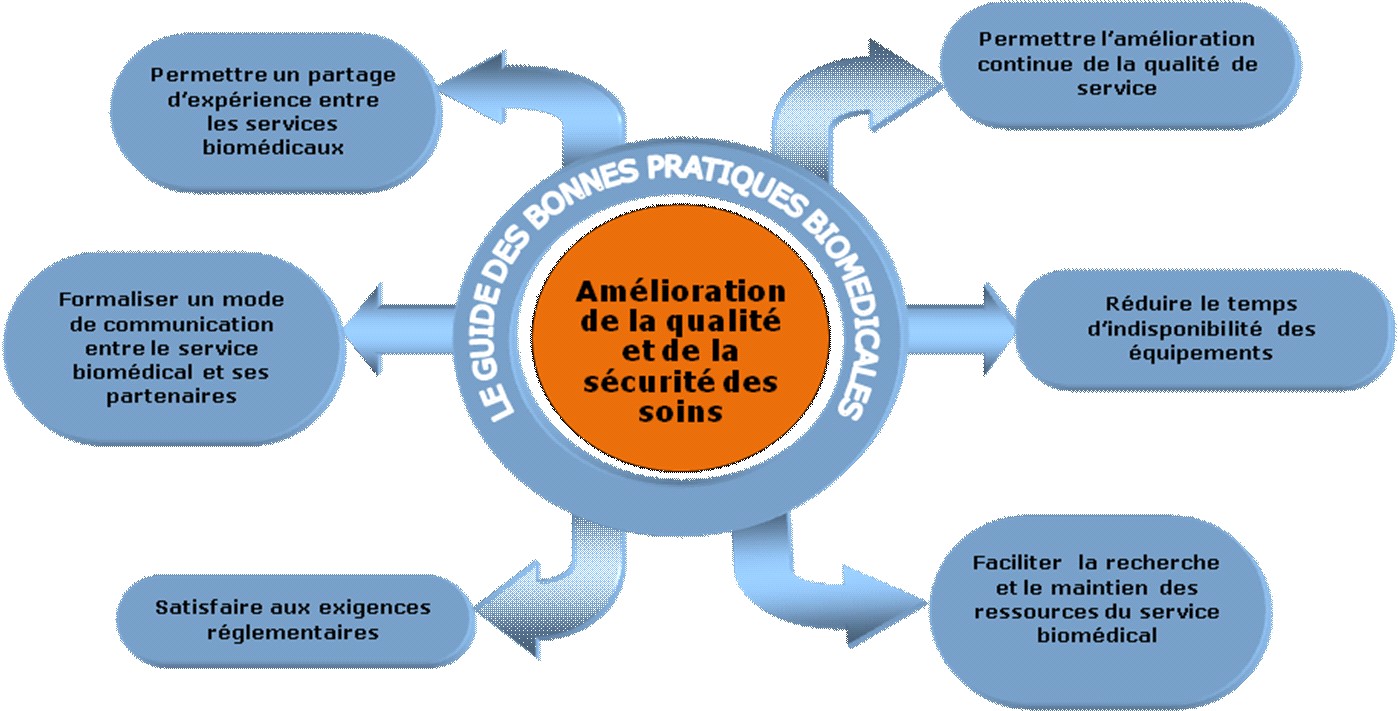
Le guide des bonnes pratiques
version 2010 se présente comme un
outil pratique, dynamique et progressif mis à la disposition des
acteurs biomédicaux pour les aider à optimiser leurs
activités quotidiennes et formaliser leurs
traçabilités.
Il prend en compte toutes les contraintes
juridiques, réglementaires, sécuritaires et
fonctionnelles des équipements biomédicaux mise
à la disposition de l’ensemble du personnel soignant.
Il met à disposition plusieurs procédures permettant :
- L’amélioration continue de
la
qualité de service
- La réduction du temps
d’indisponibilité des équipements
- La planification des actes de
maintenance et
de contrôle qualité
- La mise en place d’une politique
de formation
du personnel médical, soignant et médicotechnique
- La satisfaction aux exigences
réglementaire
- La formalisation du mode de
communication
entre les services biomédicaux et leurs partenaires
- La gestion des ressources
matérielle,
financière et humaine
-
Cette nouvelle version du Guide des Bonnes Pratiques
Biomédical
en établissement de santé, ce propose d’être aussi
un espace d’échange d’expérience entre les acteurs de
maintenance hospitalière. Un site interactif sera donc mise
à la disposition des acteurs biomédicaux sur Internet
pour faciliter ces échanges technologiques.
Le Guide des Bonnes Pratiques Biomédical, en facilitant la
gestion et la maintenance des équipements biomédicaux,
participe ainsi à l’amélioration de la qualité de
soin fourni aux patients.
4. DEMARCHE
Planification
Dynamique et stratégique
La
réalisation d’une planification dynamique et
stratégique, a permis d’identifier les étapes
nécessaires pour mener à terme notre projet.
Celui- ci regroupe les différentes phases précisent : les
missions, visions, objectifs, résultats et actions de
progrès de notre projet d’intégration.
Cela implique un certain nombre de contraintes :
-
Méconnaissance des pratiques
Biomédicales à l’étranger
- notion de
ressources assez vague.
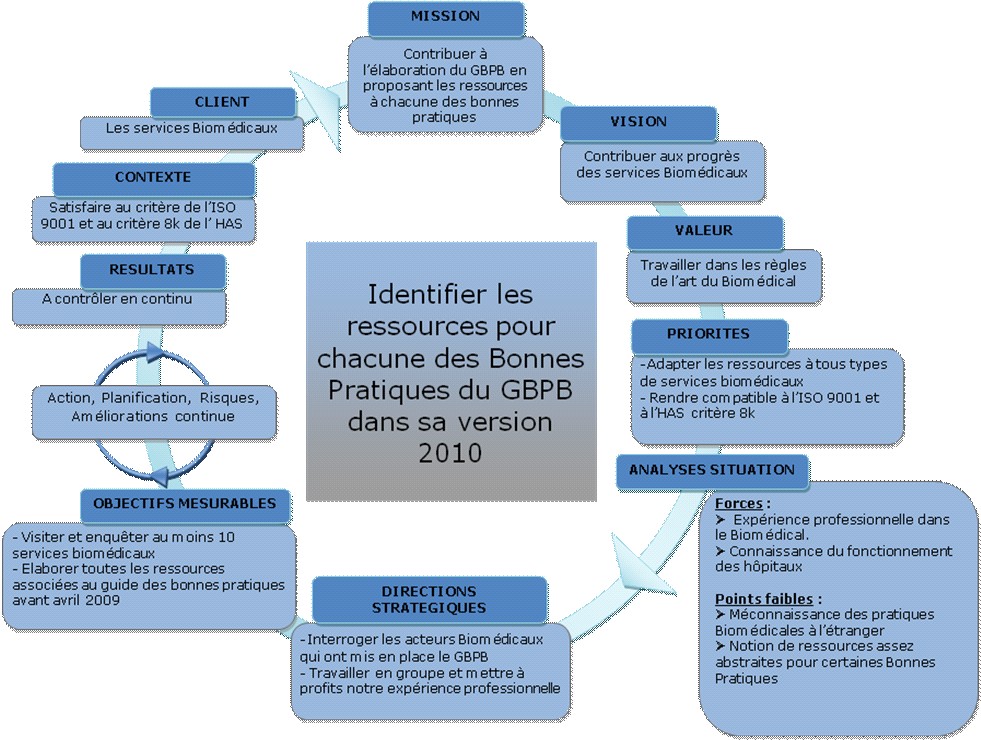
Déroulement de la démarche
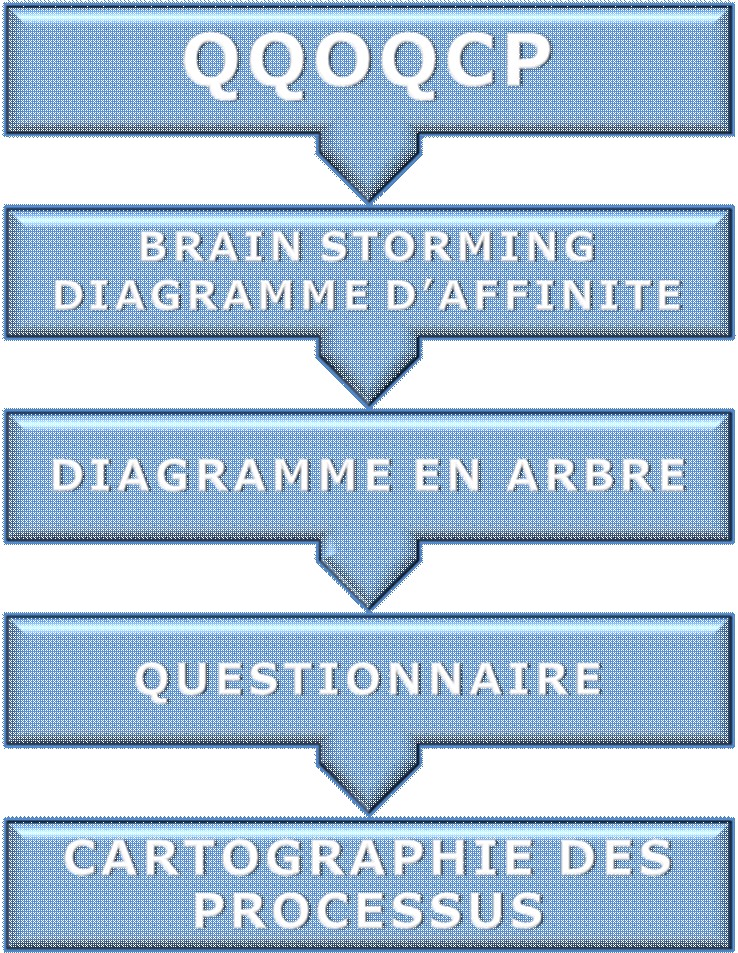
L’utilisation des outils de management
qualités a permis d’identifier deux grands axes
à explorer pour l’identification des ressources :
- Partager l’expérience
avec les services biomédicaux
- Analyser les Bonnes Pratiques
| Donnée
d'entrée : |
Difficulté
à l’identification des ressources des bonnes
pratiques du GBPB |
| Qui est concerné par le
problème? |
Les
Services Biomédicaux |
C'est quoi le problème ?
|
Identification des
ressources pour la V2 du GBPB...
|
Où apparaît le
problème ?
|
Début de la
démarche Qualité du service
|
| Quand apparaît le
problème ? |
Depuis
quelque mois avec le recul de la 1° version
|
| Comment mesurer le
problème et ses solutions ? |
Par la mise en place du guide |
| Pourquoi faut-il résoudre
ce problème ? |
Mise en place du guide
facilité et permettant l’intégration de l’ISO 9001
et de l’HAS ainsi que l’ouverture à l’international.
|
| Donnée
de sortie : |
Comment identifier les ressources
nécessaires aux bonnes
pratiques ?
|
Une rencontre a été décidée,
avec divers services biomédicaux (4 visites de
programmées dont 2 effectuées), acteurs sur le terrain et
professionnels qui ont mis en œuvres le GBPB, de manières
à :
- ciblés les difficultés
qu’ils ont rencontrées
- d’identifier les ressources
mobilisées pour la bonne application du guide.
Ses renseignements ont été
recueilli à l’aide d’un questionnaire un peu plus
détaillé que celui envoyé par mail , à un
panel d’acteurs biomédicaux ,ayant mis en place une
démarche qualité basé sur le guide des bonnes
pratiques.
D’autre part le questionnaire a été posté sur le
forum du site Internet « Technologies
Biomédicales.com » afin de toucher un maximum d’acteurs
biomédicaux impliqués dans une démarche
qualité.
La synthèse de ces questionnaires a permis de cerner, au mieux,
les besoins des services biomédicaux et faciliter la mise
en place des ressources nécessaires pour les Bonnes Pratiques
qu’elle soit d’Organisation (BPO), de Réalisation (BPR) ou de
Management (BPM).
Cartographie des processus
L’utilisation de cet outil qualité,
appliquée à toutes les bonnes pratiques, a
facilitée l’identification des ressources nécessaires au
guide des bonnes pratique s.
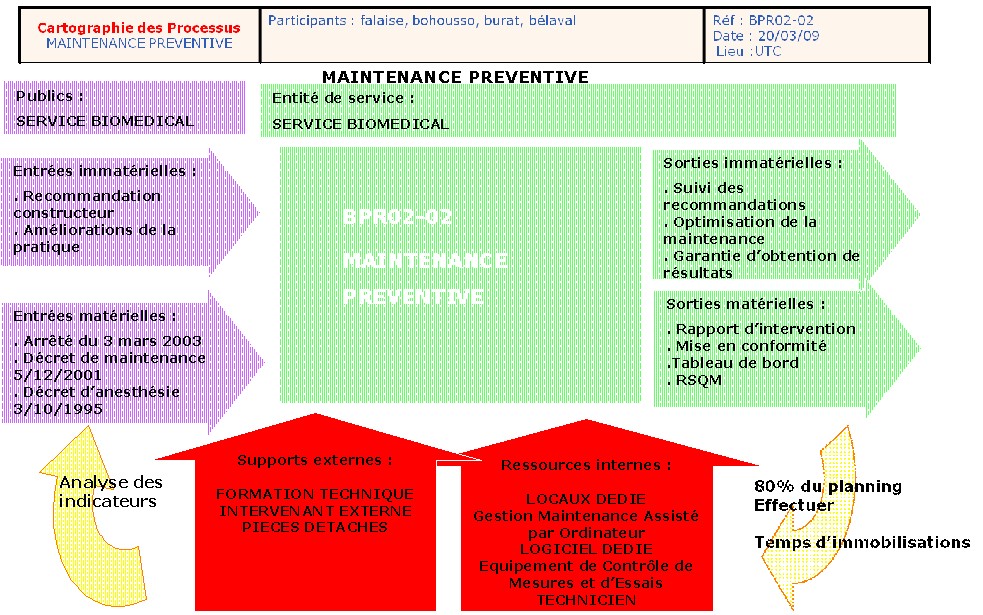
5.
ANALYSE DES RESULTATS DE L’ENQUÊTE
Pourquoi
ce questionnaire ? (annexe 1 et 2)
Ce
questionnaire confirmera la nécessitée de faire
apparaître un paragraphe « ressources nécessaires
» et de lister ces ressources pour chaque bonnes pratiques du
GBPB v2010
| L’identification des
ressources a été un facteur tempsimportants dans la mise
en place du guide Version 1. Cela permettra d’affirmer que si les
ressources
principales sont déjà listées
dans le GBPB v2010, la mise en
place sera facilitée et surtout un gain de temps dans
l’application de celui-ci. |
Questions
posées 1,3 et 5
|
Connaitre la difficulté des
services biomédicaux à recenser les ressources et les
moyens mis en œuvre pour les identifier.
|
Questions
posées 2et 4 |
Synthèse de l’enquête et des visites :
- 80 mails ont été envoyés aux
différents services biomédicaux qui ont mis en place le
guide des bonnes pratiques et qui ont répondu à la
cartographie radars depuis 2002.
- 15 adresses n’étaient plus
d’actualités soit 19% des mails envoyés.
- 12 questionnaires nous ont été
retournés soit 15% des mails envoyés.
- 8 questionnaires sont exploitables soit 10% des
mails envoyés.
- 53 mails sont sans réponse soit 66% des
mails envoyés
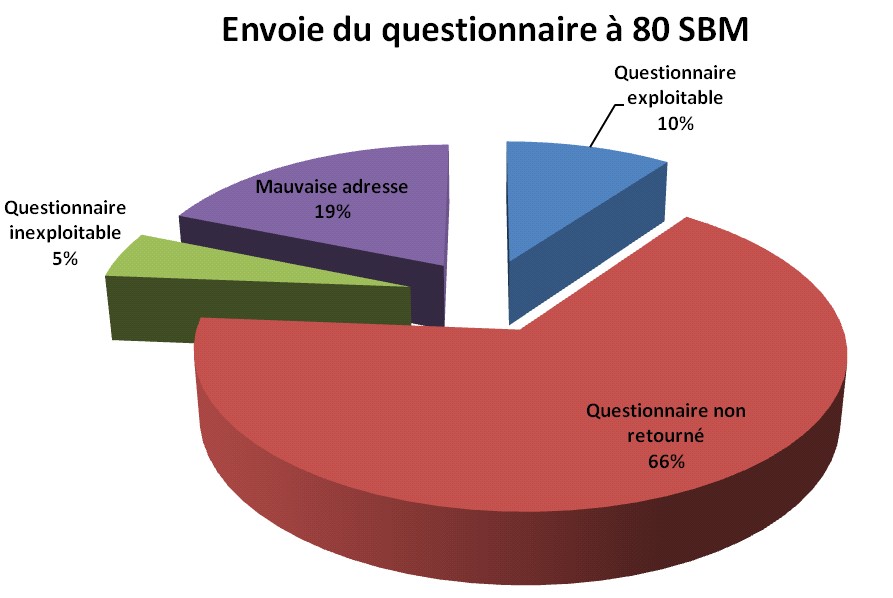
Synthèse des réponses
exploitables
|
|
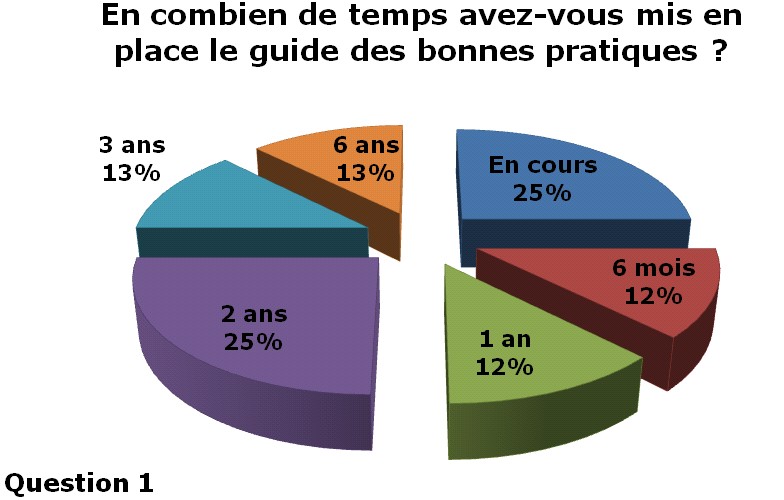
La durée de mise en place
du guide des bonnes pratiques diffère selon les services
Biomédicaux,
en effet elle s’échelonne entre 6mois et 6ans
|
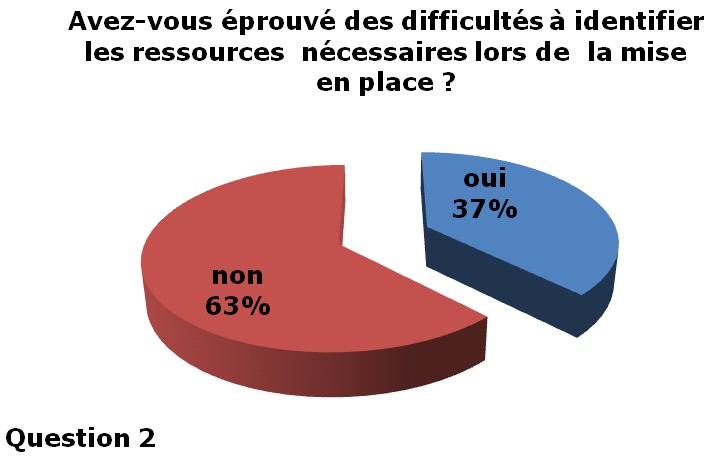
63% des services
intérrogés n’ont pas éprouvés de
difficultées à identifier les ressources
|
|
|
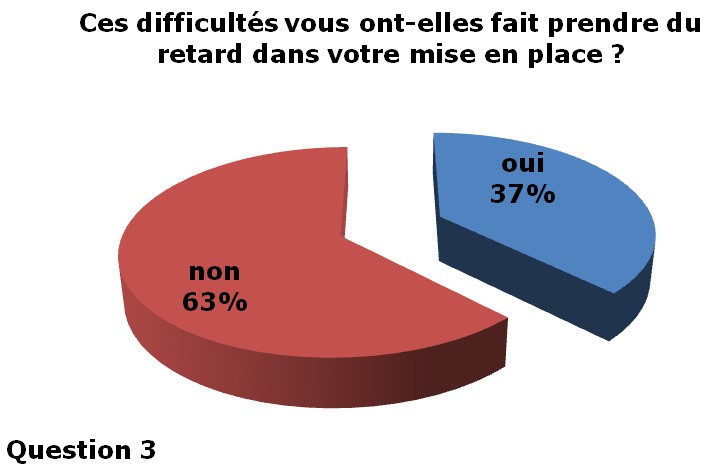
37% ont pris du retard du
à l’identification des ressources
|
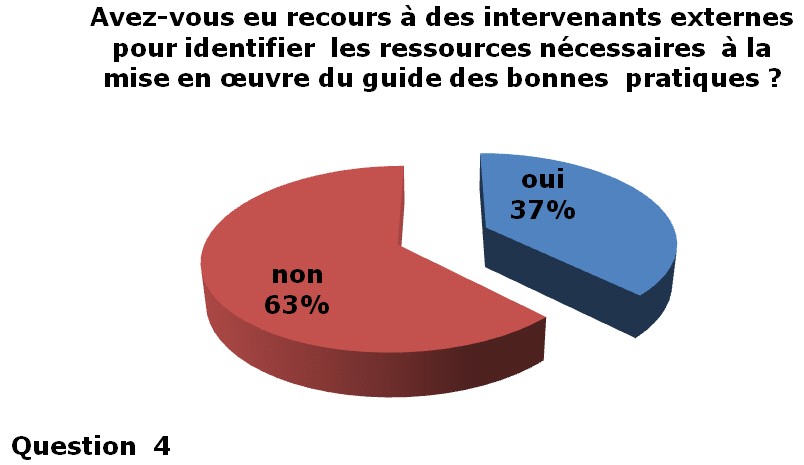
63% des services
biomédicaux intérrogés n’ont pas
eu recours
à d’autres intervenants pour l’identification des
ressources. |
|
|
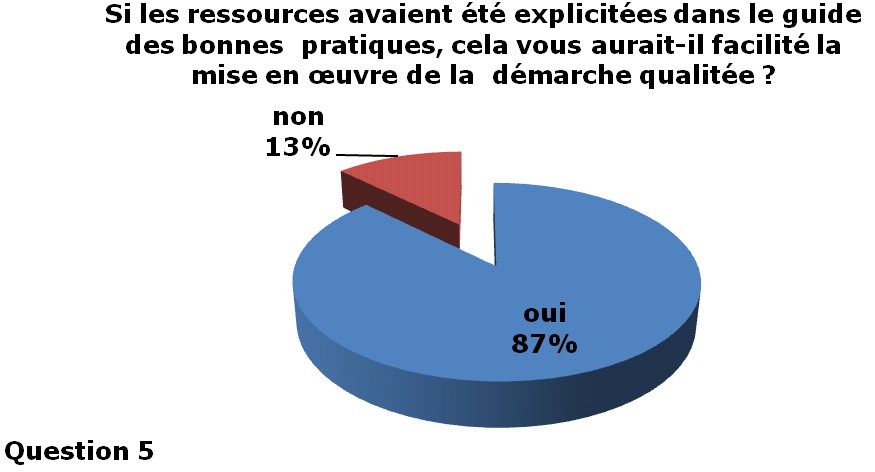
La majorité des services
biomédicaux interrogés (87%) pensent que la mise en place
du guide
des bonnes pratiques aurait été facilitée si
les ressources avaient été explicitées.
|
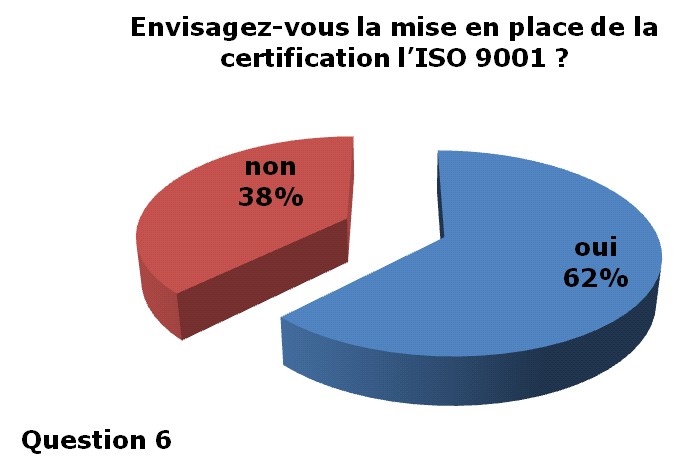
62% des services
biomédicaux envisagent la
certification ISO 9001. |
Le questionnaire posté sur le
forum du site
www.technologies-biomedicales.com a été consulté
146 fois (au 01/04/2009).
Une seule réponse nous a
été retournée.
CH A :
Entretien avec Mr X, ingénieur biomédical
La mise en place du guide s’est effectuée à moyen
constant, en parfaite intégration dans le travail quotidien.
L’interaction entre services a été très bonne,
aucun blocage, très bonne participations des acteurs, et
beaucoup de communications. La réflexion du départ c’est
basé sur le fait de mettre le guide en place avec les moyens
dont ils ont disposés.
Différence de moyens entre niveaux de ressources et besoin en
ressources.
Pour être bon et organisé, un service biomédical
doit avoir le GBPB. Cela peut permettre à la structure de ne
plus avoir de signe négatif, donc des pertes financières.
Notion importante, les ressources dépendent de ce que l’on
maintient. Difficile de les généralisé à un
ensemble d’établissement. De plus le recensement des ressources
n’est valable qu’à un instant T. Cela ne peut pas être
établis à l’avance sur du long terme, car
l’évolution est rapide et permanente.
L’ISO 9001 doit intégrer la Direction de l’établissement
et déboucher sur un CONTRAT D’OBJECTIF ET DE MOYEN. Cela permet
de faire une cartographie de l’activité. Tenir compte de la
gestion des risques de façon à prioriser la maintenance.
Si un DM n’a pas été vérifié le signaler
à la DDASS.
CH B : Entretien avec Mr Y, ingénieur
biomédical
Recensement des ressources :
Humain/local : établissement d’un
ratio surface/technicien et technicien/nbre d’équipements. De
quels moyens disposent l’agent pour travailler (local et niveaux de
formation) Positionner son métier/autres CH, participé
à des rencontres régionales régulières.
La DRH de l’établissement doit avoir une position claire pour
défendre et encourager le cursus biomédical.
Notion de biomécanique, nous abordons le sujet car au CH B des agents
sont appelés « biomécaniques »,
ils ont en charge la maintenance des lits, table d’opérations,
voir CQ de perfusions. Un technicien supérieur serait plus
employé sur du matériel d’imagerie, échographie,
etc.…..
Deuxième notion abordée, l’équipement : Cela
induit une remarque, la seule partie biomédicale commune aux
établissements est la perfusion, que l’on retrouve partout qui
est de classe 2b qui est fragile et qui fait l’objet de correctif
régulier.
Le
monitorage est la deuxième classification d’appareils communs.
Troisième notions abordés la communication :
Définition de l’urgence, rien en soit n’est urgent, exemple un
pousse seringue en panne n’a pas de caractère urgent, en
revanche faire passer l’information comme quoi le DM est
inopérationnel est primordial. Il y a trop de « pollution
» due à l’urgence, un agent doit arrêter son CQ
parce qu’il est déranger par un appel téléphonique
d’un service et la demande est urgente. En fait son CQ est prioritaire.
Communication également avec la GMAO, qui est un fournisseur
d’indicateurs économiques.
Relation avec les services administratifs, réelle mais mal
définis.
En conclusion, les intervenants ne sont pas contre une aide mais il
faut tenir compte des moyens (humains, financiers, technique) dont
chacun dispose pour mettre le GBPB en place. La direction doit
être partie prenante du projet. Il doit être
rédigé un Contrat d’objectif et de moyens. La formation
est une partie également très importante du service
biomédical, à la fois niveau de formation au recrutement
mais aussi niveau de formation interne à acquérir.
Le métier évolue, un technicien fait et fera de plus en
plus de procédures et de contrôle.
La communication revient aussi très souvent durant nos
échanges, elle occupe une grande place dans nos activités
et cela à tous les niveaux.
Serait- il souhaitable d’établir des ratios ? Par exemple
humains/local ; humains/nombre de DM ; maintenance/formation.
L’identification des ressources est une aide incontestable à
l’application du GBPB, mais il ne faut pas s’y focaliser, cela doit
être une aide et non pas une contrainte.
Conclusion :
Les services biomédicaux
n’éprouvent pas de
difficultés à identifier les ressources, mais ne
sont pas contre une aide. L’identification de ces ressources ne leurs
fait pas prendre de retard dans la mise en place du guide. Beaucoup de
services interrogés envisagent la certification ISO 9001.
Nous sommes
étonnés du peu de réponses de la part
des professionnels.
6.
IDENTIFICATION DES RESSOURCES
Sur la base des travaux des
étudiants en MASTER, nous proposons
une évolution de l’item « Ressources Nécessaires
». En effet il nous parait important de détailler cet item
en quatre parties bien distinctes.
Une première partie (a.) identifier sous l’appellation «
Générique » regroupant l’ensemble des ressources
non spécifique et nécessaire au déroulement de la
bonne pratique.
La seconde (b.) rassemble les ressources spécifiques à la
« Communauté Européenne » (ex : Code des
Marchés Publics).
Une troisième partie (c.) regroupe, qu’en a elle, les ressources
spécifiques à la « France » (ex :
Arrêté du 3 mars 2003).
Et enfin la quatrième partie (d.) « Autre pays »
rassemble les ressources spécifiques d’autre Pays, soit
Européen ou international.
Pour faire vivre cet item il est important que la communauté
biomédicale s’implique et fasse évoluer cet item et plus
généralement, qu’elle fasse évoluer le guide des
bonnes pratiques biomédicales. La capitalisation de ces
informations pourrait ce faire par le biais du site internet. Par un
système d’échange numérique, sous la forme d’une
base de données et d’un forum. Permettant l’échange
d’informations entre les acteurs biomédicaux. Ce travail reste
à faire et n’est pas développé dans notre projet
d’intégration.
Une fois les ressources
identifiées, nous les avons
classées par différentes catégories et suivant le
plan ci-dessous :

Ce modèle type est celui
utilisé dans la maquette du
nouveau Guide des Bonnes Pratiques.
A- Ressources nécessaires
Cette étape définit les ressources nécessaires ou
spécifiques à la bonne réalisation de la pratique.
Les ressources peuvent être matérielles (outils,
infrastructures, fournitures, documents) et/ou immatérielles
(compétences, informations).
a. Générique
- Ressources matérielles et
immatérielles nécessaires à la bonne pratique.
b. Communauté Européenne
- Ressources spécifiques à l’Europe
nécessaires à la bonne pratique (Ex : Normes, …)
c. France
- Ressources spécifiques à la France
nécessaire à la bonne pratique (Ex : Décrets,
arrêtés, …)
d. Autres pays
- Ressources spécifiques nécessaires
à chacun des pays appliquant le guide (Ex : Normes, …)
BPM : Bonnes Pratiques "Management"
Les ressources nécessaires aux bonnes Pratiques de «
Management » sont :
a. Générique
- Gestion de Maintenance Assistée par
Ordinateur (GMAO) ou système équivalent
- Logigrammes des différents processus du
service biomédical
- Documents de liaison avec les autres services
- Système
d’archivage de la documentation
b. Communauté Européenne
c. France
d. Autres pays
BPM 01 : Processus de gestion des
interfaces avec les services
Les ressources nécessaires au processus de gestion des
interfaces avec les services :
a. Générique
- Contrat de service
- Cahier de transmission de courrier
et d’informations
- Bons de demande de travaux
- Bons de travaux réalisés
- Planning de gestion
des activités
- Bon de demande d’achat
- Bon de livraison
- Logigramme décrivant les différents
processus
- Pod-cast des procédures d’utilisation des
équipements
- Gestion de Maintenance Assistée par
Ordinateur (GMAO) ou système équivalent
b. Communauté Européenne
c. France
d. Autres pays
BPM 02 : Processus de gestion d’une
coopération
biomédicale internationale
Les ressources nécessaires au processus de gestion d’une
coopération biomédicale internationale :
a. Générique
- Contrats de partenariat entre établissements
de santé
- Site d’échange sur Internet
- p od-cast des procédures
de maintenance
- Organisation de forum d’échange
technologique entre acteurs biomédicaux
b. France
- RSQM (faire suivre avec le dispositif
médical)
c. Communauté Européenne
d. Autres pays
BPM 03-01 : Processus de gestion
des
risques
Les ressources nécessaires au processus de gestion des risques
et de la qualité :
a. Générique
- Formation des utilisateurs aux bonnes pratiques
d’utilisation des équipements
- Planning de maintenance
et de contrôle
qualité des équipements biomédicaux
- Gestion
de Maintenance Assistée par
Ordinateur (GMAO) ou système équivalent
b. Communauté Européenne
c. France
- Textes de loi et réglementaire relatif
à la gestion des risques (France X PS 99-171)
- RSQM (Registre
de Sécurité, de
Qualité et de Maintenance)
- Matériovigilance : fiche
CERFA
- Détermination de la criticité des DM
(méthode PIEU ou AMDEC)
- Procédure dégradée de gestion
des équipements critique
d. Autres pays
BPM 03-02 : Processus de gestion de la
qualité
Les ressources nécessaires au processus de gestion de la
qualité sont :
a. Générique
- Une politique qualité.
- Un manuel qualité.
- Des documents qualités permettant la gestion
des activités du service biomédical.
- Audit périodique.
- Autoévaluation de la politique
qualité.
b. Communauté Européenne
c. France
d. Autres pays
Bonnes Pratiques
"Organisation" (BPO)
BPO 01 : Processus de
gestion du personnel
Les ressources nécessaires au processus de gestion du personnel
sont :
a. Générique
- Un service des ressources humaines existant.
- Une hiérarchie claire, et disponible,
organigramme du service.
- Des formations professionnelles
régulières. (Plan de formation).
- Fiche de poste des techniciens.
- Planning de gestion de taches (emploi du temps).
- Evaluation annuelle des agents.
- Réunion de service
hebdomadaire.
- Autoévaluation annuelle du service.
b. Communauté Européenne
c. France
d. Autres pays
BPO02 : Processus de gestion des locaux
Les ressources nécessaires au processus de gestion des
locaux
sont :
a. Générique
- Des locaux adaptés à
l’activité.
- Plan architectural du service.
- Identifications des zones dans le service. (Ex
: Zone de Maintenance, zone curative, zone de retour dans les
services, …).
b. Communauté Européenne
c. France
d. Autres pays
BPO 02-03 : Prévention des
risques pour le personnel au service
biomédical
Les ressources nécessaires à la prévention des
risques sont :
a. Générique
- Mise en place de moyens permettant d’éviter
les accidents (procédures, formations extérieures,
sensibilisation…),
- Préconisations des comités
réglementaires.
b. Communauté Européenne
c. France
- Visite et rapport du CHSCT
- Visite et rapport du CLIN
d. Autres pays
BPO 03 : Processus de gestion et de
suivi des matériels
techniques et équipements de contrôle, de mesure et
d'essai (ECME)
Les ressources nécessaires au processus de gestion et de
suivi
des matériels techniques et ECME sont :
a. Générique
- ECME.
- Liste des ECME à jour.
- Liste d’organismes de contrôle des ECME
à jour, avec coordonnées.
- Certificats d’étalonnages
des ECME.
- Gestion de Maintenance Assistée par
Ordinateur (GMAO) ou système équivalent.
b. Communauté Européenne
c. France
- Décret no 2001-387 du 3 mai 2001 relatif au
contrôle des instruments de mesure, JORF n° 106 du 6 Mai 2001
page 7164NOR : ECOI0100116D
d. Autres pays
- Suisse : Ordonnance sur les instruments de mesures
du 15/02/2006
Bonnes Pratiques
"Réalisation" (BPR)
BPR01 : Processus de gestion et de
suivi des dispositifs médicaux
BPR 01-01 : Processus d'achat
Les ressources nécessaires au processus d’achat
sont :
a. Générique
- Cahier des charges précis des
besoins
- Installations techniques et implantations, plan,
architecture et garantie
- Plan pluriannuel d’équipements
- Bon de commande
: montant ht, adresses, délai de livraison, identification et raison
sociale vendeur
- Documentation techniques et liste de pièces
détachées
- QO : Qualification Opérationnelle
b. Communauté Européenne
- Code des Marchés publics
- Marquage CE : classifications
DM (établissement politique de maintenance), durée
d’utilisations
c. France
- Marché A Procédure Adaptés
(MAPA)
d. Autres pays
- Suisse : Loi fédérale sur les
médicaments et les dispositifs médicaux du 15/01/2000
article 46 (procédure d’évaluation de la
conformité)
- Cote D’Ivoire : Code des marchés publics
BPR 01-02 : Réception
Les ressources nécessaires au processus de
réception sont
:
a. Générique
- Archiver les bons de livraison,
- Procès verbal de réception, adresse
de réception, identification du destinataire, …
- Contrat
de mise à disposition,
- Contrat de location
- C ontrat de prêt
b. Communauté Européenne
c. France
d. Autres pays
BPR 01-03 : Mise en service et
formation des utilisateurs
Les ressources nécessaires au processus de mise en service
et
formation des utilisateurs sont :
a. Générique
- Formation technique et utilisateurs,
procédures particulières ; nettoyage,
désinfection, décontamination, stérilisation,
- Procès
verbal de mise en service
b. Communauté Européenne
c. France
d. Autres pays
BPR 02 : Maîtrise en
exploitation
Les ressources nécessaires au processus de
maîtrise en
exploitation sont :
a. Générique
- Gestion de Maintenance Assistée par
Ordinateur (GMAO) ou système équivalent
b. Communauté Européenne
c. France
d. Autres pays
BPR 02-01 : Données
d'organisation pour la maintenance et le
contrôle qualité
Les ressources nécessaires au processus des
Données
d'organisation pour la maintenance et le contrôle qualité
sont :
a. Générique
- Annuaire fournisseurs
- Dérogation d’emploi en cas de
non-conformité d’un DM suite a une maintenance ou CQ
- Planning de maintenance
- Procédures
- Equipements de Contrôle de Maintenance et
d’Essais (ECME)
- Gestion de Maintenance Assisté par
Ordinateur (GMAO) ou système équivalent
b. Communauté Européenne
c. France
- Décret n° 2001-11-54 du 5
décembre 2001 Relatif à l’obligation de maintenance et au
contrôle qualité des dispositifs médicaux
prévu à l’article L. 5212-1 du code de la santé
public.
- Arrêté du 3 octobre 1995 relatif aux
modalités d'utilisation et de contrôle des
matériels et dispositifs médicaux assurant les fonctions
et actes cités aux articles D.712-43 et D.712-47 du code de la
santé publique, JORF octobre 1995
- Arrêté du 03/032003 fixant les listes
des dispositifs médicaux soumis à l’obligation de
maintenance et au contrôle de qualité soumis aux articles
L.5212-1 et D.665-5-3 du code de la santé public
d. Autres pays
- Suisse : Loi fédérale sur les
médicaments et les dispositifs médicaux du 15/01/2000
article 49 (obligation d’assurer la maintenance)
- Cote D’Ivoire
: SYGEPAS (GMAO)
BPR 02-02 : Maintenance
préventive
Les ressources nécessaires au processus de la
maintenance
préventive sont :
a. Générique
- Kits constructeurs
- Pièces détachées
- Rapports d’interventions,
archivage papiers ou GMAO
- ECME
- Lieu dédié pour ce type de
maintenance,
- Formation du personnel
- Documentation technique du fabriquant
- Gestion de Maintenance
Assisté par
Ordinateur (GMAO) ou système équivalent
b. Communauté Européenne
c. France
- Décret n° 2001-11-54 du 5
décembre 2001 Relatif à l’obligation de maintenance et au
contrôle qualité des dispositifs médicaux
prévu à l’article L. 5212-1 du code de la santé
public.
- Arrêté du 3 octobre 1995 relatif aux
modalités d'utilisation et de contrôle des
matériels et dispositifs médicaux assurant les fonctions
et actes cités aux articles D.712-43 et D.712-47 du code de la
santé publique, JORF octobre 1995
- Arrêté du 03/032003 fixant les listes
des dispositifs médicaux soumis à l’obligation de
maintenance et au contrôle de qualité soumis aux articles
L.5212-1 et D.665-5-3 du code de la santé public.
- Arrêté du 22/10/1993 relatif au
contrôle des instruments de pesage (Organisme agréer par
la DRIRE et carnet de métrologie)
- Norme NF EN554 octobre
1994 Stérilisation
des dispositifs médicaux (Exploitation des dispositifs sous
pression)
d. Autres pays
- Cote D’Ivoire : SYGEPAS (GMAO)
BPR 02-03 : Maintenance corrective
Les ressources nécessaires au processus de la
maintenance
corrective sont :
a. Générique
- ECME,
- Lieu dédié pour ce type de
maintenance,
- Pièces de rechange,
- Formation du personnel
- Documentation technique
- Tenir à jour un annuaire
de contacts
- Gestion de Maintenance Assisté par
Ordinateur (GMAO) ou système équivalent
- Bon d’intervention
- Mettre en place un Contrats externe
(si pas les compétences)
b. Communauté Européenne
c. France
d. Autres pays
BPR 02-04 : Contrôle
Qualité
Les ressources nécessaires au processus de
contrôle
qualité sont :
a. Générique
- Protocoles de contrôle qualité fiches
SNITEM (www.snitem.fr)
- Bon d’intervention
- Gestion de Maintenance Assisté par
Ordinateur (GMAO) ou système équivalent
b. Communauté Européenne
c. France
d. Autres pays
- Cote D’Ivoire : SYGEPAS (GMAO)
BPR 02-04-01 :
Contrôle
Qualité interne en mammographie
analogique de dépistage systématique
Les ressources nécessaires au processus de Contrôle
Qualité interne en mammographie analogique de dépistage
systématique sont :
a. Générique
b. Communauté Européenne
c. France
- Décision du 07/10/2005 fixant les
modalités du contrôle de qualité des installations
de Mammographie analogique
d. Autres pays
BPR 03 : Réforme
Les ressources nécessaires au processus de
réforme sont :
a. Générique
- Zone dédiées pour stocker les DM
réformés
- Contrat de cession et de transfert de
responsabilités en cas de cession du DM
- Fiche de réforme
ou renseigner la GMAO
b. Communauté Européenne
c. France
- RSQM et le conserver 5 ans après la
réforme
d. Autres pays
- Cote D’Ivoire : SYGEPAS (GMAO)
7. CONCLUSION
ET PERSPECTIVES D’AVENIR
Les différentes
enquêtes réalisées ont
permis la clarification de la démarche adoptée pour
l’identification des ressources souhaitées par les acteurs de
terrains.
L’organisation structurelle proposée par les MASTER 2008 a
servit de base pour l’identification des ressources. Il a donc
été possible d’identifier des ressources très
proches des activités des services biomédicaux.
L’expérience professionnelle des acteurs biomédicaux que
nous sommes est sollicitée pour l’identification des ressources
nécessaire pour la mise en place des bonnes pratiques de
REALISATION. Nous avons donc utilisé la CARTOGRAPHIE des
PROCESSUS pour faciliter l’identification de l’ensemble de ces
ressources pour chaque bonne pratique. Les différentes
enquêtes réalisées à cet effet n’ont pas
permis la mise en évidence de ces ressources.
Cette proposition de ressources devra être proposée
à la communauté biomédicale pour
amélioration ou validation.
L’évolution de l’activité et l’expérience de
chaque acteur devra permettre une réactualisation constante et
permanente dans le temps des ressources. Cela pourra se faire par
l’intermédiaire de la plateforme Internet qui sera mis place
lors de la validation de la nouvelle version du Guide. L’accès
sera ainsi simplifié pour chaque service biomédical
à un instant T ou qu’il soit.
Il convient de préciser que seule une identification des
ressources génériques serait pertinente.
Les ressources spécifiques dépendent de chaque
établissement, suivant leurs importances, leurs moyens, leurs
implantations etc. De plus certains pays avec de faibles moyens
pourront plus facilement s’intégrer dans ses démarches en
restant sur une base simplifié et généraliste des
ressources.
Cela reste a étudié avec les services en question, et ne
sera efficient que sur un retour d’expérience dans le temps.
Face aux différents enjeux qui s’imposent aux services
biomédicaux, la version 2010 du Guide des Bonnes Pratique
Biomédicales en établissement de santé se
présente comme le seul outil mis à la disposition des
acteurs de la maintenance hospitalière pour justifier la bonne
exécution de leurs missions. Il devra donc accompagner chaque
acteur dans sa tâche quotidienne.
BIBLIOGRAPHIE
ET REFERENCES
- [1] Guide des Bonnes
Pratiques Biomédicales
en Etablissement de Santé, Farges G. (UTC), Wahart G. (Pdte
AFIB), Denax J.M. (Pdt AAMB), Métayer H. (Pdt ATD) et 45
co-auteurs, ITBM/RBM News, Ed Elsevier, novembre 2002, vol. 23, Suppl.
2, 23s-52s).
- [4] Guide des bonnes pratiques biomédicales
en établissement de santé : adaptation
québécoise - juin 2005 http://www.utc.fr/~farges/
Relative aux Normes
( http://www.afnor.fr )
Maintenance :
- XP S99-171 : Maintenance des dispositifs
médicaux - Modèle et définition pour
l'établissement et la gestion du registre
sécurité, qualité et maintenance d'un dispositif
médical (RSQM). Edition Afnor. Décembre 2001. Indice de
classement : S99-171. Statut : Norme expérimentale
Décrets :
- Décret no 2001-1154 du 5 décembre
2001 relatif à l'obligation de maintenance et au contrôle
de qualité des dispositifs médicaux prévus
à l'article L. 5212-1 du code de la santé publique
(troisième partie : Décrets), JORF n° 284 du 7
Décembre 2001, NOR : MESP0123968D
- Décret no 2001-387 du 3 mai 2001 relatif au
contrôle des instruments de mesure, JORF n° 106 du 6 Mai 2001
page 7164NOR : ECOI0100116D
- Décret no 96-442 du 22 mai 1996 relatif aux
instruments de pesage à fonctionnement non automatique, JORF
n° 120 du 24 Mai 1996, page 7763 , NOR : INDB9600264D
-
Décret no 96-32 du 15 janvier 1996 relatif
à la matériovigilance exercée sur les dispositifs
médicaux et modifiant le code de la santé publique
(deuxième partie : Décrets en Conseil d'Etat), JORF
n° 14 du 17 Janvier 1996 page 803, NOR : TASH9523427D
-
Décret no 95-292 du 16 mars 1995 relatif aux
dispositifs médicaux définis à l'article L. 665-3
du code de la santé publique et modifiant ce code
(deuxième partie: Décrets en Conseil d'Etat), JORF n°
65 du 17 Mars 1995 page 4175 , NOR : SPSH9500005D
-
Décret no 93-973 du 27 juillet 1993 relatif
aux instruments de pesage à fonctionnement non automatique, JORF
n° 177 du 3 Août 1993, NOR : INDB9300529D
- Décret n° 91-330 du 27 mars 1991 relatif
aux instruments de pesage à fonctionnement non automatique
modifié par décrets 93-973 du 27 juillet 1993 et 96-442
et du 22 mai 1996, JORF, NOR: INDD9100113D
- Décret n° 88-682 du 6 mai 1988 relatif
au contrôle des instruments de mesure, JORF, NOR: INDD8800287D
-
Décret n° 61-501 du 3 mai 1961. relatif
aux unités de mesure et au contrôle des instruments de
mesure, JORF du 20 mai 1961 et rectificatif du 11 août 1961.
Arrêtés :
- Arrêté du 25 février 2002
relatif à la vérification primitive de certaines
catégories d'instruments de mesure, JORF n° 68 du 21 Mars
2002 page 5003, NOR : INDI0200169A
- Arrêté du 3 octobre 1995 relatif aux
modalités d'utilisation et de contrôle des
matériels et dispositifs médicaux assurant les fonctions
et actes cités aux articles D.712-43 et D.712-47 du code de la
santé publique, JORF octobre 1995
- Arrêté du 22 mars 1993 relatif au
contrôle des instruments de pesage à fonctionnement non
automatique, en service modifié par les arrêtés du
15 octobre 1993, du 6 mai 1997 et du 17 septembre 1998, NOR:
INDB9300311A
-
Arrêté du 03/03 /2003 fixant les
listes des dispositifs médicaux soumis à l’obligation de
maintenance et au contrôle de qualité soumis aux articles
L.5212-1 et D.665-5-3 du code de la santé public
Relative aux Bonnes
Pratiques :
- Contrôle de Qualité en Mammographie,
Protocole de contrôles qualité des installations de
mammographie, Ministère de la santé Français,
Direction Générale de la Santé, Edition
révisée de juillet 1998, http://www.hosmat.fr/assurqualite/mammo.pdf
- Guide des bonnes pratiques biomédicales en
établissement de santé : adaptation
québécoise - juin 2005 http://www.utc.fr/~farges/
- Bonne pratiques de la maintenance des dispositifs
médicaux SwissMédic mai 2005 http://www.swissmedic.ch
- AAMB :
Association des Agents de Maintenance Biomédicale
- AFIB :
Association Française des Ingénieurs
Biomédicaux
- ATD :
Association des Technicien de Dialyse
- AP-HP :
Assistance Publique des Hôpitaux de Paris
- BPM : Bonne
Pratique de Management
- BPO : Bonne
Pratique Opérationnelle
- BPR : Bonne
Pratique de Réalisation
- Certification :
Procédure par laquelle une tierce partie donne
une assurance écrite qu’un produit, qu’un processus, qu’une
organisation ou qu’un service sont conformes à des exigences
spécifiées.
- CH : Centre
Hospitalier
- CHSCT :
Comité d’Hygiène et de Sécurité des
Conditions de Travail.
- CHU : Centre
Hospitalier Universitaire
- Client :
Organisme ou personne qui reçoit un produit (ISO
9000:2000).
- CQ : Contrôle
Qualité : Activités telles que
mesurer, examiner, essayer ou passer au crible une ou plusieurs
caractéristiques d’une entité, et comparer les
résultats aux exigences spécifiées en vue de
déterminer si la conformité est obtenue pour chacune de
ces caractéristiques (ISO 9000).Ensemble des opérations
destinées à évaluer le maintien des performances
revendiquées par le fournisseur ou, le cas
échéant, fixées par le directeur
général de l’Agence française de
sécurité sanitaire de produits de santé
(décret n°2001-1154) .
- Critère :
Enoncé d’un moyen ou d’un élément
plus précis permettant de satisfaire la référence
d’accréditation.
- Démarche
qualité : Ensemble des dispositifs mis en place
par une structure en vue de répondre aux objectifs et aux
conditions de l’accréditation ou à des exigences de
qualité librement adoptées. Ce programme rend
nécessaire une évaluation régulière et
permanente des activités concernées, et la fourniture des
preuves correspondantes.
- Décret : Décision, ordre émanant du pouvoir
exécutif.
- ECME : Equipement de Contrôle de Mesure et d'Essai.
- GBPB : Guide des Bonnes Pratiques Biomédicales
- GMAO : Gestion de la Maintenance Assistée par Ordinateur.
- HAS : Haute Autorité de Santé
- ISO : Organisation Internationale de Normalisation
- DM : Dispositifs Médicaux
- Dispositif
médical : On entend par dispositif médical
tout instrument, appareil, équipement, matière, produit,
à l'exception des produits d'origine humaine ou autre article
utilisé seul ou en association, y compris les accessoires et
logiciels intervenant dans son fonctionnement, destiné par le
fabricant à être utilisé chez l'homme à des
fins médicales et dont l'action principale voulue n'est pas
obtenue par des moyens pharmacologiques ou immunologiques ni par
métabolisme, mais dont la fonction peut être
assistée par de tels moyens. Les dispositifs médicaux qui
sont conçus pour être implantés en totalité
ou en partie dans le corps humain ou placés dans un orifice
naturel et qui dépendent pour leur bon fonctionnement d'une
source d'énergie électrique ou de toute source
d'énergie autre que celle qui est générée
directement par le corps humain ou la pesanteur sont
dénommés dispositifs médicaux implantables actifs
(Article L. 665-3 du Code de la Santé Publique Français,
septembre 1998)
- Gestion des interfaces
avec les services: Gestion des relations qui
sont mises en place entre le service biomédical et les services.
- Gestion de la
qualité : Processus par lequel le service
biomédical organise sa démarche qualité et la met
en œuvre.
- Gestion des risques : Application
systématique des politiques de
gestion, des procédures et des pratiques à des
tâches d’analyse, d’évaluation et de maîtrise des
risques (NF EN ISO 14 971).
- Gestion du personnel :
Art de manager ses employés afin
d'optimiser les résultats des activités.
- Gestion des locaux :
Art d'organiser, de maintenir et d'entretenir
l'espace de travail, qui est mis à la disposition du service
biomédical.
- Gestion des
matériels et ECME : Gestion de l'ensemble des outils
et appareils électriques divers (tels que perceuse, soudeuse,
multimètre, etc.), qui permet au service biomédical de
mener ses missions de maintenance et de contrôle à bien.
- Maintenance corrective :
Maintenance effectuée après
défaillance (NF X 60-010).
- Maintenance
préventive : Maintenance effectuée selon des
critères prédéterminés, dans l’intention de
réduire la probabilité de défaillance d’un bien ou
la dégradation d’un service rendu (NF X 60-010).
- Mise en service :
Installation et la mise en marche de celui-ci dans le
service utilisateur en présence des utilisateurs, du service
biomédical et/ou du fournisseur.
- Processus d’achat :
Différentes étapes qui permettent de
renouveler le parc de dispositifs médicaux de
l'établissement.
- Réception :
phase pendant laquelle le service biomédical
s’assure de la conformité du colis livré et
prépare, si nécessaire, la formation des utilisateurs.
- Réforme :
Retrait du parc de dispositifs médicaux.
- RSQM : Registre
de Sécurité, de Qualité et de
Maintenance
- UTC :
Université de Technologie de Compiègne
(http://www.utc.fr)
ANNEXES
Annexe 1
Questionnaire envoyer par mail
1. Sur combien de
temps avez-vous mis en place le
guide ?
6 mois 12 mois +de 12
mois autre
2. Avez-vous éprouvé des
difficultés à identifier les ressources
nécessaires lors de la mise en place des bonnes pratiques ?
Oui Non
Si oui préciser lesquelles ? Et comment vous avez pu les
surmontées ?
3. Ces difficultés vous ont-elles fait prendre
du retard dans votre mise en place ?
Oui Non
4. Avez-vous eu recours à des intervenants
externes pour la mise en place du guide des bonnes pratiques ?
(ressources)
Oui Non
Si oui qui ? externe (à
l’hôpital) interne (à
l’hôpital)
5. Si les ressources avaient été
clairement identifiées, cela vous aurait-il facilité la
mise en place de la démarche qualité ?
Oui Non
6. Envisagez-vous la mise en place de la
certification de l’ISO 9001 ?
Oui Non
Annexe 2
Questionnaire des Visites
1. De quand date la mise en place de votre
démarche qualité ?
2. La mise en place du Guide des Bonnes Pratiques
a-t-elle modifié votre façon de travailler ?
Oui Non
3. En combien de temps avez-vous mis en place le
guide des bonnes pratiques ? (ex : 6 mois, 1 an...)
4. Quels à été le degré
d’implication de chaque service au niveau de votre démarche
qualité ?
5. Avez-vous éprouvé des
difficultés à identifier les ressources
nécessaires lors de la mise en place des bonnes
pratiques
opérationnelles et fonctionnelles ?
Oui Non
Si oui préciser lesquelles ? Et comment vous avez pu les
surmontées ?
6. Ces difficultés vous ont-elles fait prendre
du retard dans votre mise en place ?
Oui Non
7. Avez-vous eu recours à des intervenants
externes pour identifier
les ressources nécessaires à la mise en œuvre du
guide des bonnes pratiques ?
Oui Non
Si oui qui ? (ex : service qualité du CH, entreprise externe)
8. Si les ressources avaient été
explicitées dans le guide des bonnes
pratiques, cela vous aurait-il facilité la mise en œuvre de
la
démarche qualité ?
Oui Non
9. Envisagez-vous la mise en place de la
certification de l’ISO 9001
Oui Non




















