|
Avertissement
|
|
|
Si vous arrivez directement sur cette page,
sachez que ce travail est un rapport d'étudiants et doit
être pris
comme tel. Il peut donc comporter des imperfections ou des
imprécisions
que le lecteur doit admettre et donc supporter. Il a été
réalisé
pendant la période de formation et constitue avant-tout un
travail de
compilation bibliographique, d'initiation et d'analyse sur des
thématiques associées aux technologies
biomédicales. Nous ne faisons
aucun usage commercial et la
duplication est libre. Si vous avez des raisons de contester ce droit
d'usage, merci de nous en faire part .
L'objectif de la présentation sur le Web est de
permettre
l'accès à l'information et d'augmenter ainsi les
échanges
professionnels. En cas d'usage du document, n'oubliez pas de le citer
comme source bibliographique. Bonne lecture...
|
|
|
Angioplastie Angioplastie par IRM interventionnelle Procédés de stérilisation
|
|
 DEGRAIN Marc |
 KARTOUBI Aissam |
|
Référence à rappeler
: Traitement de
la sténose par angioplastie et procédés de
stérilisation liés à l'IRM interventionnelle, DEGRAIN Marc,
KARTOUBI Aissam, Projet d'Intégration, MASTER Management des Technologies
en Santé
(MTS), UTC, 2005-2006
URL : https://www.utc.fr/formations/master/professionnelle/technologie_sante.html ; Université de Technologie de Compiègne |
|
|
L’athérosclérose
est
la première
cause de mortalité en France. la méthode chirurgical par
le pontage
aorto-coronarien est peu utilisée.L’angioplastie avec
ou sans pose
d’endoprothése coronaire « stent », sous
angiographie est la
méthode
la plus courante en athérosclérose interventionnelle. D’autres méthodes comme l’angioplastie laser, le rotablator et l’athérectomie existe mais ne sont pas trop répandu. Mots clés : athérosclérose,
angioplastie,
stent,angiographie, athérectomie,rotablator, IRM
interventionnelle |
|
|
Key words: atherosclerosis, angioplasty, stent, angiography, atherectomy, rotablator, interventional MRI |
|
Remerciements
Nous tenons à remercier les sociétés PHILIPS et SIEMENS pour nous avoir permis de réaliser ce projet enrichissant.
Nous remercions également toutes les personnes qui, directement ou indirectement, nous ont apporté leur concours pour la réalisation de ce projet.
I Historique
II Pathologie
2.1. Comment se forme les plaques d’athéromes
2.2. Athérosclérose coronarienne
III Différents techniques d’imagerie cardio-vasculaire
3.1.
Angiographie
numérisée
3.2. Angio-CT:
3.3. Angio-RM ou Angiographie par Résonance Magnétique (ARM)
3.3.1. Avantages et inconvénients de l’Angio-RM interventionnel
3.4. Echographie-doppler
IV Intérêts de l’imagerie interventionnelle
4.1. Intérêts
4.2. Imagerie interventionnelle et chirurgie
V Procédés invasif d’élimination des plaques d’athéromes (plasmaphérèse, angioplastie)
5.1.
Plasmaphérèse
5.2.
Angioplastie
5.2.1. Angioplastie coronarienne transluminale percutané
5.2.2. Angioplastie coronaire avec pose de « stent »
5.2.3. Angioplastie laser
5.3. Autres méthodes
VI Percpective d’avenir :
VII Désinfection des systèmes invasifs
7.1 Réglementation
7.2 Evaluation du risque infectieux et du niveau de traitement requis
7.3 Stérilisation
7.3.1. Principes
7.3.2. Méthodes de mise en œuvre
7.3.2.1. La stérilisation à la vapeur d'eau:
7.3.2.2. La stérilisation par la chaleur sèche:
7.3.2.3. Stérilisation par l'oxyde d'éthylène:
7.3.2.4. Stérilisation centralisée
7.4 Aménagement des locaux et les travaux de construction
VIII L’impact humain et économique lié aux éléments d’athérosclérose
IX Conclusion
X Références bibliographiques
XI Bibliographie
XII GLOSSAIRE
I Historique
(Dr Mazoyer, Clinique St Jean – Lyon)(Revue de l’évolution de l’imagerie vasculaire)
En 1927 a eu lieu la première « artériographie » (encéphalographie artérielle). En 1929, ce fut la première aortographie – Dos Santos.
Les techniques d’imagerie vasculaire se sont ensuite généralisées après guerre grâce aux innovations dans le domaine des produits de contraste. En effet, suite à l’utilisation de l’iodure de sodium ou du ThorotrastÒ (produit radioactif responsable de tumeurs), les produits mis sur le marché furent de moins en moins toxiques, jusqu’à l’apparition de dérivés hexaiodés et de produits non osmolaires.
En parallèle, les voies d’abord des vaisseaux étaient de moins en moins agressives.
L’innovation majeure a lieu en 1960 avec la mise au point par des médecins suédois du principe du cathétérisme : l’exploration de l’ensemble des vaisseaux, y compris du système porte devenait alors possible. Ce fut la porte ouverte à l’interventionnel vasculaire » (Djindjan et Dotter).
Entre 1960 et 1975, c’est l’âge d’or de l’angiographie : excepté la radiologie classique, il n’existe pas d’autre technique d’exploration des parenchymes. L’échographie et le scanner n’en sont qu’à leurs balbutiements, que ce soit au niveau technique ou de leurs indications.
Au début des années 80, on assiste à une embellie technique : c’est l’apparition de l’angiographie numérisée qui créée l’illusion de la voie veineuse ; on pense alors que toutes les explorations seront possible grâce à une injection intraveineuse. Cependant, cette méthode se révèle rapidement limitée à l’exploration des systèmes vasculaires courts du fait de ses complications toxiques et hémodynamiques. Dans ce domaine, on assiste aujourd’hui à un recentrage sur la voie artérielle justifié par :
- un gain de rapidité (obtention des images en temps réel),
- l’utilisation de produits de contraste en moindre quantité,
- l’utilisation de cathéter de petits calibres.
Dans un même temps (1975 – 1980) se sont développées les techniques d’imagerie tissulaire (échographie, scanner puis IRM). L’angiographie n’a donc plus le monopole dans le domaine de l’imagerie, d’autant que de manière plus lente mais tout aussi certaine se sont développées des imageries directes des flux. Il s’agit en particulier de l’écho-doppler qui a constitué la première limite au débordement de l’angiographie par voie veineuse. Plus tardivement, ce furent l’angio-IRM et l’angio-scanner rendu possible par une nouvelle technologie du scanner, le scanner hélicoïdal. Ces technologies sont encore en progrès et les derniers domaines réservés de l’angiographie (membres inférieurs et cerveau) sont en train de céder.
II Pathologie :
2.1. Comment se forme les plaques d’athéromes
Le
cholestérol lié au protéines LDL est le
« mauvais
cholestérol » en
excès, il se dépose dans les parois des artères
provoquant des plaques
d’athéromes. On parle donc d’athérosclérose
coronarienne.
2.2. Athérosclérose coronarienne
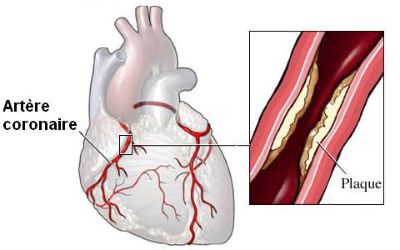
L’athérosclérose est un processus caractérisé par un dépôt de graisses et de fibres scléreuses à l’intérieur de la lumière de toutes les artères de l’organisme. Compte tenu de leur petit calibre, les artères coronaires sont plus exposées que d’autres à l’obstruction par l’athérosclérose. Il existe donc lors de l’athérosclérose coronarienne un rétrécissement du calibre des artères, ce qui gêne l’apport de sang et donc d’oxygène au niveau du muscle cardiaque. Cette perturbation peut être à l’origine de douleurs thoraciques (anone de poitrine) ou, en cas d’occlusion totale, d’un infarctus du myocarde.
L’infarctus résulte de la destruction d’une partie du muscle cardiaque consécutive à la privation de sang, elle-même consécutive à une occlusion d’une branche d’une artère coronaire.
Les causes de
l’athérosclérose
sont encore
mal connues mais il est possible d’identifier des patients qui sont
plus
exposés que d’autres à l’athérosclérose
coronarienne : ces
patients
présentent des « facteurs de risque ». Les
principaux
facteurs
de risque sont :
- Essentiellement le tabac,
- Les perturbations des graisses sanguines et en particulier l’élévation du cholestérol,
- L’hypertension artérielle.
- Maladies mono géniques (cardiomyopathie familial)
- Obésités
Le diabète, une certaine prédisposition familiale sont aussi des facteurs de risque
- L’athérosclérose coronarienne provoque la formation des plaques d’athéromes :
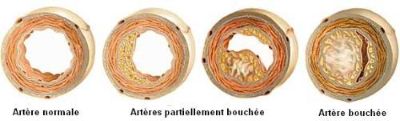
[2] : Image d’artère : formation d une plaque d’athérome compliquée
- Les lésions d’athérome se développent le plus souvent au niveau du carrefour entre les deux carotides (externe et interne)
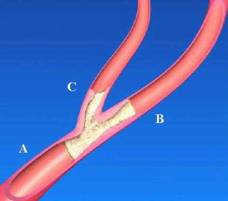
[3] : Image à un croisement
d’une
artère avec
athérosclérose
Pour rétablir le flux sanguin dans les artères coronaires, et l’apport de sang au niveau du muscle cardiaque, il n’existe que deux méthodes :
- le pontage aorto-coronaire,
- l’angioplastie transluminale coronaire.
Le pontage aorto-coronaire ne supprime pas la lésion au niveau de l’artère coronaire mais effectue une dérivation permettant de ramener du sang au-delà de l’obstacle coronarien.
L’angioplastie transluminale coronaire se propose de rétablir le flux en élargissant le diamètre de l’artère à l’endroit du rétrécissement.
Avant de décider l’emploi de l’une de ces deux méthodes, il est nécessaire que le siège, la sévérité, la diffusion des lésions aient été préalablement reconnus par la radiographie des coronaires, appelée coronarographie, il convient immédiatement de signaler que l’angioplastie transluminale coronaire ne diffère pratiquement pas de l’artériographie coronaire.
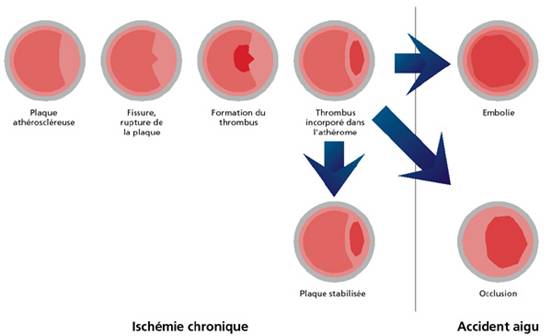
[4] : Image d’un processus pathologique d’athérothrombose
III Différents techniques d’imagerie cardio-vasculaire.
L’imagerie cardio-vasculaire diagnostique est répartie entre
différents
départements techniques. Elle comprend les opacifications
artérielles
et/ou
veineuse par angiographie conventionnelle (vaisseaux
périphériques,
digestifs,
pulmonaires), l’angio-CT (aorte, carotides, rénales coronaires),
l’angio-IRM
(rénales, membres inférieurs, carotides, greffons
rénaux, la cardio-IRM
(viabilté, masses, pathologies infiltratives, coronaires) et
l’échographie-Doppler (toutes régions sauf
intra-crânien). Les
activités de
radiologie interventionnelle recouvrent les angioplasties, le stenting,
le
traitement de cancers par chimioembolisation et radiofréquences,
les
embolisations, la mise en place d’accès veineux centraux et de
TIPS,
les
biopsies osseuses, les vertébroplasties, les infiltrations.
3.1. Angiographie numérisée :
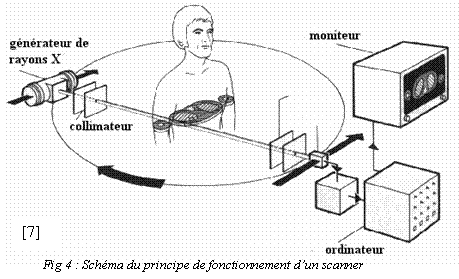
L’angiographie permet la visualisation des vaisseaux sanguins (artères et veines) après injection de produit de contraste. Le patient est couché sur une table radio transparente qui peut se déplacer horizontalement.
L’ensemble tube RX et Ampli de brillance (permettant des images dynamiques) est solidarisé sur un arceau qui peut aussi se déplacer dans tous les sens. De ce fait, le patient peut être examiné sous tous les angles sans être bougé (facilité et sécurité).
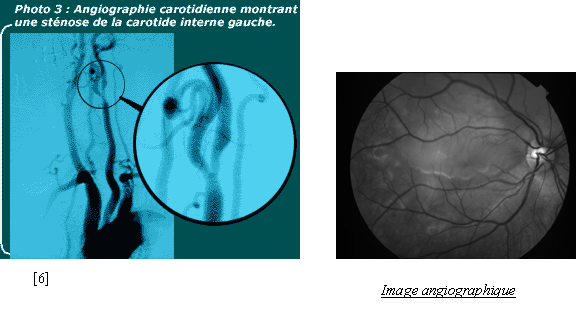
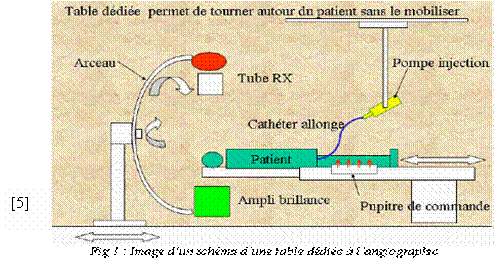
[6] : Image : angiographie carotidienne - image angiographique
Elle est
utilisée
pour toutes les
interventions vasculaires (périphérique, coronaire,
neurologique,…).
80%
d’angioplastie s’effectue désormais grâce à ce
système et non plus en
chirurgie
classique. Aujourd’hui cela représente en France près de
72000
interventions.
3.2. Angio-CT:
L'angio-CT est une
technique
évolutive. La nouvelle génération des scanners
multibarrettes et le
développement de logiciels permettant un seuillage automatique
pour
s'affranchir de l'obstacle des calcifications de la paroi
artérielle
ont pour
but d'améliorer la performance de l'angio-CT dans
l'évaluation de la
sténose de
la carotide tant pour la quantification du degré de
sténose que pour
l'étude de
la caractérisation de la plaque.
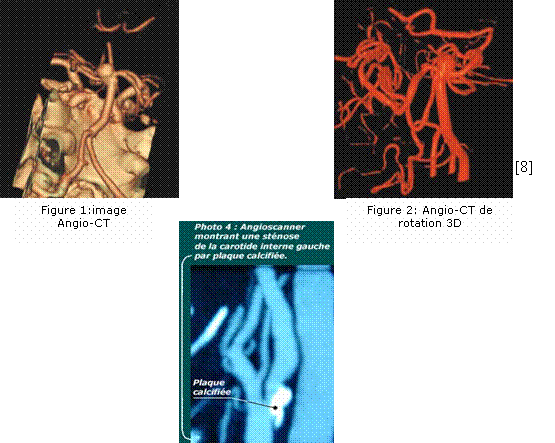
[8] : Angioscanner montrant une sténose
3.3. Angio-RM ou Angiographie par Résonance Magnétique (ARM)
L’angiographie par résonance magnétique (ARM) permet de faire une exploration des déplacements du sang en IRM afin de visualiser les vaisseaux.
Il existe différents types d’angiographie par résonance magnétique, sans et avec, injection de produit de contraste :
- L’ARM sans injection de produit de contraste, basée uniquement sur l’étude des flux (se rapprochant du Doppler couleur); il en existe de deux types : l’angiographie par temps de vol (TOF) et l’angiographie par contraste de phase (CP), cette dernière permettant de réaliser une étude des débits grâce à la cartographie des vitesses.
- L’ARM avec injection de produit de contraste utilise des produits à base de Gadolinium, c’est une angiographie plus coûteuse mais nettement plus rapide avec moins de problèmes d’interprétation liés aux artéfacts de flux, elle est le plus souvent utilisée actuellement.
L’angiographie par résonance magnétique permet le bilan des artères et des veines thoraciques mais aussi cervicales sans radiation ionisante.
Il existe des limites liées à la résolution spatiale de l’examen, la durée de la séquence ainsi qu’un problème de placement lors des études de l’avant-bras et du bras.
Une amélioration de la technologie, des antennes, et de nouveaux produits de contraste à rémanence vasculaire (10) pourrait être prometteur.
[9]Salle d’Angio-RM
[9] :
Salle d'angio IRM
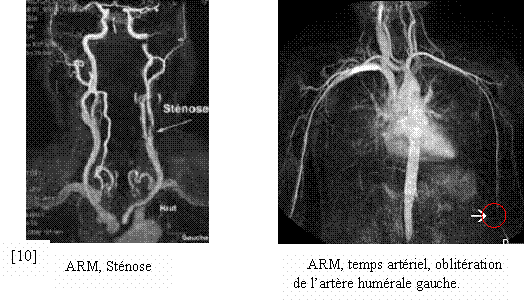
[10] : Image
d'angiogrophie par résonance magnétique
3.3.1. Avantages et inconvénients de l’Angio-RM interventionnel:
Avantages :
- Intervention directe sur le patient tout en bénéficiant en continu d’une image IRM pour surveiller et contrôler les gestes chirurgicaux
- Imagerie tridimensionnelle
- Qualité de la résolution en signal
- Anesthésie locale
- Prise en charge plus légère (temps de séjour réduit, coût moins élevé)
- Technique moins invasive (point de ponction de 1 à 3 mm de diamètre)
Inconvénients :
- Sont ceux de l’IRM conventionnelle : les personnes portant des pace-maker, des corps étranger dans l’organisme, des objets ferromagnétiques, ainsi que les femmes enceintes (inférieur à trois mois) ne peuvent passer l’examen.
- Difficulté pour les personnes claustrophobes.
- Achat d’instrumentation amagnétique et repérable sous imagerie
- Autres contraintes : l’appareil doit être installé dans une salle d’intervention dédiée car:
- L’aménagement doit permettre que des interventionnistes (chirurgien et/ou radiologistes et anesthésistes) puissent y effectuer des procédures allant de la simple biopsie à la chirurgie du cerveau
- Les procédures se font dans le champ de l’appareil
- Les instruments et appareils servant aux procédures doivent tous être compatibles à l’IRM.
3.4. Echographie-doppler :
L’échographie est une technique d’exploration basée sur les ultrasons. Une sonde envoie un faisceau d’ultrasons dans la zone du corps à explorer. Selon la nature des tissus, ces ondes sonores sont réfléchies avec plus ou moins de puissance. Le traitement de ces échos permet une visualisation des organes observés.
Elle est employée pour les biopsies et ponctions percutanées, examens fréquents et relativement banals en imagerie interventionnelle.
En mode doppler l’échographe permet de quantifier approximativement les vitesses et le sens des flux, l’intensité de la couleur étant proportionnelle à la vitesse d’écoulement.
![]() Diagnostic en echo-doppler:
Diagnostic en echo-doppler:
Le doppler est un examen
qui utilise les
ultrasons. Il mesure la vitesse à laquelle circule le sang. Il
permet
de
détecter un ralentissement du flux sanguin en aval d’un
rétrécissement
signe
qu’un vaisseau est obstrué, artère ou veine. Il permet
également
d’explorer la
circulation sanguine à travers les cavités cardiaques.
Très souvent, il
est
couplé à l’échographie, on parle alors
d’écho doppler.
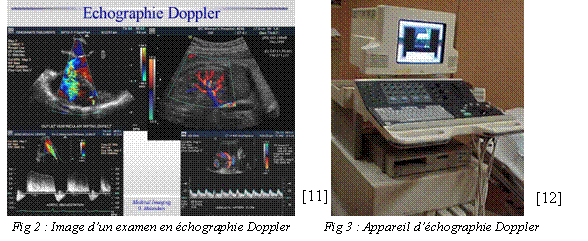
[11] : Image d'un examen en échographie doppler
IV Intérêts de l’imagerie interventionnelle
4.1. Intérêts
L’imagerie présente deux
intérêts
principaux. En effet, elle constitue :
- Un progrès pour le malade : les procédures sont plus simples, plus rapides : plusieurs heures d’intervention peuvent être replacées par un acte interventionnel d’une demi heure. Elles sont aussi moins gênantes pour le malade : l’hospitalisation est réduite à 1 ou 2 jours et moins risquées.
- Un progrès thérapeutique : la technique prépare, complète ou remplace l’acte opératoire. Elle propose de nouveaux traitements inaccessibles à la chirurgie (ponction de sang fœtal, prélèvement d’ovocytes,…).
L’angiographie restera intéressante pour des lésions très particulières :
- Artériographie carotidienne pour le diagnostic d’artérite cérébrale.
- Exploration lors de bilans pré-thérapeutiques : c’est le cas lors d’embolisation de lésions tumorales attendues aux méninges avant chirurgie, dont le diagnostic aura été effectué par d’autres techniques.
Le
tableau [1] ci-dessous fait la
comparaison des techniques d’imagerie interventionnelle :
|
|
Limites |
Risques |
Invasif |
Opérateur dépendant |
Patient dépendant |
Disponibilité |
|
Angiographie |
Ignore la structure de la plaque |
Contraste local |
+++ |
+++ |
+ |
+++ |
|
Echo Doppler |
Idem échographie |
Nul |
0 |
+++ |
++ |
+++ |
|
AngioScanner hélicoïdal |
Apnée |
Contraste (Allergie, Complications hémodynamiques) |
+ |
+ |
+ |
+ |
|
Angio-RM |
Déglutition |
|
+/- |
+ |
++ |
+ |
4.2. Imagerie interventionnelle et chirurgie.
L’imagerie d’intervention prépare, complète ou remplace la chirurgie. Ces deux disciplines semblent donc fonctionner en synergie pour le traitement du patient afin d’aboutir à la guérison de celui-ci. En effet, elles présentent deux intérêts différents :
- Le chirurgien voit directement le champ opératoire par incision large et protège les organes fragiles.
- L’interventionniste, surveille le trajet par imagerie 2D (rayons X ou ultrasons) avec un point de ponction réduit.
L’intérêt d’utiliser l’imagerie interventionnelle par rapport à la chirurgie est fonction de plusieurs critères :
- les lésions sont plus localisées
- plus de précision dans l’acte opératoire
- moins de gène pour le patient (perte de sang minime, pas de séjour en réanimation, convalescence de courte durée)
- coût d’hospitalisation plus faible
L’imagerie interventionnelle regroupe un éventail de techniques très diversifiées c’est pourquoi l’IRM interventionnelle est considérée comme une technique prometteuse.
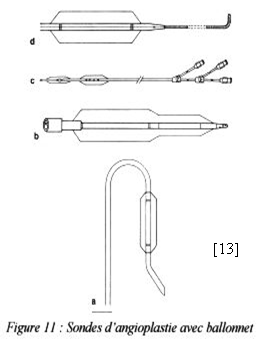
[13] : Sonde d'angioplastie avec ballonnet
Déroulement d’une intervention : Exemple de
l’angioplastie
d’une
artère coronaire
Afin d’avoir une approche pratique de l’acte d’imagerie interventionnelle, voici une brève description d’une intervention effectuée au service de Radiologie Vasculaire du professeur Gaux de l’hôpital Broussais.
La photo ci-dessous
montre une
intervention angiographique.
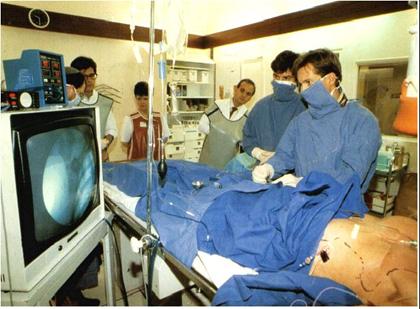
[14] : Photo d’une
intervention angiographique
Après une préparation de la salle et du malade (anesthésie locale), un guide fin souple est introduit à travers le cathéter porteur par voie fémorale sous contrôle angiographique sous amplificateur de brillance. Le guide, toujours sous contrôle angiographique, est dirigé jusqu’au franchissement de la sténose passant par la veine cave inférieure et atteignant la coronaire droite. Sur ce guide coulisse une sonde (cathéter) comportant un ballonnet gonflable (voir figure 11-a), que l’on gonfle progressivement une fois la sténose franchie. Le ballonnet rompt l’endothélium en tassant les plaques d’athéromes dans l’épaisseur de la paroi du vaisseau, puis il est retiré.
Il y a 90 à 97% de succès primaire d'une telle opération mais également 40% de chance de resténose. Pour éviter cela, en plus du ballonnet, on pose ensuite, à l'aide d'une nouvelle sonde, une endoprothèse coronaire, le " stent ", qui va maintenir le diamètre du vaisseau plus efficacement et empêcher la resténose.
V Procédés invasif d’élimination des plaques d’athéromes (plasmaphérèse, angioplastie)
5.1. Plasmaphérèse :
La
plasmaphérèse permet d’éliminer du corps des
substances pathogènes par
centrifugation, et en particulier permet l’élimination du
mauvais
cholestérol
LDL. La centrifugation permet de récupérer sous effet
gravitationnel
les
molécules les plus légères sur la face interne de
la cloche.
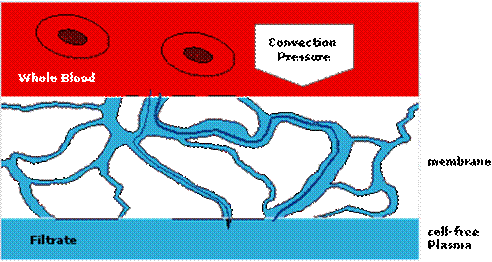
[15] : Image représentant le schéma de principe d’une menbrane de plasmaphérese

[16] : Image représentant un
appareil de plasmaphérese
5.2. Angioplastie :
5.2.1. Angioplastie coronarienne transluminale percutané
D'introduction
encore récente (1977), elle se développe très
rapidement. Elle se
réalise en
cours de coronarographie. Au travers d'un cathéter guide
placé dans le
tronc de
la coronaire gauche ou droite, on introduit successivement :
- Un guide en Téflon très fin et très souple, que l'on fait progresser dans l'artère sténosée, jusqu'à franchir la sténose.
- Puis le cathéter de dilatation (environ l mm de diamètre), muni à son extrémité d'un ballonnet marqué de repères radio opaques. Ce cathéter coulisse sur le guide, jusqu'à positionner le ballonnet à cheval sur la zone sténosée.
- Plusieurs inflations sont ensuite réalisées pendant des durées et à des pressions croissantes, jusqu'à faire "céder" la sténose. En rompant l'intima et en redistribuant le contenu de la plaque d'athérome à l'intérieur de la média, on élargit la lumière artérielle, jusqu'à recréer un diamètre interne le plus proche possible de la normale.
Le taux de succès primaire (sténose résiduelle inférieure < 50 %) est de l'ordre de 95 %. En cours de procédure, les principaux risques sont ceux de dissection étendue de la paroi de l'artère pouvant aboutir à une occlusion aiguë, et de thrombose. Dans ce cas, une intervention chirurgicale en urgence peut être nécessaire, c'est pourquoi "les angioplasties à risques" doivent toujours être réalisées sous "couverture chirurgicale" (équipe chirurgicale en attente, prête à intervenir).
La mortalité en cours de procédure est d'environ 0,5 %, et le risque d'infarctus du myocarde compris entre 2 et 4 %. En cas de succès, le patient peut quitter l'hôpital au bout de deux ou trois jours, et reprendre très rapidement des activités normales. Il en résulte un coût économique et social beaucoup moins lourd que celui de la chirurgie coronarienne. Secondairement, persiste un risque de resténose qui intéresse 40 % environ des lésions dilatées, et environ 50 % des patients. On connaît encore mal la physiopathologie de cette complication, et les facteurs qui y prédisposent. Elle s'observe essentiellement entre le 1er et le 3ème mois suivant la procédure, justifiant une surveillance régulière (clinique et ergométrique) pendant cette période. Les resténoses sont très rares au delà du sixième mois. En cas de resténose, une nouvelle ATC peut être tentée avec un risque identique de re-resténose ultérieure. Ce risque peut être éventuellement réduit par l'insertion d'une prothèse endo-coronarienne (STENT).
En cas de resténoses multiples, une indication chirurgicale doit être reconsidérée.

[17] : Image
représentant une angioplastie transluminal percutané.
Image de la Fondation
Suisse de
Cardiologie sur l’angioplastie transluminal percutané
5.2.2. Angioplastie coronaire avec pose de « stent »
L’indication d’angioplastie coronaire ne peut être posée qu’après visualisation de vos artères coronaires par coronarographie; dans la moitié des cas, la coronarographie est immédiatement suivie de la procédure de dilatation au cours d’une séance dont la durée excède rarement 60 minutes. Dans les autres cas, l’angioplastie est programmée suite à une coronarographie réalisée au préalable dans un hôpital.
Introduction
L’angioplastie coronaire consiste à rendre aux artères coronaires rétrécies par la maladie un diamètre suffisant pour une circulation sanguine efficace. En pratique, cela consiste à introduire dans l’artère et jusqu’à l’endroit rétréci un fin ballonnet qui sera ensuite gonflé pendant quelques secondes pour dilater le segment malade. Dans la majorité des cas, on placera alors dans l’artère une petite prothèse ou « stent « qui permettra de maintenir le résultat en empêchant l’élasticité de l’artère d’en réduire à nouveau le diamètre.
PRÉPARATION À L’ ANGIOPLASTIE CORONAIRE
La veille de l’angioplastie coronaire, différents examens seront effectués et en particulier une analyse soigneuse de votre groupe sanguin. Il est en effet possible, si l’angioplastie coronaire ne parvenait pas à obtenir un résultat satisfaisant, que vous soyez opéré immédiatement et qu’un pontage aortocoronaire soit effectué. Il est donc nécessaire d’avoir un bilan très précis du groupe sanguin ; divers médicaments préparant à l’angioplastie vous seront administrés. Comme pour l’artériographie coronaire, la région de l’aine aura été désinfectée et rasée.
L’ ANGIOPLASTIE CORONAIRE
Elle s’effectue exactement comme une artériographie
coronaire. Dans
un
premier temps après une anesthésie locale, un
introducteur est mis en
place au
niveau de l’artère fémorale.
L’angioplastie coronaire s’effectue sur une table d’examen ; en
permanence, le médecin contrôle votre
électrocardiogramme et la
pression
sanguine. L’angioplastie comporte d’abord la mise en place d’un tube
radio
opaque aux rayons X, au niveau de l’orifice des artères
coronaires ; son
calibre est un peu plus gros que celui avec lequel on a effectué
l’artériographie coronaire.
Après
avoir vérifié
que les lésions ne se sont pas modifiées depuis le
dernier examen
coronarographique, le médecin injecte de l’Héparine,
c’est-à-dire un
anticoagulant.
A l’intérieur du tube radio opaque est introduit un guide métallique extrêmement fin (de différents calibres, le plus gros étant égal à 0,4 mm) ; l’extrémité de ce guide est très fine, très souple, très flexible. Le guide est poussé sous le contrôle radiologique dans le tube et dans l’artère coronaire. Par diverses manoeuvres d’avancement et de rotation, le médecin lui fait franchir le rétrécissement qu’il faut dilater. Une fois que le guide est passé à travers les lésions et qu’il a été poussé dans l’extrémité la plus reculée de l’artère, il sert de rail pour guider un autre tube de petit calibre qui est porteur d’un ballonnet. Ce ballonnet a 20 mm de longueur. Il est gonflé en injectant à l’intérieur de ce ballonnet un produit opaque aux rayons X (figure 2d) ; le diamètre peut atteindre différentes tailles : 2 mm, 2,5 mm, 3 mm, 3,5 mm, 4 nuit. Au milieu du ballon, il existe un petit repère métallique qui permet de positionner très exactement le ballonnet à l’endroit du rétrécissement à dilater. Le ballonnet est gonflé à une pression variable suivant les cas. La durée de gonflage varie de quelques secondes à 45 secondes ou une minute.
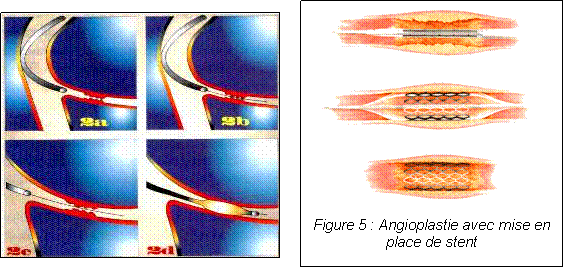
[18]
[19]
[18] :
Image représentant une angioplastie transluminal percutané
[19] :
Image représentant une angioplastie avec pose de stent
Il est possible de ressentir pendant le gonflage du ballonnet une douleur identique à celle que l’on ressent habituellement en marchant, ou en faisant des efforts. Ceci n’est pas inattendu compte tenu du fait que lorsque le ballonnet est gonflé, l’artère est occluse. Après un Ou plusieurs épisodes de gonflage, le médecin retire le ballonnet, le guide reste en place dans le vaisseau, les contrôles radiographiques sont effectués. D’autres gonflages seraient éventuellement réalisés si le résultat n’apparaissait pas entièrement satisfaisant.
Une fois que l’artère est bien ouverte, et qu’un flux satisfaisant est rétabli dans le vaisseau, le tube guide et le ballon sont retirés ; par contre les introducteurs qui avaient été placés au niveau de l’artère et au niveau de la veine resteront en place pour une période de 4 heures, compte tenu du fait qu’il faut laisser épuiser l’action de l’anticoagulant qui a été injecté au début de la procédure. Les introducteurs sont ensuite retirés et vous resterez allongé 12 à 18 heures.
SURVEILLANCE PENDANT ET APRÈS L’ ANGIOPLASTIE
Pendant l’angioplastie, le patient est relié à un électrocardiographe qui en permanence surveille les contractions de votre coeur ; de la même manière, les médecins surveillent en permanence la pression artérielle. Dans un petit nombre de cas (3 à 4 %), la dilatation de l’artère peut se compliquer d’une réocclusion du vaisseau. Cette réocclusion peut apparaître alors même que que le patient est dans la salle de traitement ou alors, qu’il est revenu dans sa chambre. Cette réocclusion de l’artère se manifeste généralement par des douleurs, et/ou des modifications électrocardiographiques. Dans ce cas, le médecin peut être amené à redilater la lésion de façon à maintenir l’artère parfaitement ouverte. Il peut aussi décider de mettre en place une prothèse métallique permettant de maintenir largement béante l’artère. Cette prothèse métallique encore appellée « stent » nécessitera un traitement médical particulier qui sera poursuivi pendant un mois à six semaines.
Dans un très petit nombre de cas, si la recanalisation ou la pose d’un stent n’a pu être réalisée, ou encore si le rétrécissement n’a pu être refranchi en raison de tortuosités importantes des vaisseaux, le patient peut être amené à être transféré immédiatement dans la salle d’opération pour réaliser un pontage aorto-coronaire.
Il faut en effet rappeler que l’angioplastie coronaire et le pontage aorto-coronaire sont les deux principales méthodes qui permettent de rétablir un flux dans les artères coronaires rétrécies.
Lorsque le patient revient dans sa chambre, on continuera la surveillance de l’électrocardiogramme, la mesure de la pression artérielle et la surveillance des introducteurs qui ont été laissés en place au niveau de la région de l’aine. Comme après une artériographie coronaire, il ne doit pas mobiliser sa jambe, c’est-à-dire la plier et surtout ne pas se lever. Quatre heures après l’angioplastie coronaire, après la prise d’un antalgique par la bouche, l’introducteur sera retiré, une compression locale sera effectuée pour éviter le saignement et le patient restera allongé pendant encore 24 h.
Le lendemain de l’angioplastie le patient sera autorisé à se lever et pourra éventuellement être amené à sortir de l’hôpital ce jour ou le jour suivant.
APRÈS L’ANGIOPLASTIE CORONAIRE
Avant de quitter l’hôpital, on remettra au patient une ordonnance avec des médicaments qu’il devra prendre pendant quelque temps ; les résultats de l’angioplastie seront contrôlés tout d’abord par des examens (épreuve d’effort, scintigraphie myocardique) qui seront programmés à une date variable suivant les établissements. Ces examens s’effectuent en externe et ne nécessitent pas d’hospitalisation.
Les facteurs de risque seront complètement supprimés ; mais le patient devra :
- cesser totalement et définitivement de fumer,
- faire contrôler son taux de cholestérol et normaliser sa tension artérielle si il est hypertendu.
Le traitement d’un diabète ou d’une obésité doit être entrepris.
Dans 25 à 30 % des cas,
il est
possible
que le rétrécissement qui a été
dilaté, se reconstitue ; la
reconstitution
de ce rétrécissement s’effectue le plus souvent entre 3
et 6 mois après
l’intervention. Il est donc indispensable que le patient soit suivi
régulièrement par son cardiologue qui décidera de
l’opportunité
d’effectuer des
contrôles (épreuve d’effort, scintigraphie ou
éventuellement une
nouvelle
artériographie coronaire). Dans tous les cas, la
réapparition des
symptômes
doit amener à consulter rapidement son cardiologue.
5.2.3. Angioplastie laser :
L’athérome est
pulvérisé par un
rayonnement très énergétique provenant d'un laser. Il
s’agit de la revascularisation transmyocardique par laser (RTML) avec 3
lasers
les plus couramment utilisé.
Il existe 3 types de laser pour l'angioplastie :
- Le laser Excimere : Le milieu actif est un mélange de gaz rare et d’halogène. Sa longueur d’onde dans les ultraviolets est à 0,308 um. L’utilisation se fait par l’intermédiaire de la fibre optique
- Le laser Ho-YAG (yttrium, aluminium,garney) : Sa longueur d’onde est de 21 um et appartient aux infrarouge, et le milieu actif est cristallin. Ce cristal est dopé à l’Holmium. L’utilisation se fait par l’intermédiaire de la fibre optique
- Le laser CO2 : Le milieu gazeux de ce laser est constitué de gaz carbonique, d’azote et d’hélium. Sa longueur d’onde est de 10,6 um et appartient à l’infrarouge. Puisque sa tache focal est invisible, il est couplé avec un laser hélium néon de longueur d’onde 633nm afin que la lumière rouge de ce dernier serve de point de repère pour viser la cible.
Tableau
[2] représentant les caractéristiques des trois
types de lasers
:
|
Laser |
Energie photonique (eV) |
Longueur d’onde (um) |
|
Excimer |
4,01 |
0,308 |
|
Ho-YAG |
0,58 |
2,1 |
|
CO2 |
0,12 |
10,6 |
Le laser est surtout utilisé pour creuser dans l'amas de calcium avant de procéder à une dilatation par ballonnet.
La revascularisation transmyocardique par laser (RTML) est une technique en cours d'évaluation dans le cadre de protocoles de recherche clinique. Elle est proposée à des patients atteints d'angor sévère réfractaire au traitement médical et pour qui des traitements plus classiques (pontage aorto-coronarien, angioplastie transluminale percutanée) sont contre-indiqués en raison du faible diamètre ou de l'atteinte diffuse de leurs artères coronaires.
Le principe de la revascularisation transmyocardique par laser est inspiré du modèle reptilien : le cœur du reptile est dépourvu de circulation coronaire et le myocarde est directement irrigué par le ventricule grâce à des canalicules internes. La revascularisation transmyocardique par laser a pour objectif d'établir une communication entre la cavité ventriculaire gauche et la micro circulation coronaire. L'énergie du laser est utilisée pour créer des canaux de 1 mm de diamètre. Ces canaux augmenteraient la perfusion myocardique en créant un lien entre la micro circulation sous-endocardique et le sang circulant dans le ventricule gauche.
Les lasers utilisés pour créer des canaux transmyocardiques sont des lasers CO2 et Ho-YAG. En raison de l'importance de l'énergie délivrée par le laser CO2, seul l'abord chirurgical est possible. Deux approches moins invasives utilisant le laser Ho-YAG sont proposées : l'abord du myocarde par thoracoscopie et, moins invasive encore, la revascularisation transmyocardique percutanée par voie endocavitaire. Cependant, un laser CO2 couplé à une fibre optique vient d'être mis au point. Il pourrait être utilisé dans la revascularisation transmyocardique percutanée. Jusqu'alors seulement pratiquée par les chirurgiens, la revascularisation transmyocardique par laser est actuellement pratiquée par des cardiologues non chirurgiens. Compte tenu des résultats obtenus dans les différents centres utilisant les lasers CO2 et Ho-YAG, le bénéfice clinique chez l'homme ne paraît pas lié au type de laser.
Conclusion : L'analyse de la littérature ne permet pas de porter de jugement sur l'efficacité clinique de la revascularisation transmyocardique par laser.
Afin de conduire
une
évaluation satisfaisante de cette technologie, la Haute
Autorité de
Santé (HAS)
recommande de mener d'autres études méthodologiquement
rigoureuses. A
cet
effet, l’HAS propose une liste de questions auxquelles les
études
cliniques
devront répondre afin d'apprécier au mieux
l'efficacité et la sécurité
de la
revascularisation transmyocardique par laser. Cependant, dans les
essais cliniques,
le laser a été décevant. Cette technique semble
être en désuétude car
son
coût-efficacité est très élevé.
- Aspects réglementaire et normatifs :
Tous les lasers vendu en europe doivent étre marqués CE et doivent répondrent à la norme suivantes :
5.3. Autres méthodes :
On peut parfois associer d'autres techniques endoluminales :
- le « Rotablator » :
Le Rotablator est un appareil de
traitement des
artères calcifiées. Au lieu de déplacer et
écraser la plaque
d'athérome, il la
supprime à l'aide d'une fraise revêtue de microcristaux
diamant,
tournant à
haute vitesse. La vitesse de rotation varie selon la taille de la
fraise et la
puissance de compression. Plus la fraise a un diamètre
important, plus
sa
vitesse sera lente. La vitesse bien que très
élevée, doit être
étroitement
contrôlée et rester dans les limites indiquées par
le fabriquant. La
vitesse
varie entre 100 000 à 190 000 tours/min.La vitesse ne doit pas
être en
dessous
de 90% de celle voulue par la moteur relié à la console
de contrôle. Si
l'abaissement de la vitesse d'utilisation est de plus de 5 000
tours/min par
rapport à la vitesse initiale, cela indique une progression trop
rapide
de la
fraise et une poussée continue contre la lésion. Les
risques de
dissection, de
lésions des tissus par échauffement et la taille des
particules
ablatées
augmentent. La progression de la fraise doit se faire par petits
à
coups
réguliers
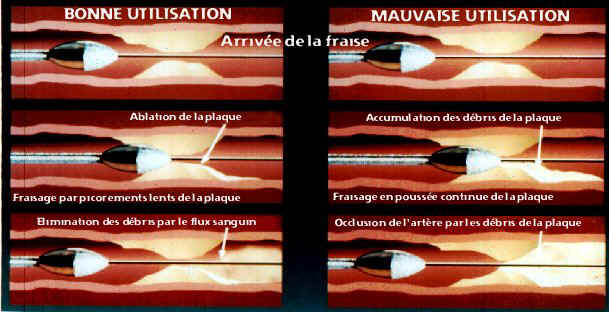
[20] : Image représentant l’utilisation d’un rotablator en angioplastie
- L’athérectomie : L'athérectomie est une méthode qui consiste à «racler» le thrombus (caillot) à l'aide d'une lame située à la pointe d'une sonde introduite dans un vaisseau coronaire.Ces indications sont adaptées aux types, aux sièges et à la nature des lésions, mais leurs indications précises restent encore à définir.
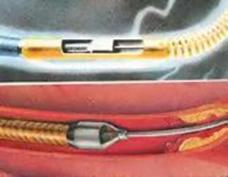
[21] : Image représentant l’utilisation de l’athérectomie en angioplastie
VI Percpective d’avenir :
- La nano-biotechnologie : fonctions biologiques et nanotechnologies
D’autres applications touchent à la santé :
Il est envisagé de construire de minuscules nano-robots, capables de se déplacer à l’intérieur du corps humain, voire dans les cellules du corps humain, à la recherche d’agents infectieux, de cellules cancéreuses par exemple, pour les marquer pour destruction par le système immunitaire, ou même pour les détruire directement.
Il a même été envisagé que ces robots aillent réparer directement l’ADN endommagé des cellules.
Des applications plus étonnantes encore sont imaginées :
- Réparation active de lésions : au lieu d’aider le corps à se raccommoder tout seul, comme le fait la médecine chirurgicale actuelle, il serait possible, par exemple, d’aider plus activement à la reconstruction, voir de recréer directement les tissus ou les organes atteints.
- Augmentation des capacités du cerveau (par exemple par interfaçage direct avec des nanoordinateurs ou des banques de données),
- Amélioration des tissus (augmentation de la solidité des os, etc.).
Évidemment,
une des retombées espérées est une augmentation
très
importante de la durée de vie, dans un état de jeunesse
préservé.
VII Désinfection des systèmes invasifs
7.1 Réglementation
- Circulaire n° 672 du 20 octobre 1997 ;
- La circulaire détaille la mise en place d’un système d’assurance qualité en stérilisation, en insistant sur les responsabilités des acteurs.
- Décret n° 1316 du 26 décembre 2000 ; (PUI).
- Arrêté du 23 avril 2002 ; mise en place d’un système d’assurance qualité en stérilisation.
- Arrêté du 22 juin 2001: relative aux Bonnes Pratiques de Pharmacie Hospitalière.
7.2 Evaluation du risque infectieux et du niveau de traitement requis
- Haut risque: ce niveau de risque correspond à l'utilisation de dispositifs médicaux qui pénètrent dans les tissus ou cavités stériles ainsi que dans le système vasculaire (cas des dispositifs médicaux invasifs de type chirurgical). Le traitement requis est la stérilisation ou l'utilisation de matériel à usage unique stérile. Si aucune des méthodes de stérilisation distante ne peut être appliquée, alors il faudra procéder à une désinfection de haut niveau.
- Risque médian: ce niveau de risque correspond à l'utilisation de dispositifs médicaux en contact avec les muqueuses ou une peau lésée superficiellement. Le traitement requis est une désinfection de niveau intermédiaire.
- Risque bas: ce niveau
de risque correspond à l'utilisation de dispositifs
médicaux qui sont
en
contact avec une peau saine ou qui ne sont pas en contact avec le
patient. Le
traitement requis est une désinfection de bas niveau concernant
essentiellement
les dispositifs non invasifs et les surfaces. Dans ce cadre,
l'utilisation de
produits détergents-désinfectants peut convenir.
Le Comité Technique national des
Infections
Nosocomiales (CTIN)
préconise la prise en compte des paramètres suivants lors
de la
détermination
du niveau d'exigences de traitement du matériel:
- Le site anatomique de destination du matériel.
- Le niveau d'asepsie de l'environnement où le matériel doit être utilisé.
- La probabilité de contamination du matériel par des liquides biologiques.
- La nature des matériaux composant le matériel.
- Les moyens technologiques disponibles pour le traitement du matériel.
Tableau [3] : Classement des dispositifs médicaux et niveau de traitement requis
|
Destination du matériel |
Classement du matériel |
Niveau de risque infectieux |
Niveau de traitement requis |
|
Introduction dans le système vasculaire ou dans une cavité ou tissu stérile quelle que soit la voie d'abord. Exemples: instruments chirurgicaux, implants, pinces à biopsie, arthroscopes, haut niveau*petite instrumentation pour pansement |
Critique |
Haut risque |
Stérilisation ou usage
unique
stérile à défaut |
|
En contact avec muqueuse, ou peau lésée superficiellement.
|
Semi-critique |
Risque médian |
Désinfection de niveau intermédiaire |
|
En contact avec la peau intacte du patient ou sans contact avec le patient.
|
Non critique |
Risque bas |
Désinfection de bas niveau |
(1) :La désinfection de haut niveau en cas d'impossibilité d'appliquer un procédé de stérilisation et s'il n'existe pas de dispositif à usage unique stérile.
- Source: "Guide de bonnes pratiques de
désinfection
des dispositifs médicaux" édité par le CTIN.
7.3 Stérilisation
La stérilisation est l'opération que doit subir un produit ou un objet pour devenir stérile, c'est-à-dire exempt de tous les micro-organismes qu'il contient ou supporte. Cependant, stériliser ne signifie pas seulement utiliser un stérilisateur. La production d'un objet stérile ne peut être mise en œuvre que dans le cadre d'un système qualité et doit être conçue dans son concept global (avant, pendant et après stérilisation).
L'ordonnance n° 96-346 du 24 avril 1996 portant sur la réforme de l'hospitalisation publique et privée stipule que les établissements de santé doivent développer une démarche continue de qualité et de sécurité des soins délivrés aux patients. Cette démarche trouve tout particulièrement son application dans la circulaire du 20 octobre 1997 où il est précisé que "le pharmacien, avec le soutien de la direction de l'établissement, met en place un système qualité pour l'ensemble des opérations de stérilisation concernant les dispositifs médicaux et ce, en travaillant avec l'ensemble des services ou instances concernées".
L'ingénieur biomédical, souvent
associé aux
décideurs
hospitaliers lors des propositions de choix d'acquisition,
d'implantation et de
maintenance du matériel de stérilisation se trouve ici
naturellement
placé en
position d’interlocuteur privilégié auprès du
pharmacien de par sa
maîtrise des
référentiels normatifs et sa connaissance des
systèmes qualité.
7.3.1. Principes
Il s'agit de la mise en œuvre d'un ensemble de méthodes et de
moyens
visant à
éliminer par destruction tous les micro-organismes vivants de
quelque
nature et
sous quelque forme que ce soit, porté par un objet parfaitement
nettoyé.
Contrairement à la désinfection et à la
décontamination, ce résultat
est
durable dans la mesure où le matériel est conservé
en état de stérilité.
La stérilisation appartient au domaine
des
probabilités. En
effet, on ne peut jamais dire que l'on stérilise à 100 %.
Il a donc été
déterminé un niveau d'assurance de
stérilité selon lequel un produit
sera
considéré comme stérile si on à une chance
sur 106 de
trouver un
germe après l'opération de stérilisation.
7.3.2. Méthodes de mise en œuvre
Il existe différentes méthodes de stérilisation
reconnues par la
pharmacopée et
utilisées de manière courante dans les
établissements de soins.
7.3.2.1. La stérilisation à la vapeur d'eau:
C'est le procédé de
référence pour la
stérilisation en
milieu hospitalier. Par l'association de la chaleur et de l'eau
sous forme
saturée, on réalise une dénaturation
protéique par l'hydrolyse
partielle des
chaînes peptidiques. Deux types de charges peuvent être
distingués:
- les charges à protection perméable où la vapeur d'eau apporte la chaleur et l'eau (matériel enveloppé en sachet papier).
- les charges à protection imperméable où la vapeur d'eau apporte uniquement les calories, le contenu du flacon apportant l'eau (soluté en flacons bouchés).
Les deux paramètres essentiels de mise en œuvre sont la température de la vapeur d'eau ainsi que la durée du cycle. La stérilisation est effectuée au moyen d'appareils à pression de vapeur d'eau appelés autoclaves. Ces appareils sont constitués d'une chambre en acier inoxydable simple ou double que l'on peut charger ou décharger par une ou deux portes opposées. Dans ce cas, l'autoclave est dit à double ouverture, il sert alors de barrière entre la zone de préparation du matériel et la zone de stockage des produits stériles. On ne peut que recommander ce circuit.
Tableau [4], Guide de bonnes pratiques de désinfection des dispositifs médicaux" édité par le CTIN :
|
Etape |
Elément à contrôler |
Contrôle à effectuer |
|
Périodiquement |
Ambiance de travail |
Contrôle de l'air Contrôle des surfaces Contrôle de la contamination initiale |
|
Autoclave |
Avant la mise en service: validation selon la norme EN 554. Contrôle de routine annuel par le fournisseur ou un organisme agréé. Tous les 10 ans: épreuve de pression |
|
|
Avant la stérilisation |
Chargement de l'autoclave |
Passage optimal de la vapeur par espacement des éléments de la charge (volume charge < 70 % volume enceinte) |
|
Fuite |
Sur stérilisateur froid: Réalisation du premier vide Arrêt de la pompe à vide Surveillance de la pression sur 10 minutes Fuite max tolérée: 1,3 mbar/min |
|
|
Pénétration de la vapeur |
Test de BOWIE & DICK |
|
|
Pendant la stérilisation |
Cycle |
Bon déroulement |
|
Après la stérilisation |
Témoin de passage |
Virage effectif |
|
Intégrateur physico-chimique |
Virage effectif |
|
|
Diagramme de Regnault |
Durée et température de chaque phase du cycle |
|
|
Stérilité |
Prélèvement d'échantillons et ensemencement |
La
charge est libérée après vérification:
- du test de BOWIE & DICK.
- du diagramme de Regnault.
- de l'intégrateur physico-chimique.
- des essais de stérilité (industrie).
7.3.2.2. La stérilisation par la chaleur sèche:
- L'agent stérilisant est l'oxygène de l'air porté à une température élevée et provoque la dénaturation des protéines bactériennes par coagulation.
- Les deux paramètres essentiels de mise en œuvre sont la température de l'air ainsi que la durée du cycle. Simple et peu coûteux, l'appareillage n'est véritablement fiable que s'il est suffisamment perfectionné pour maintenir tous ses paramètres. En effet, l'air utilisé comme vecteur de l'agent stérilisant est un isolant, la température n'est alors homogène que s'il existe un système de ventilation. On préférera donc l'utilisation de l'autoclave à celui du poupinel.
Tableau [5] ,
Guide
de bonnes pratiques de désinfection des dispositifs
médicaux" édité par
le
CTIN :
|
Etape |
Elément à contrôler |
Contrôle à effectuer |
|
Avant la stérilisation |
Chargement du poupinel |
Volume charge < 70 % volume enceinte |
|
Pendant la stérilisation |
Température |
Stabilité, correspondance de la valeur programmée par rapport à la valeur mesurée |
|
Minuterie |
Absence de dérive |
|
|
Après la stérilisation |
Témoin de passage |
Virage effectif |
|
Intégrateur physico-chimique |
Virage effectif |
|
|
Indicateur biologique |
Absence de germes |
7.3.2.3. Stérilisation par l'oxyde d'éthylène:
L'agent stérilisant est un gaz: l'oxyde d'éthylène (OE) qui a la propriété d'être un puissant bactéricide, virucide et également sporicide qui agit par alkylation des macromolécules (ADN, ARN, protéines) des micro-organismes. C'est l'agent de stérilisation le plus utilisé à l'heure actuelle. Il comporte un phénomène d'adsorption important sur les matières plastiques d'où une législation très stricte, mais reste le seul moyen utilisable pour le matériel thermosensible.
Toxicité : L’OE est toxique pour le personnel et pour le patient (dépression du système nerveux central (SNC), irritation du système respiratoire), c’est un gaz explosif et inflammable.
Paramètres de stérilisation :
- La concentration en gaz (400 à 800 mg/l), il est utiliser pur dans les appareils en dépression et en mélange avec un gaz neutre dans les appareils en surpression (1 à 6 bars)
- La durée d’exposition au gaz (3 à 12 heures),
- La température (50 à 60 °C),
- L’humidité relative (30 à 60 %) indispensable à la réaction.
Normes :
- NE EN 550 : Stérilisation des DM – validation et contrôle de routine pour la stérilisation à l’OE.
- NE EN 1422 : stérilisateur à usage médical – stérilisateur à l’OE – exigences et méthodes d’essai.
Tableau
[6] , Guide
de bonnes pratiques de désinfection des dispositifs
médicaux" édité par
le
CTIN :
|
Etape |
Elément à contrôler |
Contrôle à effectuer |
|
Périodiquement |
Ambiance de travail |
Personnel qualifié et soumis à une surveillance médicale régulière Locaux protégés contre les flammes et les étincelles Présence d'une chambre de désorption |
|
Appareil |
Validation annuelle selon la norme EN 550 |
|
|
Matériel |
Se référer à la norme ISO 10993-7 de janvier 1996 qui fixe les doses maximales admissibles d'oxyde d'éthylène en fonction des dispositifs médicaux |
|
|
Avant la stérilisation |
Chargement de l'appareil |
Volume charge < 70 % volume enceinte |
|
Pendant la stérilisation |
Cycle |
Bon déroulement |
|
Après la stérilisation |
Témoin de passage |
Virage effectif |
|
Intégrateur physico-chimique |
Virage effectif |
|
|
Diagramme d'enregistrement |
Conformité avec le graphique type du fabricant |
|
|
Indicateur biologique |
Absence de germes |
7.3.2.4. Stérilisation centralisée
- Le rôle de cette structure est de permettre de regrouper tous les sites de stérilisation sous le contrôle du pharmacien afin d'obtenir une homogénéité de fonctionnement avec la mise en place d'un système d'assurance qualité. Le but est d'assurer une rationalisation de l'utilisation du matériel en réalisant simultanément un gain financier ainsi qu'un gain de temps pour le personnel infirmier tout en obtenant une diminution du risque de faute d'asepsie.
- La stérilisation centrale doit se trouver à proximité des blocs opératoires ou à défaut être relié aux blocs par l'intermédiaire de deux monte-charges distincts, l'un est réservé au circuit propre et l'autre au circuit sale. Elle est constituée de deux zones:
- une zone sale dans laquelle s’effectue les étapes de réception du matériel souillé, de nettoyage et de tri.
- une zone propre dans laquelle s'effectuent les trois étapes suivantes: conditionnement, stérilisation, et stockage.
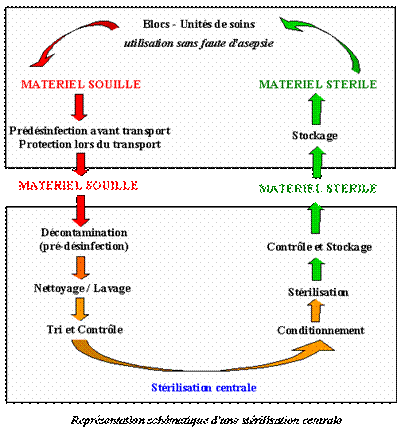
[22] : image représentant le déroulement d’une stérilisation centrale - Cours de stérilisation UTC M.Belhout
7.4 Aménagement des locaux et les travaux de construction
L'espace hospitalier est hiérarchisé en fonction de la population microbienne qu'il est susceptible d'héberger. il est possible de distinguer quatre zones :
- La zone stérile = "entrée interdite". En effet, dès qu'un individu y pénètre, cette zone cesse d'être stérile.
- La zone propre = "Réglementation", dans laquelle il sera possible de distinguer trois sous-zones: la zone ultrapropre (salle d'opération), la zone très propre (salle de soins, salle de réveil), la zone propre (services).
- La zone sale = "danger", subdivisée en deux sous-zones: la zone sale (chambre d'isolement curatif), la zone très sale (isolement absolu, stockage des déchets).
- La zone sociale, représenté par les espaces communs, bureaux, salles de détente, couloir, escalier. Ce sont des zones inclassables qui reçoivent une population variée.
Il est clair que les communications entre ces quatre zones doivent être contrôlées et réglementées afin d'éviter tout transfert de souillure. Ceci va générer deux types d'espace : les zones à accès libre et les zones à accès réglementé.
En ce qui concerne les circuits et les flux, on distinguera le circuit humain, qui concerne le personnel, les malades, les visiteurs et le circuit des matières inertes, qui concerne le matériel propre ou sale, le linge propre ou sale, les déchets, l'alimentation. Tous les circuits sont basés sur la notion de protection du "propre" et du "sale" ainsi que sur la notion de progression du propre vers le sale.
Deux types de circuits peuvent être envisagés à ce jour: le double circuit et la circulation unique.
Le double circuit:
Il comporte une individualisation de deux circuits : un circuit sale et un circuit propre. Deux variantes sont possibles:
- Le sens unique ou tout entre du côté propre et tout ressort du côté sale.
- Une circulation codifiée ou la circulation propre est réservée à l'entrée et à la sortie des malades et du personnel ainsi qu'à l'entrée du matériel propre. La circulation sale est alors réservée à la sortie du linge sale, du matériel souillé et des déchets.
L'inconvénient de ce type de circuit est qu'il concentre l'essentiel du trafic des personnes dans le couloir "propre", ce tend à donner aux utilisateurs un sentiment de sécurité pernicieux, alors que le couloir dit "sale", peu fréquenté, doté d'un personnel spécifique et faisant l'objet de soins particuliers, reste finalement propre. De plus, cette solution est coûteuse en surface et en personnel
La circulation unique:
Tout transite par le même couloir. Tout le matériel doit être protégé dans un conditionnement fermé et étanche. C'est la solution actuellement la plus avantageuse, qui permet un gain d'espace et nécessite moins de personnel. La qualité de la circulation est évaluée par la facilité de manœuvre, la possibilité de croisement et l'emplacement des issues. Tous les éléments gênants ou mal intégrés dans les circulations sont à proscrire
Rôle du personnel de maintenance et des ingénieurs hospitaliers:
Il importe de noter que c’est le
personnel
de maintenance qui pourrait être appelé à faire le
travail selon le
type de
travaux de construction qui sont effectués dans les
établissements de
soins de
santé. De même, ce sont parfois des ingénieurs qui
conçoivent le
projet. Aussi,
nous abordons leur rôle dans cette catégorie en même
temps que celui
des
entrepreneurs.
Les ingénieurs, le personnel de maintenance et les entrepreneurs également doivent se conformer aux codes du bâtiment et de prévention des incendies ainsi qu’à des normes professionnelles dans l’exécution de projets de construction. Leurs tâches consistaient à planifier et exécuter des travaux de construction ou de rénovation et à réparer les structures, l’équipement et les services dans les établissements de soins de santé. De plus, ils doivent surveiller et évaluer le système de ventilation dans la zone où se déroulent les travaux et les aires adjacentes afin de s’assurer qu’il fonctionne correctement, non seulement avant le début des travaux mais aussi pendant toute leur durée et à la fin de ceux-ci. Pour ce faire, ils doivent mesurer le débit d’air, la pression d’air et le nombre de renouvellements d’air à l’heure.
Ces tâches englobent l’évaluation, le nettoyage et la vérification de l’intégrité des filtres et des canalisations. Les ingénieurs, le personnel de maintenance et les entrepreneurs doivent également ériger un écran anti-poussière et prévenir les infiltrations de poussière dans les zones adjacentes pendant le projet de construction. Les entrepreneurs ont la responsabilité de veiller à ce que le chantier soit exempt de débris.
De plus, si la plomberie de l’hôpital est touchée par les travaux, c’est à eux que revient la tâche d’en contrôler l’intégrité, de rechercher les fuites et de réduire au minimum le nombre de conduites en cul-de-sac. Les ingénieurs et le personnel d’entretien peuvent aider à enseigner aux entrepreneurs les pratiques de construction sécuritaires pendant qu’ils travaillent dans des établissements de soins de santé. Etant donné que ce sont ces professionnels qui exécutent les travaux de construction, les professionnels en prévention des infections devraient être en contact avec eux pendant les travaux. Ces derniers, en collaboration avec les gérants de projet, doivent veiller à ce que les mesures
préventives soient appliquées et observées pendant toute la durée du projet. Ils peuvent donc donner des conseils aux ingénieurs, au personnel de maintenance et aux entrepreneurs quant aux mesures préventives indiquées pour les travaux en cours.
Une fois le projet terminé, ils devraient revoir et évaluer l’efficacité des mesures préventives avec les autres membres du comité de planification du projet de construction pour déterminer les résultats positifs et tout problème qui pourrait être survenu.
VIII L’impact humain et économique lié aux éléments d’athérosclérose
Selon l’OMS, les maladies cardiovasculaires sont la cause de 16,7 millions de décès dans le monde en 2003, soit 29,2 % des décès totaux. En France, ce pourcentage s’élève à 51 % selon le Haut comité de santé publique : les maladies cardiovasculaires sont la première cause de mortalité devant les cancers.
La maladie coronaire, les accidents vasculaires cérébraux et l’insuffisance cardiaque sont les causes principales de la mortalité. Environ 50 % des morts d’origine cardiaque sont des morts subites, le plus souvent liées à des troubles du rythme.
Chaque année, au moins 20 millions de personnes dans le monde survivent à un accident cardiaque, et la plupart doivent bénéficier de soins continus et coûteux (11,5 % des hospitalisations en France relèvent des maladies cardiovasculaires qui arrivent ainsi au premier rang).
On estime qu’en 2020 les maladies cardiovasculaires seront la première cause de mortalité dans le monde, en raison, d’une part, de la diffusion du mode de vie occidental dans les pays en voie de développement (incluant entre autres une alimentation déséquilibrée, la sédentarité et la consommation de tabac), et, d’autre part, du vieillissement des populations.
En effet,
les individus des pays industrialisés sont
de plus en plus nombreux à présenter un surplus de poids
résultants de
changements majeurs dans leurs habitudes de vie. Ainsi
l’obésité est en
voie de
devenir le problème de santé le plus commun du 21 eme
siècles, puisque
elle
contribuera de façon importante à la prévalence,
malgré tout élevé, des
maladies cardiovasculaires dans les pays en voie de
développements.
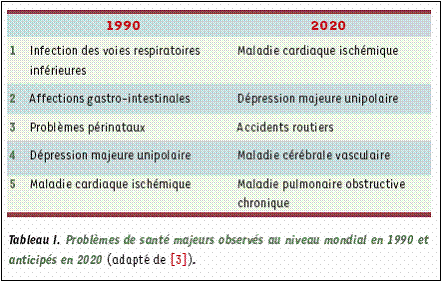
Tableau [7]
présentant le
classement des problèmes de santé majeur dans le
monde en 1990 et
extrapolé en
2020 :
Des traitements efficaces ont été développés très récemment améliorant de façon notable le pronostic de la maladie et la qualité de vie des patients. Ses traitements, pour la plupart pharmacologiques, sont le résultat de recherches d’amont, avec en particulier des avancées réelles dans la compréhension de mécanismes moléculaires transcriptionnels et génétiques de l’hypertrophie et du remodelage cardiaque et de la transition vers l’insuffisance cardiaque. D’autres contributions importantes sont en relation directe avec la compréhension des mécanismes d’adaptation périphériques, notamment neurohormonales, de la maladie. Ce domaine de l’insuffisance cardiaque est riche d’exemples de découvertes expérimentales générées par des hypothèses issues de la recherche clinique. A cet égard la recherche dans ce domaine est typiquement transversale, intégrative, avec des transferts rapides entre sciences fondamentales et recherche appliquée.
Le rapport de l’INSERM (Institut National de la Santé et de la Recherche Médical) de la version 3.2 de Février 2003 nous fait savoir que la part des moyens directs engagés sur les maladies cardiovasculaires est de 9 % du budget de l’institut. 187 Chercheurs et 167 ingénieurs et techniciens sont impliquées dans les recherches liées aux maladies cardiovasculaires. Certains CIC (Centre d’Intervention Clinique) prennent part à ces recherches, en liaison direct avec des malades cardiovasculaires.
Les pathologies cardiovasculaires les plus étudiées sont :
o athérosclérose
o thrombose
o pathologie vasculaire
o hypertension artérielle
o complication rénale des maladies cardiovasculaires
14 laboratoires sont impliqués dans la recherche génétique des maladies cardiovasculaires.
6 laboratoires sont impliqués dans la recherche en méthode de diagnostic en imagerie fonctionnel et dynamique.
En conclusion, les maladies cardiovasculaires vont devenir de plus en plus croissante d’ici les 15 prochaines années, et il est nécessaire d’être préventif vis-à-vis du surplus de poids dans les pays industrialisés. Malgré tous l’état par le biais de l’INSERM à pris en compte les problèmes liés au maladies cardiovasculaires et lancent différents projets de recherches afin de réduire et soigner ces maladies.
IX Conclusion:
L’athérosclérose est la première cause de mortalité en France, est et connue par ses conséquences comme l’infarctus du myocarde, l’angine de poitrine et l’insuffisance cardiaque. C’est un véritable problème de santé publique qui sont du à des causes comme le tabac, une habitude alimentaire trop riche, et des maladies mono génique. Les causes de l’athérosclérose sont pris en compte, et l’état commence à sensibiliser les gens par des campagnes de publicité contre le tabac et l’alimentation trop riche .Mais dans les années à venir, avant que les effets de l’athérosclérose commence à diminué, il est nécessaire de soigner ces personnes, parfois dans des situations d’urgence. Pour cela il existe deux méthodes, la première est le pontage aorto-coronarien, qui permet de faire un pontage à l’endroit ou la lumière de l’artère est rétrécie, mais il est nécessaire de faire avant un diagnostic en radiologie ; La deuxième est l’angioplastie qui consiste à faire élargir la lumière de cette artère directement en interventionnelle sous angiographie. Il existe l’angioplastie transluminal percutané qui consiste à passé un cathéter avec un ballonnet à son extrémité commandé par le médecin, pour élargir pendant un temps très court (quelques secondes à une minute) l’endroit de l’artère rétrécie. Tous cela assisté en temps réel par angiographie. La plupart des fois il est nécessaire de poser un ressort à l’endroit de l’artère rétrécie afin qu’elle ne puisse pas se rétrécir de nouveau, il s’agit d’une endoprothése coronaire ou « stent » .
D’autres méthodes comme l’angioplastie laser, le rotablator et l’athérectomie existe mais ne sont pas trop répandu.
L’angioplastie avec ou sans pose d’endoprothése coronaire « stent », sous angiographie est la méthode la plus courante en athérosclérose interventionnelle, mais pose des problèmes de radiation à cause des rayons X. C’est pour cela qu’une méthodes émarge « l’imagerie IRM en interventionnelle » qui n’irradie pas le patient et qui permet un diagnostic direct et moins coûteuse. L’inconvénient est l’aspect environnemental du au problème magnétique, comme le type de cathéter et tout consommable nécessaire à l’intervention qui doivent être paramagnétique. De plus certains patients ne peuvent utiliser l’IRM en interventionnelle comme des patients qui ont des « pacemakers ». Si cette méthodes, pris en compte par les constructeurs, règles ces problèmes (paramagnétiques, produits de contraste autre que Galvolénium…), elle risque d’évoluer et de détrôner l’angioplastie sous angiographie et la coronographie. Déjà Philips avec son IRM ouvert présage l’imagerie par résonance magnétique en interventionnelle pour les problèmes d’athérosclérose.
Nous devons rappeler que la méthode de plasmaphérèse ainsi que certain traitement thérapeutique permettent d’éviter des problèmes d’athérosclérose aigue, en effet si le patient est décelé assez top, par exemple par prise de sang (LDL) cela éviterai des interventions plus lourdes .
L’avenir très lointain, est la nano biotechnologie, qui permettra grâce à des nano robots à reconstruire et nous plus détruire une partie de l’artère endommagée. Cela reste encore fictif, mais l’évolution de la technologie étant très croissante (comme les ASIC) attendons nous à une révolution dans le domaine du traitement de l’athérosclérose.
X Références bibliographiques :
Extraction internet :
- Général :
- Programme national de recherche sur les maladies cardiovasculaires (PNRC)
- Laboratoire de cathétérisme cardiaque :
- Fondation Suisse de Cardiologie - reconnue d'utilité publique par le ZEWOFédération française de cardiologies.Source : magazine santé Giropharm n° 25
- Ischémies myocardiques transitoires Angine de poitrine Pr. Daubert Département de cardiologie et maladies vasculaires CHU de Rennes, 2 rue Henri Le Guilloux, 35033 Rennes :
- Echo-doppler :
- Poster
sur
l’échographie doppler du master MTS
2004-2005
https://www.utc.fr/~farges/Master (Cours UTC, présentation de l'échographie de Mr Alain Bectard)
- Angioplastie avec pose de stent :
- Projet
d’intégration sur « Etat
de l'art des techniques cardio-vasculaires pour le traitement de la
sténose » de L. MANGENOT
- N. NOURI ,
Projet
DESS "TBH", UTC, année 2001-2002 :
- Angioplastie laser :
- Étude d'Evaluation
Clinique des
techniques de revascularisation transmyocardique par laser :
http://www.anaes.fr/anaes/anaesparametrage.nsf/Page?ReadForm&Section=/anaes/Rechercher.nsf/Rechercher?OpenAgent&Fuzzy=c&query=laser§rec=all
- Société francaise des lasers médicaux :
- Athérectomie :
- Angioplastie abrasive par lame vibrante :
- Désinfection :
- Différents types de stérilisations des dispositifs médicaux :
http://www.hospvd.ch/swiss-noso
Fichier pdf :
http://eliot.utc.fr/eversuite/GetDoc?DBName=dPortal&ShowPath=false&UniqueKeyValue=6059
- INSERM : Etats des lieux des recherches dans les domaines cardiovasculaires 2002 éditions de Février 2002 http://www.inserm.fr/fr/recherches/etats_des_lieux/att00002003/CARDIO2002_v3.2.pdf
XI Bibliographie
Image du document
[1] Image d’artère coronaire
:
http://www.cdn-geneve.ch/4791/57348.html
[2] Image d’artère : formation d une plaque d’athérome compliquée :
http://www.cdn-geneve.ch/4791/57348.html
[3] Image à un croisement d’une artère avec athérosclérose :
http://eva3s.hegp.bhdc.jussieu.fr/index.php
suivre"
coin des patients",
puis
"procédure d'angioplastie"
[4] Image d’un processus
pathologique
d’athérothrombose :
http://www.123bio.net/revues/jleoni/3chap1.html
image"Figure 1.3 : Processus
pathologique de
l'athérothrombose".
[5] Image d’un schéma d’une table dédiée à l’angiographie :
[6] Angiographie
carotidienne:
www.carotide.com/espace_ public/public_diagnos
Image
angiographique :
http://www.snof.org/maladies/toxemie_gravidique.html
[7] Schéma
du principe de fonctionnement d’un scanner :
http://perso.wanadoo.fr/
simon.doligez/page2.htm
[8] Image angio CT et angio CT 3D :
www.clevelandclinic.org/.../
stroke/advances.htm.
Angioscanner
montrant une sténose :
www.carotide.com/espace_
public/public_diagnos
[9] Salle d’angio-RM :
www.ifc.cnr.it/assistenza/
5-risonmagnetica.html.
[10] Angiographie par résonance magnétique des abords vasculaires,Christine JAHN,CHRU Strasbourg (par fichier PDF):
http://www.sfav.org/Publication/SFAV2004/02-04.pdf
suivre "
B : ARM MIP de face, temps arterial, oblitération de
l'artère humérale gauche"
[11] Image d’un examen en
échographie Doppler :
http://www-sop.inria.fr/epidaure/personnel/malandain/cours/Imagerie-Medicale/sld105.htm
[12] Appareil d’échographie
doppler :
http://www.ch-aulnay.fr/medico-technique/radiologie.htm
[13] Image de sonde d’angioplastie
à
ballonnet :
https://www.utc.fr/~farges/dess_tbh/96-97/Projets/II/II.htm
[14] Photo d’une intervention angiographique :
https://www.utc.fr/~farges/dess_tbh/96-97/Projets/II/II.htm
[15] Image représentant le
schéma de
principe
d’une menbrane de plasmaphérese :
http://www.membrana.de/oxygenation/plasma/plasmasep.htm
[16]
Image représentant un appareil de plasmaphérese :
http://www.transfusion.be/pages/fr/plasmapherese.php
[17] Image représentant une angioplastie transluminal percutané
Fondation Suisse de Cardiologie - reconnue d'utilité publique par le ZEWO.
http://www.prevention.ch/diagnosticsmaladiecoronarienne.htm
[18] Image représentant une angioplastie transluminal percutané : Projet d’intégration sur « Etat de l'art des techniques cardio-vasculaires pour le traitement de la sténose » de L. MANGENOT - N. NOURI , Projet DESS "TBH", UTC, année 2001-2002 :
https://www.utc.fr/~farges/liste_tvx/mts_dess/tvx_mts_dess.htm
suivre "Projets DESS "TBH" 2001-2002"
[19] Image représentant une
angioplastie avec
pose de stent : Projet
d’intégration sur « Etat
de l'art des techniques cardio-vasculaires pour le traitement de la
sténose » de L. MANGENOT
- N. NOURI ,
Projet
DESS "TBH", UTC, année 2001-2002 :
https://www.utc.fr/~farges/liste_tvx/mts_dess/tvx_mts_dess.htm
suivre "Projets DESS "TBH" 2001-2002"
[20] Image représentant
l’utilisation d’un
rotablator en angioplastie :
http://www.angiocardio.com/techniqu.htm
[21] Image représentant
l’utilisation de l’athérectomie en angioplastie :
http://www.zoomsante.com/content/1
[22] Cours de stérilisation UTC M.Belhout
Tableau du document
[Tableau 1] Guide de bonnes pratiques de
désinfection
des dispositifs médicaux" édité par le CTIN , comparaison des techniques d’imagerie
interventionnelle :
http://www.sante.gouv.fr/htm/pointsur/nosoco/
[Tableau 2] Tableau récapitulatif
des
différents
lasers utilisé dans le domaine médical : Evaluation
clinique des
techniques de revascularisation transmyocardique par laser ANAES
service
évaluation technologique modifier par Marc DEGRAIN :
http://www.anaes.fr
[Tableau 3 ] "Guide
de bonnes pratiques de désinfection des dispositifs
médicaux" édité par
le
CTIN ,
classement des
dispositifs médicaux
et niveau de traitement requis :
www.sante.gouv.fr/htm/pointsur/nosoco/
[Tableau 4] Guide
de bonnes pratiques de désinfection des dispositifs
médicaux" édité par
le
CTIN :
www.sante.gouv.fr/htm/pointsur/nosoco/
[Tableau 5] Guide
de bonnes pratiques de désinfection des dispositifs
médicaux" édité par
le
CTIN :
www.sante.gouv.fr/htm/pointsur/nosoco/
[Tableau 6] Guide
de bonnes pratiques de désinfection des dispositifs
médicaux" édité par
le
CTIN :
www.sante.gouv.fr/htm/pointsur/nosoco/
[Tableau 7] Tableau extrapolant les
problèmes de santé
cardiaque entre 1990 et 2020 de Tableau de
médecine/sciences
(obésités et
maladie cardiovasculaires de Mr Poirier et Després):
http://www.erudit.org/revue/ms/2003/v19/n10/007164ar.html
suivre
"Problèmes de
santé majeurs observés au niveau mondial en 1990 et
anticipés en 2020"
tableau 1.
XII
GLOSSAIRE :
|
|
|
|
|
|
|
SYSTÈME CARDIOVASCULAIRE ET FONCTIONNEMENT |
|
PATHOLOGIES, FACTEURS DE RISQUE |
|
|
•
Activateur tissulaire du plasminogène (TPA) : |
|
•
Anémie : |
|
|
EXAMENS, EXPLORATIONS, SURVEILLANCE |
|
TRAITEMENTS |
|
|
• Analyses
biologiques : • Athérectomie technique récente consistant à introduire un instrument "décapant" la plaque d'athérosclérose à l'intérieur d'une artère : rayon laser, fraise… Technique peu utilisée à laquelle on préfère l'angioplastie. |
|
•
Anastomose :
|