|
Avertissement
|
Si vous arrivez directement
sur cette page, sachez que ce travail est un rapport d'étudiants
et doit être pris comme tel. Il peut donc comporter des
imperfections ou des imprécisions que le lecteur doit admettre
et donc supporter. Il a été réalisé pendant
la période de formation et constitue avant-tout un travail de
compilation bibliographique, d'initiation et d'analyse sur des
thématiques associées aux technologies
biomédicales. Nous ne faisons
aucun usage commercial et la duplication est libre. Si vous avez des
raisons de contester ce droit d'usage, merci de nous
en faire part . L'objectif de la présentation sur
le Web est de permettre l'accès à l'information et
d'augmenter ainsi les échanges professionnels. En cas d'usage du
document, n'oubliez pas de le citer comme source bibliographique. Bonne
lecture... |
|
Déploiement
du Guide des Bonnes Pratiques
Biomédicales
&
Acquisition
de dispositifs médicaux
|

Véronique
ARFIB
|
Référence
bibliographique à rappeler pour tout usage :
Déploiement du Guide des
Bonnes
Pratiques Biomédicales & Acquisition de dispositifs
médicaux, Arfib Véronique
Stage de fin d'études, MASTER Management des Technologies
en
Santé (MTS), UTC, 2007-2008
Université de
Technologie de Compiègne
|
RESUME
Instaurer une démarche Qualité et
exécuter le Plan
d’investissement constituent deux aspects importants de la
fonction d’un ingénieur biomédical.
Après une présentation du centre Hospitalier de Millau,
ce rapport détaille l’évaluation des pratiques du Service
Biomédical puis leur orientation dans le cadre du Guide des Bonnes Pratiques
Biomédicales.
Cette démarche a conduit à définir des objectifs
mesurables pour chacune des missions du service et à en suivre
l’avancement par l’intermédiaire d’un tableau de bord dynamique.
Enfin, la dernière partie de ce rapport évoque deux dossiers d’achat et leurs
différentes étapes, avec notamment la rédaction du
Cahier des Charges, l’organisation d’essais et l’analyse des offres.
Mots
clés: démarche Qualité, Guide des Bonnes
Pratiques, tableau de bord, Plan d’investissement, dossiers d’achats
|
ABSTRACT
Establishing a Quality approach and carrying out
the Investment Plan are two
important aspects of biomedical engineer function.
After presenting the Hospital Centre of Millau, this report details the
evaluation of the Biomedical Department practices and their orientation
within the Guide of Good Biomedical
Practices.
This approach has led to define measurable targets for each missions of
the department and monitor its progress through a dynamic dashboard.
Finally, the last part of this report refers to two cases of purchase and their
different steps, including specifications drafting, tests organisation
and offers analysis.
Keywords:
Quality approach, Guide of Good Biomedical Practices, dashboard,
Investment Plan, cases of purchases
|
Remerciements
Je remercie
chaleureusement Monsieur Christophe David,
Ingénieur Biomédical du Centre
Hospitalier de Millau, pour m’avoir accueillie dans son service ainsi
que pour sa confiance et son encadrement durant ces 5 mois.
Je remercie Messieurs Lionel Agrinier et Sébastien
Cousinié, Techniciens Supérieurs Hospitaliers de m'avoir
intégré à l’atelier biomédical et fait
partager leur enthousiasme pour leur métier.
Je remercie Monsieur Louis Blache pour ses conseils lors de sa visite
de suivi de stage.
J'adresse aussi mes remerciements à toutes les personnes que
j'ai pu rencontrer au cours de ce stage et que je ne peux citer
nommément, pour toutes les connaissances qu'elles ont pu
m'apporter.
Enfin, je tiens à remercier Messieurs Georges Chevallier et
Gilbert Farges, respectivement Responsable du Master MTS et Enseignant
Chercheur à l’UTC, pour la qualité des enseignements
dispensés.
Sommaire
Introduction
Partie 1: Présentation du Centre
Hospitalier de Millau
Partie 2 : Mise en place du Guide des Bonnes Pratiques
Biomédicales
Partie 3 : Participation à l’exécution du plan
d’investissement biomédical
Conclusion
Références
Table des annexes
retour
sommaire
Introduction
La mise en place d’une
démarche Qualité s’impose désormais à
l’ensemble des Hôpitaux et notamment aux Services
Biomédicaux. La question est maintenant de définir le
niveau d’exigences que l’on veut atteindre.
Le Service Biomédical du Centre Hospitalier de Millau a
été classé comme point fort de
l’établissement suite à la visite d’accréditation
V1 en 2006, sur la base d’un premier projet de développement
émis lors de sa création en Septembre 2002.
Après 6 années d’exercice et afin de rester dans le cadre
d’une dynamique d’amélioration continue de la Qualité de
son organisation et de ces pratiques, le service a souhaité
cette année intégrer un stagiaire, dans le but d’apporter
un regard neuf et de susciter de nouvelles pistes de progrès sur
la base de l’intégration du Guide des Bonnes Pratiques
Biomédicales.
Une discussion sur la pertinence de s’engager ou non sur la voie d’une
certification ISO 9001 version 2000 devait également être
entamée.
C’est dans ce cadre que j’ai été recrutée pour
effectuer mon stage de Master 2 « Management des Technologies en
Santé » durant 5 mois.
Après 3 premières semaines d’intégration à
l’atelier pour assimiler le fonctionnement du service, mon travail
s’est centré sur la réalisation d’un état des
lieux des pratiques du service, puis sur l’orientation de celles-ci
dans le sens du Guide des Bonnes Pratiques Biomédicales.
En marge de ces actions, j’ai également collaboré
à l’exécution du plan d’investissement de
l’établissement en réalisant différents dossiers
d’achat.
Après une présentation du Centre Hospitalier de Millau,
j’aborderai l’évaluation des pratiques et la mise en place du
Guide au sein du Service biomédical, puis j’évoquerai ma
participation aux processus d’acquisition de deux injecteurs de
produits de contraste et d’un automate d’immuno-hématologie.
Partie
1:
Présentation du Centre Hospitalier de Millau
I.
Contexte : le Centre Hospitalier Intercommunal du
Sud Aveyron
Au 1er janvier 2000, la fusion des
établissements de Millau (Figure 1) et de Saint-Affrique (Figure
2) avait permis la création du Centre Hospitalier Intercommunal
(CHIC) du Sud Aveyron. Les 2 établissements, distants d’une
trentaine de kilomètres, offrent les mêmes prestations
médicales.
Figure 1: Centre Hospitalier de Millau
Figure 2: Centre Hospitalier de
Saint-Affrique
Le CHIC disposait de 746 lits et places (respectivement 456 pour Millau
et 290 pour Saint-Affrique) et employait plus de 950 personnes dont
près de 60 médecins. Il réalisait chaque
année plus de 10 000 entrées et 235 000 journées
d’hospitalisation et d’hébergement, enregistrant près de
21 000 passages dans les Services d’urgences.
Le contexte interhospitalier difficile a entraîné au 1er
Janvier 2008 la dissolution du CHIC. Chacun des hôpitaux
fonctionne à nouveau de façon indépendante,
même si des conventions de collaboration ont été
signées, notamment pour le Service Biomédical et le
Service Qualité.
Le Centre Hospitalier de Millau est
dirigé :
- par un Directeur nommé par le Ministre chargé de la
santé, assisté d’une équipe de Direction
- par le Conseil d’Administration, présidé par un
membre élu au sein du conseil. Il est composé
d’élus de collectivités territoriales (communes, conseil
général et régional), des représentants des
personnels et des médecins hospitaliers, des
représentants des usagers et de personnes qualifiées.
Il définit
la politique générale de l’établissement. Ces
décisions s’appuient, en particulier, sur les avis donnés
par 2 instances :
- La Commission Médicale d’Etablissement
- Le Comité Technique d’Etablissement
Suite à la défusion,
l’établissement est désormais organisé comme suit
(Figure 3):
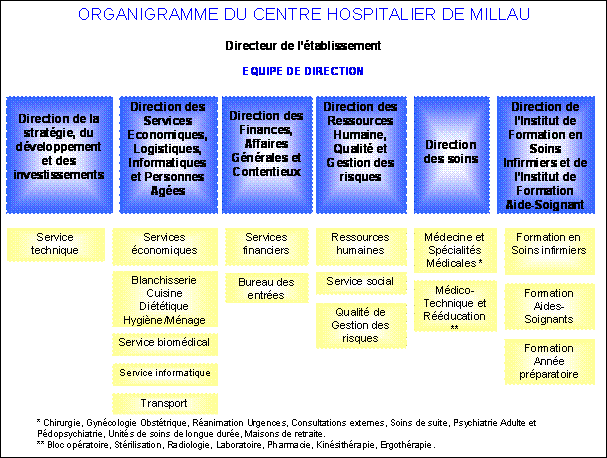
Figure 3: Organigramme général du Centre
Hospitalier de
Millau
L’action des professionnels du Centre
Hospitalier de Millau s’inscrit dans le respect des 4 principes
fondamentaux du service public hospitalier :
- assurer des soins de jour comme de nuit, tout au long de
l’année
- garantir l’accès de tous aux soins
- prendre en charge tous les usagers
- évoluer pour garantir une prestation de qualité
Le CHIC s’était engagé
dans une démarche d’amélioration continue de la
qualité et de la sécurité des soins
recommandée par la Haute Autorité de Santé (HAS).
En 2006, il a obtenu son accréditation V1.
L’accréditation est une procédure d’évaluation
externe effectuée par des professionnels, indépendante de
l’établissement de santé et de ses tutelles, concernant
l’ensemble de son fonctionnement et de ses pratiques.
La première version (V1) de l’accréditation a
été lancée sur le plan national en Juin 1999.
Le second cycle (V2) de la démarche a débuté au
dernier trimestre 2004, avec une plus grande simplicité du
manuel et de la procédure, une médicalisation plus
importante et une meilleure lisibilité des résultats. Le
Centre hospitalier de Millau suit cette voie en préparant
l’accréditation V2 pour 2010.
Outre le fait de répondre
à un besoin des utilisateurs de dispositifs médicaux, le
Service biomédical du Centre Hospitalier de Millau trouve une de
ses origines dans la nécessité d’une maîtrise
totale du parc d’équipement de l’investissement à la
réforme dans le cadre de l’accréditation V1.
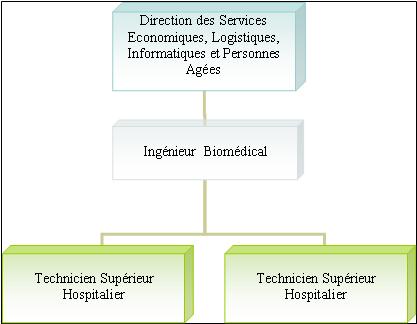
Créé en Septembre 2002 et placé sous la Direction
des Services Economiques, Logistiques, Informatiques et Personnes
Agées, il est actuellement composé d’un Ingénieur
et de deux Techniciens supérieurs hospitaliers (Figure 4).
Figure 4: Organigramme du Service Biomédical
Le personnel biomédical
intervient également sur les 6 sites annexes qui
dépendent du Centre Hospitalier, situés en centre ville
(Maison de Retraite de l’Ayrolle, Sainte-Anne…).
Depuis le 1er Janvier 2008, par convention, il gère et maintient
le parc de dispositifs médicaux du Centre Hospitalier de
Saint-Affrique en plus de celui de Millau.
Le Service biomédical dispose d’un atelier sur chacun des 2
hôpitaux :
- Atelier de Millau : localisé à l’entrée du
bloc opératoire, l’atelier est organisé en zone de
travail de manière à pouvoir traiter l’essentiel de
l’activité corrective et préventive des deux centres
hospitaliers.
- Atelier de Saint-Affrique : localisé à
proximité du Service technique, l’atelier permet de disposer sur
place d’un local de travail pour les dépannages, d’un stock de
pièces détachées minimum, d’un lieu de stockage
avant mise en service des équipements neufs sur le site et d’un
poste informatique de GMAO.
Sa mission principale est de maintenir le parc d’équipements
biomédicaux en parfait état de fonctionnement et de
sécurité pour les patients et les utilisateurs.
Dans ce cadre, le Service biomédical exerce l’ensemble de ses
activités à partir de besoins exprimés par les
Services clients et regroupés en quatre domaines :
- EQUIPEMENTS : réalisation des investissements suivants des
protocoles ou fiche technique d’achats, de mise en service et de
réforme en lien avec le Service économique.
- MAINTENANCE : réalisation et traçabilité des
interventions de maintenance interne et externes suivants des
protocoles ou fiches techniques de traitement des demandes
d’intervention, de commande, de réception, de gestion des
contrats ou de traçabilité des équipements. Des
équipements de contrôle, de mesure et d’essai (ECME)
permettent aux techniciens de réaliser les contrôles des
équipements biomédicaux lors des interventions de
maintenance préventive, de contrôle qualité ou
après intervention de maintenance curative, et un logiciel de
GMAO en assure la traçabilité informatique.
- MAITRISE BUDGETAIRE : suivi et optimisation des dépenses
d’exploitation et d’investissement afin de respecter les budgets
alloués.
- VEILLE TECHNIQUE ET REGLEMENTAIRE : suivi des évolutions
technologiques et normatives des équipements afin de planifier
ou d’organiser les renouvellements d’équipements. Le service est
intégré à l’organisation de la
matériovigilance.
Dans la limite de ses compétences et de sa capacité de
prise en charge du volume d’activité, le service
privilégie une politique de maintenance interne afin d’une part
de minimiser les temps d’immobilisation des équipements et
d’autre part de mieux maîtriser l’évolution des
dépenses de maintenance.
En parallèle, pour mener à bien sa mission sur l’ensemble
du parc d’équipements et se conformer à la
réglementation, le service fait appel à des prestataires
de maintenance ou organismes de contrôles soit par des demandes
ponctuelles soit par la mise en place de contrat de maintenance.
VI.
Intégration au Centre Hospitalier de Millau
Durant les 3 premières
semaines du stage, j’ai pu évoluer au sein de l’atelier
biomédical et suivre les techniciens au quotidien au cours de
leurs différentes interventions. Cela m’a permis de mieux
appréhender le parc de dispositifs médicaux, les moyens
du service et les méthodes de travail mises en œuvre.
Pour avoir une vision plus large du fonctionnement du Centre
Hospitalier, j’ai ensuite sollicité un entretien avec chacun des
Directeurs adjoints, afin qu’ils m’expliquent leur rôle au sein
de l’établissement et leurs attentes vis-à-vis du Service
biomédical. Ces rencontres ont été
extrêmement enrichissantes du fait de la variété
des domaines abordés (Ressources Humaines, Finances, Direction
des Soins Infirmiers…).
Partie 2 : Mise en place du Guide des Bonnes
Pratiques
Biomédicales
La mission principale qui m’a
été confiée au cours de ce stage portait sur la
réalisation d’une évaluation des pratiques du service et
sur une amélioration de celles-ci sur la base du Guide des
Bonnes Pratiques Biomédicales.
Le choix de ce « référentiel métier »
s’explique par la concrétisation d’une phase
supplémentaire atteinte dans l’évolution de la
démarche Qualité du Service Biomédical, en posant
un cadre plus formel et reconnu intégrant la mise en place
d’indicateurs et de processus d’évaluation.
I.
Présentation du référentiel
Le Guide des Bonnes Pratiques
Biomédicales en Etablissement de Santé [1],
rédigé par de nombreux acteurs biomédicaux, a
été réalisé dans un but d’accompagnement
progressif à l’amélioration quotidienne des pratiques
biomédicales en établissement de santé.
Il est divisé en 2 parties :
- les Bonnes Pratiques Fonctionnelles, répondant aux «
Pourquoi Faire »
- les Bonnes Pratiques Opérationnelles, répondant aux
« Comment Faire »
Le Guide des Bonnes Pratiques
Biomédicales recense les références minimales
à mettre en œuvre par un Service biomédical pour
déclarer son activité conforme l’état de l’art
validé par la communauté professionnelle
biomédicale française, et ce pour un établissement
exerçant tous les domaines d’activités abordés.
La finalité de sa mise en place ne doit pas être
l’obtention d’une note, mais plutôt la remise en question, la
formalisation et la progression globale des pratiques,
nécessaires à l’amélioration continue et
quotidienne de la qualité des prestations du Service
biomédical.
Cette limite posée, la démarche de déploiement du
Guide au sein du Service biomédical du Centre Hospitalier de
Millau s’inscrit dans la dynamique qualité initiée
dès la création du service en 2002. Elle se veut
également le point de départ d’une réflexion
à plus long terme sur l’intérêt ou non pour le
service de s’engager sur la voie d’une certification ISO9001.
La méthodologie suivie pour la
mise en place du Guide des Bonnes Pratiques Biomédicales a
été formalisée dans le processus suivant (Figure
5). Chacune de ces étapes sera détaillée par la
suite.
Figure 5: Processus global de mise en place du Guide des bonnes
pratiques biomédicales
IV.
Première autoévaluation
A.
Outil de diagnostic utilisé
L’évaluation des pratiques du
Service biomédical a été réalisée
à l’aide de la grille d’autodiagnostic associée au Guide
des Bonnes Pratiques Biomédicales [2]. Cet outil
(téléchargeable sur Internet) se présente sous la
forme d’un fichier Excel reprenant l’ensemble des « Bonnes
pratiques » sous la forme d’affirmation. L’évaluateur a
quatre choix de cotation pour chacune d’elles : « Faux »,
« Plutôt faux », « Plutôt vrai »,
« Vrai ». L’absence de point milieu oblige à se
positionner. Chaque réponse est ensuite pondérée,
et le résultat global est visualisable sous la forme d’un graphe
radar.
B.
Méthodologie d’évaluation
Le processus utilisé a
été élaboré dans le cadre du microprojet
Qualité portant sur l’amélioration de la confiance lors
de la réalisation d’un autodiagnostic [3]. Afin d’obtenir une
évaluation reflétant le plus fidèlement possible
les pratiques du service, l’autoévaluation a d’abord
été réalisée individuellement par chaque
agent biomédical.
Parallèlement à cela, une étude de la
documentation Qualité interne m’a permis de mieux comprendre le
fonctionnement du service et de répondre aux questions
suscitées par le remplissage de la grille d’autodiagnostic.
La confrontation des points de vue de chacun et en particulier des
divergences a ensuite permis d’élaborer une
autoévaluation en commun.
Cela a été l’occasion d’un rappel des différentes
procédures Qualité existantes et d’un échange sur
les taches réalisées par chaque agent. La
nécessité d’une meilleure communication entre niveaux
fonctionnels a pu ainsi être mise en évidence.
C.
Résultats de l’autoévaluation
commune
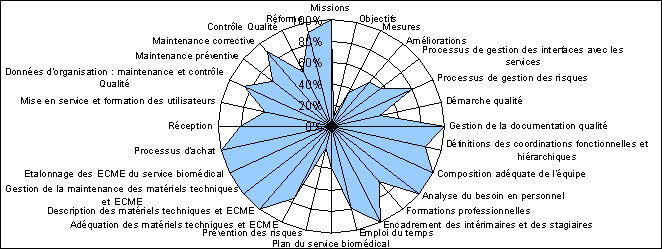
Les résultats de
l’autoévaluation réalisée en Février 2008
sont reportés sur la cartographie (Figure 6) et le tableau
(Tableau 1) ci-dessous :
Figure 6: Résultat de
l'autoévaluation
réalisée en Février 2008
Tableau 1 : Pourcentages obtenus pour
chaque Bonne Pratique
Cette première
évaluation a abouti à l’obtention d’un score total de
74,05%, reflétant une organisation du service globalement
satisfaisante. Cependant, pour être certifié «
Bonnes Pratiques », aucune d’entre elles ne devrait être
inférieure à 50%, et la note totale devrait être
supérieure à 90%.
Or l’autoévaluation fait ressortir :
- 5 pratiques dont le taux de réalisation est
inférieur à 50%
- Gestion de la documentation qualité
- Plan du Service biomédical
Ces pratiques devront être améliorées en
priorité.
- 6 pratiques dont le taux de réalisation est compris entre
50 et 75%
- Gestion des interfaces avec les Services
- Formations professionnelles
- Mise en service et formation des utilisateurs
Un progrès de ces pratiques est également à
envisager.
Les pratiques dont la cotation est supérieure à 75% ne
feront pas l’objet de modifications dans l’immédiat.
Au regard des résultats,
différentes priorités ont été
définies. Un tableau de bord de suivi de la mise en place des
bonnes pratiques (Tableau 2) a été réalisé,
sous la forme d’un classeur Excel reprenant les affirmations de l’outil
de diagnostic, leur cotation en Février 2008, les actions
associées à réaliser et leur état
d’avancement. Le tableau complet est présenté en Annexe 1.
Tableau 2: Extrait du tableau de bord
de mise en place du Guide des
Bonnes Pratiques Biomédicales
Deux thèmes de travail principaux ont été
dégagés :
- La mise en place d’objectifs mesurables et de niveaux de
réalisations acceptables, permettant d’évaluer les
différentes missions du service.
Cette démarche devra aboutir
à la création d’un tableau de bord permettant le suivi
régulier de l’activité biomédicale.
- L’identification d’actions réalisables à plus court
terme comme l’affichage du plan du service ou la mise en place de
fiches d’émargement lors des formations d’utilisateurs.
La planification des visites de l’atelier biomédical par le CLIN
et le CHSCT permettrait également d’améliorer notablement
la pratique correspondante.
V.
Création et mesure d’indicateurs
d�’activité
A.
Méthodologie générale
En prenant en compte le cours
dispensé à l’UTC sur les indicateurs [4] ainsi que
certains travaux déjà réalisés [5,6], la
définition des objectifs et la conception du tableau de bord se
sont faites selon le processus suivant (Figure 7):
Figure 7: Processus
d'élaboration du tableau de bord
B.
Propositions d’indicateurs
Sur la base des 4 missions du Service
Biomédical (Equipements, Maintenance, Maîtrise
Budgétaire, Veille Technologique et réglementaire), une
liste de différents indicateurs a été
proposée, avec leur provenance et un exemple de valeur
acceptable (Tableau 3). Après discussion, une trentaine d’entre
eux ont étés retenus.
Tableau 3: Extrait du tableau de
définition des indicateurs
C.
Importations des données
Le logiciel Excel de Microsoft a
été choisi pour réaliser le tableau de bord, car
accessible sur l’ensemble des postes informatiques dont dispose le
Service biomédical.
Une fois les indicateurs définis, une phase de test a
été nécessaire et a comporté 2
étapes :
- L’évaluation de la faisabilité et de la pertinence
des mesures. Cela a par exemple permis de vérifier, pour les
indicateurs extraits de la GMAO, la présence d’un nombre de
données suffisant pour une évaluation correcte.
- L’écriture de requêtes important toutes les
informations requises de la GMAO vers un classeur Excel.
Pour gérer l’ensemble des dispositifs médicaux dont il a
la charge, le Service biomédical utilise actuellement le
logiciel Asset Plus de General Electric. Lors d’une requête dans
cette application, la traduction en langage SQL s’affiche en bas de
l’écran, permettant d’identifier les champs de la base de
données contenant les informations recherchées (Figure 8).
Figure 8: Requête Asset
Plus
Pour importer des données
extérieures, Excel dispose du module MS Query, qui fonctionne
également par l’intermédiaire de requêtes SQL
(Figure 9). L’identification des différents champs « Asset
Plus » nécessaires au calcul des indicateurs m’a permis
d’écrire une dizaine de requêtes compilant toutes les
informations GMAO dans l’onglet « Extractions » du
tableau de bord.
Figure 9: Requête MS Query
D’autre part, une
fonctionnalité de MS Query permet de filtrer les données
selon certains critères. Celui de la date a été
retenu pour ne sélectionner que les informations relatives
à une période donnée. Deux cases du classeur ont
été réservées pour que l’utilisateur puisse
paramétrer facilement la date de début et la date de fin
des requêtes.
Le tableau de bord étant destiné à un suivi de
l’activité en temps réel, la date de début
correspond généralement au 1er janvier de l’année
en cours, et la date de fin à la date du jour. Cependant, il est
tout à fait possible de spécifier d’autres dates pour
retrouver les indicateurs des années précédentes
par exemple.
D.
Mise en forme du tableau de bord de suivi d’activité
Une fois toutes les données
brutes recueillies au sein d’un même classeur Excel, les
différents indicateurs ont pu être calculés et mis
en forme graphiquement sur un onglet « Tableau de bord ».
Celui-ci est divisé en différents encarts reprenant
chaque mission du service. Pour chacune d’entre elles, je
détaillerai les indicateurs définitifs, la façon
de les obtenir et les effets de leur mesure.
1)
Mission « Equipements »
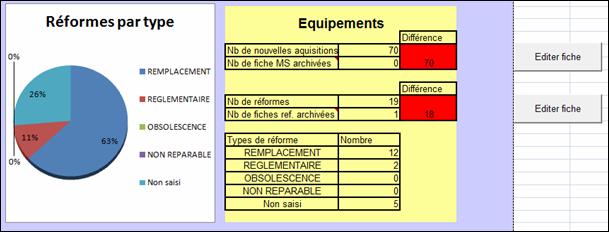
Les indicateurs choisis pour cette
mission concernent la bonne réalisation des processus de mise en
service et de réforme (Figure 10). Le nombre d’appareils mis en
service et réformés dans l’année (ou sur toute
autre période) est calculé automatiquement. L’utilisateur
indique le nombre de fiches archivées et le tableur calcule la
différence.
Ces indicateurs ont mis au jour un défaut d’archivage des fiches
papier, et ont permis de constater qu’aucun document n’était
rempli pour les appareils génériques
(thermomètres, glucomètre…).
En conséquence, la structure des fiches (Annexe 2) a
été modifiée pour prendre en compte les mises en
service et les réformes groupées de plusieurs appareils
de même nature. Une fois complétés, les documents
sont désormais scannés par les techniciens
biomédicaux, pour être retrouvés facilement, et les
procédures de mise en service (Annexe 3) et de réforme
ont été modifiées dans ce sens.
Figure 10: Indicateurs "Equipements"
De plus, une macro permet
d’éditer les listes de DM mis en service ou
réformés, permettant une comparaison plus rapide aux
fiches papier numérisées.
Les différentes causes de réforme sont visualisables sur
un graphique automatique, qui fait également apparaître le
pourcentage de champ non saisi. Cela a abouti à une
redéfinition des causes de réforme disponibles dans la
GMAO et à une meilleure saisie de cette information.
La répartition des dispositifs médicaux par classe est
également disponible dans le tableau de bord (Figure 11).
Figure 11: Répartition
des DM
par classe
2)
Mission « Maintenance »
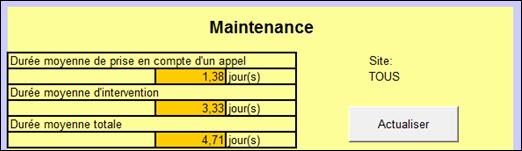
Les informations souhaitées
pour cette mission concernent :
- le délai de prise en compte d’un appel
- la durée moyenne d’intervention
- la durée totale entre l’appel et la fin d’intervention
Asset Plus ne permet pas de retrouver directement ces informations. En
revanche, les dates correspondantes sont stockées dans la base
et peuvent donc être importées. Un calcul sur une feuille
cachée du classeur permet d’inclure automatiquement ces
indicateurs dans le tableau de bord, pour la période
désirée (Figure 12).
Figure 12: Délais de
Maintenance
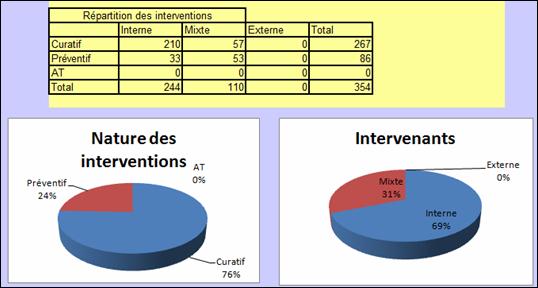
Un tableau additionnel montre la
répartition des interventions selon leur nature et leur
intervenant (Figure 13).
Figure 13: Répartitions
des
interventions
Suite à une demande de
l’ingénieur biomédical, j’ai modifié la
requête pour inclure l’établissement d’origine de la
demande d’intervention (Millau, Saint-Affrique, Maisons de retraite…),
et ajouté une macro calculant les indicateurs de délai
selon le site choisi par l’utilisateur.
Enfin, le tableau de bord permet de visualiser le taux de maintenance
préventive dont la date de planification est
dépassée.
3)
Mission « Maîtrise
budgétaire
»
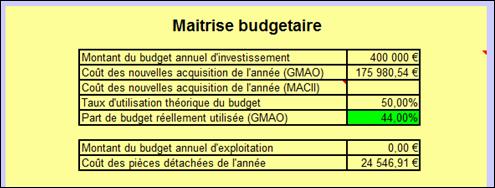
L’indicateur principal porte sur le taux d’exécution du plan
d’investissement annuel. Pour cela :
- l’utilisateur indique le budget d’investissement disponible
- une requête calcule le montant des acquisitions de
l’année d’après le GMAO
- un taux théorique d’exécution est calculé
selon le mois de l’année, permettant à l’utilisateur de
visualiser l’avance ou le retard pris dans l’investissement (Figure 14)
Figure 14: Indicateurs
"Maîtrise
Budgétaire"
La même démarche sera
effectuée pour le budget d’exploitation.
Le coût des contrats est également rapporté sur le
tableau de bord. Cependant, un premier calcul a permis de constater
qu’une mise à jour de ce volet dans la GMAO était
nécessaire avant d’exploiter correctement l’indicateur
correspondant.
4)
Mission « Veille technologique et
règlementaire »
Aucun indicateur ne permet
actuellement de mesurer le taux d’avancement de cette mission. Une
piste de travail consisterait à mettre en place des «
heures de veille », notée sur le planning GMAO et donc
importables, pour pouvoir ensuite les comptabiliser.
E.
Définition des niveaux acceptables
Une fois tous les indicateurs
recueillis, des niveaux d’acceptabilité ont été
définis pour chacun d’eux. J’ai ensuite utilisé la
fonction « Mise en forme conditionnelle » d’Excel pour
visualiser ces limites. Un indicateur conforme à l’objectif
apparaît ainsi en vert, un écart mineur se traduit par un
affichage en orange, et un écart majeur par un affichage en
rouge.
Ces limites pourront être réajustées selon les
résultats obtenus.
L’intégralité des indicateurs, de leur mode d’obtention,
de l’objectif associé et des niveaux de tolérance est
reprise en Annexe 4.
F.
Impact sur les « Bonnes Pratiques »
La définition et la mesure
d’indicateurs d’activité du Service biomédical a
nécessairement entraîné une remise en cause des
pratiques, et a permis d’améliorer certains items du Guide.
1)
BPF-02 : Objectifs
Pour chaque mission du service, des
objectifs sont désormais clairement définis et ont
été intégrés au protocole «
Fonctionnement du Service Biomédical ». Comme
évoqué précédemment, une cinquième
mission a également été ajoutée. Elle
comprend notamment l’application du Guide des Bonnes Pratiques
Biomédicales et la réalisation périodique
d’autodiagnostics.
2)
BPF-03 : Mesures
Le tableau de bord dynamique permet
de répondre à cette « Bonne Pratique ». Les
principales missions peuvent être évaluées à
tout moment, rapidement et sur une seule et même feuille Excel.
Les données sources sont mises à jour automatiquement, et
un archivage régulier du fichier permettra de suivre
l’évolution des indicateurs dans le temps. Une procédure
« Actualisation du Tableau de bord de suivi d’activité
» (Annexe 5) a été écrite pour formaliser la
saisie.
3)
BPF-04 : Améliorations
Un premier plan d’action concernant
la mise en place du Guide des Bonnes Pratiques avait été
élaboré suite à la première
autoévaluation du service. Il pourra être
réactualisé à chaque nouvel autodiagnostic. En
parallèle, l’exploitation régulière des
indicateurs d’activité devrait permettre à terme de
construire un second plan visant plus spécifiquement l’atteinte
des objectifs fixés.
4)
Bonnes Pratiques Opérationnelles
Les processus de mise en service, de
maintenance curative, préventive et de réforme font
maintenant l’objet d’une évaluation par l’intermédiaire
du tableau de bord. De nouveaux indicateurs concernant la formation des
utilisateurs et le contrôle Qualité pourrait être
ajoutés pour faire eux aussi l’objet d’un suivi.
VI.
Autres « Bonnes Pratiques »
abordées
A.
BPO-04-02: Plan du Service biomédical
Le plan du service existait, mais
n’était pas affiché. Un nouveau plan a donc
été réalisé en coopération avec les
Services Techniques, reprenant les différentes zones de
l’atelier dédiées chacune à une activité
spécifique (Figure 15).
Figure 15: Plan de l'atelier
La limitation d’accès à
l’atelier aux personnes autorisées a également
été formalisée.
B. BPO-02-2-1:
Démarche Qualité
Il a paru pertinent de formaliser une
cinquième mission du service concernant la démarche
qualité, et reprenant l’application du Guide des Bonnes
Pratiques. Deux indicateurs ont donc été
ajoutés au tableau de bord : la date du dernier autodiagnostic
et le score obtenu. Ces paramètres sont renseignés par
l’utilisateur directement sur le tableau de bord.
La mission « Démarche Qualité » a
été intégrée au protocole «
Fonctionnement du Service Biomédical ». Elle est
couplée à des objectifs mesurables.
La fiche de poste du référent Qualité a
été modifiée pour faire mention de ses
responsabilités, ce qui n’était pas encore le cas. Enfin,
un dossier « Autoévaluations Bonnes Pratiques » a
été créé dans le répertoire Intranet
du service pour archiver les différentes autoévaluations
réalisées et les plans d’actions associés.
C.
Formation des utilisateurs
Une feuille d’émargement a
été mise en place (Annexe 6), pour pouvoir conserver
l’identité des différents utilisateurs formés sur
un dispositif médical, et intégrée à la
procédure correspondante.
VII.
Seconde
autoévaluation
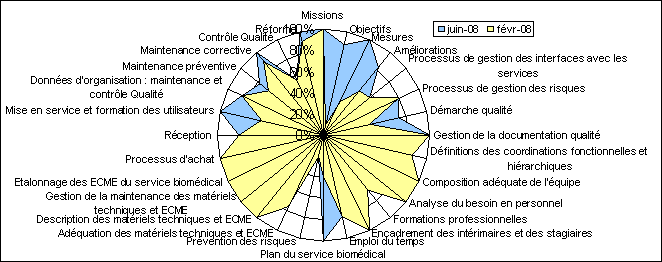
Afin de mesurer les progrès
accomplis dans le cadre du déploiement du Guide des Bonnes
Pratiques Biomédicales, j’ai réalisé une seconde
autoévaluation au mois de Juin (Figure 16).
Figure 16: Comparaison des
autoévaluations
réalisées en Février et Juin
Ce nouvel autodiagnostic donne un
score de 85,84% soit une progression de près de 12 points. Les
améliorations les plus visibles se situent logiquement au niveau
des Bonnes Pratiques Fonctionnelles (Objectifs, Mesures,
Améliorations), suite à la mise en place du Tableau de
Bord de Suivi d’Activité.
Une seule « Bonne Pratique » reste inférieure
à 50%, concernant la Prévention des Risques. Une visite
du CLIN et du CHSCT sera sollicitée d’ici fin 2008.
VIII.
Bilan et perspectives
La mise en place du tableau de bord a
permis de définir des indicateurs et des objectifs
associés pour les différentes missions du service.
Une actualisation sera réalisée au moins une fois par
mois et fera l’objet d’une réunion de l’ensemble du personnel
biomédical. Des plans d’action ciblés sur les objectifs
non atteints pourront alors être élaborés.
D’autres indicateurs pourront être ajoutés pour parfaire
le suivi de l’activité.
La mise en place du Guide des Bonnes Pratiques devra se poursuivre afin
d’atteindre les 90%, ce qui semble envisageable à court terme
notamment par un travail sur les parties maintenance préventive,
contrôle qualité, et réception en mettant en place
des évaluations et une meilleure information des services
clients.
Concernant l’engagement du service biomédical dans la voie de la
certification ISO 9001, différents éléments
amènent à s’interroger sur la pertinence d’une telle
démarche à l’heure actuelle :
- La norme ISO 9001 est généraliste. Concernant
l’activité biomédicale, le Guide des Bonnes Pratiques
permet d’atteindre en grande partie le niveau de performance requis par
la norme sans s’engager dans un processus de certification qui peut
s’avérer complexe, contraignant et coûteux selon les
retours d’expériences évoqués notamment lors d’une
réunion régionale AFIB sur le sujet [7].
- Les points non abordés par le Guide portent notamment sur
l’évaluation des fournisseurs, qui s’avère
extrêmement complexe à mettre en place. La question de la
pertinence se pose sur l’évaluation, par un effectif de 3
personnes, de structures bien plus conséquentes et parfois
elles-mêmes certifiés ISO.
- L’ISO 9001 offre une reconnaissance officielle de la
qualité des prestations, mais est soumise à l’obtention
de ressources régulières pour financer la
démarche. Un défaut de financement pourrait aboutir
à une perte de la certification malgré un même
niveau de qualité des prestations, et entraîner une
démotivation du personnel.
Une certification n’est donc pas envisagée dans
l’immédiat, le service souhaitant plutôt s’orienter
vers une amélioration continue des pratiques en s’appuyant sur
le Guide des Bonnes Pratiques Biomédicales.
Cette démarche permet d’accroître son niveau de
Qualité de fonctionnement et de prestations auprès des
services Clients (Direction et Soins) en s’appuyant sur une structure
formalisée en démarche d’amélioration continue.
Elle permet par ailleurs de se préparer à toute
évolution vers la certification ISO 9001 et ce naturellement ou
dans le cadre d’un projet d’établissement.
Partie
3 : Participation à l’exécution du plan
d’investissement
biomédical
Un deuxième axe de travail de
mon stage a été de m’initier aux procédures
d’achats qui, au sein d’un établissement hospitalier, sont
régies par le Code des Marché Publics [8]. Après
une brève présentation de celui-ci, j’aborderai les
dossiers d’achat auxquels j’ai pu participer.
I.
Synthèse du Code des Marchés Publics
A. Quand
parle-t-on de « Marché Public
» ?
Dans le Code des Marchés
Publics (Article 1), il s’agit d’un contrat conclu à titre
onéreux entre un acheteur public et des opérateurs
économiques publics ou privés, pour répondre
à leurs besoins en matière de travaux, de fournitures ou
de services.
Cette procédure doit favoriser le plus possible l’ouverture
à la concurrence. Par exemple, aucune marque ou technologie
particulière (brevet) ne doit être citée, pour ne
pas fermer le marché à certaines entreprises (Article 6).
De même, il est préférable que le
marché soit divisé en lots, afin de ne pas le limiter aux
entreprises pouvant fournir la totalité des matériels et
prestations demandées (Article 10).
B.
Seuils et types de marchés :
Comme il a pu être vu lors des
cours sur les Marchés Publics délivrés à
l’UTC [9] :
- Tous les marchés supérieurs à 4000€ HT
doivent être formalisés sous forme écrite.
- Entre 4 000€ HT et 90 000€ HT, l’acheteur peut choisir le type de
publicité en fonction du marché. On parle de
Marché à Procédure Adaptée (MAPA).
- Au-delà de 90 000€ HT, il est obligatoire de publier un
avis d'appel public à la concurrence dans le Bulletin officiel
des annonces des marchés publics et au Journal officiel de
l'Union européenne.
- A partir de 206 000€ HT, la procédure d’appel d’offre est
impérative.
Les commandes peuvent être groupées, ou passer par une
centrale d’achat (ex : UGAP). L’acheteur est alors dispensé de
procédure de mise en concurrence, puisque celle-ci est
déjà effectuée par la centrale d’achat (Articles 7
à 9).
Si les quantités à acheter ne peuvent pas être
précisément fixées, l’acheteur peut enfin avoir
recours à un marché « à tranche » ou
« à bons de commande ».
Dans le premier cas, la première tranche est ferme et les
suivantes conditionnelles. Chaque tranche est fonctionnelle seule.
Dans le cas d’un marché à « bons de commande
», le marché s’exécute au fur et à mesure
des bons de commande et ne peux excéder 4 ans.
C.
Les pièces constitutives :
Ces pièces sont décrites aux articles 11 à 13 du
Code des Marchés Publics.
1)
Le règlement de consultation
Le règlement de consultation
décrit les caractéristiques d’un marché public et
détermine les conditions d’envoi et de jugement des offres.
Il précise notamment si le marché comporte un ou
plusieurs lots, si les variantes sont autorisées, et indique les
critères de choix et leur pondération.
2)
L�’acte d’engagement
Signée par un candidat
à un marché public, il présente son offre ou sa
proposition dans le respect des clauses du cahier des charges qui
déterminent les conditions dans lesquelles le marché est
exécuté. Cet acte d'engagement est ensuite signé
par l’acheteur.
3)
Le Cahier des Charges :
Il est constitué de documents
généraux et particuliers :
- le Cahier des Clauses Administratives Générales
fixe les dispositions administratives applicables à une
catégorie de marché.
- le Cahier des Clauses Techniques Générales fixe les
dispositions techniques applicables à toutes les prestations
d'une même nature.
La
référence à ces deux documents n’est pas
obligatoire.
- le Cahier des Clauses Administratives Particulières fixe
les dispositions administratives propres à chaque marché.
- le Cahier des Clauses Techniques Particulières fixe les
dispositions techniques nécessaires à l'exécution
des prestations de chaque marché.
S’il est fait référence aux documents
généraux, les documents particuliers précisent les
articles auxquels ils dérogent.
D.
La commission d’appel d’offre :
Selon l’Article 22, le nombre, la
composition et les modalités d'organisation et de fonctionnement
de la commission d'appel d'offres ou des commissions d'appel d'offres
sont arrêtées par le Directeur de l'établissement
après avis du conseil d'administration.
Outre le directeur ou son représentant, chaque commission
comporte obligatoirement au moins un membre désigné par
le conseil d'administration en son sein ou parmi des
personnalités qualifiées proposées par le
directeur.
Chaque commission comporte un nombre impair de membres.
II.
Déroulement de la procédure :
A. Appel à
concurrence :
Le point de départ d’un achat de dispositif médical est
la rédaction du Cahier des Charges, permettant de définir
le besoin des futurs utilisateurs. Il est d’ailleurs souhaitable que
ces derniers participent à la rédaction.
Une fois le besoin identifié, une première estimation
financière permet de définir le type de procédure
à utiliser et la publicité associée.
Les différents documents (RC, CCTP, CCAP…) sont alors
rédigés pour constituer le dossier de consultation, qui
est ensuite mis à disposition des entreprises souhaitant faire
une offre.
B.
Réception et examen des offres
Les offres des différents
candidats doivent rester confidentielles jusqu’à expiration du
délai de présentation. Si l’acheteur l’autorise, les
candidats peuvent proposer des variantes, toujours en complément
de l’offre de base.
Les candidats doivent produire deux enveloppes distinctes et ce dans le
délai imparti, sous peine de rejet de l’offre.
La première contient les documents attestant leur aptitude
à soumissionner, permettant :
- de vérifier que les dossiers sont complets
- de vérifier que les entreprises peuvent faire acte de
candidatures (à jour des obligations fiscales et sociales, pas
de redressement judiciaire…)
- de vérifier que les candidats ont la capacité
d’exécuter le marché
- d’examiner les capacités techniques, professionnelles et
financières des candidats
La seconde enveloppe contient l’offre proprement dite des candidats, et
doit fournir toutes les informations nécessaires à une
évaluation correcte du matériel proposé.
C.
Choix et clôture de la procédure
L’acheteur analyse l’ensemble des
offres, choisit la mieux disante selon les critères de choix
définis, et informe les candidats non retenus qui peuvent
demander justification. Une fois le candidat choisi, un avis
d’attribution du marché est publié, point de
départ du délai de contestation.
Un rapport de présentation est publié à l’issue de
la procédure de passation, précisant les motifs du choix
ou du rejet de chaque candidat.
Les établissements publics de santé doivent
également publier tous les trimestres la liste des
marchés conclus avec les noms des attributaires.
III. Principaux dossiers
traités
Tout en étudiant les
différentes procédures d’achat public, j’ai pu participer
a l’acquisition de différents dispositifs médicaux dans
le cadre du Plan d‘investissement annuel du Centre Hospitalier de
Millau et notamment à celles de deux injecteurs de produits de
contraste et d’un automate d’immuno-hématologie.
A.
L’injecteur de produit de contraste
Pour 2008, le principal
investissement biomédical concernait l’acquisition d’un scanner
et d’un IRM. Ce marché était divisé en 2 tranches,
la première exécutable en Juin 2008 (scanner), la seconde
fin 2009 (IRM).
Mon arrivée en Février coïncidait avec la phase de
réception des offres. Pour chacune des 2 tranches, un des lots
concernait la fourniture d’un injecteur de produit de contraste.
Trois fournisseurs ont répondu à la fois pour le lot
concernant l’injecteur du scanner et pour le lot concernant celui de
l’IRM, un quatrième n’a répondu que pour l’injecteur du
scanner. J’ai donc été chargée de la suite de la
procédure pour ces 2 lots.
1)
Présentation des appareils
Lors de la réalisation de
certains examens de scanner ou d’IRM, l’utilisation de produit de
contraste s’avère nécessaire pour mettre en
évidence certains organes ou pathologies. L’injecteur permet de
réaliser cette manipulation de manière automatique,
garantissant un acte plus sûr et précis.
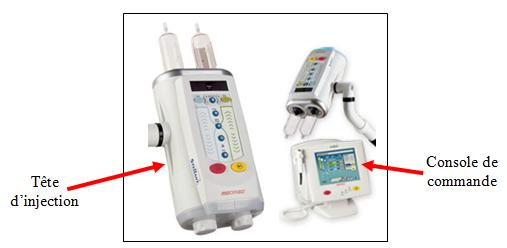
L’appareil se compose d’une tête d’injection, sur laquelle sont
placées les seringues contenant le produit de contraste, et
d’une console de commande (Figure 17). Cette dernière est
utilisée pour programmer puis pour effectuer l’injection
à distance.
Figure 17: Injecteur de produit de
contraste (Source: www.medrad.com)
Lors du la rédaction du Cahier
des Charges, le Centre Hospitalier de Millau a souhaité un
injecteur double voie, offrant la possibilité d’administrer
à un patient 2 produits différents. Cela permet
d’affecter du sérum physiologique à l’une des seringues
et de l’utiliser pour vérifier la qualité de l’injection
avant d’administrer le produit de contraste.
2)
Analyse des offres
Après avoir pris connaissance du CCPT concernant les 2
injecteurs (Scanner et IRM), j’ai compilé sous forme de tableau
Excel les différentes annexes transmises par les fournisseurs
(Tableau 4). Ces documents, demandés par l’ingénieur
biomédical, permettent de comparer les différentes offres
selon les mêmes critères (technique, SAV, maintenance,
bordereau de prix…) et en facilitent ainsi l’analyse.
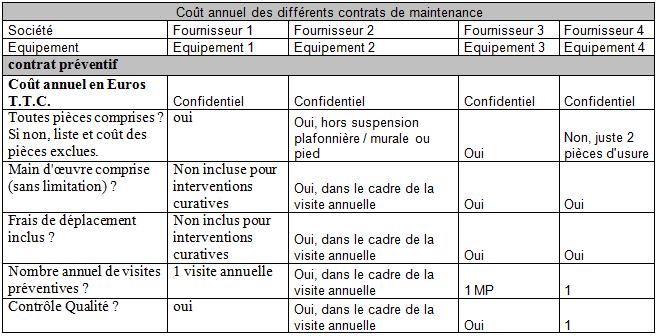
Tableau 4: Extrait de la
synthèse de l'annexe "Maintenance"
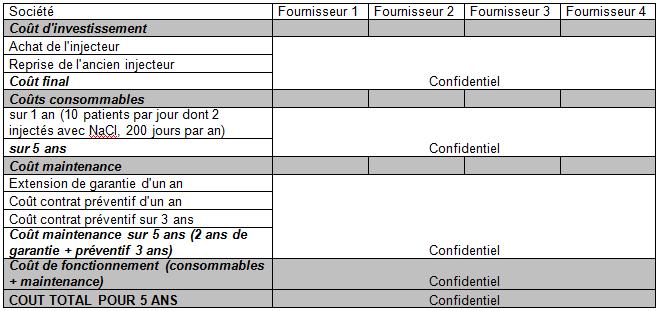
Il a également
été nécessaire de calculer le coût total de
l’acquisition et de l’exploitation du DM sur 5 ans, en intégrant
notamment les consommables et la maintenance (Tableau 5). En effet,
cela révèle parfois de grandes disparités entre
fournisseurs, non décelable sur la seule base du coût
d’achat de l’appareil.
Tableau 5: Synthèse
économique de l'achat d'un injecteur
Toutes ces informations ont abouti à l’élaboration un
tableau de synthèse global, définissant un premier
classement des différentes propositions selon les
critères de choix définis dans le CCTP.
3)
Coordination des essais
Une fois les offres reçues et
examinées, il est possible de contacter les différents
fournisseurs pour convenir d’une démonstration de leur
matériel.
Le Centre Hospitalier de Millau ne possédant pas encore d’IRM,
les essais n’ont pu être réalisés que sur
l’activité « Scanner ». Par souci
d’équité, la même période de
démonstration a été demandée à
chaque candidat, à savoir une demi-journée.
Cette phase est l’occasion de voir en fonctionnement les appareils
proposés. Pour permettre le recueil des avis des utilisateurs et
l’évaluation de la valeur technique des dispositifs, des fiches
d’évaluations ont été rédigées puis
intégrées à l’analyse des offres.
Ces essais ont également fait l’objet d’un compte-rendu
écrit et oral, l’ingénieur biomédical n’ayant pu
être présent.
4)
Présentation du rapport d’analyse
Pour clore cette phase d’analyse, j’ai élaboré le rapport
de présentation des offres pour les 2 injecteurs, sur la base de
toutes les informations recueillies.
Ce document se termine par un classement des différentes offres
par le biais de notes pondérées et permet
d’émettre un avis quant au fournisseur à retenir.
Ce rapport a ensuite fait l’objet d’une présentation en
Commission d’appel d’offres, qui a validé le choix
effectué. La même société a
été sélectionnée pour la fourniture des 2
injecteurs.
5)
Finalisation du Dossier
Une fois le titulaire du
marché informé de l’acceptation de son offre, la commande
a pu être passée pour l’injecteur du scanner, la tranche
« IRM » n’étant pas encore finalisée.
Les travaux d’installation ont été coordonnés avec
l’arrivée du nouveau scanner fin Juin.
Les consommables ont été commandés en
collaboration avec le Service de Radiologie et la Pharmacie.
B. L’automate
d’immuno-hématologie
Un second investissement concernait
l’acquisition d’un automate d’immuno-hématologie (Figure 18),
afin de remplacer l’appareil existant, arrivant en fin de vie.
Figure 18: Automate complet
d'immuno-hématologie (Source :
www.diamed.com)
Les principales analyses
effectuées par ce type d’automate concernent les
déterminations de groupes sanguins et de phénotypes ainsi
que les recherches d’anticorps irréguliers. Leur
réalisation est soumise à l’Arrêté du 26
Avril 2002 relatif à la bonne exécution des analyses de
biologie médicale [10].
Ce texte précise notamment qu’en cas d’utilisation d’un
automate, une seule détermination est suffisante pour valider un
résultat, au lieu de 2 en cas de recours à une
méthode manuelle. L’automation permet en effet de minimiser les
risques d’erreurs humaines et de garantir une meilleure
sécurité au patient.
A l’heure actuelle, 2 types de dispositifs existent :
- les automates complets, prenant en charge les échantillons
de leur chargement dans la machine jusqu’au résultat de
l’analyse sans intervention supplémentaire de la part de
l’opérateur
- les semi-automates, qui nécessitent le déplacement
manuel des échantillons entre des modules réalisant
différentes étapes de l’examen.
Dans les 2 cas, la saisie des données patient, l’identification
des échantillons et la lecture des résultats sont
automatiques.
1)
Formalisation du besoin
En m’appuyant sur les
caractéristiques minimales de l’appareil et les données
d’activité transmises par le Laboratoire du Centre Hospitalier
ainsi que sur un CCTP élaboré précédemment
pour une autre catégorie d’automate, j’ai rédigé
le Cahier des Clauses Techniques Particulières pour
l’acquisition de l’automate d’immuno-hématologie.
Différents articles y ont été
intégrés, abordant par exemple l’activité actuelle
du Laboratoire, les critères de choix et leur
pondération, les attentes vis-à-vis de l’appareil ou
encore les conditions de formation.
En parallèle, j’ai pris contact avec différents
fournisseurs afin d’adapter au mieux le CCTP à la demande des
utilisateurs sans pour autant écarter de fournisseurs
potentiels. Ce travail a notamment permis de chiffrer approximativement
le coût d’investissement lié à l’automate et donc
le type de procédure à utiliser et de scinder le
marché en 3 lots différents (automate, réactifs,
maintenance) offrant aux candidats la possibilité de
répondre totalement ou partiellement au besoin du Centre
Hospitalier.
Le CCTP ayant été validé par l’ingénieur
biomédical, j’ai construit le questionnaire technique et les
annexes associées.
2)
Publication
Une fois réunis tous les
documents nécessaires à la constitution du Dossier de
Consultation (CCTP, CCAP, Actes d’engagements…), ceux-ci sont mis
à la disposition des fournisseurs. S’agissant d’un Marché
à Procédure Adaptée, ils ont été
publiés sur un site Internet dédié aux
Marchés Publics. Ils peuvent aussi être obtenus
directement sur demande auprès du Centre Hospitalier.
3)
Dépouillement des offres
A l’issue du délai
mentionné dans le règlement de consultation, trois
fournisseurs ont répondu à l’ensemble des lots et un n’a
répondu qu’aux lots « Automate » et «
Maintenance ».
J’ai réalisé, comme pour les injecteurs, un tableau
comparatif des différentes offres proposées en
intégrant les coûts de consommables et de maintenance sur
5 ans (Annexe 7).
En complément, l’activité actuelle du Laboratoire a
été chiffrée en termes de gains pour le Centre
Hospitalier, en s’appuyant sur le nombre de « B »
associés à chaque analyse. Cette démarche a permis
de mettre en parallèle les dépenses et les gains
liés à l’acquisition de l’automate.
A ce jour, le rapport d’analyse est en cours de rédaction, et
des essais devraient être organisés afin de pouvoir mieux
évaluer les offres reçues.
Conclusion
Ces 5 mois de stage ont
été l’occasion d’aborder parallèlement deux
thèmes centraux de l’activité d’un Ingénieur
biomédical : la conduite d’une démarche Qualité et
la réalisation d’investissements.
La mise en œuvre du Guide des Bonnes Pratiques Biomédicales au
sein d’un Service déjà fortement sensibilisé
à la culture Qualité, a permis non seulement une remise
en question du personnel et de son fonctionnement, mais
également d’instaurer un second souffle. Cette nouvelle
dynamique de progrès devra se poursuivre pour que le service
puisse atteindre les 90% requis par le Guide et déclarer ses
pratiques conformes à l’état de l’art validé par
la profession.
Ma participation à une réunion régionale de l’AFIB
sur la certification des services biomédicaux m’a
également fait comprendre combien cette démarche concerne
l’ensemble des hôpitaux.
Dans ce cadre, la mise en place d’objectifs et d’indicateurs de suivi
de l’activité m’a permis d’appréhender la politique de
maintenance dans sa globalité, et d’engager des actions
concrètes pour résoudre des problèmes quotidiens,
tels que la traçabilité des documents, le respect des
délais et des échéances, et le suivi
budgétaire.
Par ailleurs, mon implication dans différents dossiers d’achat a
été l’occasion de participer à
l’intégralité du processus d’investissement, de
l’élaboration du plan d’équipement jusqu’à la mise
en service des dispositifs médicaux. J’ai ainsi pu en
appréhender concrètement les différentes
étapes et me rendre compte de l’importance des interactions avec
les différents intervenants tels que la Direction et le corps
médical.
Ce stage aura été extrêmement riche en
enseignements qui me seront d’une aide précieuse par la suite.
Constituant une confrontation directe aux nombreux aspects de la
fonction d’ingénieur biomédical mais aussi à ses
contraintes et à ses difficultés, ces cinq mois ont plus
que jamais renforcé ma conviction de vouloir exercer ce
métier.
Références
- Mise en place du Guide des Bonnes Pratiques :
[1] Guide des Bonnes Pratiques Biomédicales en Etablissement de
Santé, Farges G. (UTC), Wahart G., Denax J.M., Métayer
H., et 45 co-auteurs, ITBM-RBM News, Ed Elsevier, novembre 2002, Vol.
23, Suppl2, 23s-52s.
[2] Contribution à la démarche de validation en «
Bonnes Pratiques Biomédicales » : la grille
d'évaluation, A.Guyard, L. Tamames, G. Farges, Edition Elsevier,
ITBM-RBM News, 2004, ITBM-RBM News 2004, Vol.25, n°2.
[3] Comment améliorer la confiance dans l'autodiagnostic
associé au Guide des Bonnes Pratiques Biomédicales ? V.
Arfib, C. Driard, F. Hanoomie, M. Plantevin, G. Farges, Projet «
Management de la Qualité », UTC, 2007-2008.
[4] Indicateurs Qualité dans un établissement de
santé, G. Farges, UTC, Octobre 2007.
[5] Recherche et création d'indicateurs des équipements
biomédicaux, Jean-Baptiste Beck, Projet MASTER MTS, UTC,
2004-2005.
[6] Tableau de bord et rapport d'activité automatisés
depuis la GMAO, H. Szymczak, Stage MASTER MTS, UTC, 2004-2005.
[7] La certification des Services Biomédicaux, Réunion
régionale AFIB, CH Rodez, 6 Juin 2008.
[8] Code des marchés publics, édition 2006, version
consolidée au 30 Avril 2008.
[9] Biomédical et Marchés Publics : Aspects Pratiques, A.
Jaborska, UTC, 22 Novembre 2007.
[10] Arrêté du 26 avril 2002 modifiant
l’arrêté du 26 novembre 1999 relatif à la bonne
exécution des analyses de biologie médicale (GBEA), JORF
n ° 104 du 4 mai 2002 p.8375, NOR : SANP0221588A.
www.legifrance.gouv.fr
www.colloc.minefi.gouv.fr/colo_struct_marc_publ/_code.html
www.utc.fr/~farges
Table
des Annexes (sur
demande)
Annexe 1 : Tableau de Bord de Mise en place du Guide des Bonnes
Pratiques Biomédicales
Annexe 2 : Fiche de Mise en Service d’un dispositif médical
Annexe 3 : Procédure de mise en service d’un dispositif
médical
Annexe 4 : Tableau récapitulatif des indicateurs
Annexe 5 : Fiche technique d’actualisation de tableau de bord de suivi
d’activité biomédicale
Annexe 6: Fiche d’émargement – Formation à l’utilisation
d’un DM
Annexe 7 : Synthèse du Questionnaire Technique de l’automate
d’immuno-hématologie
retour
sommaire